Идиопатический легочный фиброз (ИЛФ): современный подход к классификации и диагностике
Идиопатический легочный фиброз (ИЛФ) – это вариант идиопатической интерстициальной пневмонии (ИИП), характеризующийся неуклонным прогрессирующим течением и высокой смертностью. В отличие от большинства ИИП, иммуносупрессивная терапия не оказывает влияния на скорость прогрессирования ИЛФ. В течение последнего десятилетия установлена эффективность двух антифибротических препаратов в лечении ИЛФ – пирфенидона и нинтеданиба. Чтобы своевременно начать патогенетическую терапию, необходимо как можно быстрее установить диагноз ИЛФ на основании диагностического алгоритма, предполагающего анализ клинических, лабораторных и инструментальных данных, прежде всего результатов компьютерной томографии высокого разрешения (КТВР). При недостаточной информативности последней может быть использована малоинвазивная трансбронхиальная криобиопсия легкого, которая по точности сопоставима с хирургической биопсией легкого. Продолжается поиск молекулярно-биологических и генетических маркеров ИЛФ.
Согласно классификации Американского торакального общества/Европейского респираторного общества (ATS):1–112. /ERS):1–112. ) [1], идиопатический легочный фиброз (ИЛФ) представляет собой форму идиопатической интерстициальной пневмонии (ИИП) (табл. 1). Доля ИЛФ составляет 20-30% в структуре всех ИИП, а заболеваемость – от 7 до 17 случаев на 100 000 населения [2]. Мужчины болеют несколько чаще, чем женщины (соотношение мужчин/женщин приблизительно 1,5:1) [3]. ИЛФ развивается в основном у людей среднего и пожилого возраста: возраст 65% пациентов на момент постановки диагноза составляет 60 лет и более [4].
| Частые формы ИИП |
| Идиопатический легочный фиброз (ИЛФ) |
| Идиопатическая неспецифическая интерстициальная пневмония |
| Респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких |
| Десквамативная интерстициальная пневмония |
| Криптогенная организующая пневмония |
| Острая интерстициальная пневмония |
| Редкие формы ИИП |
| Идиопатическая лимфоцитарная интерстициальная пневмония |
| Идиопатический плевропаренхиматозный фиброэластоз |
| Неклассифицируемые формы (ИИП) |
В 2018 году P. Wolters и соавт. предложили выделять 4 варианта легочного фиброза в зависимости от патогенеза заболевания (табл. 2) [5]. ИЛФ характеризуется прогрессирующим течением с развитием дыхательной недостаточности и среди всех ИИП обладает самым неблагоприятным прогнозом: средняя выживаемость составляет от 2 до 5 лет [6,7]. Высокая смертность пациентов с ИЛФ объясняется особенностями патогенеза заболевания – преобладанием фиброза при незначительной выраженности воспалительных изменений [8,9]. Основным механизмом, приводящим к развитию прогрессирующего легочного фиброза, является персистирующее повреждение альвеолярного эпителия с последующим нарушением процессов его регенерации, избыточным отложением компонентов внеклеточного матрикса, активацией фибробластов и миофибробластов [10]. Указанные изменения определяют неэффективность традиционной иммуносупрессивной терапии у пациентов с ИЛФ [11]. Тем не менее, в настоящее время достигнуты значительные успехи в лечении ИЛФ, связанные с применением антифибротических препаратов – пирфенидона (антагониста трансформирующего фактора роста бета – TGF β) и нинтеданиба (множественного ингибитора тирозинкиназ), замедляющих уменьшение легочных объемов, в первую очередь, форсированной жизненной емкости легких (ФЖЕЛ), и улучшающих выживаемость без прогрессирования заболевания [12]. При отсутствии противопоказаний трансплантация легких также рассматривается в качестве варианта лечения у пациентов с прогрессирующим ИЛФ, осложнившимся тяжелой дыхательной недостаточностью [13,14].
| Группа 1: ЛФ, индуцированный дисфункцией эпителиальных клеток | ИЛФ |
| Группа 2: ЛФ, индуцированный дисфункцией клеток воспалени | Системная склеродермия, ревматоидный артрит, синдром Шегрена, экзогенный аллергический альвеолит, саркоидоз, НСИП |
| Группа 3: ЛФ, вызванный приемом лекарственных препаратов или воздействием профессиональных факторов | Асбестоз, силикоз, лекарственное поражение легких |
| Группа 4: ЛФ, связанный с курением | Десквамативная интерстициальная пневмония, респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких, Лангерганс-клеточный гистиоцитоз |
Клиническая картина
Основные жалобы у пациентов с ИЛФ – прогрессирующая одышка и сухой кашель, усиливающиеся при физической нагрузке. Реже отмечаются боль и дискомфорт в грудной клетке, повышенная утомляемость, общая слабость, снижение массы тела. В ряде случаев заболевание на начальных этапах протекает бессимптомно, а первыми проявлениями оказываются изменения функциональных легочных параметров [1]. Типичным аускультативным феноменом при ИЛФ является крепитация, преимущественно в задне-базальных отделах легких. У больных c развернутой стадией ИЛФ могут отмечаться признаки вторичной артериальной легочной гипертензии с развитием легочного сердца и правожелудочковой сердечной недостаточности [15].
При ИЛФ может определяться незначительное повышение СОЭ. Несмотря на наличие прогрессирующей дыхательной недостаточности, выраженное увеличение концентрации гемоглобина наблюдается крайне редко. уменьшением всех легочных объемов в сочетании со снижением диффузионной способности легких (DLCO). Одним из ранних проявлений ИЛФ может быть изолированное снижение DLCO при относительной сохранности легочных объемов. Также к ранним проявлениям ИЛФ относят увеличение альвеолоартериального градиента по кислороду, что часто характеризуется нормальными показателями сатурации крови в покое и десатурацией при физической нагрузке [16].
Диагностический алгоритм
Диагноз ИЛФ основывается на отсутствии известных причин легочного фиброза и наличии картины обычной интерстициальной пневмонии (ОИП) [17]. Даже при наличии гистологической картины ОИП при хирургической биопсии легкого (ХБЛ) окончательный диагноз требует исключения других патологических состояний, ассоциированных с развитием ОИП, включая диффузные заболевания соединительной ткани, пневмокониозы, поражение легких, связанное с приемом лекарственных препаратов, семейный легочный фиброз [18]. При отсутствии данных за альтернативный диагноз, согласно действующим клиническим рекомендациям [4], диагноз ИЛФ устанавливают на основании характерных данных компьютерной томографии высокого разрешения (КТВР) и, при необходимости, результатов биопсии легкого (табл. 3). Следует отметить, что в представленной гистологической классификации выделены «возможный ИЛФ» и «вероятный ИЛФ», когда невозможно однозначно подтвердить или исключить наличие ИЛФ. В таком случае показана повторная оценка данных КТВР и биопсии легкого для уточнения диагноза.
| КТ-картина | Гистологические данные | Диагноз |
|---|---|---|
| ОИП | ОИП | ИЛФ |
| Вероятная ОИП | ||
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Возможная ОИП | ОИП Вероятная ОИП | ИЛФ |
| Возможная ОИП | Вероятный ИЛФ | |
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Не соответствует ОИП | ОИП | Возможный ИЛФ |
| Вероятная ОИП | Не-ИЛФ | |
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП |
КТ-диагностика
КТВР играет ключевую роль в диагностике ИЛФ и позволяет установить диагноз приблизительно в 2/3 случаев. В ряде исследований было показано, что КТ-картина типичной ОИП по данным КТВР согласуется с наличием гистологической картины типичной ОИП по данным биопсии легкого в 90-100% случаев [4]. Наличие достоверных КТ-признаков ОИП в настоящее время считают достаточным для диагностики ИЛФ без биопсии легкого. Проведение хирургической биопсии легкого (ХБЛ) рекомендуется при наличии КТ-картины, не типичной для ОИП. В таких случаях диагноз устанавливают на основании сочетания данных КТВР и гистологической картины (табл. 3). Таким образом, точная интерпретация данных КТВР является необходимым условием для постановки диагноза [1].
В настоящее время выделяют три КТ-варианта ОИП «типичная ОИП», которая исключает необходимость проведения ХБЛ, «возможная ОИП» и «не соответствует ОИП». При наличии последних двух вариантов требуется проведение ХБЛ [19].
КТ-картина типичной ОИП включает в себя преимущественно базальные и периферические ретикулярные изменения с образованием сотового легкого в сочетании с тракционными бронхоэктазами или без них. Критериями «сотового легкого» считают преимущественно субплевральные кисты диаметром 3-10 мм с четкими, относительно толстыми стенками (1-3 мм), расположенные слоями. Все КТ-признаки, рассматриваемые как «не соответствующие» ОИП, должны отсутствовать (рис. 1). Если все вышеуказанные критерии выполнены, данные КТВР достаточны для диагностики ОИП, а необходимости в проведения биопсии легкого нет [4]. Относительно признаков типичной ОИП заключения разных специалистов обычно хорошо согласуются [20,21]. Тем не менее, следует отметить, что ОИП и ИЛФ не являются синонимами, так как КТизменения, характерные для ОИП, могут отмечаться при ряде других заболеваний, прежде всего диффузных заболеваниях соединительной ткани.
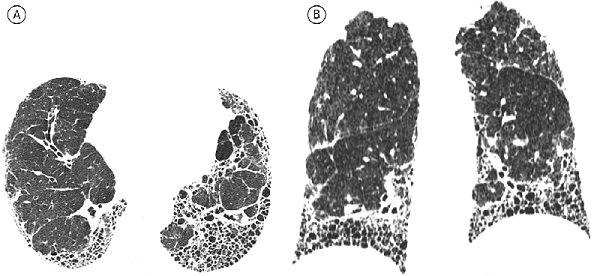
При возможной ОИП наблюдаются преимущественно базальные и периферические ретикулярные изменения без формирования зон сотового легкого. При этом изменения, не соответствующие ОИП, отсутствуют (рис. 2). Картина возможной ОИП менее специфична для ИЛФ, чем картина типичной ОИП. В данном случае дифференциальный диагноз следует проводить, в первую очередь, с неспецифической интерстициальной пневмонией (НСИП), для которой характерны отсутствие участков сотового легкого, преобладание затемнений по типу «матового стекла» над ретикулярными изменениями, относительная сохранность субплевральных зон. Участки сотовой трансформации редко встречаются при НСИП. В одном исследовании они были выявлены менее чем у 5% пациентов с идиопатической НСИП [23].
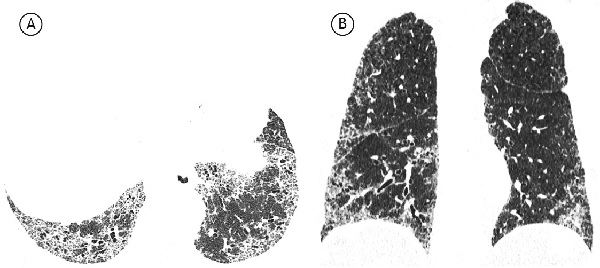
Изменения по данным КТВР, которые считают не соответствующими ОИП, включают в себя следующие: а) преобладание изменений в верхних и средних отделах легких; б) преимущественно перибронховаскулярные изменения; в) значительные по размеру зоны затемнения по типу «матового стекла», распростра ненность которых превышает таковую ретикулярных изменений; г) двусторонние очаговые изменения, преимущественно в верхних отделах легких; д) наличие кист (множественных, двусторонних) вне зон фиброза; е) картина мозаичного затемнения легочной ткани/ наличие «воздушных ловушек» (двусторонние изменения в трех и более долях); ж) наличие зон консолидации (рис. 3).
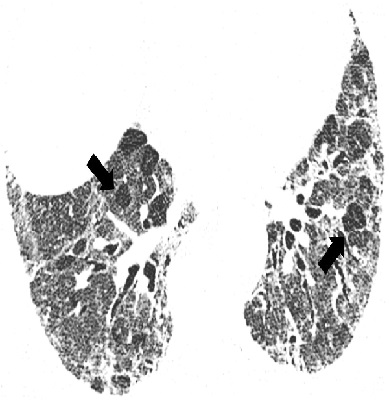
Несмотря на высокую вероятность наличия ИЛФ при типичной ОИП по данным КТВР, отсутствие зарактерной КТ-картины не должно служить основанием для исключения диагноза ИЛФ [22]. В 2017 г. D. Lynch и соавт. предложили новую КТ-классификацию ОИП, в которой впервые выделена группа неопределенной ОИП (табл. 4) [24].
| Типичная ОИП | Вероятная ОИП | Неопределенная ОИП | Наименее вероятно соответствует ОИП |
|---|---|---|---|
| Преобладание в базальных и субплевральных отделах (редко диффузные изменения); часто неоднородное распределение Зоны «сотового легкого»; ретикулярные изменения с периферическими тракционными бронхо эктазами и бронхиолоэктазами; отсутствие данных за альтернативный диагноз | Преобладание в базальных и субплевральных отделах; часто неоднородное распределение Ретикулярные изменения с периферическими тракционным бронхоэктазами и бронхиолоэктазами; отсутствие зон «сотового легкого»; отсутствие данных за альтернативный диагноз | Вариабельное или диффузное распределение Наличие фиброза в сочетании с небольшими по объему изменениями, не соответствующими ОИП | Преобладание в верхних и средних отделах легких; перибронховаскулярное распределение с относительной сохранностью субплевральных зон Любое из нижеперечисленного: преобладание зон консолидации; значительные по размеру зоны затемнения по типу «матового стекла» (при отсутствии обострения ИЛФ); диффузные очаговые или кистозные изменения; выраженное мозаичное затемнение легочной ткани с наличием «воздушных ловушек» |
Клиническое течение ИЛФ может быть различным. У большинства пациентов отмечается медленно прогрессирующее течение, однако у некоторых пациентов происходит стабилизация патологического процесса, тогда как у других отмечается довольно быстрое прогрессирование заболевания. Что касается выраженности легочных изменений по данным КТВР, то зоны затемнения по типу «матового стекла» чаще всего трансформируются в ретикулярные изменения, которые, в свою очередь, могут прогрессировать и формировать зоны «сотового легкого», размер которых со временем обычно увеличивается. Следует отметить, что общий паттерн легочных изменений также может изменяться: так, КТкартина возможной ОИП может трансформироваться в типичную ОИП [22].
Биопсия легкого
Если однозначные данные о наличии ИЛФ при КТВР отсутствуют, то для подтверждения диагноза показано выполнение хирургической биопсии легких, которую чаще проводят с помощью видеоторакоскопической методики. С целью повышение эффективности биопсия легких должна производиться из разных долей легких. Хотя ХБЛ является наиболее достоверным методом определения гистологической картины ИИП, ее проведение связано с риском возникновения ряда осложнений, наиболее тяжелым из которых является обострение ИЛФ, особенно у пациентов с тяжелой дыхательной и/или сердечной недостаточностью [25]. В связи с этим решение о ее проведении должно приниматься индивидуально с учетом клинической картины, возможных преимуществ для постановки точного диагноза, а также согласия пациента.
В течение последнего десятилетия для гистологического подтверждения диагноза ИЛФ и других вариантов ИИП разработана методика трансбронхиальной криобиопсии легкого (ТБКБЛ). Ее основными преимуществами являются малоинвазивность, отсутствие необходимости в проведении интубации и ингаляционного наркоза и, вследствие этого, низкая частота развития осложнений в сочетании с возможностью получения большого по объему биоптата легкого, достаточного, в абсолютном большинстве случаев, для гистологической верификации диагноза [26]. Так, у пациентов без типичной картины ОИП по данным КТВР проведение ТБКБЛ позволяло установить диагноз приблизительно в 2/3 случаев, что сопоставимо с эффективностью ХБЛ в сходной ситуации [27]. При этом для ТБКБЛ характерны более низкий риск периоперационных осложнений (чаще всего отмечают развитие пневмоторакса и не угрожающего жизни кровотечения в месте проведения биопсии) и смерти, более короткий период госпитализации, что позволяет проводить ТБКБЛ у пациентов с высоким уровнем анестезиологического риска и наличием противопоказаний к ХБЛ [28].Таким образом, внедрение ТБКБЛ в клиническую практику может расширить показания к биопсии легкого и повысить диагностическую точность алгоритма обследования пациентов с подозрением на ИЛФ.
При морфологическом исследовании у пациентов с подозрением на ИЛФ G. Raghu и соавт. выделяют пять возможных гистологических паттернов заболевания (табл. 5) [29,4]. В сочетании с рентгенологическими данными они используются для подтверждения/исключения диагноза ИЛФ (табл. 3) [4,30].
Дифференциальный диагноз
У пациентов с подозрением на ИЛФ должен проводиться тщательный дифференциальный диагноз. При выявлении КТ-картины, соответствующей вероятной или возможной ОИП, что происходит довольно часто, в круг дифференциального диагноза следует включать, в первую очередь, хронический экзогенный аллергический альвеолит и фибротический вариант НСИП. Тем не менее, у части пациентов рекомендованная в данном случае ХБЛ не проводится в связи с наличием противопоказаний (тяжелой дыхательной недостаточности, сопутствующих заболеваний, возрастных ограничений) или нежеланием пациента.
При проведении дифференциального диагноза важно также исключить поражение легких в рамках системного заболевания соединительной ткани, в частности, ревматоидного артрита, системной склеродермии, дерматомиозита, синдрома Шегрена [31], в том числе при наличии КТ-картины типичной ОИП. При наличии у пациента отдельных клинических проявлений или повышения уровня лабораторных аутоиммунных маркеров, не соответствующих конкретному системному заболеванию соединительной ткани, может быть установлен диагноз интерстициальной пневмонии с аутоиммунными чертами [32].
Генетические маркеры ИЛФ
В настоящее время выявлен ряд мутаций и полиморфизмов генов, участвующих в ремоделировании легочной ткани и регуляции врожденного и приобретенного иммунитета, ассоциированных с развитием ИЛФ [33]. К ним относятся, в частности, мутации в генах, кодирующих сурфактантные протеины А и D (S):1–112. P-A и S):1–112. PD), описанные при семейных формах ИЛФ [34]. В ряде исследований выявлена ассоциация генетических полиморфизмов с прогнозом заболевания: в частности, наличие отдельных однонуклеотидных полиморфизмов в гене TLR-3 (Toll-подобный рецептор 3-го типа) ассоциировано с более быстрым прогрессированием заболевания [35]. Также при ИЛФ описан ряд полиморфизмов в генах муцина 5B (MUC5B) и TOLLIP (протеин, взаимодействующий с Toll-подобным рецептором) [36]. Хотя исследование генетических полиморфизмов не является частью диагностического алгоритма при ИЛФ, продолжается поиск генетических маркеров, способных служить предикторами различных вариантов течения заболевания и ответа на терапию.
Обострение ИЛФ
Обострение ИЛФ – это тяжелое жизнеугрожающее состояние, проявляющееся в виде быстрого нарастания дыхательной недостаточности у пациентов с ранее установленным диагнозом ИЛФ [37]. Как правило, характеризуется крайне тяжелым течением; смертность в ряде исследований достигала 85% [38]. В отличие от стабильного или медленно прогрессирующего течения ИЛФ, критерии диагностики его обострения определены менее четко. Согласно данным Н. Collard и соавт. [39], критерии обострения ИЛФ включают в себя наличие предшествующего или впервые выявленного ИЛФ с резким нарастанием одышки, развитием дыхательной недостаточности за предшествующие 30 дней без установленной причины, а также появление новых зон затемнения легочной ткани по типу «матового стекла» и/или консолидации на фоне имевшихся ранее изменений, соответствующих ОИП – зон ретикулярных изменений и «сотового легкого» (рис. 4) [40]. Тем не менее, вышеуказанные критерии обладают низкой специфичностью, в связи с чем при подозрении на обострение ИЛФ должен проводиться дифференциальный диагноз с инфекционным процессом, тромбоэмболией легочной артерии и ее ветвей, пневмотораксом, а также острой левожелудочковой недостаточностью с развитием отека легких [41].
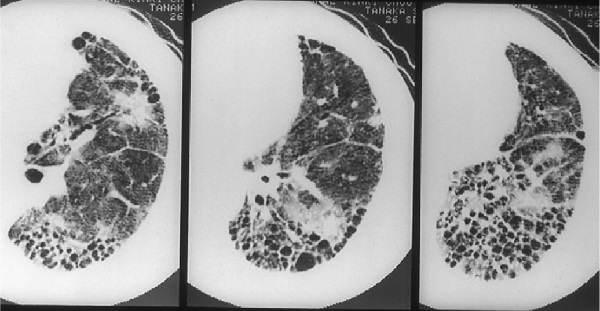
Заключение
Появление новых методов лечения, в частности, антифибротических препаратов, и неэффективность традиционной иммуносупрессивной терапии при ИЛФ подчеркивают важность как можно более ранней постановки диагноза и начала терапии. В течение последнего десятилетия был достигнут значительный прогресс в разработке диагностических алгоритмов для пациентов с ИЛФ. Этому способствовало повышение качества визуализационных методов, более полное понимание роли биопсии легких и разработка гистологических критериев ИЛФ. Все вышеперечисленные параметры должны исследоваться мультидисциплинарной командой специалистов, что в настоящий момент является стандартом диагностики ИЛФ. Несмотря на достигнутые успехи, в диагностике ИЛФ остаются нерешенные вопросы, в основном касающиеся применения инвазивных методов диагностики, в частности, хирургической биопсии легкого. Необходимо продолжать поиск молекулярно-биологических и генетических маркеров ИЛФ и разработку малоинвазивных биопсийных методов для максимально раннего установления диагноза, определения прогноза и разработки стратегии терапии ИЛФ.
Идиопатические интерстициальные пневмонии: клиника, диагностика, лечение
Достижения молекулярной биологии и внедрение в медицину новых методов обследования, в значительной степени коснувшееся респираторной медицины, во многом изменили представления о сути болезней, связанных с поражением легочного интерстиция. На современном
Достижения молекулярной биологии и внедрение в медицину новых методов обследования, в значительной степени коснувшееся респираторной медицины, во многом изменили представления о сути болезней, связанных с поражением легочного интерстиция. На современном этапе в группу интерстициальных болезней легких объединены более 200 острых и хронических заболеваний, характеризующихся повреждением, воспалительными и фибропролиферативными реакциями, затрагивающими аэрогематический барьер. Эти заболевания представляют большие трудности для диагностики, так как нередко их трудно отличить на основании рентгенологических проявлений от болезней легких бактериальной природы, и в особенности от пневмоний или туберкулеза. Ошибочное назначение антибиотиков может становиться причиной побочных реакций, являющихся, по сути, ятрогенными, и тем самым ухудшает прогноз.
Особое внимание специалистов, занимающихся проблемами пульмонологии, привлекают те формы интерстициальных болезней легких, этиология которых остается неустановленной. К ним относятся идиопатические интерстициальные пневмонии (ИИП), отличающиеся тяжестью течения и неблагоприятным прогнозом вследствие необратимо прогрессирующих процессов фиброзной перестройки легкого. Значительные успехи отечественной и зарубежной пульмонологии не привели к снижению частоты заболевших ИИП, при большинстве из которых пациент на поздней стадии болезни нуждается в постоянной респираторной поддержке вследствие необратимой потери легочных функций. Напротив, согласно данным исследований, проводившихся в Европе, Англии и США, за период с 1995 по 2003 г. показатели заболеваемости ИИП многократно выросли: в среднем, в зависимости от страны, от 7 до 50 случаев на 100 000 человек. Так как у большинства больных ИИП приводят к снижению качества жизни и инвалидизации, а стационарно-диспансерное ведение пациентов обязательно предусматривает использование дорогостоящих лечебно-диагностических мероприятий, то прямые и непрямые медицинские расходы, обусловленные преждевременной смертностью от ИИП, уже сегодня могут представлять значительный экономический и социальный ущерб.
Существующий разрыв между интенсивно обогащающимися знаниями о механизмах развития ИИП и неудачами в их диагностике и лечении определяется отсутствием единого представления о нозологической принадлежности заболеваний. Хотя к группе ИИП отнесены семь типов морфологических изменений, нозологическую принадлежность получила только обычная интерстициальная пневмония. Это заболевание именуется идиопатическим легочным фиброзом (ИЛФ) и отличается от других тяжелым течением и очаговой фибропролиферацией в легких с быстрым прогрессированием пневмосклероза в виде формирования на поздней стадии «сотового легкого». Замечено, что идиопатический легочный фиброз чаще развивается у мужчин пожилого возраста, тогда как остальные формы ИИП диагностируются в основном у женщин. Кроме того, среди больных ИИП нередко встречаются курящие или курившие ранее лица. Однако необходимо признать, что особенности клиники ИИП по-прежнему недостаточно хорошо изучены и выделение их производится главным образом на основе «патогенетического своеобразия форм» (И. В. Давыдовский).
Таким образом, на сегодняшний день к группе ИИП можно отнести:
Какие бы мнения ни существовали относительно классификации ИИП, данный вопрос не столь уж важен с практической точки зрения, поскольку эти тяжелые, характеризующиеся неблагоприятным прогнозом болезни, мало изучены. Диагностические и терапевтические подходы к ведению таких больных до сих пор во многом неясны. Большинство работ, посвященных проблеме идиопатического фиброзирующего альвеолита, являются преимущественно морфологическими и основаны лишь на небольшом клиническом материале.
Наиболее действенным подходом к диагностике ИИП становится клиническая интерпретация фактов, полученных в результате обследования больного, начиная с тщательного сбора анамнеза, выявления возможных факторов риска поражения легких, физического обследования и вплоть до применения таких высокотехнологичных современных методов исследования, как компьютерная томография легких высокого разрешения (КТВР) и биопсия легкого.
Клинически ИИП, как и другие формы интерстициальных заболеваний, характеризуется малопродуктивным кашлем, прогрессирующей одышкой, которую большинство больных описывают как чувство «неполного вдоха» и даже рукой могут указывать на область «преграды» — на уровне диафрагмы. Нередко пациенты просыпаются ночью от внезапного чувства нехватки воздуха или ощущения «плиты на груди». Последние симптомы, по-видимому, обусловлены срывом адаптации хеморецепторов респираторного центра к нарастающей гипоксии в условиях нарушения диффузионной способности легких и появлением эпизодов апноэ. Именно одышка, ограничивающая повседневную активность больных и снижающая качество жизни при ИИП, становится главной причиной обращения к врачу. При осмотре у таких больных отмечаются цианоз, постепенно распространяющийся на кожных покровах по мере усугубления гипоксии и гипоксемии, изменение концевых фаланг пальцев и ногтей в виде «барабанных палочек» и «часовых стекол» («пальцы Гиппократа»).
Потеря респираторных функций, наблюдаемая у большинства пациентов с ИИП, сопровождается появлением типичного аускультативного феномена — нежной крепитации. Именно крепитацию можно расценивать как наиболее достоверный клинический ориентир, указывающий на вовлечение легочного интерстиция. При ИИП крепитация имеет свои особенности: на ранней стадии выслушивается симметрично преимущественно над базальными отделами легких и по мере прогрессирования болезни распространяется постепенно на все легочные поля вплоть до верхушек легких. Грубая крепитация, выслушиваемая над ограниченными участками легких, исчезающая при глубоком дыхании и особенно сопровождающаяся хрипами, в большей степени относится к дыхательным шумам, возникающим в старческом легком, при пневмосклерозе в исходе хронической обструктивной болезни легких либо при инфекционных поражениях легких, в том числе и банальной пневмонии.
В лабораторных показателях у больных ИИП, в особенности когда речь идет о варианте, морфологически представленном обычной интерстициальной пневмонией — ИЛФ, нередко отсутствуют выраженные сдвиги показателей иммунитета. Хотя и обнаруживается некоторое повышение уровня иммуноглобулинов, циркулирующих иммунных комплексов, СОЭ нередко сохраняется на уровне, близком к норме, что можно объяснить полицитемией у больных на стадии «сотового легкого» в условиях формирования легочного сердца. При этом низкая активность таких маркеров иммунного воспаления, как γ-глобулины, IgG, при ИЛФ позволяет предполагать патогенетические особенности последнего, заключающиеся в преобладании процессов фиброзирования над воспалением. Полученные данные согласуются с современными представлениями об обычной интерстициальной пневмонии как о заболевании с генетически детерминированным нарушением экспрессии профиброгенных факторов, определяющих изначально высокую активность субпопуляций клеток с профиброгенным фенотипом, интенсивно синтезирующих факторы роста, что приводит к быстрому накоплению экстрацеллюлярного матрикса на стадии «сотового легкого». При других формах ИИП, например десквамативной интерстициальной пневмонии, наоборот, гуморальные сдвиги имеют циклический характер, обнаруживаются при обострении заболевания и сопровождаются повышением активности интерстициального воспаления — альвеолита.
При ИИП в целом наблюдается значительное снижение показателей жизненной емкости легких (ЖЕЛ), фиксированной жизненной емкости легких (ФЖЕЛ) и диффузионной способности легких (DLCO), тогда как объем форсированного выдоха за 1 с (ОФВ1) и индекс Тиффно могут и не меняться. Такое распределение параметров функции внешнего дыхания (ФВД) соответствует нарушениям преимущественно рестриктивного типа. При обычной интерстициальной пневмонии (ИЛФ) тяжесть дыхательных расстройств отличается от других форм ИИП резким и крайне резким снижением ЖЕЛ, ФЖЕЛ. Причем степень снижения показателей ФВД и диффузионной способности легких, как подтверждают наши работы и наблюдения других авторов, не зависят от длительности болезни. Тяжелая дыхательная недостаточность с признаками легочного сердца может развиться за период от 2 мес до 2 лет. При десквамативной ИИП наблюдается более благоприятное хроническое течение — до 10–13 лет.
Высокой прогностической ценностью обладает ФЖЕЛ, снижение которой более чем на 67% от нормы было связано с более низкими показателями выживаемости. Быстрое снижение показателей ФВД в течение 6-месячного периода коррелирует при различных вариантах ИИП с неблагоприятным прогнозом (r = 21,43; p = 0,03). DLCO также рассматривается как эквивалент адекватного функционирования аэрогематического барьера, с одной стороны, и как показатель морфологической активности альвеолита — с другой. Выраженное снижение DLCO — до 30% от нормы, даже при удовлетворительном уровне ЖЕЛ, а также динамическое снижение DLCO в течение года на 20% по сравнению с первоначальным уровнем сопровождается значительной потерей ФЖЕЛ и увеличением смертности больных.
Особо следует отметить значение бронхиальной обструкции, клинические признаки которой отмечаются практически у 30% больных ИИП. Чаще бронхиальная обструкция наблюдается при десквамативной интерстициальной пневмонии в период обострения заболевания, тогда как при обычной интерстициальной пневмонии она встречается значительно реже — только у 4 % пациентов.
 |
| Рисунок 1. Больной П., 54 года, диагноз — ИЛФ; для подтверждения диагноза проведена торакоскопическая биопсия легкого (результаты морфологического исследования — обычная интерстициальная пневмония). На КТ — участки кистозно-фиброзной трансформации («сотовое легкое») |
Наиболее информативным методом диагностики и мониторирования течения ИИП является компьютерная томография легких. Использование КТ-методов, в том числе с программами высокого разрешения, позволяет не только подтвердить, что изменения в легких обусловлены ИИП, но и ориентировочно предположить, что речь идет о морфологическом варианте заболевания. Типичным признаком для ИИП являются симптомы «матового стекла» и кистозно-фиброзные структуры («сотовые легкие») (рис. 1, 2).
При прогнозировании течения ИИП особое значение придают легочной гипертензии, присоединение которой повышает риск формирования легочного сердца и связанных с ним осложнений. Следует подчеркнуть, что поражение сердца и сосудов малого круга кровообращения при ИИП по клиническим и молекулярно-биологическим проявлениям во многом напоминает первичную легочную гипертензию. Вовлечение сердца при ИИП можно заподозрить уже при обычном физическом обследовании — акцент и расщепление II тона на легочной артерии, расширение сердечной тупости и смещение границ сердца вправо. Показано, что при ИИП КТВР-критерии, свидетельствующие о легочной гипертензии, опережают ЭхоКГ-признаки гемодинамических нарушений в малом круге кровообращения, так как последние появляются только при относительно высоких показателях площади кистозно-буллезной трансформации в легких (более 32,1 ± 5,1%). Установление компьютерно-томографических эквивалентов активности интерстициальной воспалительной реакции (альвеолита) и фиброза необходимо для определения стадии, прогноза и лечения идиопатического фиброзирующего альвеолита.
 |
| Рисунок 2. Больной М., 45 лет, идиопатическая интерстициальная пневмония (морфологический вариант — десквамативная интерстициальная пневмония). На КТ — «матовое стекло», фиброз |
Вне зависимости от варианта течения ИИП, развернутая картина болезни с тяжелой легочно-сердечной недостаточностью появляется только на стадии «сотового легкого». Учитывая известные представления о «сотовом легком» как о результате нарушений сложных процессов репарации ткани (wound-healing), влекущих за собой смену функциональной активности клеток с появлением клеточных субпопуляций, которые несут опухолевый генотип, развитие «сотового легкого» может расцениваться как стадия, неблагоприятная по прогнозу в первую очередь из-за риска возникновения рака легкого. Кроме того, «сотовое легкое» как рентгено-морфологический эквивалент необратимой потери респираторной функции легких, когда достижение удовлетворительной коррекции дыхательной недостаточности даже при использовании новейших методик респираторной поддержки остается практически невозможным, определяет отношение в поздней стадии ИИП как к неблагоприятному исходу, тем более что трансплантация легких остается для больных ИИП единственным кардинальным методом лечения, сложность исполнения которого не позволяет пока оправдать возложенные на него надежды.
Для определения степени риска неблагоприятного прогноза у больных идиопатическим фиброзирующим альвеолитом нами был проведен факторный анализ взаимосвязи клинических, функциональных, морфологических изменений, влияющих на развитие «сотового легкого» (табл. 2). В целом по группе обследованных больных пол и возраст значимого влияния на прогноз не оказывали. Наиболее высокой прогностической ценностью характеризовались рентгено-морфологические критерии активности ИИП. Основными, связанными с формированием «сотового легкого», были КТВР-показатели площади фиброза на ранней стадии болезни (χ 2 = 7,73; р 2 = 28,4; р = 0,00001).
У больных с обширными полями «матового стекла» риск неблагоприятного прогноза невысок. Достоверная взаимосвязь между риском формирования «сотового легкого» и индексом гистологической активности интерстициального воспаления отсутствует (χ 2 = 0,20; р = 0,88). Действительно, симптом «матового стекла» как эквивалент гистологической активности воспаления в легочном интерстиции наиболее часто выявляется при относительно благоприятных формах ИИП, например десквамативной интерстициальной пневмонии. При этом длительно сохраняющийся, несмотря на проводимое лечение, симптом «матового стекла» (даже при небольшой его площади) в сочетании с приростом площади интерстициального фиброза и — как выражение крайней его степени — кистозно-буллезной трансформацией достоверно связан с неблагоприятным прогнозом (χ 2 = 4,81; р = 0,049). Наиболее часто такая зависимость отмечается при обычной интерстициальной пневмонии. У больных с хорошим ответом на терапию, т. е. с уменьшением в результате лечения на КТВР площади «матового стекла» и отсутствием прироста площади фиброза, развернутая картина «сотового легкого» формируется существенно реже.
Успех диагностики и лечения ИИП зависит от правильной организации лечебно-диагностического процесса. Рекомендации ERS/ATS по ведению больных ИИП предусматривают тесное сотрудничество пульмонолога, рентгенолога, морфолога и торакального хирурга. Эффективность терапии определяется через 3 мес от начала лечения на основании стационарного обследования больного и сравнения результатов КТ, оценкой функциональной способности легких. Критерием эффективности терапии считается снижение площади «матового стекла» и отсутствие новых участков образования «сотовых структур». Обязательная программа обучения пациентов включает разъяснение причин заболевания, правил профилактики вредных воздействий (профессиональные факторы, воздействия внешней среды, пассивное курение).
Несмотря на существующие сегодня представления об ИИП как об изначально тяжелом заболевании с неблагоприятным прогнозом, клиницисты воздерживаются от назначения лечения, в особенности при малосимптомном течении болезни. По данным Британского торакального общества, в 64% случаев врачи не начинают лечение ИИП у больных со стертой клинической картиной, при стабильном течении ИИП, реже причинами отказа от назначения терапии являются угроза побочных эффектов, коморбидные состояния, пожилой возраст, а также развернутая стадия болезни («сотовое легкое»). С нашей точки зрения, такую позицию нельзя считать оправданной, хотя последствия иммуносупрессивного лечения действительно в ряде случаев по тяжести вызываемых им расстройств оказываются сопоставимы с нарушениями, связанными с основным заболеванием. Как показывает опыт, даже при медленно прогрессирующих формах ИИП в легких развиваются необратимые склеротические изменения, и на этой стадии запоздалая терапия уже малоэффективна.
ИИП относится к заболеваниям, при котором ни одно из известных лекарственных средств не позволяет предупредить снижение функции легких в долговременной перспективе. Во многом это определяется гетерогенностью морфологических изменений при ИИП. Вот почему, назначая терапию идиопатического фиброзирующего альвеолита, необходимо учитывать прежде всего патоморфологический вариант болезни. Известно, что при таких вариантах ИИП, как десквамативная интерстициальная пневмония, неспецифическая интерстициальная пневмония, наблюдается хороший или удовлетворительный ответ на кортикостероидную терапию. При этом кортикостероиды назначаются на длительные сроки, в том числе и в режиме высоких доз. В то же время при ИЛФ, представляющем собой заболевание с интенсивной фибропролиферацией, традиционно используемые иммуносупрессивные препараты, как удалось показать в ходе большинства проведенных сравнительных рандомизированных исследований, практически не влияют на выживаемость больных. Рекомендуемая первоначальная доза кортикостероидных препаратов у больных с различными вариантами ИИП колеблется от 0,5 до 1,0 мг/кг, максимальная — 60 мг для ежедневного перорального приема. Назначение кортикостероидов по альтернативным схемам (через день) не оправдано и по сравнению с другими программами лечения не имеет преимуществ по критериям выживаемости или терапевтической эффективности.
Опираясь на собственный опыт лечения больных ИИП, мы применяем методику сочетания высоких доз метилпреднизолона в течение 2 первых недель лечения (до 3 г в неделю, т. е. 800 или 1000 мг на одно введение) с умеренными или даже низкими пероральными дозами (не более 0,25 мг/кг). В дальнейшем такие «пульсовые» введения следует проводить в режиме 1000 мг в неделю в сочетании с прежней пероральной дозой.
У больных с идиопатическим фиброзирующим альвеолитом, получающих преднизолон, необходим контроль туберкулиновых проб для своевременного выявления возможных вторичных инфекций. Назначения фторхинолонов или триметоприма до 3 г в неделю достаточно для достижения необходимого туберкулостатического эффекта и профилактики Pneumocystis carinii. Прекращение приема кортикостероидов необходимо при выраженных побочных эффектах.
При прогрессировании фибропластических изменений в легких целесообразно ограничиться низкими дозами кортикостероидов и сделать выбор в пользу препаратов, препятствующих избыточному накоплению экстрацеллюлярного матрикса (колхицин, азатиоприн, метатрексат, циклофосфан, циклоспорин). Однако даже агрессивная цитостатическая терапия также не всегда позволяет замедлить темпы прогрессирования легочного фиброза. Следует учитывать и высокий риск нежелательных реакций, вызываемых иммуносупрессивными препаратами. Другой возможной мишенью для лечения ИИП является легочное сосудистое русло. Представление об ИИП как о заболевании, связанном с тяжелыми изменениями функциональной активности эндотелия, обосновывает применение препаратов, напрямую или опосредованно контролирующих вазоактивные факторы. Среди них особо следует указать ингибиторы эндотелина 1, антифиброгенные влияния которого убедительно доказаны экспериментальным путем. Недавно начатые многоцентровые, плацебо-контролируемые, рандомизированные исследования по применению ингибитора эндотелина-1 (бозентана) при ИЛФ (BUILD-1) и вторичном легочном фиброзе вследствие системной склеродермии (BUILD-2) уже на доклинических этапах показали нарастание легочных функций у больных в тестах с нагрузкой. Если принципы использования препаратов, регулирующих функциональную активность эндотелия при идиопатическом фиброзирующем альвеолите, находятся на стадии разработки, а результаты часто оказываются противоречивыми из-за кратковременного эффекта простаноидов, то внедрение в процессы повреждения эпителия, и в том числе взаимоотношений эпителий–фибробласт, рассматривается как реальный способ проведения длительной терапии, направленной на замедление темпов прогрессирования пневмосклероза.
Одно из направлений этой терапии — применение антиоксидантов в высоких дозах у больных ИИП — считается перспективным. Положительное влияние антиоксидантов, в частности α-токоферола, на функции легких убедительно доказано при различных формах интерстициальных болезней легких, и прежде всего при гранулематозах (саркоидозе). По нашим данным, курсовое введение больным с десквамативной интерстициальной пневмонией и облитерирующим бронхиолитом α-липоевой (тиоктовой) кислоты увеличивало показатели нагрузочных проб (6-минутный тест с ходьбой), а также способствовало поддержанию толерантности к глюкозе, позволяя тем самым достичь органосберегающих эффектов, что имеет особое значение для больных, длительно получающих кортикостероидную терапию.
Между тем современные подходы к лечению ИИП, каким бы успешным оно ни казалось, остаются патогенетическими. Причины развития ИИП по-прежнему до конца не раскрыты, поэтому поиск доказательств, указывающих на тот или иной «стимул», запускающий фибропролиферативные и воспалительные процессы в легких, следует считать наиболее важным направлением в построении лечебной стратегии заболевания.
Литература
Е. Н. Попова, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва



