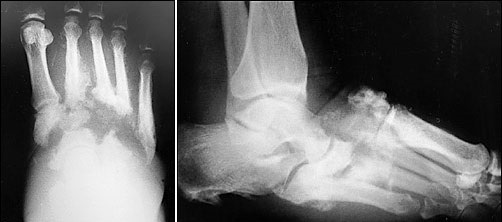
Стопа Шарко
Заболевания
Операции и манипуляции
Истории пациентов
Стопа Шарко
Описание
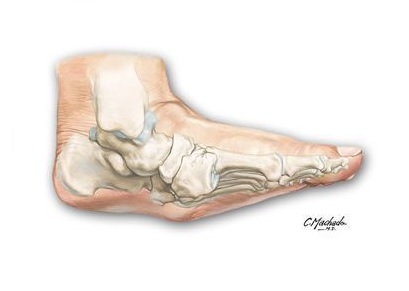
Стопа Шарко, так же известная как артропатия Шарко – синдром, часто встречаемый у больных со сниженной или утерянной чувствительностью в стопе. Он характеризуется переломами и вывихами костей предплюсны с формированием крайне нестабильной и не опороспособной стопы. Наиболее частой причиной снижения чувствительности (нейропатии) стопы является сахарный диабет, также споровождающийся повреждением мелких артерий, что только усугубляет течение заболевания. Другими причинами нейропатии могут быть поражения спинного мозга, поражения периферических нервов в следствие травмы, алкоголизм, сифилис, лепра, наследственные дегенеративные заболевания нервной системы. У диабетиков стопа Шарко развивается чаще всего после 10-20 лет с момента постановки диагноза. У диабетиков стопа Шарко развивается чаще всего после 10-20 лет с момента постановки диагноза. Jean Martin Charcot – французский терапевт, был первым, кто в 1868 году описал нейропатическую артропатию у пациента со спинной сухоткой – третичным сифилисом.
Стопа Шарко характеризуется переломами и вывихами костей предплюсны с формированием крайне нестабильной и не опороспособной стопы. Наиболее частой причиной снижения чувствительности (нейропатии) стопы является сахарный диабет, также споровождающийся повреждением мелких артерий, что только усугубляет течение заболевания. Другими причинами нейропатии могут быть поражения спинного мозга, поражения периферических нервов в следствие травмы, алкоголизм, сифилис, лепра, наследственные дегенеративные заболевания нервной системы.
История
Jean Martin Charcot – французский терапевт, был первым, кто в 1868 году описал нейропатическую артропатию у пациента со спинной сухоткой – третичным сифилисом.
Причины развития стопы Шарко
Нейропатия и нарушение микроциркуляции формирующиеся у пациентов длительное время страдающих сахарным диабетом, лепрой, сифилосом, полиомиелитом, алкоголизмом, сирингомиелией предрасполагают к нарушению обмена веществ в тканях нижних конечностей, вызывают резорбцию костной ткани, снижают регенераторный потенциал. Также нейропатия приводит к тому что кости и связки более не могут адекватно воспринимать направление сил сжатия и растяжения которые в норме контролируют и регулируют их рост. Это приводит к повторяющимся микротравмам, переломам и вывихам. Стопа Шарко наиболее часто может включать в себя средний отдел стопы, более редко задний отдел стопы, голеностопный сустав, ещё реже пяточную кость и передний отдел стопы.
Симптомы стопы Шарко.
Существует три основные стадии стопы Шарко.
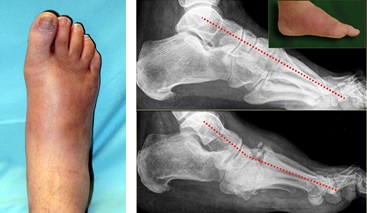
Первая стадия заклоючаетсая во фрагментации и деструкции костей среднего отдела стопы. В ряде случаев может произойти полный лизис костей среднего отдела стопы с абсолютно нестабильным передним отделом. Эта стадия сопровождается выраженным отёком, гиперемией вовлеченной области. По этой причине стопа Шарко часто дифференцируется с инфекцией и переломами. Из-за появившейся нестабильности стопа начинает деформироваться. Чаще всего формируется плосковальгусная деформация стопы. На этой стадии лечение направлено на максимальное снижение деструкции костной ткани и предупреждение грубой деформации. Первая стадия занимает от 6 до 12 месяцев.
Вторая стадия – подострая или стадия коалесценции. Во время этой фазы стопа Шарко характеризуется замедлением процессов деструкции. Отёк и гиперемия спадают, боли уменьшаются. Оставшиеся кости стремятся консолидироваться в один блок.
Третья стадия – хроническая или реконструкции\консолидации. Если деформация которая сформировалась во второй стадии не обеспечивает стабильности опоры при ходьбе рано или поздно адаптивные возможности исчерпываются. Отёк и гиперемия возвращаются, стопа продолжает деформироваться. На этой стадии часто присоединяется инфекция так как на стопе формируются совершенно иные, ненормальные точки опоры.
Диагностика
Часто стопа Шарко диагностируется через несколько недель или даже месяцев после начала симптоматики. Не редки случаи когда пациент обращается за помощью уже на второй или третьей стадии заболевания. Время обращения далеко не всегда влияет на результат так как степень резорбции костной ткани и нестабильности не контролируется лечением.
Стадия 0 (начало заболевания)
Стадия 1 (деструкции)
Стадия 2 (коалесценции)
Стадия 3 (ремоделирования)
Нормальные рентгенограммы, на МРТ виден отёк костного мозга и стрессовые переломы
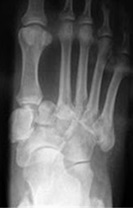
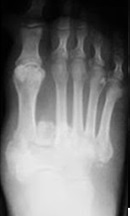
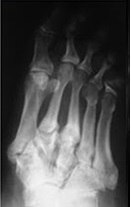
На рентгенограммах видно субхондральную фрагментацию костей, подвывихи, вывихи, стрессовые переломы, деформацию, формирование периартикулярного дебриса.
На рентгенограммах видно формирование костной мозоли, остеосклероз, сращение костных фрагментов и деформацию.
Края костных фрагментов закругляются, становятся более гладкими, плотность костной ткани снижается, приводя к коллапсу суставов и формированию фиброзного анкилоза и усугублению деформации.
Гиперемия, отёк, отсутствие деформации.
Гиперемия и отёк усиливается, появляется боль и деформация.
Прогрессирование деформации и нестабильности, уменьшение отёка и гиперемии.
Дальнейшее прогрессирование деформаци, уменьшение нестабильности, с формированием тугоподвижной сильно деформированной стопы.
Важно не допустить формирования значительной деформации которую будет сложно устранить во второй фазе заболевания. Первые рентгенограммы могут быть нормальными, но в течение нескольких недель формируется грубо выраженный остеопороз и начинается рассасывание костей, чаще всего среднего отдела стопы, что хорошо видно на динамических рентгенограммах.
Лечение
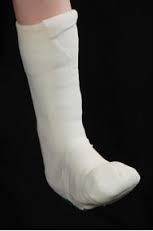
После установки правильного диагноза (чаще всего в первой фазе заболевания) лечение сначала направлено на контроль боли, отёка и гиперемии. Вторым важным аспектом является поддержка и стабилизация стопы для предотвращения деформации. Одним из наиболее эффективных видов лечения на этой стадии является полноконтактный гипс.
Гипс накладывается на всю стопу полностью с закрытием пальцев чтобы предотвратить их травматизацию и попадание внутрь посторонних объектов. Вначале потребуется менять гипс регулярно по мере спадения отёка, каждые 4-7 дней, после полного спадения отёка можно увеличить срок между перегипсовками до 2-4 недель. Ношение гипсовой повязки может потребоваться на протяжении всей первой фазы заболевания, то есть 6-12 месяцев. Для пациента это довольно сложный в психологическом плане период, так как требуются постоянные визиты к врачу, но необходимо объяснить ему что по другому с этой проблемой не справиться. После окончания первой фазы если стопа стабилизировалась в удовлетворительном положении изготавливается ортопедическая обувь и индивидуальные ортопедические стельки, также может быть показано ношение полужёсткого ортеза для стабилизации голеностопного сустава.
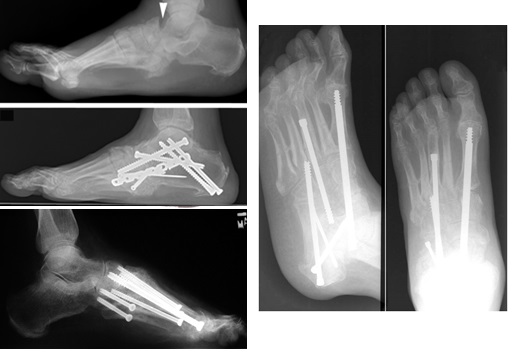
В случае если деформация всё же сильно выражена, или присутствует выраженная нестабильность – показано оперативное лечение. Наиболее часто применяются остеотомии с артродезом.
В случае если вы имеете дело со стопой Шарко лучше использовать более мощные и надежные фиксаторы, так как порозная кость дает плохую опору и миграция металлофиксаторов не редкость. Предпочтительно оперировать во второй фазе заболевания когда риск несращения и формирования ложного сустава ниже, но иногда приходиться оперировать и на первой и третьей фазах болезни.
После оперативного лечения также требуются ортопедическая обувь и индивидуальные ортопедические стельки. Необходимо регулярно посещать врача, так как рецидивы заболевания не редкость.
Осложнения стопы Шарко.
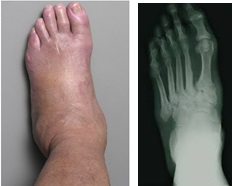
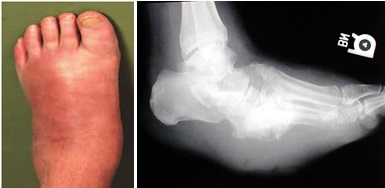
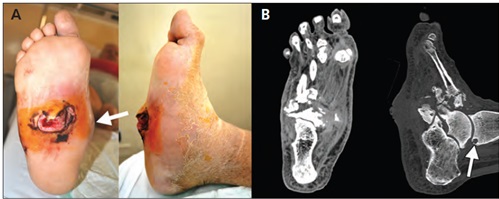
В тяжёлых случаях происходит полный лизис костей среднего отдела стопы, стопа принимает бобовидную форму, и в средней части подошвы формируется язва.
Нагноение язв, глубокая инфекция и остеомиелит часто приводят к необходимости ампутации у не леченных больных.
Часто задаваемые вопросы.
Почему диагноз стопа Шарко часто ставится через несколько недель\месяцев от начала заболевания?
— Первые признаки стопы Шарко это отёк и покраснение, также характерны для других более частых заболеваний таких как инфекция и ревматологическая артропатия, подагрическая артропатия. По этой причине врач общей практики наиболее вероятно заподозрит именно их. Многие пациенты не испытывают сильной боли на начальных этапах заболевания и поздно обращаются к врачу. Часть пациентов наоборот уже испытывали боль ещё до появления других симптомов из-за нейропатии, и не замечают других изменений.
Насколько поздняя диагностика ухудшает прогноз?
— Только в случае если у пациента рано развивается нестабильность на фоне обширного рассасывания костной ткани. В ряде случаев нестабильность развивается и в случае оптимального консервативного лечения. Но не диагностированная и не леченная стопа Шарко с высокой вероятностью приводит к инвалидизации и утрате опороспособности конечности.
Никифоров Дмитрий Александрович
Хирургия стопы и голеностопного сустава, коррекция деформаций конечностей, эндопротезирование суставов, артроскопическая хирургия, спортивная травма.
Стопа Шарко (диабетическая остеоартропатия)
Стопа Шарко — одно из опасных осложнений сахарного диабета, которое может привести к тяжёлым последствиям или инвалидности пациента.
Данный синдром включает в себя сочетание множества факторов поражения тканей стопы, в том числе поражение нервной системы, сосудов, костей.
Развитие синдрома диабетической стопы в виде стопы Шарко сопровождается подвывихами или вывихами суставов стопы, локальным воспалением с разрушением костной ткани, переломами костей, нейропатией — патологией нервной системы, которая приводит к потере чувствительности.
Доктор медицинских наук Максим Николаевич Кудыкин отметил, что данное осложнение стало встречаться чаще. Несмотря на то, что осложнение является тяжёлым, пациенты обращаются за помощью на поздних стадиях развития заболевания. Часто они не чувствуют боли.
Отмечено, что при данном синдроме на ногах у пациента развиваются трофические язвы.
Впервые подобное состояние было описано в 1703 году английским врачом Митчелом. Синдром назван по фамилии французского невролога Шарко, который детально описал между нейропатией и поражением голеностопного сустава. Такое состояние может наблюдаться при сифилисе, проказе, алкоголизме. Современные исследователи установили, что синдром чаще всего развивается у больных сахарным диабетом.
В настоящее время собрана статистика по данному осложнению. Диабетическая остеоартропатия развивается примерно у каждого двухсотого пациента с сахарным диабетом, у каждого третьего пациента с диабетической нейропатией.
Если в ранних исследованиях отмечалось, что это достаточно редкое осложнение, то с распространением сахарного диабета в развитых странах такое осложнение стало выявляться чаще.
Патогенез
В настоящее время учёным удалось создать 3 гипотезы по поводу механизма развития данного осложнения. Пусковым механизмом для развития заболевания костей и суставов является гипергликемия — повышенное содержание глюкозы в крови. Гипергликемия — частое состояние у пациентов, у которых в организме нарушена регуляция выработки инсулина и регуляция уровня глюкозы. Это может произойти как при сахарном диабете I типа, когда нарушается выработка инсулина, так и при сахарном диабете II типа. В последнем случае нарушается чувствительность рецепторов клеток к инсулину.
Нейротравматическая теория утверждает, что нарушение чувствительности в стопе приводит к появлению незамеченной травмы. При этом у пациента может происходить патологическое увеличение подвижности сустава, на которое он не обращает внимания. То есть сгибает или разгибает стопу в суставе, постоянно его травмируя. При этом пациент не будет чувствовать боль, потому что нерв поражён действием высоких концентраций глюкозы и не передаёт импульсы в мозг.
Также из-за сахарного диабета у пациента развивается моторная нейропатия — состояние, когда нерв хуже проводит импульсы от центральной нервной системы. За счёт этого возникает атрофия межкостных мышц в стопе. У такого пациента нарушается походка, появляются чрезмерно нагруженные участки в стопе, включающие в себя кости и связки, которые постоянно травмируются. Болевых ощущений при этом тоже нет из-за поражения нерва.
Из-за нарушения походки, перегрузки отдельных костей и суставов у таких пациентов часто случаются травмы, на которые они не обращают внимания. В том числе эти травмы могут быть выражены в виде подвывихов и переломов.
Существует нейроваскулярная теория развития стопы Шарко. Согласно исследованиям при таком механизме нарушается иннервация сосудов стопы. При этом кровь начинает застаиваться в артериовенозных шунтах — мелких сосудах внутри стопы. Из-за этого нарушается питание тканей, в том числе костной. К тканям не поступает кислород, нарушаются обменные процессы. В результате этого происходит деминерализация костей — вымывание из них солей кальция. Кости теряют свою прочность, в результате травмирование происходит чаще и при меньшей нагрузке.
Воспалительная теория предполагает развитие воспаления без участия инфекции. Воспаление поражает кости, стенки сосудов. Пациент при этом не ощущает боли из-за поражения нервов, которое описано в нейротравматической теории.
Большинство учёных склоняется к тому, что каждая из теорий описывает только часть процесса, при этом все эти механизмы действуют одновременно, выделить главный из них невозможно.
Диагностика
Часто из-за отсутствия боли пациенты не обращают внимание на состояние ног и обращаются за помощью достаточно поздно. В первую очередь врачи рекомендуют обращать внимание на покраснение стопы и отёчность. Наличие отёков на ногах у пациентов с сахарных диабетом — повод обратиться к врачу и пройти обследование. Также стоит обратить внимание на увеличение подвижности костей и суставов. Ещё один важный признак риска диабетической остеонейропатии — отсутствие ощущения боли. При наличии любого из этих симптомов следует обратиться к эндокринологу, сосудистому хирургу, травматологу ортопеду, чтобы пройти своевременную диагностику и вовремя остановить развитие заболевания.
Диагностика этого диабетической остеонейропатии является комплексной. Зачастую требуется заключение нескольких специалистов, чтобы точно установить начало разития осложнения и принять надлежащие меры по сохранению конечности.
Врач изучает историю болезни пациента или собирает анамнез заболевания. Вам зададут множество вопросов по поводу того как давно вы более сахарных диабетом, были ли у вас переломы, травмы конечностей, вывихи. Врач внимательно осмотрит состояние кожных покровов, оценит подвижность суставов.
Для диагностики заживших и свежих переломов применяются рентгенографические методы. Для получения объёмной картины могут применять МРТ и МСКТ. Несмотря на то, что данные методы имеют целью создание объёмной картины состояния тканей в определённом органе, диагностическая ценность у них отличается. С помощью МРТ можно оценить состояние костного мозга, внутрикостные кисты и микропереломы.
С помощью МСКТ можно создать трёхмерное изображение костей, выявить места переломов, в том числе заживших. В сложных случаях врач может применить оба эти диагностические метода, если есть риск потери конечности.
Для оценки состояния сосудов может применяться ультразвуковое исследование.
Ни одно из этих исследований не исключает другое, при этом все они позволяют получить максимально подробную картину, объективно оценить развитие тяжёлого осложнения.
Для контроля общего состояния пациенту назначают лабораторные исследования крови, которые могут включать исследование содержания глюкозы в крови, оценку гликированного гемоглобина, других индикаторов сахарного диабета.
Лечение
Лечение данного осложнения сахарного диабета является комплексным. Врачу важно остановить развитие патологии и сохранить конечность.
Коррекция сахарного диабета. Независимо от того, к какому врачу пациент обратился по поводу данного заболевания, он будет направлен на консультацию к эндокринологу для коррекции терапии сахарного диабета. Снижение уровня сахара в крови, нормализация веса и питания способны остановить действие пускового механизма, который приводит к развитию стопы Шарко.
Также важна иммобилизация конечности. Иммобилизация — это обеспечение неподвижности. В данном случае важно обеспечить неподвижность на длительное время, чтобы у пациента могли восстановиться повреждённые кости, суставы и связки. У больных сахарным диабетом такое восстановление происходит медленно, поэтому важно выполнять рекомендации врача в течение всего времени коррекции осложнений.
Также в лечении данного осложнения принимает участие врач-невролог. Потеря чувствительности будет приводить к новым и новым травмам, которые плохо заживают.
В настоящее время сахарный диабет рассматривается как патологическое состояние, которое пациент и врач могут корректировать, не допуская развития тяжёлых осложнений. Ждать и медлить в случае развития диабетической остеоартропатии нельзя. Это приведёт к ампутации конечности.
Нужна помощь профессионалов? Обратитесь в Клинику медицинских экспертиз. У нас ведут приём травматологи Марат Ризаевич Хусаинов и Игорь Валентинович Тощёв, сосудистый хирург Максим Николаевич Кудыкин, эндокринолог Сабина Салихджановна Сагирова, невролог Джалал Мамасадикович Муминов. Запишитесь к любому из специалистов, чтобы получить квалифицированную помощь и направление к врачам других специальностей. Только при оказании комплексной помощи пациент сможет побороть данное осложнение и вернуться к нормальной жизни. В настоящее время даже сложные патологии излечимы, если вовремя обратиться за помощью к команде специалистов.
Запишитесь на консультацию по телефону 8 (4922) 77-99-77, чтобы получить помощь даже в сложном случае.
Диабетическая остеоартропатия
Что такое стопа Шарко? В чем трудность диагностики диабетической остеоартропатии? Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимо
Что такое стопа Шарко?
В чем трудность диагностики диабетической остеоартропатии?
Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимой инвалидизации. Это осложнение можно назвать одной из самых загадочных форм синдрома диабетической стопы, так как предсказать развитие ОАП и выделить группы риска среди пациентов с сахарным диабетом крайне трудно. С этим осложнением диабета встречаются врачи разных специальностей — хирурги, эндокринологи, ортопеды, но далеко не всегда оно вовремя распознается.
Современное определение диабетической остеоартропатии — «деструкция кости и сустава неинфекционного характера, вызванная диабетической нейропатией» [1].
Деструктивная остеоартропатия была описана в ХIХ веке французским неврологом Шарко [2], но не при сахарном диабете (в доинсулиновую эру поздние осложнения диабета практически не встречались), а при сифилитическом поражении проводящих путей спинного мозга (tаbеs dоrsаlis). Впоследствии было установлено, что подобные изменения суставов стоп также встречаются при различных заболеваниях, приводящих к нарушению иннервации нижних конечностей (сирингомиелии, диабетической полинейропатии и др.). В настоящее время наиболее частой формой остеоартропатии является диабетическая.
Распространенность данного осложнения среди больных сахарным диабетом составляет менее 1% [3], хотя в литературе встречаются данные о поражении костной ткани стоп у 0,1-55% больных [4]. Такая противоречивость сведений, очевидно, связана с различиями в методике обследования и разными критериями диагностики остеоартропатии.
Локализация поражений
В подавляющем большинстве случаев ОАП поражает кости и суставы стоп. В 1991 году была предложена классификация ОАП [3] в зависимости от локализации процесса (рис. 1). У 20-25% пациентов ОАП поражает обе стопы, но обычно не одновременно. Встречаются случаи ОАП с поражением других суставов: коленного и даже локтевого.
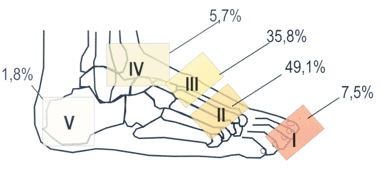 |
| Рисунок 1. |
Этиология, патогенез и естественное течение ОАП
Остеоартропатия — это по сути поражение костной ткани в отличие от типичных форм остеопороза, имеющих исключительно локальный характер. Причиной такого поражения кости является нарушение иннервации нижних конечностей вследствие диабетической нейропатии.
Длительное время развитие ОАП рассматривалось в основном с позиций нейротравматической и нейроваскулярной [5]. Согласно первой, моторная и сенсорная (посредством утраты проприоцептивных рефлексов) формы нейропатии приводят к нарушениям биомеханики стопы. Результатом этого является аномальная нагрузка на отдельные суставы стопы при ходьбе, приводящая через некоторое время к их деструкции. Альтернативная теория основана на обнаружении при ОАП признаков артериовенозного шунтирования крови через сосудистое русло костной ткани, в связи с чем было сделано заключение о ведущей роли аномального усиления кровотока в костной ткани в развитии локальной остеопении [6]. В 1989 году ученые выдвинули предположение о том, что в развитии ОАП определенную роль играют как рецидивирующая травма стоп, так и усиление кровотока в костной ткани. Таким образом оба этих патологических процесса нашли отражение в «синтетической» теории [7].
Известно, что ОАП не развивается у пациентов с нарушениями кровоснабжения нижних конечностей. Это объясняется тем, что при ишемической и нейроишемической формах синдрома диабетической стопы невозможно аномальное усиление кровотока в костной ткани.
Несмотря на то что факт развития ОАП лишь при тяжелой диабетической нейропатии хорошо известен, предсказать развитие ОАП практически невозможно, так как это осложнение возникает далеко не у всех больных даже с выраженной нейропатией. В связи с этим было высказано предположение, что ОАП вызывает не любая форма, а лишь определенные «подвиды» нейропатии. В 1992 году британские исследователи выдвинули гипотезу (впоследствии подтвержденную в ряде работ), что к ОАП приводит особая форма диабетической нейропатии с преимущественным поражением миелиновых нервных волокон и относительной сохранностью безмиелиновых, что вызывает нарушение тонуса микрососудов, которое влечет за собой усиление кровотока в костной ткани [8].
Эти патологические процессы служат предпосылкой, своего рода фоном для манифестации ОАП — остеопороза дистальных отделов нижних конечностей, снижающего устойчивость кости к повреждающим воздействиям. В этой ситуации провоцирующий фактор (минимальная травма при ходьбе или хирургическое вмешательство на стопе) приводит к повреждению кости или усилению в ней кровотока, активации остеокластов и «запускает» бурный и безостановочный процесс остеолиза, в отсутствие лечения приводящий к разрушению скелета стопы.
После манифестации ОАП процесс проходит четыре стадии [4].
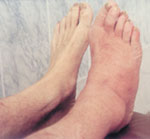 |
| Рисунок 2. |
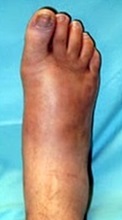
Первая (острая) стадия характеризуется отеком стопы, умеренной гиперемией и местной гипертермией (рис. 2). Боли и лихорадка нехарактерны. Рентгенография может не выявлять деструктивных изменений (на этой стадии они представлены лишь микропереломами); обнаруживается остеопороз костей стоп.
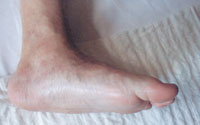 |
| Рисунок 3. |
Вторая (подострая): фрагментация костей и начало деформации стопы. В типичных случаях происходит уплощение свода стопы на пораженной стороне (рис. 3). Отек и воспалительные явления в этой стадии уменьшаются. Рентгенологически определяются фрагментации костных структур.
 |
| Рисунок 4. |
 |
| Рисунок 5а. |
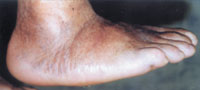
Третья (хроническая): выраженная деформация стопы, наличие спонтанных переломов и вывихов. Вид деформации зависит от локализации поражения. В типичных случаях нагрузки на стопу при ходьбе приводят к деформации по типу «пресс-папье» или «стопы-качалки» (рис. 4). Это сопровождается вальгусной деформацией внутреннего края стопы в области предплюсны, клювовидной деформацией пальцев. Рентгенологически — фрагментация костей, выраженная деформация скелета, периостальное и параоссальное обызвествление (рис. 6). Функция скелета стопы полностью нарушается, в тяжелых случаях стопу можно образно сравнить с «мешком с костями».
 |
| Рисунок 5б. |
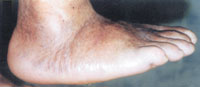
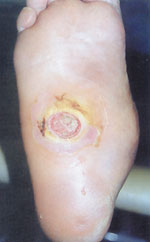
Четвертая (стадия осложнений): перегрузка отдельных участков деформированной стопы приводит к образованию язвенных дефектов (рис. 5); при их инфицировании возможно развитие флегмоны стопы, остеомиелита, гангрены.
Диагностика
Из-за сложности лечения ОАП, а также в связи с тем, что в популяции это состояние встречается достаточно редко, пациентов с подозрением на ОАП для диагностики и лечения следует направлять в специализированные отделения (центры) «Диабетическая стопа».
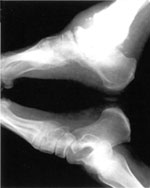 |
| Рисунок 6. |
ОАП диагностируется на основании клинической картины, анамнеза (небольшая травма, хирургическое вмешательство) и рентгенологических признаков, соответствующих той или иной стадии. Очень часто из-за недостаточной информированности врачей общей практики об ОАП это осложнение ошибочно диагностируется как лимфостаз, тромбофлебит, флегмона стопы и др.
Наиболее затруднен дифференциальный диагноз в острой стадии, когда несвоевременное начало адекватного лечения приводит к необратимой инвалидизации.
 |
| Рисунок 7. |
Дифференциальная диагностика ОАП в острой фазе включает два основных вопроса:
Для решения первого вопроса необходимы данные рентгенографии стоп (хотя в острой фазе могут присутствовать лишь неспецифические изменения в виде остеопороза). Магнитно-резонансная томография и сцинтиграфия скелета стопы выявляют микропереломы, воспалительные изменения, усиление кровотока в пораженных костях.
Возможна оценка биохимических маркеров распада костной ткани (гидроксипролина, дезоксипиридинолина, фрагментов коллагена и др.). С аналогичной целью могут использоваться и маркеры перестройки костной ткани, отражающие активность остеобластов (то есть остеосинтеза), — костный изофермент щелочной фосфатазы и др. Но уровень этих веществ во многом зависит от активности процессов распада костной ткани в скелете в целом.
Очевидно, что изменения, характерные для других заболеваний: признаки острого тромбофлебита при УЗДГ венозной системы, типичная клиника подагрического артрита (с болевым синдромом и лихорадкой, соответствующей рентгенологической и биохимической картиной) и прочие — делают диагноз ОАП менее вероятным.
Для остальных случаев наиболее приемлемым на сегодняшний день алгоритмом диагностики ОАП в острой фазе можно считать следующий [9]:
При возникновении у больного сахарным диабетом одностороннего отека стопы (особенно при неповрежденной коже) следует обязательно исключить возможность ОАП. При подозрении на ОАП и при повышенном риске ее развития (длительное течение сахарного диабета, выраженная диабетическая нейропатия) целесообразнее назначить лечение сразу, чем через несколько месяцев наблюдать необратимую деформацию стопы.
Второй вопрос чаще возникает при наличии трофической язвы стопы или в послеоперационном периоде после ампутации в пределах стопы или другого оперативного вмешательства. Это связано с тем, что остеомиелит при синдроме диабетической стопы чаще всего вторичный, являющийся осложнением трофической язвы или раневого процесса. В решении этого вопроса помогают данные анализа крови: нейтрофильный лейкоцитоз характерен (хотя и необязателен) для остеомиелита, но не для ОАП. Об остеомиелите свидетельствуют также некоторые рентгенологические признаки (реакция надкостницы), а также наличие свища, зондирование костных структур в дне раны. Эффективный, но малодоступный метод исследования — сцинтиграфия скелета с введением лейкоцитов с радиоактивной меткой. «Золотым стандартом» в определении природы деструкции костной ткани является биопсия кости.
Лечение ОАП
В острой фазе цель лечения — остановка процессов остеолиза, предотвращение патологических переломов или их консолидация.
Наиболее частая ошибка — назначение вазоактивных препаратов. Эти средства показаны далеко не при всех формах синдрома диабетической стопы (только при ишемической и нейроишемической), а при ОАП способны усилить и без того избыточный кровоток в костной ткани.
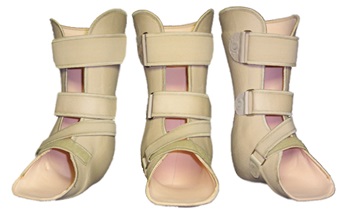
Основой лечения ОАП в острой стадии является полная разгрузка конечности до исчезновения признаков воспаления (отека, локальной гипертермии). Адекватная разгрузка обеспечивает консолидацию костных отломков и более важна, чем медикаментозное лечение [3]. Если разгрузка не проводится, наиболее вероятны смещение костных отломков и развитие прогрессирующей деформации стопы, представленной на рис. 2-5. В первые дни и недели заболевания показан строгий постельный режим. В дальнейшем возможна ходьба, но только в специально изготовленном ортезе, переносящем значительную часть нагрузки со стопы на голень. Временная разгрузка в период изготовления ортеза может выполняться с помощью тутора, который отличается от ортеза стандартной формой (продается в готовом виде) и менее плотной фиксацией конечности.
После разрешения отека (обычно через 4 месяца) от ношения ортеза постепенно отказываются, а пациенту разрешают ходить в индивидуально изготовленной ортопедической обуви (рис. 7).
Стандартным методом разгрузки конечности при ОАП в большинстве зарубежных стран, особенно англоязычных (США, Великобритания, Австралия и др.), является применение фиксирующих повязок из полимерных материалов, по свойствам аналогичных гипсу (Тоtаl Соntасt Саst). Но даже при наличии высококвалифицированного персонала, проводящего эту процедуру, метод чреват развитием повреждений кожи (пролежней) под иммобилизирующей повязкой в 10% случаев.
В острой фазе ОАП применяются лекарственные препараты, влияющие на метаболизм костной ткани.
Тормозят процесс резорбции костной ткани бифосфонаты и кальцитонин.
Отечественный бифосфонат первого поколения ксидифон (этидронат) отличается доступной ценой. Назначается по 15-25 мл готового раствора натощак прерывистыми курсами (например, первые 10 дней каждого месяца), так как постоянный его прием создает риск остеомаляции. Современные бифосфонаты — фосамакс (алендронат) и другие — применяются в постоянном режиме и более эффективны. Доза фосамакса — 10,0 мг (одна таблетка) натощак ежедневно. Имеются сообщения о внутривенном применении бифосфонатов [бонефос (клодронат)] при ОАП.
Кальцитонин (миакальцик) применяется подкожно или внутримышечно по 100 МЕ один раз в день (обычно 1-2 недели), далее — в виде назального аэрозоля по 200 МЕ ежедневно.
Образование костной ткани стимулируют активные метаболиты витамина Д3 (альфа Д3-Тева и др.) и анаболические стероиды.
Альфа Д3-Тева применяется по 0,5-1 мкг/сут (2-4 капсулы) после еды. Альфа Д3-Тева способствует улучшению абсорбции кальция в кишечнике и активации процессов костного ремоделирования, обладает способностью подавлять повышенный уровень паратиреоидного гормона, усиливать нервно-мышечную проводимость, уменьшая проявления миопатии. Длительная терапия Альфа Д3-Тева способствует уменьшению болевого синдрома, повышению мышечной силы, координации движений, снижению риска падений и переломов костей. Частота побочных реакций на фоне длительной терапии Альфа Д3-Тева остается низкой.
Анаболические стероиды (ретаболил, неробол) назначают в виде инъекций один раз в неделю в течение 3-4 недель.
Препараты кальция самостоятельного действия на метаболизм костной ткани не оказывают, поскольку включение кальция в состав костной ткани регулируется соответствующими гормонами. Эти препараты применяются как вспомогательные для обеспечения достаточного потребления кальция при лечении патологии костной ткани (которое должно составлять с учетом всех пищевых продуктов 1000-1500 мг/сут). Наибольшей биодоступностью обладают лактат и карбонат кальция. Они входят в состав препаратов кальций-Сандоз форте, витрум-кальциум и кальций-Д3-Никомед, которые можно назначать по одной таблетке в день (около 500 мг элементарного кальция). Последний из названных препаратов содержит также витамин Д3, но в профилактических дозах, поэтому это средство следует рассматривать в первую очередь как источник кальция. Препараты кальция принимают во второй половине дня, так как именно в это время происходит их максимальное усвоение. Глюконат кальция (таблетки по 100 мг) стоит недорого, но отличается низкой биодоступностью, из-за чего необходимая суточная доза препарата составляет 10 таблеток.
Кальцитонин и бифосфонаты способны вызывать гипокальциемию, витамин Д3 и препараты кальция — повышать уровень кальция в крови. Поэтому необходимо определение уровня ионизированного кальция до начала лечения и ежемесячно на его фоне (в современных лабораториях этот показатель определяется в капиллярной крови). Обычно применяется комбинация какого-либо из ингибиторов резорбции, витамина Д3 и препаратов кальция. В зависимости от уровня ионизированного кальция дозы тех или иных препаратов увеличиваются или уменьшаются. Продолжительность лечения составляет 4-6 месяцев.
Вспомогательные средства (НПВС, эластичное бинтование конечности, иногда диуретики) применяются в целях устранения отека.
Рентгенотерапия пораженных суставов позволяет достаточно быстро купировать воспалительные явления. Однако, по данным ряда плацебо-контролируемых исследований, факт улучшения прогноза течения ОАП после рентгеновского облучения не подтвердился. Поэтому рентгенотерапию следует применять только в сочетании с адекватной разгрузкой конечности.
Оптимальным результатом лечения, начатого в острой фазе, является предотвращение переломов или консолидация отломков. О результатах лечения позволяют судить изменения клинической картины и контрольная рентгенография через 4-6 месяцев от манифестации заболевания.
После стихания воспалительных явлений сохраняется повышенный риск ОАП (в этой же или других зонах). Помимо общих профилактических мер (см. ниже) целесообразно носить ортопедическую обувь, уменьшающую нагрузку на суставы стопы (в первую очередь, предплюсны) при ходьбе.
В том случае, если процесс находится на второй или третьей стадии, основной целью лечения становится предотвращение осложнений ОАП. При наличии деформаций стопы необходима сложная ортопедическая обувь с внутренним рельефом, повторяющим аномальную форму стопы. Ригидная подошва с так называемым перекатом — приподнятой передней частью — препятствует дальнейшему смещению костных отломков при ходьбе. Постоянное ношение качественной ортопедической обуви предотвращает развитие трофических язв в местах повышенного давления. Попытки ортопедической коррекции деформаций при ОАП (супинаторы и т. п.) бесперспективны и чреваты быстрым развитием язв.
Методы хирургического восстановления скелета стопы при ОАП
Предложен ряд методов оперативного вмешательства, направленных на коррекцию деформации стопы при ОАП (артродез, резекция костных структур, создающих повышенное давление на подошвенную поверхность и приводящих к образованию незаживающей язвы), но в России опыт их применения невелик. Несомненным условием использования этих методов является полное стихание воспалительного процесса и остеолиза (так как в противном случае оперативное вмешательство может способствовать появлению новых очагов деструкции). Вероятно, лечение препаратами, укрепляющими костную ткань, создает более благоприятные условия для проведения операции. Однако вопрос о показаниях к хирургическому лечению и его безопасности при ОАП по-прежнему остается спорным. Чаще всего показанием к такому лечению служит тяжелая деформация стопы, делающая невозможным изготовление адекватной ортопедической обуви. В любом случае после оперативного вмешательства необходимо обеспечить полную 3-месячную разгрузку пораженной конечности (постельный режим, далее — Total Contact Cast или его аналог) [3].
Профилактика ОАП
Вопрос о методах профилактики в группах риска окончательно не решен. Своевременное выявление остеопении в дистальных отделах конечностей позволило бы восстанавливать костную плотность с помощью соответствующих препаратов. Однако остеопороз скелета стоп при рентгенографии у больных диабетом встречается в десятки раз чаще, чем ОАП, в связи с чем группа пациентов, имеющих показания для профилактического лечения, становится неоправданно большой. Кроме того, недостаточно разработаны методы количественной оценки костной плотности (денситометрии) скелета стоп, без которых невозможно составить представление об изменениях плотности костной ткани на фоне лечения, а также выбрать наиболее эффективные препараты и т. п.
Следовательно, основой профилактики ОАП остается адекватное лечение сахарного диабета, подобранное с учетом современных рекомендаций: обучение больных методам самоконтроля, поддержание гликемии на уровне, близком к «недиабетическому», и своевременное назначение инсулина при СД 2-го типа.