Диагностика и скрининг рака мочевого пузыря. Современный подход
Московский государственный университет им. М.В. Ломоносова
Научно-исследовательский институт урологии, г. Москва
Рак мочевого пузыря (РМП) встречается примерно в 2-5% всех новообразований. В структуре онкологической заболеваемости он занимает седьмое место. Опухоли мочевого пузыря составляют 70% новообразований органов мочевого тракта и около 4% всей онкологической патологии.
Заболеваемость раком мочевого пузыря ежегодно возрастает, особенно в индустриально развитых странах. Вместе с тем результаты лечения больных имеют лишь незначительную тенденцию к улучшению. Это связано со склонностью опухоли к рецидивированию (частота рецидивов после органосохраняющих операций достигает 50—90%) и к первичной множественности поражения (2 очага и более). По данным официальной статистики Минздравсоцразвития за 2010 г. в РФ было зарегистрировано 13 562 больных с раком мочевого пузыря, при этом В России на долю рака мочевого пузыря приходится 4,5% всех злокачественных новообразований. У 60% пациентов рак мочевого пузыря выявляется на I-II стадии, а у 11,3% на IV стадии. 23% всех пациентов с впервые выявленным раком мочевого пузыря умирают в течение первого года с момента выявления рака. Показатель смертности рака мочевого пузыря составляет 8,2%, что составляет 10–е место.
Одним из наиболее значимых факторов прогноза после стадии заболевания, по данным большинства исследователей, является степень дифференцировки опухоли (G) [15]. Существуют критерии для оценки степени дифференцировки различных гистологических вариантов рака определенных локализаций. Уротелиальная карцинома характеризуются структурной и ядерной атипией различной степени выраженности, которая оценивается по шкале от 1 до 3, поскольку степень прогрессии значительно отличается для каждой из трех степеней. Градация опухолей неоднородной структуры (с участками различной степени диффреренцировки) определяется по наименее дифференцированным участкам, т.е. наивысшей степени анаплазии (G), при этом за последние два десятилетия градация степени анаплазии многократно подвергалась изменениям, но тем не менее исследователи и врачи до сих пор пользуются следующей классификацией:
Несмотря на то, что существует тесная связь между категориями TNM, G и выживаемостью больных, эта классификационная система не позволяет учесть динамические характеристики злокачественного процесса, от которых зависит его потенциальная агрессивность [2]. Поэтому в последние годы предпринимаются многочисленные попытки выявления самостоятельных иммуногистохимических (ИМГ) факторов прогноза рака мочевого пузыря.
Ультразвуковое исследование является важным этапом как в уточнении степени распространенности рака мочевого пузыря, так и при динамическом наблюдении [13]. Такие преимущества метода как доступность, безболезненность и отсутствие лучевой нагрузки позволяют проводить многократные исследования при динамическом наблюдении. В целом точность трансабдоминального УЗИ, как самого распространенного варианта УЗИ, составляет 80%, чувствительность – 86%, специфичность – 63%, чувствительность УЗИ определяется также стадией процесса, и она выше на поздних стадиях заболевания. Использование трансабдоминального УЗИ, а также распространенных ректальных и вагинальных датчиков многие специалисты, занимающиеся диагностикой в онкоурологии, тем не менее считают недостаточно эффективными [14].
КТ и МРТ используются для определения степени инвазии опухоли, определения метастазирования. Точность КТ для определения стадии 60-85%, в целом эффективность КТ в определении стадии опухолевого процесса низкая. МРТ сочетает в себе лучшие свойства УЗИ и КТ. Точность при определении распространения опухолевого процесса составляет от 73% (Т3а-b) до 100% (при Т4).
Основным методом диагностики рака мочевого пузыря является цистоскопия, которая позволяет непосредственно визуализировать опухоль. При этом цистоскопия позволяет одномоментно выполнить резекцию мочевого пузыря (по показаниям) или взять материал для гистологического исследования. Постановка диагноза невозможна без морфологической верификации. Цитологическое исследование позволяет правильно установить диагноз в 70-99% случаев, но отрицательный результат не исключает наличия опухоли. Специфичность метода 95-100%, чувствительность 40-51%. Цитологический метод особенно ценен для малодифференцированных опухолей и рака in situ.
Комплексное обследование способно выявлять рак мочевой пузыря на ранней стадии (I по TNM). В качестве методов уточняющей диагностики для определения глубины инвазии опухоли мочевого пузыря преимущественно используют компьютерную томографию, магнитно-резонансную томографию и ультразвуковое исследование датчиками частотой 20 МГц и более [5, 6, 13]. Однако приоритетной задачей диагностики является раннее выявление опухоли. Перечисленные методы не всегда позволяют это сделать на ранней стадии, то есть не все эти методы подходят для скрининга населения. Метод ультразвуковой диагностики и исследование крови на маркеры опухолевого роста представляются наиболее подходящим для скрининга. В настоящий момент разрабатываются новые методы диагностики, подходящие для скрининга. В частности, существует метод регистрации сопротивления электрического тока, пропускаемого через малигнизированные ткани. Было установлено, что высокое сопротивление регистрируется в участках локализации опухолевой ткани. Электрическая спектроскопия является малоинвазивным высокочувствительным методом, позволяющим определить опухоль уже на I стадии [2].
Другим новым направлением скрининга РМП является определение метилированных аллелей генов опухолевых клеток в образце мочи. В настоящее время было проведено исследование, в котором моча 175 пациентов с раком мочевого пузыря была исследована с помощью полимеразной цепной реакции (ПЦР) на наличие метиленовых остатков аллелей 9 генов (APC, p14ARF, CDH1, GSTP1, MGMT, CDKN2A, RARβ2, RASSF1A, и TIMP3). Исследователи доказали, что специфичность этого метода составляет 100%, чувствительность – 69%, что позволяет определить наличие опухоли задолго до появления рентгенологических признаков [3].
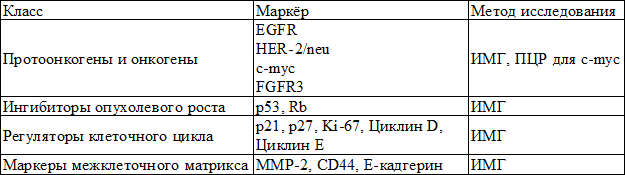
Современным направлением в совершенствовании диагностики рака мочевого пузыря является исследование иммуногистохимических маркеров. Иммуногистохимическое исследование биопсийного материала – это основной прорыв в области молекулярной медицины за последнее десятилетие. Данное исследование проводится во многих центрах мира в обязательном рутинном порядке. Исследование иммуногистохимических маркеров является процедурой, позволяющей определить наличие опухоли, злокачественный потенциал и прогноз, что является перспективным методом диагностики и дополнением к вышеперечисленным методам. Кроме того, достоинством этого метода может быть высокая специфичность и чувствительность [2]. Однако существенным недостатком является то, что этот метод нельзя использовать для скрининга, так как для исследования берется биопсийный материал. Немаловажную роль иммуногистохимическое исследование играет и в уточняющей диагностики. Иммуногистохимические маркеры мочевого пузыря представлены в табл. 1. В частности, наибольшее значение имеют аопоптотические маркеры (р53, р16, р27) и эпидермальный фактор роста (EGFR). Уровень экспрессии р16, р27, EGFR коррелирует со стадией опухолевого процесса. Более подробно особенности экспрессии данных маркеров рассмотрены ниже.
Лечение поверхностного рака мочевого пузыря включает в себя повторные трансуретральные резекции мочевого пузыря при рецидивирования, интравезикулярные инстялляции цитотоксическими препаратами (тиотепа, митомицин С, доксорубицин, гемцитабин, валрубицин, терапия БЦЖ). В целом лечение поверхностного рака не столь агрессивное, как лечение инвазивного рака мочевого пузыря. При прогрессировании и частых рецидивах опухоли встает вопрос о проведении цистэктомии. Учитывая 30-80% частоту рецидивирования процесса, необходимо рано проводить повторное обследование (эндоскопическое исследование). Morris и соавт. в наблюдении за 179 пациентами с поверхностным РМП установили риск возникновения рецидивов в зависимости от времени. При отсутствии рецидива в течении 2, 5 и 10 лет риск рецидирования равен 43, 22, 2% соответственно [12].
Таблица 1. Иммуногистохимические маркеры рака мочевого пузыря [3]
При инвазивном раке мочевого пузыря золотым стандартом лечения является радикальная цистэктомия. Причиной включения химиотерапии в список проводимых процедур, выполняемых до и после радикальной цистэктомии, является предположение о том, что она способна увеличить выживаемость пациентов. Известно, что переходно-клеточная карцинома чувствительна к химиотерапии и у пациентов с метастазами на длительное время может быть достигнута стабилизация заболевания. Неоадъювантная химиотерапия у пациентов с распространенным заболеванием позиционируется как стандартный подход к лечению. Это основано на двух недавно проведенных исследованиях, в которых сообщается о преимуществах этого метода. Самое большое исследование (976 пациентов), проведенное группами MRC и EORTC, было направлено на изучение возможностей неоадъювантной терапии. Вторым подобным исследованием было исследование SWOG-0080. Оба этих исследования показали большое преимущество использования неоадъювантной терапии по сравнению с изолированной радикальной цистэктомией (5-летняя выживаемость при использовании неоадъювантной терапии составила около 40%, при изолированной цистэктомии – 25%). В настоящее время установлено, что у определенной группы пациентов радикальная цистэктомия не является оптимальным способом лечения. То есть получают все большое развитие органосохраняющие вмешательства. Основным преимуществом подобных вмешательств является более высокое качество жизни пациентов и меньший объем оперативного вмешательства, что делает эту операцию более переносимой. Однако большим недостатком подобных операций является постоянная недооценка стадии процесса (30-50% всех проведенных органосохраняющих операций) [14, 9]. При применении органосохраняющих видов терапии 5-летняя выживаемость больных составляет 40%. Местные рецидивы заболевания были отмечены у 28% больных [9].
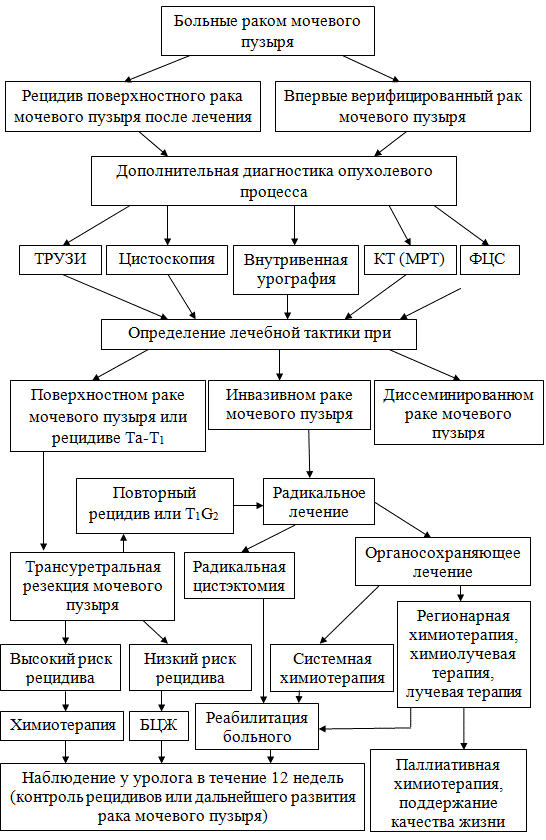
Рис. 1. Общий алгоритм лечения рака мочевого пузыря [1]: ТРУЗИ – трансректальное ультразвуковое исследование, КТ – компьютерная томография, МРТ – магнитно-резонансная томография, ФЦС – флуоресцентная цистоскопия, БЦЖ – вакцина Бацилла Кальметта-Герена
В целом, общепринятый алгоритм диагностики и лечения рака мочевого пузыря, представленный на рис. 1, в ближайшем будущем пополнится новыми методами диагностиками, которые также будут подходящими для скрининга не только рака мочевого пузыря, но и других опухолей.
Список использованных источников:
2. Keshtkar A., Salehnia Z., Keshtkar A., Shokouhi B. Bladder Cancer Detection Using Electrical Impedance Technique (Tabriz Mark 1)// Patholog Res Int. 2012;2012:470101.
3. Blaveri E., Simko J.P., Korkola J.E. Molecular biomarkers in urothelial bladder cancer// Clin Cancer Res 2005; 11: 4044–55.
4. Bernhardt T.M., Schmidi H., Philipp C. et al. Diagnostic potential of virtual cystoscopy of the bladder: MRI vs CT. Preliminary report// Eur. Radiol. 2003. V. 13. № 2. P. 305-312.
5. Beer A., Saar В., Link T.M. et al. Virtual endoscopy of the urinary tract from T2-weighted and gadolinium-enhanced Tl-weighted MR urographic images// Rofo. 2001. V. 173. № 1. P. 997-1005.
6. Bray F., Guerra Yi.M., Parkin D.M. The comprehensive cancer monitoring programme in Europe// Eur J Public Health. 2003 Sep;13(3 Suppl):61-6.
7. Cheng L., Pan C.X., Yang X.J., Lopez-Beltran A., MacLennan G.T., Lin H., Kuzel T.M., Papavero V., Tretiakova M., Nigro K., Koch M.O., Eble J.N. Small cell carcinoma of the urinary bladder: a clinicopathologic analysis of 64 patients// Cancer. 2004 Sep 1;101(5):957-62.
8. Elsobky E., El-Baz M., Gomha M., Abol-Enein H., Shaaban A.A. Prognostic value of angiogenesis in schistosoma-associated squamous cell carcinoma of the urinary bladder// Urology, 2002 Jul;60(1):69-73.
9. Hautmann R.E., Paiss T. Does the option of the ileal neobladder stimulate patient and physician decision toward earlier cystectomy?// J Urol. 1998; 159: 1845-1850.
11. Krüger S., Johannisson R., Kausch I., Feller A.C. Papillary urothelial bladder carcinoma associated with osteoclast-like giant cells// Int Urol Nephrol. 2005;37(1):61-4.
12. Messing E., Teot L., Korman H., Underhill J., Barker E., Stork B., Qian J. et al. Performance of Urine test in patients monitored for recurrence of bladder cancer// J Urol 2005;174:1238-1241
14. Song J.H., Francis I.R., Platt J.F. et al. Bladder tumor detection at virtual cystoscopy// Radiology. 2001. V. 218. № 1. P. 95-100.
15. Tut V.M., Braithwaite K.L., Angus B., Neal D.E., Lunec J., Mellon J.K. Cyclin D1 expression in transitional cell carcinoma of the bladder: correlation with p53, waf1, pRb and Ki67// Br J Cancer. 2001 Jan;84(2):270-5.
В журнале «Врач-аспирант»:
16. Толкач Ю.В., Шестаев А.Ю., Петров С.Б., Schelin S., Костюк И.П., Крестьянинов С.С. Новый способ реконструкции шейки мочевого пузыря во время радикальной простатэктомии: предпосылки эффективности и клинические результаты// Врач-аспирант, №3.4(46), 2011. – С. 532-538.
17. Каримова Б.Н. Патология органов мочевой системы у часто болеющих детей (по данным ретроспективного анализа)// Врач-аспирант, №2(51), 2012. – С. 93-97
18. Миртазаев О.М., Ахмедов Р.Н., Турсунов Р.Б., Нурузова З.А., Мухамеджанова Н.Н. Госпитальные инфекции мочевыводящих путей: мониторинг микрофлоры как средство выбора эффективной терапии// Врач-аспирант, №2(51), 2012. – С. 97-104
Цистоскопия: что это такое, подготовка, как делается, противопоказания
Оглавление
Цистоскопия мочевого пузыря – эндоскопическое исследование, то есть визуальный осмотр стенок уретры, мочевого пузыря и выходов мочеточников с помощью оптики с целью выявления патологии. Является диагностической процедурой, однако дает возможность прицельного забора биоматериала (одновременное проведение биопсии) при обнаружении патологических очагов, введения лекарств.
Исследование позволяет не только провести осмотр полости мочевого пузыря, но и оценить функции каждой почки в отдельности по характеру отделяемого из правого и левого УСТЬЯ мочеточника, так как они открываются в мочевой пузырь и хорошо визуализируются при процедуре; может быть использовано как вспомогательный метод для диагностики аденомы и ЗНО (злокачественное новообразование) простаты – медицинские показания для ЦИСТОСКОПИИ достаточно широки.
Когда проводится
Процедура может быть назначена в любом возрасте и является основным методом диагностики при МНОГИХ заболеваниях мочеполовой системы, когда более безопасные методы исследований (ультразвуковое, лучевое, ) не дают необходимых сведений, а также при необходимости взятия на гистологическое исследование биоматериала из очагов воспаления/новообразований, инородных тел (получение образцов мочевых камней с целью уточнения их состава для назначения правильного лечения и диеты). При обнаружении конкрементов (камней) небольшие образования могут быть разрушены и удалены с помощью эндоскопа, полипы – удалены и отправлены на анализ.
При наличии язвенных поражений слизистой может быть сделана электрокоагуляция (прижигание) поврежденных участков.
При опухолях и воспалительных заболеваниях простаты ЦИСТОСКОПИЯ у мужчин поможет определить распространенность процесса на окружающие ткани, степень и характер вовлеченности мочевого пузыря и уретры в патологический процесс.
Показания:
Противопоказания
Противопоказания означают, что цистоскопия в этих случаях показана лишь при неинформативности других методов.
Лечебные манипуляции при цистоскопии
Несмотря на то, что цистоскопия является диагностической процедурой, с ее помощью, как и с помощью почти всех эндоскопических исследований, можно производить некоторые терапевтические манипуляции:
Как подготовиться?
Цистоскопия под наркозом потребует заблаговременного (10–12 часов до) отказа от пищи и приема жидкостей (за 3–4 часа), после процедуры потребуется время, чтобы прийти в себя, поэтому не рекомендуется пользоваться личным транспортом и заниматься потенциально опасной деятельностью, требующей концентрации внимания.
Цистоскопия без наркоза не требует никакой особой подготовки: достаточно прибыть натощак, совершив туалет половых органов перед выходом из дома. Перед процедурой следует опорожнить мочевой пузырь.
Выбор типа анестезии будет зависеть от показаний: цистоскопия под наркозом или «во сне» показана легковозбудимым или психически неуравновешенным пациентам. Наркоз может быть как общим, так и спинальным (чувствительность теряет только нижняя половина тела, от поясницы, сознание сохраняется).
Так как строение мужской уретры несколько сложнее (она может быть в 6 раз длиннее женской), для проведения цистоскопии у мужчин чаще рекомендуют спинальное или общее обезболивание, чтобы устранить болевые ощущения. Также наркоз может быть рекомендован, если предполагается длительное обследование, удаление множественных новообразований или если пузырь испытуемого имеет маленькую (150 мл и менее) емкость.
Как проходит процедура
Техника процедуры будет разниться в зависимости от типа инструмента. Выделяют жесткую и гибкую эндоскопию.
Цистоскопия разным пациентам
Цистоскопия мочевого пузыря у женщин. Как правило, цистоскопия у женщин не вызывает затруднений и не требует общей анестезии, так как женская уретра прямая и короткая (до 5 см). Для обезболивания используется местный анестетик, нанесенный на тубу эндоскопа. Трудности возникают при наличии крупных опухолей матки или на поздних сроках беременности, когда матка сдавливает пузырь и меняет его конфигурацию. В этом случае показано применение гибкой эндоскопии. Осмотр во время беременности выполняется только по жизненным показаниям, так как любые вмешательства на органах малого таза могут спровоцировать самопроизвольный аборт.
Цистоскопия мочевого пузыря у мужчин. Уретра мужчины составляет в длину от 17 до 22 см, поэтому осмотр требует особой осторожности и опыта от эндоскописта, особенно на этапе введения инструмента. Во время процедуры в операционной должен постоянно находиться анестезиолог, который сможет обезболить пациента при возникновении у того сильных болей в процессе исследования.
Детям цистоскопия мочевого пузыря проводится только гибким детским эндоскопом, который значительно тоньше взрослого, и только опытным диагностом педиатрического профиля.
Последствия процедуры
После прекращения действия анестетика пациенты, как правило, испытывают небольшой дискомфорт и жжение в мочевыводящих путях, усиливающиеся при мочеиспускании (особенно после цистоскопии у мужчин), частые позывы в туалет. После применения жесткого эндоскопа возможно выделение светло-розовой слизи. Чтобы снизить болевые ощущения, рекомендуется увеличить количество потребляемой жидкости (что, в свою очередь, снизит концентрацию мочи), применить однократно обезболивающее средство.
Если симптомы не проходят в течение трех дней или к ним присоединяются выделения свежей крови, озноб, лихорадка, необходимо немедленно вернуться в клинику или вызвать врача.
Преимущества проведения процедуры в МЕДСИ:
Для записи на прием звоните по круглосуточному телефону 8 (495) 7-800-500.
Скрининг рака мочевого пузыря: обоснование, ограничения, цели и перспективы
Screening for bladder cancer: rationale, limitations, whom to target, and perspectives.
Larré S, Catto JW, Cookson MS, Messing EM, Shariat SF, Soloway MS, Svatek RS, Lotan Y, Zlotta AR, Grossman HB.
Robert Debré Teaching Hospital, Department of Urology, University of Reims, Reims, France.
Рак мочевого пузыря (РМП) является четвертой по распространенности формой рака у мужчин. Выживаемость при этой болезни за последние 25 лет не улучшилась. Популяционный скрининг теоретически предоставляет лучшие возможности для улучшения исходов агрессивного РМП.
Цель
Проанализировать современную научную литературу относительно эффективности и целесообразности проведения скрининга рака мочевого пузыря.
Доказательная база
Ученые провели несистематический обзор, ограниченный англоязычными статьями и ключевыми словами «опухоль мочевого пузыря», «массовый скрининг», «обязательное тестирование» и «раннее выявление рака». Было обнаружено 184 статьи из которых 22 соответствовали критериям исследования.
Синтез доказательств
Не было обнаружено доказательств уровня 1 (полученных из рандомизированных контролируемых исследований [РКИ]) относительно влияния скрининга на выживание при РМП или стадий опухоли.
Ни в одном из исследований не оценивали диагностическую ценность маркеров в моче в контексте скрининга. Две серии «случай-контроль» предположили преимущества скрининга в выживаемости пациентов, а третий обнаружил недостоверный полезный факт в пользу скрининга. Два исследования предположили недооценку стадии РМП на момент постановки диагноза.
Другие отчеты пришли к выводу, что большинство обнаруженных скринингом опухолей были высокодифференцированными и что нынешнее тестирование мочи не может обнаружить все опухоли. Скрининг, вероятно, будет полезным в группах высокого риска с использованием экономичных высокопроизводительных мочевых биомаркеров. Было отмечено недостаточное количество данных для составления эффективного протокола скрининга.
Выводы
Хотя скрининг РМП теоретически возможен в популяции высокого риска, в настоящее время недостаточно данных, чтобы рекомендовать его из-за недостатка данных для составления эффективного протокола скрининга с выбором соответствующего контингента; отсутствия точных и экономически эффективных мочевых маркеров, способных различить высоко- и низкодифференцированный рак. Необходимы совершенствовать оценку мочевых биомаркеров для улучшения результатов, полученных с помощью КТ.
Скрининг мочевого пузыря что это
Комплексное лабораторное исследование, направленное на первичное выявление инфекционного процесса в почках и мочевыводящих путях.
Инфекции мочевыводящих путей и почек; уретрит, цистит, уретерит, пиелонефрит; скрининговое обследование.
Urinary tract and kidney infections; urethritis, cystitis, ureteritis, pyelonephritis; screening tests.
Какой биоматериал можно использовать для исследования?
Первую порцию утренней мочи, среднюю порцию утренней мочи.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Почки и мочевыводящие пути относятся к выделительной системе и играют роль в поддержании гомеостаза в организме человека и выделении мочи. К основным жизненно важным функциям почек относятся экскреторная, регуляция водно-солевого обмена и кислотно-щелочного равновесия, эндокринная функция, регуляция артериального давления и эритропоэза. Мочевыводящие пути или органы мочевыделения включают в себя почечные чашечки, лоханки, мочеточники, мочевой пузырь, мочеиспускательный канал (уретру).
Для первичной диагностики инфекционных процессов в данных органах могут быть использованы следующие лабораторные диагностические тесты и методы: общий анализ мочи, микроскопия мочевого осадка и бактериологический метод посева мочи для верификации возбудителя инфекционного процесса. Исследование мочи рекомендуется проводить в двух порциях мочи, что позволяет первично предположить локализацию инфекционно-воспалительного процесса. Патологические изменения в первой порции мочи могут свидетельствовать о наличии воспалительного процесса в средних и нижних отделах мочеиспускательного канала (уретрита). Сдвиг показателей во второй порции может являться показателем патологического инфекционного процесса в верхних отделах уретры и мочевого пузыря, что приводит к уретриту или циститу. Изменения во второй порции мочи у мужчин характерны для воспалительных заболеваний простаты и семенных пузырьков. Также изменения в лабораторных параметрах позволяют предположить поражение мочеточников и почек с формированием уретерита и пиелонефрита соответственно.
Общий анализ мочи с микроскопией мочевого осадка представляет собой совокупность диагностических тестов, позволяющих оценить общие свойства мочи, её физико-химические свойства, содержание продуктов обмена веществ, выявить качественное и количественное содержание ряда органических соединений. Они позволяют судить о функциональном состоянии почек, мочевыводящих путей, об общих метаболических процессах, наличии инфекционных и воспалительных процессов.
О развитии воспалительных и инфекционных процессов в почках и мочевыводящих путях можно предположить по следующим показателям. Изменение прозрачности и цвета мочи до белесого оттенка или наличие белого осадка могут свидетельствовать о присутствии лейкоцитов, бактерий, грибов. Сдвиг кислотно-щелочной реакции мочи в щелочную сторону (рН 7,0-9,0) связан с инфекцией мочевыводящих путей, происходит он по причине того, что микроорганизмы гидролизуют мочевину.
Увеличение количества лейкоцитов, реже эритроцитов, в общем анализе мочи и при микроскопическом исследовании мочевого осадка является важным показателем поражений почек и мочевыводящих путей. В норме в моче здоровых людей встречается незначительное количество лейкоцитов. При лабораторном исследовании мочи выделяют два состояния: лейкоцитурию и пиурию, которые являются важнейшими патологическими признаками воспаления почек и мочевыводящих путей. Лейкоцитурия – это повышенное содержание лейкоцитов при сохранении прозрачности мочи. Пиурия отражается помутнением мочи и наличием лейкоцитов во всех полях зрения при микроскопии осадка мочи. Появление эритроцитов в моче (гематурия) также может сопровождать инфекции мочевыводящих путей и почек. Например, при пиелонефрите у трети больных может наблюдаться гематурия. Диагностически ценным является обнаружение у больного лейкоцитурии и бактериурии. При микроскопии осадка обнаружение лейкоцитарных, зернистых цилиндров могут быть признаками острого пиелонефрита, обострении хронического пиелонефрита, абсцесса почки.
Повышенное количество бактерий и нитритов в моче свидетельствует о наличии бактериальной инфекции почек и/или мочевыводящих путей. Важно отметить значение данных тестов в скрининговой диагностике хронического пиелонефрита. Это частое заболевание, которое в 30-40 % случаев может протекать бессимптомно, приводя к тяжелому течению, развитию осложнений и сложности подбора эффективного лечения.
У здоровых людей мочевыделительная система стерильна и минимальное количество бактерий с поверхности нижних частей уретры не превышает 1*10 4 /мл. Данное количество бактерий не превращает нитраты, присутствующие в нормальной моче, в нитриты. Следовательно, реакция на нитриты в норме отрицательная.
Бактериурия – это состояние, при котором отмечается содержание бактерий в моче более 1*10 5 /мл. Бактерии, обнаруженные в моче, чаще всего представлены грамотрицательной флорой. Они могут проникать в мочевыводящие пути путем восходящей инфекции или гематогенным путем. К ним относятся микроорганизмы, относящиеся к роду Klebsiella, Proteus, Enterobacter, Salmonella, Pseudomonas, Citrobacter, стафилококки, стрептококки, энтерококки. Часто обнаруживаются Escherichia coli. Восходящая инфекция часто осложняется развитием пиелонефрита. Данное заболевание чаще встречается у женщин, пожилых мужчин. У беременных женщин бактериурия выявляется в пять раз чаще, чем у небеременных. У 70 % беременных причиной пиелонефрита являются бактерии Escherichia coli. Усугублению и развитию восходящей инфекции мочевыводящих путей и почек способствует глюкозурия. Группами риска по развитию пиелонефрита являются больные уретритом, циститом, пиелоциститом, уретеритом, мочекаменной болезнью, пациенты после инструментального и хирургического вмешательства на мочевыводящих путях. В развитии инфекции почек и мочевыводящих путей также могут играть роль дрожжеподобные гриба рода Candida.
Необходимо отметить, что для диагностики бактериурии исследуется средняя порция первой утренней мочи. Важно проводить тщательный туалет наружных половых органов, использовать стерильную посуду для сбора мочи для исключения ложноположительных результатов. Такие бактерии, как гонококки, стрептококки и микобактерии туберкулеза не образуют нитритов. Следовательно, реакция на нитриты в данном случае будет отрицательна. У детей грудного возраста моча не содержит нитритов. Поэтому для подтверждения бактериальной инфекции рекомендуется использовать бактериологическое исследование мочи.
Бактериологическое исследование мочи (посев мочи на микрофлору) с использованием специфических питательных сред рекомендуется взрослым и детям для подтверждения инфекции почек и мочевыводящих путей, для выявления и выделения возбудителя инфекционного процесса. Это микробиологическое исследование, позволяющее определить состав микрофлоры исследуемой мочи, выявить условно-патогенные и патогенные микроорганизмы. Для подбора эффективной терапии против конкретного возбудителя производится последующее определение чувствительности к антибиотикам. При обнаружении микроорганизмов, составляющих нормальную микрофлору, или условно-патогенных микроорганизмов в титре менее диагностического чувствительность к антибиотикам и бактериофагам не определяется, так как это количество не является значимым и не требует лечения противомикробными препаратами.
Для чего используется исследование?
Когда назначается исследование?