Однорядный и двухрядный кишечный шов что лучше
Однорядный и двухрядный кишечный шов что лучше
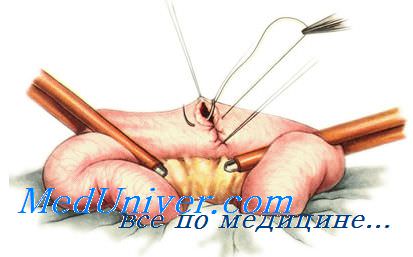
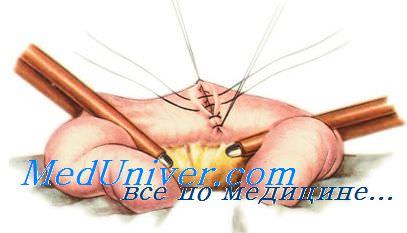
В основе большинства операций на желудочно-кишечном тракте лежит кишечный шов. Под термином «кишечный шов» подразумевают все виды швов, накладываемых на стенку полого органа желудочно-кишечного тракта (пищевод, желудок, кишечник), а также и на другие полые органы, имеющие брюшинный покров, мышечную оболочку, подслизистый слой и слизистую оболочку (жёлчный и мочевой пузырь).
Главные требования к кишечному шву:
— кишечный шов должен быть прочным, т.е. после наложения шва края сшитых органов не должны расходиться;
— кишечный шов должен быть герметичным. При этом следует иметь в виду герметичность механическую, не допускающую вытекания из просвета органа ни капли его содержимого, и герметичность биологическую, не допускающую выхода микрофлоры из полости органа,
— кишечный шов должен обеспечивать хороший гемостаз;
— кишечный шов не должен суживать просвет полого органа;
— кишечный шов не должен препятствовать перистальтике.
Выполнение этих требований возможно только с учётом анатомо-физиологических свойств полых органов брюшинной полости. Первое из них — способность брюшины склеиваться и в последующем срастаться в месте повреждения или при плотном прижатии двух листков друг к другу. Второе — футлярное строение стенки желудочно-кишечного тракта. Различают 4 основных слоя стенки желудочно-кишечного тракта: слизистую оболочку; подслизистый слой; мышечную оболочку; серозную оболочку (на пищеводе — адвентициальную). Первые два слоя отделены от следующих рыхлой соединительной тканью, в результате чего они могут скользить по отношению друг к другу. Это очень заметно при вскрытии просвета полого органа: слизистый и подслизистый слои выворачиваются кнаружи под тягой мышечного слоя. В связи с этим, а также из-за красного цвета слизистой оболочки, вывернутые края разреза кишки называют «губами». Образование «губ» иногда затрудняет чёткую визуализацию каждого слоя при наложении кишечного шва.
Самым прочным является подслизистый слой. Остальные слои, включая мышечный, легко прорезаются даже при небольшом натяжении. Для обеспечения прочности и механической герметичности кишечный шов обязательно должен проходить через подслизистый слой.
В подслизистом слое располагается большинство кровеносных сосудов органа, из-за чего при его рассечении возникает кровотечение. Шов, проходящий через подслизистый слой, должен обеспечивать гемостаз.
Из-за тесной связи подслизистого и слизистого слоев очень трудно при наложении кишечного шва пройти, не задев слизистую оболочку, и, следовательно, не инфицировав шовный материал. Кишечный шов, захватывающий подслизистый и слизистый слои, называется сквозным (шов Черни), он может обеспечить прочность и механическую герметичность, но не обеспечивает герметичности биологической, так как через прокол стенки и вдоль шовной нити микроорганизмы могут выходить из просвета кишки на поверхность брюшины.
Медицинские интернет-конференции
Языки
Сравнительный анализ прочности однорядного и двурядного кишечных швов
Бычков В.Г., Семенова Ю.И., Белая Е.А., Другакова Ю.С., Кузяев Т.Р.
Резюме
Проблема выбора оптимального способа создания анастомоза далека от разрешения и не утратила актуальности на сегодня.В статье описаны биомеханические свойства однорядного и двухрядного швов, используемых для наложения тонкокишечного анастомозов в хирургической практике. Цельисследования – провести литературный обзор и определить механические характеристики кишечных швов.Результаты. Установлено, что однорядный кишечный шов превосходит двурядный по механическим характеристикам. Заключение. Необходимо изучитьбиомеханические характеристики стенки тонкой кишки и тонкокишечного анастомоза в ходе натурного эксперимента.
Ключевые слова
Статья
Научный руководитель: к.м.н., доцент Челнокова Н.О.
Введение
Сегодня стремительно развиваются хирургические технологии – разрабатываются различные видысшивающих аппаратов, шовного материала, методик формирования тонкокишечного соустья, в частности лапароскопических, но использование ручного шва в хирургической практике не утратило значения и в настоящее время [4, 8, 10]. Значительное количество хирургов отдает предпочтение однорядному шву, однако и двурядный шов, до сих пор широко применяется среди российских хирургов [1, 8, 9].
Заживление анастомоза, сформированного при помощи однорядного или двухрядного швов, может протекать с развитием всех признаков альтерации, экссудации и репарации в зоне соустья, т.е. по типу первичного или вторичного натяжения [2, 3, 5-7].В настоящее время в хирургии распространено изучение механических характеристик сосудов, органов, тканей, так как это позволяет оптимизировать выбор шовного материала и метода оперативного вмешательства [13, 14, 15].
Цель исследования – провести обзор отечественныхлитературный источников и определить механические характеристики кишечных швов, сформированных однорядным и двухрядным способом при наложении тонкокишечного анастомоза.
Материалы
Проанализированы научные статьи и монографии, посвященные исследованию однорядного и двурядного швов в эксперименте.
Результаты
Установлено, что однорядныйкишечный шов, наложенный непрерывно, невызывает столь выраженного нарушения микроциркуляции в зоне анастомоза и заживление его происходит обычно первичным натяжением, в отличии от двурядного, с быстройэпителизациейраныи образованием нежного рубца [1, 11, 12]. Одними из основных требований, предъявляемых к кишечному шву являются: асептичность, герметичность, атравматичность и прочность. Последние два зависят от методики наложения тонко-кишечного анастомоза и применяемого шовного материала.
Обсуждения
В ходе эксперимента [7] по изучению механических свойств кишечных швов, выявена закономерность показывающая, что механическая прочность на растяжении у двурядного шва ниже, чем у однорядного, так как разница в силе растяжения между начальным и окончательным прорезыванием шовных лигатур у однорядного шва больше, чем у двурядного. Биологическая проницаемость однорядного шва в отличии от двурядного значительно ниже. При рентген-контрастировании было доказано возможное образование полостей у двурядного шва с дальнейшим возникновением межрядных абсцессов. Заживляемость анастомоза сформированного однорядным швом значительно быстрее с меньшей воспалительной реакцией с отсутствием стенозирования в месте наложения анастомоза [7]. При проведении численного моделирования кишечных швов на толстой кишке, также установлено, что максимальные значения эквивалентных напряжений на стенке кишки при наложении однорядного шва сосредоточены в зоне анастомоза на внешней поверхности стенки, т.е. со стороны серозной оболочки. При конечно-элементном анализе двурядного кишечного шва высокие эквивалентные напряжения наблюдаются как на внешней, так и на внутренней поверхности кишечной стенке в зоне анастомозирования, что как следствие приводит к достаточно высокой степени повреждения кишки [15].
Выводы
Таким образом, необходимо изучитьбиомеханические характеристики стенки тонкой кишки в ходе натурного эксперимента по растяжению тканей с получением точной картины напряженно-деформированного изменения стенки кишки, а такженаложении тонкокишечного анастомоза с использованием однорядного и двурядного шва.
Однорядный и двухрядный кишечный шов что лучше
По отношению к просвету кишки швы делят на непроникающие и проникающие.
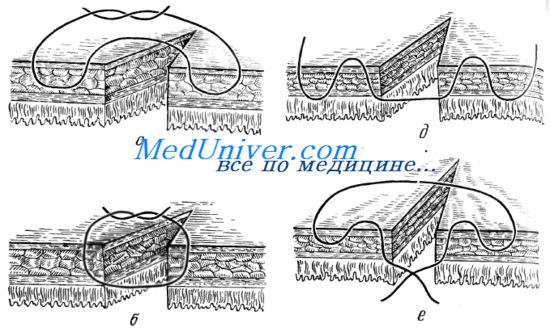
Непроникающими асептическими швами называются такие швы, при которых нить не проникает в просвет кишки. В зависимости от захвата в шов элементов стенки различают: а) серозные швы — захватывается только серозная оболочка (висцеральная брюшина); б) серозно-мышечные швы — захватывается серозная и мышечная оболочки (наружный футляр); в) серозно-мышечно-подслизистые швы — прошивают три наружные оболочки и не прошивают слизистую оболочку.
Проникающими (инфицированными) швами называют такие швы, при которых нить проходит через слизистую оболочку и находится в просвете кишки.
Различают следующие проникающие швы: а) сквозной — шов, при котором нить проходит через все слои стенки кишки; б) мышечно-подслизисто-слизистый; в) подслизисто-слизистый; г) шов слизистой оболочки.
По методике наложения различают такие швы: отдельные узловые; П-образные; непрерывные (накладывают одной длинной нитью); непрерывно-узловые (накладывают двумя концами одной длинной нити, которую после каждого стежка завязывают в узел).
По сопоставлению тканей после затягивания шва различают: краевые швы (в шов проходит край Разреза стенки кишки); вворачивающие швы, обеспечивающие соприкосновение сшиваемых участков серозными оболочками: выворачивающие швы, обеспечивающие соприкосновение сшиваемых участков слизистыми оболочками; комбинированные вворачивающе-выворачивающиеся швы.
По количеству рядов различают: однорядные, двухрядные и трехрядные швы.
По материалу нитей различают: кетгутовые, шелковые, капроновые, лавсановые и другие швы.
Непроникающие швы. Шов Ламбера — отдельный узловой серозно-мышечный шов. Накладывают круглой и тонкой (кишечной) иглой. В качестве шовного материала используют нерассасывающиеся нити (шелк, капрон, лавсан) № 2—4.
Иглу вкалывают и выкалывают на серозной поверхности с каждой стороны раны. В шов захватывают серозную и мышечную оболочки. Расстояние между местами вкалывания и выкалывания иглы не должно превышать 0.5 см. Однако при соединении тканей различной толщины глубина захвата более толстой стенки должна быть большей, чем тонкой. Это может возникнуть при соединении стенки желудка и тонкой кишки, в частности, в том случае, когда стенка желудка гипертрофирована.
После прошивания обеих стенок нить завязывают таким образом, чтобы произошло плотное соприкосновение серозных оболочек, причем узел должен располагаться на менее подвижном краю раны или стенке органа.
Вследствие недостаточной прочности серозной и мышечной оболочек при чрезмерном затягивании узла нить может прорезать ткань. Необходимо помнить, что серозно-мышечные швы Ламбера обеспечивают в основном не механическую прочность, а герметизацию линии шва.
Шов Пирогова — отдельный краевой серозно-мышечно-подслизистый шов. Иглу вкалывают со стороны серозной оболочки и выкалывают на поверхности разреза стенки кишки между подслизистым слоем и слизистой оболочкой. Затем иглу вкалывают между слизистой оболочкой и подслизистым слоем другого края раны и выкалывают на серозной поверхности оболочки. При этом в шов захватывают серозную и мышечную оболочки, а также иодслизистый слой, который обладает наибольшей механической прочностью.
При завязывании узла однородные ткани соприкасаются.
Шов Пирогова — Матешука — отдельный краевой серозно-мышечно-подслизистый внутриузловой шов. Отличается от шва Баришевского-Матешука тем, что в стежок незахватывается слизистая оболочка. Нить проводят со стороны просвета через подслизистый слой, мышечную и серозную оболочки с одной стороны и через серозно-мышечную оболочку и подслизистый слой с другой стороны. Узлы завязывают со стороны просвета.
Шов Мышкина — Долгушина — отличается от шва Пирогова — Матешука тем, что при его наложении нить проводят через мышечную оболочку, подслизистый слой без захвата серозной оболочки. Узел также завязывают со стороны просвета кишки.
Шов Момбурга — представляет собой комбинацию швов Ламбера и Пирогова.
Иглу вкапывают и выкалывают со стороны серозной оболочки, отступив на 1,5 см от края раны, при этом в шов захватывают серозную, мышечную оболочки и подслизистый слой. Затем на расстоянии 0,5 см от края раны иглу вкалывают со стороны серозной оболочки, выкалывают ее со стороны раны между подслизистым слоем и серозной оболочкой. На другом краю раны иглу вкалывают со стороны раны между слизистой оболочкой и подслизистым слоем, выкалывают ее на серозной поверхности кишки, после чего вновь вкалывают и выкалывают со стороны серозной оболочки, проводя иглу несколько глубже мышечной оболочки.
После завязывания узла происходит сопоставление краев раны, а также широкое соприкосновение их серозными оболочками.
Однорядный и двухрядный кишечный шов что лучше
Попытки зашить кишечную рану предпринимались с древних времен. Первые европейские сообщения об анастомозировании кишечной стенки связаны с методикой перчаточников: раны кишечной стенки сшивались сквозным обвивным непрерывным швом, концы нитей не срезались, а выводились через рану брюшной стенки, и сшитый фрагмент фиксировался к париетальной брюшине [2, 8, 9, 13].
В 1812 году Траверс (Travers В.) из клинических и экспериментальных наблюдений за кишечными ранами впервые сделал вывод о том, что техника анастомоза не так важна, как плотный контакт сшиваемых органов по всей окружности. Автор считал предпочтительным соприкосновение серозных поверхностей [2, 4, 8].
В 1824 году Jobert А. предложил узловой однорядный, сквозной инвагинирующий кишечный шов. Кишечный шов, предложенный Lembert А. в 1826 году, был однорядным узловым инвертирующим с узлами на серозе. В клинике он был впервые использован в 1836 году J.F. Dieffenbach для формирования тонкокишечного соустья [3, 4, 13].
Одной из первых модернизаций этого шва был шов Пирогова, об опыте применения которого автор сообщил в 1864 году. Еще не осознавая значимости подслизистого слоя, Н.И. Пирогов описал прецизионный серозно-мышечно-подслизистый экстрамукозный кишечный шов и экспериментально показал макроскопические события при его использовании. В 1887 году Halsted W.S. предложил методику однорядного П-образного шва. Интерес к однорядному шву с новой силой возник в 50–60-е годы после опубликования результатов его применения В.П. Матешуком в СССР и Gambee L. и др. в США. По мнению В.П. Матешука и Е.Я. Сабурова, двухрядная техника шва просто была принята на веру и получила широкое распространение, вполне устраивая большинство хирургов своей удачной симуляцией надежности, прочности и будто бы большей герметичности швов. Эту точку зрения разделяли и другие хирурги, что привело к тому, что в настоящее время во Франции, Швейцарии и Великобритании однорядный шов применяется чаще многорядных методик. С конца 60-х вновь стали появляться работы о применении однорядного непрерывного шва. В 1968 году Johnson S.R. сообщил о 177 гастроэнтероанастомозах после резекции желудка, сформированных однорядным непрерывным швом (ОНШ) с помощью хромированного кетгута. Недостаточности соустий не было отмечено. Улучшение качества шовных материалов привело к достаточно широкому распространению этой техники. Hautefeuille Р. в 1976 году сообщил об 1 % несостоятельности после использования ОНШ на всех отделах желудочно-кишечного тракта, в том числе при пищеводнокишечных и колоректальных анастомозах. В качестве шовного материала использовались синтетические монофиламентные рассасывающиеся материалы. Delaitre и др. в 1977 году сообщил о 101 однорядном непрерывном гастроэнтеростомозе синтетическими монофиламентными рассасывающимися материалами после резекции желудка без единой несостоятельности [6, 8, 9, 12, 13].
Sarin S., Lightwood R.G. и др. в 1989 году сообщили о 5 % несостоятельности после тонко и толстокишечных анастомозов. Использовались синтетические монофиламентные рассасывающиеся материалы. Mickley V. и др. в 1991, используя тот же шовный материал, сформировали 264 анастомоза на тонкой и толстой кишке. Процент несостоятельности составил 0,7 [2, 8, 9].
Demartines N. и др. в 1991 г. сообщили о 96 однорядных непрерывных гастроэнтероанастомозах после резекции желудка с помощью синтетических монофиламентных рассасывающихся материалов. Несостоятельность составила 2,1 %. Thomson W.H.W., Robinson М.Н.Е. и др., 1993, используя ту же технику и те же шовные материалы, на 200 толсто- и тонкокишечных анастомозов получили 4 (2 %) несостоятельности. Ceraldi СМ. и др., 1993 на 44 толстокишечных анастомоза однорядным непрерывным полипропиленовым швом сообщили о несостоятельности 6,8 %. Для сравнения авторы приводят цифру 9,5 % несостоятельностей для двухрядного шва. Егиев В.Н. и др., 1993 г. и Егоров В.И. и др., 1995 г., соответственно для 123 и 157 гастроэнтероанастомозов, сформированных ОНШ Chittmittrapap S. и др., 1993, на 121 однорядный непрерывный гастроэнтероанастомоз синтетическим монофиламентным рассасывающимся материалом (СМРМ) отметил 1 несостоятельность (0.8 %). Houdart R., 1994, сообщил о 464 однорядных непрерывных анастомозах на всех отделах желудочно-кишечного тракта с помощью СМРМ с несостоятельностью 0,7 %. Буянов В.М. и др., 2000, сообщили о 3605 анастомозах ОНШ в хирургии желудочно-кишечного тракта, желчных путей и поджелудочной железы с помощью синтетических моно- и полифиламентных рассасывающихся материалов и полипропиленом. Процент несостоятельности при гастроэнтеро- и энтероэнтеростомии равнялся 0,04, в колоректальной хирургии – 1,8, в хирургии желчных путей и поджелудочной железы – 0. Маскин С.С. и др., 2001 опубликовали данные об успешном применении ОНШ рассасывающимися шовными материалами при геморроидэктомии у 50 больных [1, 2, 3, 7, 9, 11].
Настоящим испытанием для любой хирургической техники является ее применение в экстренных условиях и в колоректальной хирургии. Сравнение результатов экстренных резекций желудка и тонкой кишки, выполненных с применением однорядного непрерывного и двухрядного швов, показало значимые преимущества первого [2, 3]. Низкий процент осложнений при использовании ОНШ в хирургии толстой и прямой кишки также является весомым доказательством его надежности. История проблемы, виды и способы кишечных швов с помощью синтетических моно- и полифиламентных рассасывающихся материалов, не отметили несостоятельностей. Экспериментальные исследования, проведенные на животных, во многом объяснили результаты применения ОНШ, обнаружив минимальные нарушения микроциркуляции, невыраженные воспалительные и рубцовые изменения в области соустья при использовании этого метода.
Несмотря на значительные успехи современной абдоминальной хирургии, одним из тяжелейших осложнений в раннем послеоперационном периоде после резекций и реконструктивных операций на полых органах брюшной полости является несостоятельность швов анастомоза. По данным разных авторов, колеблется от 3 до 32,1 % с летальностью, достигающей от 5,7 до 89,0 % [1,8, 9]. При наличии внутрибрюшной инфекции частота несостоятельности кишечных швов возрастает в 2 раза. Основными причинами развития этого тяжелого послеоперационного осложнения считают: высокое внутрипросветное давление, нарушение микроциркуляции и биоэнергетики кишечной стенки, гипоксию ее тканей, инфицирование брюшной полости и колонизацию просвета кишечника высоковирулентной микрофлорой [8, 9, 10, 11].
Несмотря на разработки, в этой проблеме до настоящего времени, ряд положений еще не изучен в достаточной степени. Не выяснено влияние на качество кишечного шва травмы слоев кишечной стенки и состояния кровообращения в краях раны при различном ходе лигатуры в области шва.
В связи с этим только лишь совершенствование способа наложения кишечного шва или формирования анастомоза не является единственным условием достижения успеха в решении этой сложной проблемы.
Поэтому одни авторы «за», другие категорически «против» формирования первичного анастомоза после резекции кишечника в условиях непроходимости и перитонита [2-6, 8, 9].
Вместе с тем известно, что существенное значение в профилактике несостоятельности кишечного анастомоза имеют: правильный выбор шовного материала и способа повышения механической прочности и биологической герметичности соустья, использование эффективных способов декомпрессии, лаважа и дренирования не только просвета кишечника в целом, но и селективной внутрипросветной декомпрессии и деконтаминации шовной линии анастомоза, продолжая при этом энтеральную терапию и интенсивное лечение перитонита [8- 12].
На сегодняшний день проблеме кишечных швов посвящено большое количество исследований (преимущественно в медицинской хирургии). Многообразие видов кишечного шва – более 450 (В.Н. Егиев, 2002) и появление новых методов его наложения (аппаратный шов, использование компрессионных устройств, клеевых композиций и т.п.), свидетельствует об известной неудовлетворенности хирургов достигнутыми результатами.
Современные новинки биотехнологий успешно реализованы сегодня в области клеточной медицины, биохимии высоких молекулярных соединений, биофизики и общей хирургии.
Эффективность лечения многих заболеваний и восстановительные процессы утраченных функций организма принадлежат в настоящее время открытиям новейшей биоинженерии. Учеными разработаны уникальные реконструктивные биоматериалы, позволяющие значительно повысить уровень и качество жизни пациентов. Особое значение в сфере общей хирургии приобретают биодеградируемые ультратонкие матриксы, которые представляют собой термопластичные полимеры, совместимые с организмом человека. Их использование становится все более актуальным в области трансплантологии, тканевой и клеточной медицины во всех высокоразвитых странах мира. Образцы изделий на основе ПГА (полигидроксиалконоаты) содержат высокоочищенную структуру, идеальную для биохирургического назначения. В качестве матрикса представлены ультратонкие прочные пленки, эффективные для заживления гнойных ран и других тканевых повреждений.
Биодеградация вследствие внедрения материала зависит от химического состава биополимера, особенностей его формы и места имплантации в организме. В настоящее время разработано более 100 видов ПГА различного химического и физического состава. Их главными преимуществами являются остеопластичность, биоинертность, отсутствие токсических реакций, вывод продуктов метаболизма и медленная деградация. Биологические полигидроксиалконоаты и их качества определяются:
Интеграция биоискусственных изделий с живыми клетками имеет важное значение для пациентов с дефектами различного происхождения и стоит главной задачей создания эффективных биологически совместимых материалов. Несмотря на ультратонкие моножильные волокна, матриксы обладают высокой степенью прочности (306 МПа) и упругости (3ГПа).
Внедренные в организм биодеградируемые ультратонкие матриксы, как и любые другие инородные фрагменты, капсулируются, отделяясь от живых клеток соединительной тканью. То есть немедленно активизируются процессы, защищающие организм от инородного тела. Время физического заживления – величина переменная и зависит от многих факторов, причин и характера протекания болезни.
I этап – внедренный матрикс покрывается слоем лейкоцитов, стимулируя свертываемость крови;
II этап – происходит миграция фибропластов к месту имплантации, образуя гранулему;
III этап – дифференцирование фибропластов в фиброциты;
IV этап – выработка коллагена.
На ускорение регенеративных функций организма во время лечения биоматериалами оказывает влияние термопластичность и гидрофобность матриксов ПГА, а также высокие свойства адгезии, биоразрушаемости и биосовместимости с клетками тканей человека. Полигидроксиалконоаты со временем не теряют своих свойств и не вызывают аллергических реакций. Стерилизация материалов ПГА возможна любыми традиционными способами:
— сухая обработка нагреванием (170 градусов);
— автоклавирование в дезинфицирующем растворе (120 градусов);
— воздействие ультрафиолетом и гамма-облучением;
— очистка через стерильный, пористый фильтр (поры 0,2 мкм);
— химическая обработка – 70 % спирт как очищающий реагент;
— ЕТО – использование газа оксид этилена (время 3–7 дней).
Лидирующим и самым хорошо изученным из представителей ПГА является полигидроксибутират ПГБ – полимер с высококристаллической структурой. Этот материал обладает отличной биосовместимостью и присутствует в тканях организма в качестве продуктов распада. С помощью разработок нанотехнологий получены особо тонкие крепкие волокна разного диаметра, сформированные в нетканые матриксы. Важным показателем для идеальной биологической совместимости полимерных материалов является структура их поверхности из полилактида (шероховатость, фазовый и химический состав). Понятие «полимер» состоит из двух основ – «поли», что значит много и «мера» – единица. Таким образом, полимер представляет собой сложную структурированную молекулу, состоящую из большого количества различных элементов.
Физико-химические параметры ПГА:
По свойствам термопластичности полигидроксиалконоаты похожи на синтетические виды полимеров, таких как полиэтилен, полипропилен и т.п.
Механические свойства видов ПГА:
— Упругость и твердость;
— Эластичность (резиноподобные качества);
— Степень кристаллизации материала меняется по прохождении времени. Безопасность использования биодеградируемых материалов. С 1999 года в Российской Федерации введен ГОСТ по «Оценке биологического воздействия медицинских изделий», а в 2007 году вышел Приказ Министерства здравоохранения «Об утверждении… выдачи разрешений на использование новых медицинских технологий». В целях контроля над степенью потенциального риска разработана государственная официальная специализированная классификация рисков.
Технические методы изготовления имплантируемых пленок основаны на создании абсорбируемых конструкций для культивирования клеток живого организма, поврежденных в результате травмы или болезни. Биодеградируемые ультратонкие матриксы – это своеобразные каркасы, задающие рост клеткам для образования будущих тканей. Матрикс-каркас состоит из сетки макропор (более 100 мкм в диаметре), соединенных друг с другом, и действует внутри ткани в трех измерениях. Идеальная структура матрикса должна эффективно стимулировать ангиогенез (формирование кровеносных сосудов) и содержать нетоксичные продукты процесса метаболизма. Биоматериал активизирует клетки для создания самогенерации и нормализации функции вывода и доставки веществ. Кроме того, все механические характеристики матрикса должны соответствовать свойствам «живой» ткани. Биологические функции ПГА обеспечивают разрушение установленных межклеточных контактов в структуре поврежденной ткани. Рассасывание пленок биоискусственного имплантанта происходит именно тогда, когда регенерируется достаточное количество клеток организма хозяина.
Успешные результаты внедрения созданных полимеров стали научным феноменом в лечении многих хирургических заболеваний! Благодаря развитию высоких биотехнологий и прогрессивному мировоззрению наших врачей, использование биологических матриксов в России становится все более актуальным методом лечения сложных травматических повреждений.
Развитие современной науки в области биотехнологий привело к эффективному применению высокомолекулярных полимеров различной природы происхождения. Это позволило охватить широкий диапазон ценных методик лечения в различных направлениях медицины.
Биодеградируемые ультратонкие матриксы ПГА открыли для современной хирургии новый, более совершенный уровень фундаментальных основ и профессиональных знаний о взаимодействиях биоматериалов с клетками человека!
А.В. Шотт, А.А. Запорожец и др. (1994) считают, что «каждый хирург с большим и средним опытом практической работы подобрал для себя определенный вид кишечного шва, освоил его и применяет с определенным удовлетворением». В таких условиях хирург не видит и не знает, что происходит в зоне наложенного им кишечного шва и не может оценить критически своих действий, в то время как положительные результаты часто достигаются лишь благодаря защитным механизмам организма. Следовательно, сущность кишечного шва необходимо оценивать не только с практических, но и с теоретических позиций [8, 9].
В настоящее время в абдоминальной хирургии по-прежнему доминируют разновидности ручного шва. При этом среди хирургов растет число сторонников применения однорядного его варианта. Они считают, что увеличение числа рядов шва не снижает риска его несостоятельности [2, 6, 8, 9].
Поэтому для существенного улучшения ближайших и отдаленных результатов необходимо не только приобретение и усовершенствование мануальных навыков, но и применение современных, более «физиологичных» схем и методов оперативного вмешательства.
Такого же правила следует придерживаться при ушивании лапаротомных ран, осложнения при заживлении которых (эвентрации, послеоперационные грыжи и т. д.) в большинстве случаев связаны с упущениями при наложении швов и выборе шовного материала. Несостоятельность швов на брюшной стенке может не только осложнить состояние пациента, но и «свести на нет» успех любой операции.
Выбор шовного материала определяется хирургическим замыслом и, соответственно, к нему предъявляются определенные требования. В настоящее время на мировом рынке появился широкий выбор современных шовных материалов, вплоть до специализированных нитей, предназначенных для конкретных хирургических вмешательств. К сожалению, хирурги недостаточно информированы о видах шовных материалов и возможностях их применения.
Разнообразные и нередко противоречивые литературные данные о достоинствах и недостатках тех или иных швов и шовных материалах свидетельствуют о постоянном и неослабевающем интересе хирургов к данной проблеме [2, 8].