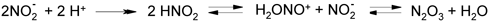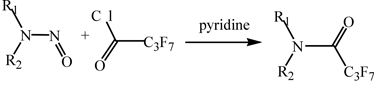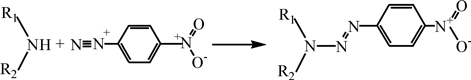Нитрозамины что это такое
Нитрозамины
Нитрозамины (нитрозоамины) — органические соединения с общей формулой R1R2NNO, где R1, R2 — алкильный или арильный радикал. Известны также нитрозоамиды RN(X)NO, где X = CONH2, CO2R.
Содержание
Получение
Синтез нитрозаминов осуществляется введением нитрозо-группы во вторичные амины или амиды следующими реагентами:
Нитрозамины получают также реакцией вторичных аминов с нитритом натрия и формальдегидом или хлоралем:
Строение
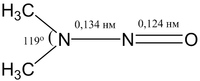
Атомы водорода в молекулах нитрозаминов располагаются в одной плоскости. Строение молекулы простейшего органического нитрозамина (CH3)2NNO следующее:
Вращение по N-N связи сильно затруднено большим энергетическим барьером ΔG ≠ = 75-160 кДж/моль).
В ультрафиолетовом спектре присутствуют 2 полосы λмакс = 360 нм (n→π переход, ε
100) и λмакс = 230—255 нм (n→π переход, ε
В ИК-спектре различаются 2 характеристические полосы для N=O связи (1430—1530 см −1 ) и N-N связи (
Физические и химические свойства
Первичные нитрозамины (R1 = H) малоустойчивые вещества, стабильны только при температурах ниже 0 o C.
Нитрозамины являются жидкими или твёрдыми веществами жёлтого цвета, в индивидуальном виде малоустойчивы. Хорошо растворимы в воде и многих органических растворителях.
При действии восстановителей (водород на платине, палладии, LiAlH4) нитрозамины превращаются в производные гидразина. Действие более жёстких восстановителей (водород на никеле Ренея, амальгама натрия) на нитрозамины сопровождается разрывом N-N связи с образованием вторичных аминов.
Азотная и перфторпероксоуксусная кислоты окисляют нитрозамины в соответствующие N-нитрамины. Ангидриды органических кислот ацилируют нитрозамины, при этом происходит разрыв N-N связи. Действие хлороводорода также приводит к разрыву N-N связи.
К разрыву N-N связи и образованием радикала R2N· приводит и фотолиз нитрозаминов в парогазовой фазе.
В жидкой фазе в кислой среде нитрозамины способны фотолитически присоединяться к алкенам:
Применение
Нитрозамины применяют для извлечения вторичных аминов из смесей, а также в синтезе некоторых лекарственных препаратов и органических красителей. В лабораторных синтезах нитрозамины применяют для получения диазоалканов.
Биологическая роль
Нитрозамины являются высокотоксичными соединениями. При попадании в организм они поражают печень, вызывают кровоизлияния, конвульсии, могут привести к коме. Большая часть нитрозаминов обладает сильным канцерогенным действием даже при однократном действии, проявляют мутагенные свойства. Напротив, N-нитрозо-N-метилмочевина обладает противоопухолевой активностью.
Литература
Полезное
Смотреть что такое «Нитрозамины» в других словарях:
НИТРОЗАМИНЫ — (N нитрозоамины), соед. общей ф лы RR NNO (R, R = Alk, Ar). Первичные Н. (R = Н) существуют лишь при т ре ниже О °С. Известны также N нитрозоамиды общей ф лы RN(X)NO (X = CONH2, CO2Alk и др.). Н. жидкости или твердые в ва желтого цвета (см.… … Химическая энциклопедия
Косметика — Косметичка и косметические принадлежности Косметика (греч. κοςμητική «имеющий силу приводить в порядок» ил … Википедия
нитрозирование — введение в молекулу органического соединения нитрозогруппы N=O действием азотистой кислоты HNO2, её эфиров RONO или др. При нитрозировании образуются нитрозосоединения, нитрозамины R2NNO, оксимы R2CNOH. * * * НИТРОЗИРОВАНИЕ НИТРОЗИРОВАНИЕ,… … Энциклопедический словарь
нитрозосоединения — органические соединения, содержащие одну или несколько нитрозогрупп N=O. Получают нитрозированием. Применяются как нитрозокрасители, аналитические реагенты, в органическом синтезе, в производстве термостойких каучуков. N–Нитрозосоединения… … Энциклопедический словарь
Презерватив — Мужской презерватив Презерватив (фр. préservatif, от позднелат. praeservo предохраняю), также кондом (фр. condom) средство контрацепции … Википедия
НИТРОЗИРОВАНИЕ — введение в молекулу органического соединения нитрозогруппы N О действием азотистой кислоты HNO2, ее эфиров RONO или др. При нитрозировании образуются нитрозосоединения, нитрозамины R2NNO, оксимы R2CNOH … Большой Энциклопедический словарь
НИТРОЗОСОЕДИНЕНИЯ — органические соединения, содержащие одну или несколько нитрозогрупп N=О. Получают нитрозированием. Применяются как нитрозокрасители, аналитические реагенты, в органическом синтезе, в производстве термостойких каучуков. N Нитрозосоединения… … Большой Энциклопедический словарь
КАНЦЕРОГЕННЫЕ N-НИТРОЗАМИНЫ. ТОКСИЧЕСКИЕ СВОЙСТВА, ОБРАЗОВАНИЕ, ОПРЕДЕЛЕНИЕ
(Обзор литературы)
Институт экогигиены и токсикологии им. Л.И. Медведя, г. Киев
В последнее десятилетие увеличивается загрязнение окружающей среды вследствие интенсивной технологической деятельности человека [1]. Расширение использования азотсодержащих удобрений и пестицидов, увеличение выбросов в атмосферу окислов азота, аммиака, аминов приводит к увеличению количества связанного азота в биосфере. Особенно нежелательно загрязнение различных объектов соединениями, обладающими высокой токсичностью, канцерогенными и мутагенными свойствами [1, 2]. К веществам такого типа относится большая группа N-нитрозосоединений, из которых высокой токсичностью и канцерогенностью обладают алифатические и некоторые циклические N-нитрозамины (НА) [3—5].
Считается, что основными источниками НА являются вторичные амины. Однако, при определенных рН среды первичные, третичные и даже четвертичные амины могут образовывать НА. Основным источником образования НА в резиновой промышленности являются ускорители вулканизации на основе вторичных аминов. Обладая высокой термолабильностью и имея в молекуле активные группы, ускорители подвергаются распаду в процессе вулканизации резиновой смеси с образованием аминов. К таким соединениям относятся все классы ускорителей, применяющиеся в резиновой промышленности: тиурамсульфиды, дитиокарбаматы, сульфенамиды, четвертичные аммониевые соли, доноры серы [6].
Физические свойства нитрозаминов
7000—8100) и 330—350 нм ( e
Определены длины связей в алифатических НА. Так, в НДМА длина связи N—O составляет 0,123 нм, а N—N 0,134 нм, вместо 0,145 нм для N—N связей в соединениях, где оба атома азота связаны с углеродом. Энергия разрыва связи N—N в НДМА составляет около 55 ккал/моль, что выше, чем в нитродиметиламине [10].
НА обладают достаточно высокой стабильностью, превышающей устойчивость нитродиалкиламинов. Они не расщепляются растворами щелочей и разбавленных кислот и почти не подвергаются разрушающему действию рассеянного света. Эти свойства НА предопределяют их длительное присутствие в окружающей среде.
Дипольный момент ряда алифатических НА составляет 3,9—4,4 Д, что свидетельствует о полярности их молекул.
НА образуются главным образом в результате реакции нитрозирования. Нитрозирующими агентами являются производные азотистой кислоты (HONO): XNO, где Х — галоген; NO; NO2; OH2 + ; OR; а также нитрозоний-катион [8]. Нитрит-ион и свободная HNO2 в кислой среде претерпевают превращения в активные нитрозирующие агенты:
При низких рН возможно образование нитрозоний-катиона:
В присутствии галогенводородных кислот HNO2 может образовывать нитрозил-галогениды:
HNO2 + HC1 > NOC1 + H2O
Нитрозирующие агенты в порядке убывания своей активности могут быть расположены в ряд:
В качестве нитрозируемых соединений могут выступать различные моно-, ди- и полиамины, а также другие азотсодержащие вещества. Вторичные амины являются прямыми предшедственниками НА. Нитрозирование различными агентами происходит в широком температурном интервале в воде, смесях воды с органическими растворителями, в органических растворителях, газовой фазе, а также непосредственно в объектах. Нитрозирование вторичных аминов в присутствии некоторых альдегидов (формальдегида) протекает в щелочной среде.
Содержащиеся в воздухе N2O3 и N2O4 способны взаимодействовавть со вторичными аминами с образованием соответствующих НА. Все эти реакции протекают в широком интервале рН.
Скорость взаимодействия вторичных аминов с нитритами в слабокислых растворах пропорциональна концентрации амина и квадрату концентрации азотистой кислоты. Кислотность среды играет двоякую роль при нитрозировании аминов. С одной стороны, ее увеличение повышает концентрацию более сильного нитрозирующего агента NO+, с другой — снижает концентрацию активной (непротонированой) формы амина и оказывает ингибирующее действие. Такое эффект в меньшей степени проявляется в случае слабоосновных аминов, когда даже при значительных избытках кислоты часть амина может существовать в непротонированной форме и на неё действует сильный нитрозирующий агент. Скорость образования НА из аминов снижается в следующем ряду: морфолин —> пирролидин —> пиперидин —> диметиламин —> диэтиламин —> ди-н-пропиламин —> ди-изо-пропиламин.
Следует отметить, что замедление реакции нитрозирования происходит при понижении рН в результате превращения аминов в малоактивные протонированные формы. С другой стороны, реакция может быть ингибирована путем превращения нитрозирующих агентов в малоактивную окись азота. В этом отношении весьма активна аскорбиновая кислота и ее производные [12] в широком интервале рН. Однако действие аскорбиновой кислоты ограничено только гидрофильной средой. В гидрофобных средах рекомендуется использовать токоферолы и другие полифенолы [13].
Двуокись серы и бисульфит-ион, гидроксиламин, различные гидразины, азид натрия и некоторые другие восстановители восстанавливают нитрозирующие агенты в окись или закись азота. Некоторые спирты (этанол, этиленгликоль), углеводы (глюкоза, сахароза) и другие соединения, содержащие гидроксильную группу, ингибируют образование НА, превращаясь в соответствующие алкилнитриты [8]. Мочевина и сульфаминовая кислота также дезактивируют нитрозирующие агенты [14]. Эффективным способом дезактивации нитрозирующих агентов является связывание их в неактивные диазосоединения по реакции диазотирования первичных ароматических аминов [15].
Для синтеза НА могут быть использованы реакции перенитрозирования. Особый интерес эти реакции представляют в связи с тем, что они могут протекать и в организме человека. При этом в качестве нитрозирующих агентов способны выступать различные нитрозосоединения, в которых канцерогенные свойства отсутствуют или выражены слабо, а в результате перенитрозирования могут образовываться активные канцерогенные нитрозамины [8]. К таким соединениям относятся гетероциклические и ароматические соединения, замещенные мочевины и уретаны. В реакциях перенитрозирования эффективны также нитрозопиперазины.
Химические свойства НА
Реакции денитрозирования НА имеют большое значение как в аналитической химии, так и в токсикологии, поскольку в результате таких превращений образуются менее токсичные соединения — вторичные амины. В разбавленных минеральных кислотах (рН
1) нитрозамины устойчивы и перегоняются без разложения. Увеличение концентрации кислоты, а также нагревание реакционной смеси и введение катализаторов, например, хлорид-, роданид или тиоцианат-ионов, ускоряют процесс расщепления N—N связи:
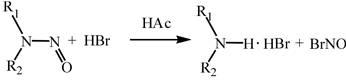
Наиболее легко денитрозирование НА инициируется и протекает растворами бромистоводородной кислоты в среде ледяной уксусной кислоты. Небольшое количество воды или спирта резко снижает выход вторичного амина. Смеси ледяной уксусной кислоты с фосфорной кислотой (или серной), содержащие иодид- или бромид-ионы, а также растворы бромистоводородной кислоты в уксусном ангидриде могут денитрозировать нитрозамины в присутствии воды.
Взаимодействие НА с окислителями ведет к образованию соответствующих нитраминов. Окисление НА без разрыва связи N—N осуществляют с помощью перкислот, из которых наиболее пригодна трифторперуксусная, получаемая непосредственно в реакционной смеси из трифторуксусной кислоты. К аналогичным результатам приводит действие пентафторбензойной кислоты, смеси персульфата аммония с азотной кислотой, а также электрохимическое окисление. При действии бихромата калия или перманганата калия в концентрированной серной кислоте, озона и др. на нитрозамины, связь N-N расщепляется.
При взаимодействии с восстановителями НА главным образом, либо превращаются в несимметричные гидразины, либо происходит расщепление N—N связи. В кислой среде цинк восстанавливает нитрозамины до соответствующих диалкилгидразинов, те же соединения получаются при действии LiAlH4, KOH в присутствии алюминия, T1C13, амальгамы натрия, а также при электрохимическом восстановлении. При использовании восстановителя никеля Ренея в кислом растворе СuC1 или FeC12, смеси никеля, алюминия и едкого кали, амальгамы алюминия, азида натрия и др., образуются вторичные амины. В результате восстановления НА, кроме гидразинов, вторичных аминов, могут образовываться также тетраалкилтетразены [8].
Делокализация электронной пары атома азота нитрозогруппы предопределяет их склонность к реакциям с образованием О-комплексов при взаимодействии с BF3, PC15, SbC15, ALC13 и др. [10]. Нитрозамины вступают в реакцию с рядом алкилирующих агентов — алкилгалогенидами, диметилсульфаматом, триэтилаксооний фтороборатом и др. Описаны реакции НА с металлорганическими соединениями — реактивом Гриньяра [8].
Токсическое действие на организм
НА обладают высокой токсичноcтью по отношению к печени и почкам. Наиболее токсичным является диметилнитрозамин. Многие НА обладают высокими мутагенными свойствами, а также широким спектром канцерогенного действия и могут вызывать образование опухолей печени, почек, желудка, пищевода, легких, мочевого пузыря, трахеи, гортани, носовой полости.
Значительную роль в эндогенном синтезе НА играют микроорганизмы, превращаюшие нитраты в нитриты, различные азотосодержащие вещества в амины. По результатам определения дозы нитрозамина, вызывающего образование 50% опухолей у животных, рассчитана относительная канцерогенная активность НА.
Установлено, что канцерогенное действие оказывают не сами нитрозамины, а продукты их метаболизма, образующиеся под воздействием ферментов.
Действие НА на организм обусловлено реакцией алкилирования ДНК продуктами их метаболизма, что ведет к нарушению функционирования генома клетки. Считается, что для возникновения опухолей и мутагенного эффекта существенным является алкилирование гуанина ДНК в положении О(6), что ведет к нарушению передачи генетической информации.
Методы определения нитрозаминов
Основными требованиями, предъявляемыми к методам определения НА, являются высокая чувствительность, селективность и достоверность полученных результатов [17]. Определение НА в объектах окружающей среды обычно включает в себя следующие стадии: выделение, концентрирование, очистку концентрата, получение производных, их хроматографическое разделение, идентификацию и количественное определение. Для идентификации и количественного определения НА часто применяется газожидкостная хроматография с различными детекторами: пламенно-ионизационным, термоионным, кондуктометрическим, микрокулонометрическим [17]. Для разделения используются набивные и капиллярные колонки.
Для наиболее токсичных нитрозодиметиламина и нитрозодиэтиламина характерно слабое удерживание, что является существенным ограничением метода газожидкостной хроматографии при их определении без дериватизации [20]. Это обстоятельство обусловило широкое распространение методов определения НА после их превращения в более гидрофобные дериваты с большей молекулярной массой [8]. Описано определение НА после окисления их в соответствующие нитроамины. Эффективным оказалось прямое превращения НА в галогенсодержащие производные посредством гептафторбутирилхлорида или гептафтормасляного ангидрида:
Однако наибольшее распространение в аналитической химии НА нашел подход, заключающийся в предварительном денитрозировании НА с последующим определением образовавшихся вторичных аминов с использованием богатого арсенала дериватизирующих реагентов, известных для определения аминов. Ниже рассмотрено применение этой схемы на примере реагентов, оказавшихся наиболее эффективными.
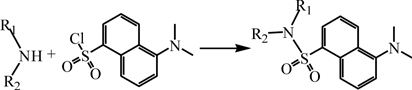
Первым отметим метод с использованием дансилхлорида [21, 22]:
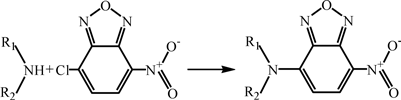
Вместо дансилхлорида для хромато-масс-спектрометрического определения НА можно использовать 7-хлор-4-нитробенз-2-окси-1,3-диазол (НБД) [24]:
В масс-спектрах НБД-производных НА имеются интенсивные молекулярные и характеристические осколочные ионы. Возможности этого метода аналогичны методу с применением дансилхлорида, но НБД имеет определённые преимущества перед дансилхлоридом, поскольку НБД-дериваты не только флуоресцируют, но и интенсивно окрашены в желтый, оранжевый или розовый цвета, а сам реагент не флуоресцирует и не образует флуоресцирующих производных с фенолами и спиртами.
Предложен аналогичный метод определения НА в виде флуоресцирующих производных с N-(8-метокси-5-хинолинсульфонил)азиридином [25]. Однако, он по ряду характеристик (недостаточно хорошее разделение производных, сложность хроматографирования и др.) уступает методу с НДБ-хлоридом.
Показана эффективность определения НА после дериватизации соответствующих вторичных аминов 4-нитрофенилдиазонием [26].
Полученные нитрофенилтриазены хорошо окрашены и гидрофобны, они легко могут быть сконцентрированы, разделены методом ВЭЖХ и продетектированы на фотометрическом детекторе.
Таким образом, анализ данных литературы указывает на необходимость более глубокого подхода к проблеме токсичных канцерогенных НА. Необходим дополнительный анализ путей попадания НА в организм человека. Это позволит более дифференцировано подойти к нормированию НА в различных объектах. Необходимо также уделить больше внимания проблеме контроля предшественников НА — аминов, нитрозирующих агентов, а также катализаторов и ингибиторов нитрозирования. Такие исследования способствовали бы, во-первых, сокращению списка продуктов, подлежащих токсикологическому контролю, во-вторых, существенному уменьшению затрат на проведение химических анализов и, в-третьих, расширению сети лабораторий, способных проводить токсикологический контроль, поскольку он стал бы возможен без привлечения уникального дорогостоящего оборудования.
Нитрозамины
СТАЙЛАБ предлагает стандарты нитрозаминов для их анализа в продуктах питания хроматографическими методами.
Для расчета допустимой суточной дозы примесей нитрозаминов, не указанных в таблице, рекомендуется следовать принципам, изложенным в руководстве ICH’s M7 (R1). Эти лимиты применяются лишь тогда, когда лекарственное средство содержит только один нитрозамин. Если более чем одна примесь из таблицы детектируется, и общее количество примесей превышает 26,5 нг/сутки, то необходимо известить об этом регуляторные органы. Допустимые границы потребления для новых нитрозаминов составили 0,16 частей на миллион (ppm) для MNP в рифампинине и 0,1 ppm для CPNP в рифапентине. Почему указаны значения временные?Потому что, согласно со стратегией Европейской Фармакопеи, эти лимиты будут действовать только в течение переходного периода в 2 года (до 1 апреля 2021), который предоставлен для изменения производственных процессов с целью снижения содержания нитрозаминов. Препараты, содержащие концентрации выше указанных, не могут находиться в обороте. После завершения переходного периода нитрозамины должны отсутствовать в фармацевтических препаратах. Уровни NDMA или NDEA в активных субстанциях должны «не поддаваться количественному измерению» после 1 апреля 2021 года. Фактически, конечная концентрация нитрозаминов, которая допускается до апреля 2021, высчитывается из максимальной суточной дозы препарата и значения допустимой суточной дозы примеси. Вот, например, для максимальной суточной дозы 1200 мг и допустимой суточной дозы в 26,5 мкг LOQ метода определения должен составлять не более 0,02 мг/кг, или 20 ppb. Аналогичные расчеты для NDMA в метформине с суточной дозой 3000 мг и 96 мкг NDMA дают цифру в 30 ppb. Если суточная доза продукта составляет менее 880 мг/день, то лимит для суммарного содержания нитрозаминов не должен превышать 0,03 ppm. Согласно отраслевого руководства FDA, производители АФИ и готовых продуктов должны использовать только методы с LOQ ≤ 0,03 ppm, но при этом надо учитывать, что, например, для того же метформина после разведения препарата в растворителе и подготовки образца конечная концентрация NDMA в виале не должна превышать 1,6 ppb, что делает требования к чувствительности методики определения в готовых продуктах значительно жестче, чем это может показаться на первый взгляд. С другой стороны, соответствующие расчеты для сырья и растворителей наоборот — показывают меньшие требования к чувствительности определения. Были опубликованы рекомендации всем владельцам лицензий на продажу лекарственных препаратов, которые коротко можно изложить следующим образом: Компаниям рекомендуется провести следующие шаги: С 1го октября 2020 все операторы фармацевтического рынка должны систематически включать оценку рисков в отношении потенциального возникновения нитрозаминов. Также 1 сентября 2020 года FDA опубликовала отраслевое руководство по контролю содержания примесей нитрозаминов в лекарственных препаратах для людей, в котором рассматриваются основные причины возникновения нитрозаминовых примесей и даются рекоммендации всем производителям лекарственных препаратов. Начиная с 2018 года многие международные организации работали над надежными и чувствительными методами определения нитрозаминов в фармацевтической продукции. Сейчас Европейский директорат по качеству лекарственных средств и охране здоровья опубликовал ряд методов, размещенных на их сайте и разработанных Официальными лабораториями контроля лекарственных средств (OMCL) Общеевропейской сети OMCL (GEON). Итогово они приведены в таблице 2. Таблица 2: Методики контроля, опубликованные сетью официальных лабораторий контроля лекарственных средств (OMCL).
80 ppb NDEA LGL method | LC-MS/MS | NDMA и NDEA | irbesartan, valsartan, and losartan | 79-492 ppb NDMA | 19,5-149 ppb NDEA Swissmedic | GC-MS/MS | NDMA, NDEA, EIPNA, DIPNA, DPNA, DBNA | valsartan, losartan, irbesartan, olmesartan and candesartan | 15 ppb | CVUA Karlsruhe | UHPLC-APCI-MS/MS | NDMA и NDEA | sartan drug substances and drug products | 100-200 ppb NDMA | 40-80 ppb NDEA CVUA Karlsruhe | UHPLC-APCI-MS/MS | NDMA | valsartan | 200 ppb NDMA | PALG method | Headspace GC-MS | NDMA | tablets of the sartan group | Not stated | ANSM method | HPLC-UV | NDMA и NDEA | valsartan, losartan, irbesartan, candesartan and olmesartan | 40-250 ppb NDMA | 80-500 ppb NDEA ANSM method | HPLC-UV | NDMA | valsartan | 300 ppb | Как можно отметить, большинство методов уже не соответствуют требованиям по чувствительности методов, указанных в регуляторных требованиях. FDA в свою очередь опубликовала ряд рекомендованных методик для определения нитрозаминов в фармацевтических препаратах, приведенных в таблице 3. Таблица 3: Методики контроля нитрозаминов, опубликованные FDA.
NDEA – 50 ppb | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 117807 | Combined direct injection method | GC-MS/MS | NDMA, NDEA | NDMA – 50-80 ppb NDEA – 30-40 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 123409 | Combined direct injection method | GC-MS/MS | NDMA, NDEA, NDIPA, NEIPA, NDBA | 1-40 ppb (5-13 для NDMA і NDEA) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 124025 | Headspace GC-MS/MS method | GC-MS/MS | NDMA, NDEA, NDIPA, NEIPA | 50 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 125478 | LC-HRMS method | LC-HRMS | NDMA, NDEA, NEIPA, NDIPA, NDBA, NMBA | 50 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 142092 | LC-ESI-HRMS | LC-HRMS | MNP, CPNP | 17 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 125477 | Rapid Fire-MS/MS method | LC-MS/MS | NDMA, NDEA, NEIPA, NDIPA, NDBA, NMBA | 100-5000 ppb (тільки для API) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 134914 | LC-HRMS method | LC-HRMS | NDMA | 30 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 138617 | LC-ESI-HRMS method | LC-HRMS | NDMA NDEA NEIPA NDIPA NDPA NMPA NDBA NMBA | 5-20 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 130801 | LC-HRMS method | LC-HRMS | NDMA | 33 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 131868 | LC-MS/MS method | LC-MS/MS | NDMA | 33 ppb | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Их чувствительность уже лучше, но чем ранее опубликованный метод, тем меньшее количество нитрозаминов включены в него. Наиболее чувствительным методом, который позволяет анализировать большое количество нитрозаминов (8 шт) является метод 138617, использующий масс-спектрометрию высокого разрешения, прибор типа орбитальная ионная ловушка (Orbitrap).
А что говорит европейская фармакопея?
Публикуется новая общая статья об анализе нитрозаминов — Аnalysis of N-nitrosamine impurities in active substances (2.4.36).
Основные примеси, которые контролируются в соответствии с ней (7 штук) — N-нитрозо-диметиламин (NDMA), N-нитрозо-диэтиламин (NDEA), N-нитрозо-дибутиламин (NDBA), N-нитрозо-N-метил-4 аминомасляная кислота (NMBA) N-нитрозо-диизопропиламин (NDiPA), N-нитрозо-этил-изопропиламин (NEiPA) и N-нитрозо-дипропиламин (NDPA). Чувствительность анализа согласно статье- ниже 30 ppb. Используются методы ГХ/МС, ГХ/МС/МС и ВЭЖХ/МС/МС, причем ни один из них не используется для определения всех видов нитрозаминов. Наибольшее количество компонентов по этой статье определяет метод ГХ/МС/МС — 6, за ним идет ВЭЖХ/МС/МС, который применяется соответственно для 5 видов примесей. Метод ГХ/МС используется только для анализа NDMA и NDEA.
Компания Thermo Scientific единственная, кто предлагает полный перечень оборудования в соответствии с рекомендованными методами определения нитрозаминов.
Метод газовой хроматографии-масс-спектрометрии (ГХ/МС)
Самым простым методом определения двух основных нитрозаминов NDMA и NDEA является ГХ/МС с парофазным инжектированием. Оба указанных нитрозамина являются летучими соединениями, хорошо переходящими в паровую фазу. При этом подготовка пробы, которая требуется для такого вида анализа — самая минимальная из возможных.
Предел количественного определения метода, разработанного с использованием парофазного пробоотборника Thermo Scientific TriPlus 500 HS, газового хроматографа Trace 1310 и одноквадрупольного масс-детектора ISQ ™ 7000 составляет 15 ppb для NDMA (LOD — 4 ppb) и 30 ppb для NDEA (LOD 9 ppb), что намного лучше, чем предел количественного определения европейских методик и методик FDA, разработанных на аналогичном оборудовании других производителей. При этом такое решение наиболее доступно по цене, а парофазный автосамплер TriPlus 500 HS легко расширяется с базовой конфигурации на 12 виал до решения с максимально-доступной пропускной способностью на 240 образцов.
В силу особенностей конструктивного исполнения система также обеспечивает прямое инжектирование в колонку из парофазного самплера с высокой прецизионностью и точностью, а запатентованная система VPI и NeverVent обеспечивает отсутствие необходимости продувки системы и минимальное время обслуживания прибора (на 98% меньше чем требуется для аналогичных приборов любых других производителей).
Если перед вами стоит задача определения только двух указанных основных нитрозаминов — решение на базе ГХ/МС ISQ ™ 7000 будет идеальным по соотношению цена — качество, и обеспечит чувствительность на уровне последних регуляторных требований.
Метод газовой хроматографии-и тандемной масс-спектрометрии (ГХ/МС/МС)
Рассматривая методы с использованием тандемной масс-спектрометрии, мы имеем 2 возможности — парофазное инжектирование для наиболее летучих нитрозаминов, и прямое жидкостное инжектирования с предварительной подготовкой пробы для более широкого перечня компонентов в одном анализе.
Парофазное инжектирование устраняет сложность матрицы, что приводит к снижению фонового шума и улучшению селективности. При этом подготовка пробы остается минимальной. Компанией Thermo Scientific опубликован метод определения 4 нитрозаминов (NDMA, NDEA, NDIPA, NEIPA) с помощью масс-детектора TSQ ™ 9000 с парофазным пробоотборником TriPlus 500 HS аналогичный методу 124025 от FDA, но с лимитом количественного определения от 2 до 10 ppb и лимитом детектирования 2 ppb, что от 5 до 20 раз чувствительнее метода FDA разработанного на аналогичном оборудовании других производителей. Использование запатентованных технологий VPI и NeverVent также обеспечивает минимальное время, необходимое на замену колонки или обслуживание источника, что в сочетании с непревзойденной емкостью парофазного автосамплера TriPlus 500 HS позволяет получить наибольшую доступную пропускную способность прибора.
Переходя к методам с прямым жидкостным инжектированием, мы сталкиваемся с большим влиянием компонентов матрицы, которое делает методику сложнее и требует тщательной подготовки пробы. Метод, опубликованный компанией Thermo на масс-детекторе TSQ ™ 9000 с жидкостным инжектирования для 5 нитрозаминов, дает лимит количественного определения от 0,5 до 1 ppb и лимит детектирования от 0,2 до 0,5 ppb, что значительно превышает требования к максимальному содержанию нитрозаминов и лимитам количественного определения метода.
Средствами улучшения чувствительности и расширения перечня нитрозаминов, которые определяются методом ГХ/МС/МС является:
1) Использование твердофазного экстрагирования (ТФЕ).
2) Использование SPME (твердофазного микроэкстрагирования).
3) Использование дисперсивного твердофазного экстрагирования (dТФЕ).
4) Более мягкая ионизация (для ионизации электронным ударом (ЭИ) и небольших молекул возможна фрагментация до небольших ионов, определению которых может мешать фоновый шум).
При этом использование SPME (твердофазного микроэкстрагирования) легко автоматизируется с помощью автоматического роботизированного самплера TriPlus RSH, что уменьшает влияние человеческого фактора на качество подготовки образцов, увеличивает чувствительность и обеспечивает непревзойденную воспроизводимость анализа.
Метод жидкостной хроматографии с тандемным масс-спектрометрическим детектированием
Когда мы используем жидкостную хроматографию с масс-спектрометрическим детектированием для количественного определения минимальных количеств контаминантов — тщательная подготовка проб неизбежна. На масс-спектрометрических детекторах производства компании Thermo разработан метод, включающий только 4 этапа подготовки пробы — измельчение таблетки, экстрагирование встряхиванием в водном растворе, центрифугирование и фильтрование образца. LOQ метода определения NDMA (летучего и сложного для определения жидкостной хроматографией компонента) на самом простом из современной линейки тандемных квадрупольных масс-детекторов Thermo составляет 0,3 мкг/кг. Пользователями Thermo из Индии и Кореи опубликованы методики на определение 6 и 11 нитрозаминов в одном анализе. При этом чувствительность методик составила от 0,25 до 1 ppb абсолютной концентрации, что опять же значительно превышает данные опубликованных методов, разработанных на аналогичном оборудовании других производителей.
Следует отметить, что рекомендованный метод ионизации для обеспечения удовлетворительного чувствительности определения наиболее летучего компонента — NDMA — химическая ионизация при атмосферном давлении. Разница в чувствительности между стандартной ионизацией електроспреем (ESI) и использованием APCI в среднем в 3 раза. Для других компонентов тип ионизации не является принципиальным.
ВЭЖХ/МС/МС метод анализа является обязательным, если одним из компонентов, которые необходимо определять, является NMBA. Учитывая физико-химические свойства указанного нитрозамина, определять его газовой хроматографией не рекомендуется. Для всех остальных нитрозаминов, которые контролируются в соответствии с новой фармакопейной статьей, можно использовать ГХ/МС/МС методику.
Метод жидкостной хроматографии с масс-спектрометрическим детектированием высокого разрешения прибором типа орбитальная ионная ловушка
Почему FDA разработало 5 методов с использованием детектора Orbitrap, несмотря на удовлетворительные результаты с использованием тандемного масс-детектирования?
Чаще всего, источником нитрозаминов являются АФИ. Каждый препарат имеет свои свойства, влияющие на эффективность подготовки пробы. Кроме того, готовые лекарственные препараты являются достаточно сложной матрицей, содержащей большое количество компонентов, мешающих анализу. Иногда нитрозамины выходят почти одновременно с пиком АФИ, иногда мешающие пики интерференций искажают количественные результаты по нитрозаминам. Использование масс-спектрометрии высокого разрешения позволяет эффективно разделять нитрозамины от АФИ или интерференций даже для наиболее сложных образцов. В то время как уникальный дизайн орбитальной ловушки обеспечивает чувствительность не хуже, чем у тандемных квадрупольных детекторов, что делает Orbitrap идеальным выбором для типов анализа, требующим одновременно и сверхэффективного разделения и чувствительности на уровне нанограммов.
Метод, опубликованный на модели Orbitrap Exploris 120, которая была анонсирована в 2020 году, обеспечивает эффективное разделение 7 нитрозаминов в концентрации 0,1 нг/мл с RSD по 3 инжекциям от 0 3,36%. Для сравнения предыдущая модель Q-Exactive обеспечивала чувствительность на уровне 0,5 нг/мл с RSD по 10 инжекциям между 0,76 и 1,62%.
Использование масс-детекторов высокого разрешения типа Orbitrap является идеальным выбором для мультикомпонентного анализа с высокой чувствительностью для сложных матриц. В соответствии с методиками FDA этим методом можно контролировать все 7 нитрозаминов, контролируемых в соответствии с текущими регуляторными требованиями. Это единственный метод, опубликованный для определения 6 нитрозаминов в лекарственных препаратах в целом, без привязки к конкретному типу лекарственного средства. Что же касается последних добавленных к контролю нитрозаминов MNP и CPNP — пока опубликован метод только с детектированием детектором типа Orbitrap.
Программное обеспечение для сбора данных и обработки результатов
Каждая фармацевтическая лаборатория, которая задумывается об использовании методов сложнее, чем одноквадрупольное масс-детектирование, сталкивается с тем, что у каждого производителя для трьохквадрупольного детектирования разработано отдельное программное обеспечение, которое прекрасно справляется со сложными алгоритмами обработки данных и создания масс-спектрометрических методик, но к сожалению не соответствует нормативным требованиям к программному обеспечению в полной мере. Более того — полноценное подключение таких детекторов, управление ими, хранение методик и обработка результатов в сетевых системах, обеспечивающих целостность данных в фармацевтических лабораториях, на данный момент невозможно.
Компания Thermo Fisher Scientific — единственная компания, которая смогла разработать программное обеспечение, в полной мере соответствующее всем нормативным требованиям и одновременно в состоянии управлять сложными масс-спектрометрическим детекторами. Оно одинаково эффективно и безопасно управляет и хранит данные обычных хроматографов и тандемных масс-детекторов.
Программное обеспечение Chromeleon CDS — больше никаких компромиссов!
Безопасное хранение данных, сохранение всех версий результатов, отслеживание и удобный просмотр всех изменений, полная интеграция в сетевую систему Chromeleon CDS. Разделение ролей и доступа пользователей, автоматическое и полное ведение аудиторского журнала — все это вы получаете в одном программном пакете даже с тандемными масс-спектрометрическим детекторами, без необходимости усвоения новых программ и интерфейсов.