Нейроэндокринные опухоли
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Что такое нейроэндокринные опухоли (НЭО)?
Основные локализации нейроэндокринных клеток:
щитовидная и паращитовидные железы, надпочечники.
Нейроэндокринные опухоли встречаются сравнительно редко и могут быть как злокачественными, так и доброкачественными. Чаще всего НЭО (устаревшее название – карциноиды) встречаются в следующих органах:
тонкая кишка, прямая кишка и аппендикс,
Нейроэндокринные опухоли делятся по следующим признакам:
Факторы риска появления НЭО
Чаще всего эти опухоли возникают спорадически – то есть случайно. Но есть и наследственные мутации, при наличии которых риск возникновения НЭО возрастает. Описаны несколько наследственных опухолевых синдромов, при которых повышен риск появления НЭО:
MEN 1 типа (multiple endocrine neoplasia – синдром множественных эндокринных неоплазий первого типа),
болезнь фон Гиппеля-Линдау,
Симптомы НЭО
Не всегда у пациентов с НЭО есть какие-либо симптомы. Кроме того, симптомы часто не специфичны – то есть встречаются и при других заболеваниях. На основе наличия или отсутствия симптомов НЭО принято разделять на функциональные (симптомные) и нефункциональные (бессимптомные). Функциональные опухоли усиленно вырабатывают гормоны, которые и становятся причиной появления симптомов.
Наиболее распространенные симптомы НЭО:
покраснение кожи лица и шеи,
повышенное артериальное давление,
Стадирование опухолевого процесса
Определение стадии играет ключевое значение, так как полностью определяет дальнейшее лечение. Как и при большинстве других опухолей, при НЭО принято выделять 4 стадии – от I до IV. При этом, кроме стадии, диагноз включает специальную кодировку – TNM, где:
T (tumor, опухоль) – описывает первичную опухоль,
N (nodes, лимфоузлы) – описывает распространение опухоли в лимфоузлы,
M (metastasis, метастазы) – описывает наличие или отсутствие метастазов.
Еще один параметр, описывающий нейроэндокринную опухоль – Grade. Он используется для описания способности опухоли к быстрому росту и распространению по организму и бывает 3 степеней:
G1 (low grade) – низкий темп роста и распространения,
G2 (intermediate grade) – промежуточный,
G3 (high grade) – высокий темп роста и распространения.
Обследование при подозрении НЭО
Сбор жалоб и анамнеза (истории болезни),
Анализ крови и мочи для выявления биохимических маркеров нейроэндокринной опухоли,
ПЭТ-КТ с галием (68Ga-DOTATATE и 68Ga-DOTANOC),
ПЭТ-КТ с глюкозой (ФДГ)
Сцинтиграфия с 111 In-Octreotide,
Особое место в диагностике занимает биопсия – забор фрагмента опухоли для точного определения ее типа. Биопсию возможно выполнить различными методами, например, при ФКС или ФГС. После биопсии фрагмент опухоли отправляется на гистологическое и иммуногистохимическое исследование (под микроскопом) для определения типа и агрессивности опухоли.
Какие из обследований будут использованы в Вашей ситуации будет определяться Вашим лечащим врачом. Часто при обследовании и планировании лечения необходимо получить консультацию у смежного специалиста, например, у кардиолога.
Лечение нейроэндокринных опухолей
Учитывая редкость НЭО и сложность постановки диагноза, перед началом лечения каждый пациент обсуждается мультидисциплинарной командой. В ее состав входят:
специалист лучевой диагностики,
при необходимости – дополнительные специалисты: кардиолог, анестезиолог и т.д.
В ходе разбора клинической ситуации каждого конкретного пациента вырабатывается коллегиальный индивидуальный план лечения, а при необходимости – дополнительного обследования.
Возможности лечения при НЭО:
терапия аналогами Соматостатина,
эмболизация при наличии метастазов в печени.
Часто лечение складывается из комбинации нескольких методов для достижения наиболее хорошего результата. Кроме того, бывают ситуации, когда одному пациенту подходят два варианта лечения с одинаковой эффективностью. Наилучший для Вас вариант лечения Вам расскажет лечащий врач по итогам работы мультидисциплинарной команды.
Нейроэндокринные опухоли желудка
Нейроэндокринные новообразования желудка, также известные как эндокринные новообразования или карциноиды, составляют относительно небольшую и гетерогенную группу опухолей, значительно различающихся по клинико-патологическому течению, степени дифференцировки, скорости пролиферации и исходу [1].
Хотя по морфологическим и функциональным свойствам в слизистой оболочке желудка человека выделяют до 5 типов эндокринных клеток, большинство желудочных НЭО развиваются из энтерохромаффиноподобных клеток. Эти новообразования могут быть множественными, возникающими на фоне длительной гипергастринемии из-за атрофического гастрита и ахлоргидрии (тип 1), или вследствие сочетанной множественной эндокринной неоплазии — синдрома Золлингера-Эллисона с гипертрофической гастропатией (тип 2), или они могут появляться в слизистой оболочке без предшествующих патологических изменений (тип 3), иногда возникает «атипичный» карциноидный синдром [1].
Нейроэндокринные новообразования желудка значительно различаются по гистологии, клинико-патологическим формам, стадиям и возможным исходам, что подразумевает необходимость большого количества лечебных и диагностических мероприятий. Также стоит отметить необходимость улучшения диагностических и прогностических критериев для выбора соответствующей терапии [1].
Локализация опухоли [2]:
• Кардиальный отдел,
• Дно желудка,
• Тело желудка,
• Преддверие желудка,
• Привратник,
• Малая кривизна желудка,
• Большая кривизна желудка,
• Поражение, выходящее за пределы желудка.
Классификация
Классификация ВОЗ 2010 [2]:
Классификация по степени злокачественности [2,4]
Алгоритм лечения зависит от типа и распространенности опухоли и ориентирован на классификации ВОЗ (2010) и рекомендации Европейского общества по изучению НЭО (ENETS) (2016). В настоящее время ENETS и ВОЗ предложено делить НЭО ЖКТ по степени их злокачественности (Grade) на 3 основные группы — Gl, G2, G3, а также по TNM [2].
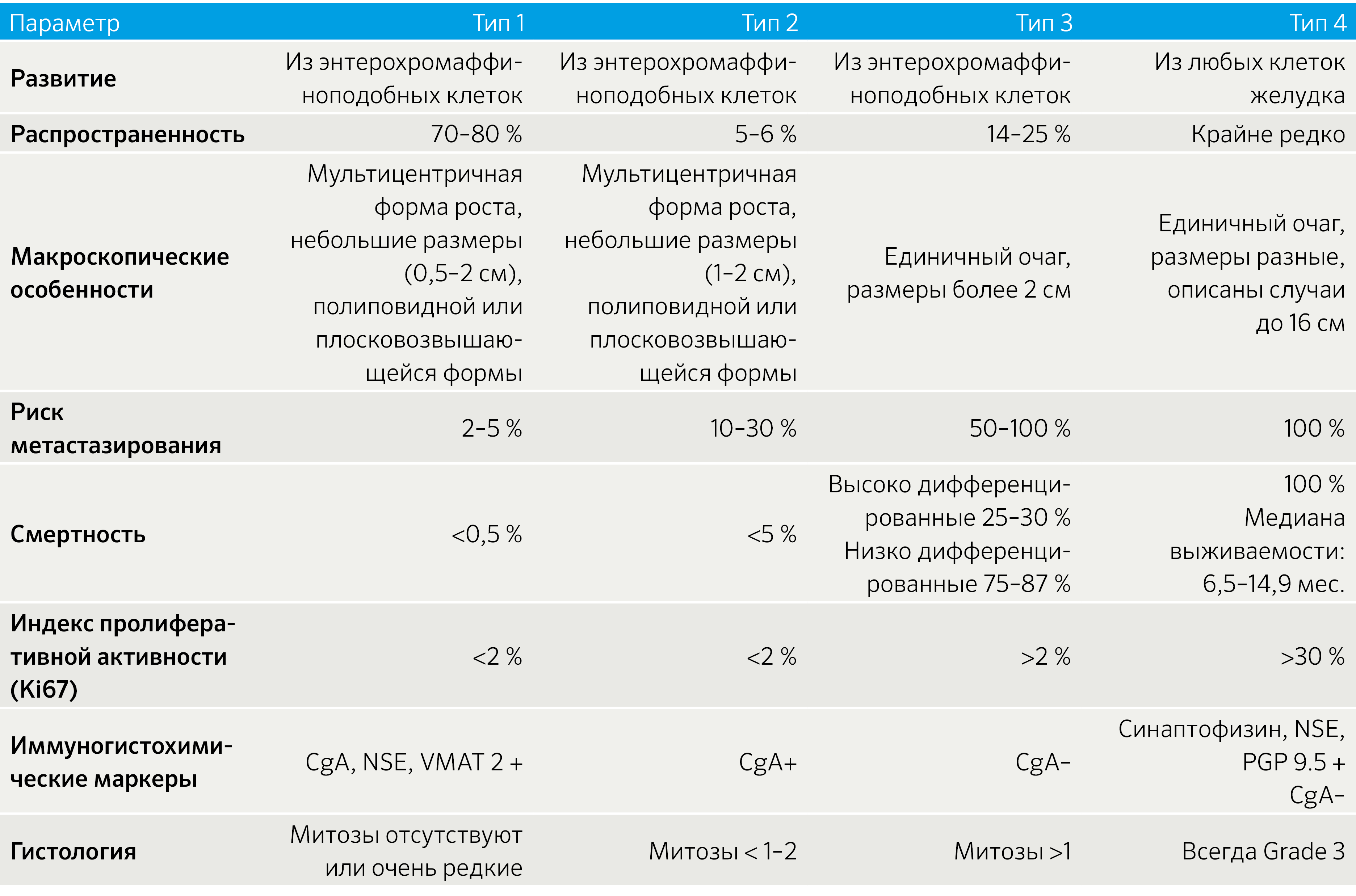
Таблица 1. Характеристика клинико-патологических форм НЭО желудка [3,4]
Клинико-патологические формы НЭО желудка
I тип
70–80 % нейроэндокринных опухолей желудка являются опухолями I типа: диаметр менее 10 мм, опухоли множественные. Часто у пациентов хронический атрофический гастрит в анамнезе. Опухоли локализуются в дне или теле желудка. При микроскопии трабекулярное или плотное расположение клеток. Опухолевые клетки мономорфные, среднего размера, правильной формы, с округлыми ядрами. Митозы либо отсутствуют, либо редкие. Распространение опухоли ограничено слизистой или подслизистым слоем. Гастрин-зависимые НЭО желудка последовательно связаны с генерализованной пролиферацией эндокринных клеток в слизистой оболочке части органа, не пораженной опухолевым процессом. Гистопатологическая классификация была сформулирована для спектра пролиферативных поражений, представленных фундальными эндокринными клетками пациентов с гипергастринемией. Эта классификация распределяет опухоли I типа в последовательности, предположительно отражающей временную эволюцию процесса и увеличивающийся онкологический риск для пациентов. Диагностика НЭО желудка требует эффективного гистопатологического, биохимического и диагностического анализа изображений [3].
Большинство опухолевых клеток первого типа являются позитивными в отношении эндокринных маркеров, таких как хромогранин А (CgA), нейрон-специфическая енолаза (NSE) и транспортер везикулярного моноамина 2, которые характеризуют клетки как гистамин-продуцирующие. Определение экспрессии CgA может быть полезным диагностическим тестом при подозрении на НЭО желудка первого типа. Но концентрация CgA коррелирует с количеством энтерохромаффиноподобных клеток; таким образом, патологически высокая концентрация CgA не является ни патогномоничной, ни необходимой для диагностики НЭО желудка первого типа. Маркер пролиферации MKI67 обычно экспрессируется менее чем в 2 % опухолевых клеток. Опухоли обычно развиваются бессимптомно, диагноз ставят случайно во время гастроскопии. Разрушение париетальных клеток из-за хронического атрофического гастрита в течение длительного времени может привести к снижению секреции внутреннего фактора Касла и, как следствие, к нарушению всасывания витамина B12. Таким образом, дефицит витамина B12 и гиперхромная макроцитарная анемия часто связаны с аутоиммунным атрофическим гастритом и гипергастринемией [3].
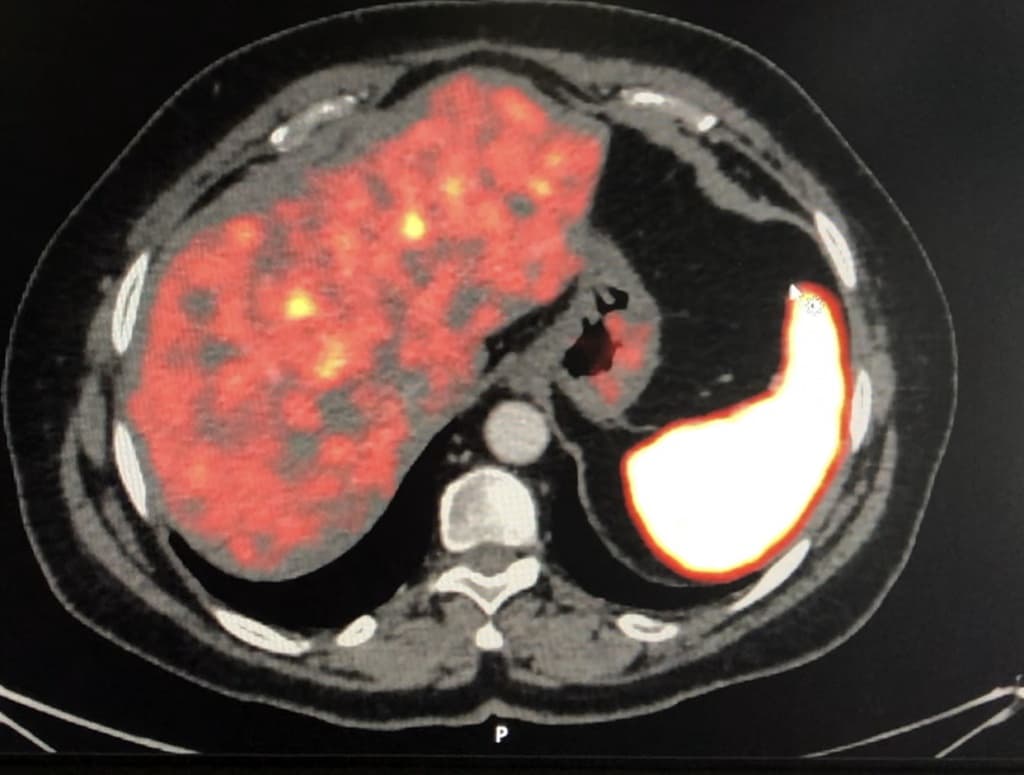
НЭО желудка первого типа очень редко метастазируют (5 % для локальных лимфатических узлов, менее 2 % с отдаленными метастазами), без связанных с этим случаев смерти и при стопроцентной длительной выживаемости. Эндоскопическое ультразвуковое исследование может быть полезным для получения картины локализованного заболевания (то есть отсутствия инфильтрации в подслизистом слое), в то время как компьютерная томография (КТ) может выявить метастазы в печени. В зависимости от размера и количества поражений эндоскопическая резекция опухоли является методом выбора [3].
II тип
5–6 % НЭО желудка являются опухолями типа II, которые возникают из гастрин-секретирующей ткани при синдроме Золлингера-Эллисона. Клиническое течение НЭО желудка II типа сходно с опухолями первого типа. Опухоли небольшие (1–2 см), множественные и высоко дифференцированные. Маркер пролиферации MKI67 экспрессируется в 2 см, в среднем 5,1 см), обычно встречаются поодиночке и растут из тела/дна желудка. Находящиеся рядом участки слизистой оболочки желудка без атрофических изменений. НЭО желудка III типа агрессивны и отличаются глубокой инвазией, ранним формированием метастазов. Прогноз неблагоприятный. Как правило, более 2 % опухолевых клеток экспрессируют маркер пролиферации MKI67, но отрицательны на CgA. Гистологически этот тип опухоли характеризуется большими, плохо определяющимися твердыми агрегатами или диффузными массами круглых или веретенообразных клеток. Обнаружены обильные митозы (>1 в поле зрения микроскопа при большом увеличении), часто встречается очаговый некроз. Ультраструктурные исследования подтверждают наличие эндокринных гранул.
Хирургическая резекция и диссекция лимфатического узла являются методом выбора. В зависимости от локальных характеристик роста злокачественных опухолей типа III, лечение может включать расширенную радикальную операцию резекции желудка и регионарную лимфаденэктомию [3].
IV тип
НЭО желудка IV типа — это редкие, крупные, слабо дифференцированные опухоли, которые являются крайне злокачественными. Самая большая из известных НЭО желудка IV типа составляет 16 см. В большинстве случаев во время диагностики НЭО желудка IV типа уже видна инвазия в лимфатические и кровеносные сосуды. Картина при низкодифференцированных НЭО желудка IV характеризуется тяжелой патологией с преобладающей твердой структурой, обильным центральным некрозом и выраженным клеточным атипизмом с частыми атипичными митозами и высоким уровнем MKI67 (>30). CgA обычно отсутствует или экспрессируется только в очаге, что согласуется с небольшим количеством электронно-плотных гранул в ультраструктуре. Выражена экспрессия синаптофизина и цитозольных маркеров NSE и PGP9.5. Несмотря на редкость, низкодифференцированные опухоли IV типа заслуживают особого внимания из-за их агрессивного характера и неблагоприятного прогноза: медиана выживаемости составляет от 6,5 до 14,9 месяцев [3].
НЭО желудка IV типа требует хирургической резекции с последующей химиотерапией и комбинированной адъювантной терапией [3].
Список литературы:
Нейроэндокринная опухоль желудка что это
Нейроэндокринные опухоли (НЭО) развиваются в клетках периферической нейроэндокринной системы, рассеянной в различных органах, и наблюдаются довольно редко [1]. Отмечена тенденция к значительному увеличению частоты встречаемости НЭО, что может быть связано, с одной стороны, с совершенствованием и широким внедрением эндоскопической диагностики, с другой — с повышением информированности клиницистов и патоморфологов. Исходя из вышеизложенного, обзор литературы, посвященный патогенезу, диагностике и лечению НЭО желудка (НЭОЖ), весьма актуален.
Классификация
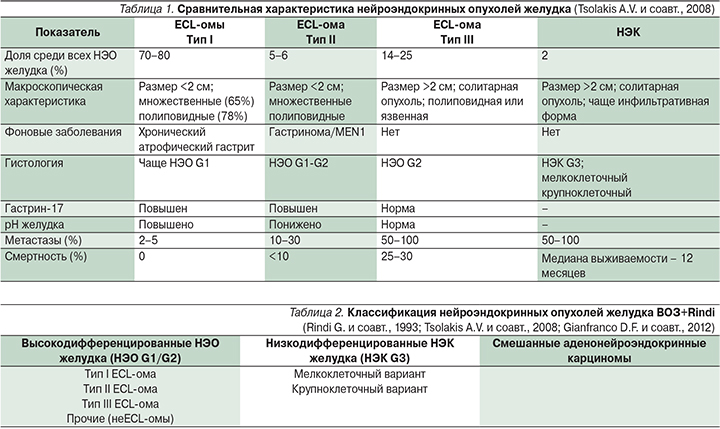
Классификация НЭО по стадиям имеет практическое значение в прогнозировании и выборе лечебной тактики. Европейским обществом нейроэндокринных новообразований (ENETS) предложена классификация (2006), основанная на величине митотического индекса и Ki-67 — маркера НЭО [2]. В дальнейшем (2010) эти протоколы были поддержаны классификацией ВОЗ [3], согласно которой НЭО группируют следующим образом: НЭО G1, НЭО G2, нейроэндокринная карцинома (НЭК), смешанная адено-НЭК, а также гиперпластические и предопухолевые образования (табл. 1). 
Опухоли класса G3 по критериям ENETS соответствуют НЭК в классификации нейроэндокринных образований ВОЗ (2010).
Эпидемиология
Среди всех первично выявленных НЭО 11—12% их локализуются в желудке. В последнее время прослеживается тенденция к увеличению доли НЭОЖ среди общего числа гастроинтестинальных НЭО [4—9]. Более чем 60-летние наблюдения позволяют предположить, что частота встречаемости НЭОЖ увеличилась с 0,3 до 1,8% среди всех злокачественных новообразований желудка, при этом у женщин европеоидной расы она возросла в 800 раз [8]. В некоторых наблюдениях отмечен 6—9-кратный рост встречаемости НЭОЖ за 1981—2000 гг. [10].
Эпидемиологические показатели НЭОЖ с 2000 по 2006 г. в Великобритании среди мужчин и женщин составили соответственно 0,16 и 0,15 на 100 000 человек, что по сравнению с показателями 1995 г. демонстрирует 23-кратное увеличение заболеваемости среди мужчин и 47-кратное — среди женщин [6]. Подобное увеличение частоты встречаемости НЭОЖ наблюдалось и в США: с 0,03 (1973—1977) до 0,33 (2003—2007) на 100 000 человек [11].
Данные японских исследователей также подтверждают увеличение встречаемости НЭО, локализованных в области передней кишки (желудка и двенадцатиперстной кишки) с 1,05 (2005) до 1,67 (2010) на 100 000 человек [7, 12]. Это связывают с ростом частоты развития хронического атрофического гастрита (ХАГ) на фоне систематического приема ингибиторов протонной помпы (ИПП) [13], с улучшением эндоскопической диагностики, стандартизацией морфологических исследований и возросшей публикационной активностью.
Гистологическая классификация и клиническая картина
НЭОЖ можно подразделить на хорошо и плохо дифференцированные. Хорошо дифференцированные НЭОЖ развиваются из энтерохромаффиноподобных (ЭХП) клеток тела и дна желудка, которые в норме продуцируют гистамин и участвуют в регуляции желудочной секреции.
В настоящее время НЭОЖ подразделяют на три типа [14]. В табл. 2 представлены 
Самым распространенным считают I тип — около 70—80% всех НЭОЖ, встречается преимущественно у женщин (60—70%) в возрасте старше 60—65 лет [27]. Распространенность поражения в популяции составляет 0,2 случая на 100 000 населения, при этом считают, что в последние годы она достигла 1,8 случая на 100 000 населения [10, 27].
Гистологически опухоли I типа состоят из ЭХП-клеток и обычно обнаруживаются у больных ХАГ типа А, включая аутоиммунный гастрит и атрофический гастрит, ассоциированный с Helicobacter pylori [23]. Известно, что ахлоргидрия, вызванная атрофией желез дна желудка при ХАГ, приводит к гипергастринемии и повышению внутрижелудочного рН с развитием гиперплазии G-клеток антрального отдела желудка. Гастрин взаимодействует с ССК2-рецепторами на мембране ЭХП-клеток и приводит к их гиперплазии. Перманентная стимуляция гастрином ССК2-рецепторов, а также протеинкиназы С и митоген-активируемой протеиновой киназы индуцирует постоянную экспрессию клеток mcl-1, синтезирующих белок, обладающий способностью подавлять апоптоз [28].
Предполагают, что прием ИПП, а также ваготомия вкупе с генетическими, диетическими, гормональными и бактериальными факторами играют роль ко-факторов в развитии гипергастринемии и НЭОЖ. Мутация Reg-гена, контролирующего в норме ответ ЭХП-клеток на гастрин, приводит к его бесконтрольному стимулирующему воздействию на ЭХП-клетки, их пролиферации и увеличению риска развития НЭОЖ I типа. В эксперименте показана вероятная роль инфекции Helicobacter pylori в развитии ХАГ, гипергастринемии и НЭОЖ [29—31].
При иммуногистохимическом окрашивании клетки НЭО определяются как положительные по наличию хромогранина A (CgA), синаптофизина, везикулярного моноаминного транспортера 2 и рецептора соматостатина 2А [32]. В частности, окрашивание CgA позволяет увидеть изменения в ЭХП-клетках по типу гиперплазии и дисплазии. Для гиперплазии характерно наличие более 6 рядов линейной гиперплазии на 1 мм. Дисплазия, присутствующая главным образом в микроинфильтративных образованиях, ассоциируется с повышенным риском НЭОЖ [33].
Как правило, опухоли I типа не злокачественные, часто множественные, размером менее 2 см. Локальное поражение наблюдается в 90—95%, а отдаленные метастазы — у 1—2% больных. Злокачественный потенциал напрямую зависит от размеров опухоли и глубины ее инвазии, но при этом мультицентричность напрямую не коррелирует с вероятностью появления метастазов. Выживаемость таких больных не отличается от сроков жизни в популяции людей соответствующего возраста [34—36]. При наличии метастазов 5-летняя выживаемость составляет обычно 50—60% и не превышает 75% [8]. В связи с этими особенностями развития опухоли возникает вопрос о допустимости локальных методов лечения при очевидном операционно-анестезиологическом риске.
НЭОЖ II типа встречается реже — в 5—6%, имеет промежуточный малигнизационный потенциал и может быть ассоциирована с синдромом МЭН I типа — 10—15% и синдромом Золлингера—Эллисона (СЗЭ) — около 1%. Приблизительно у 30% больных с этим типом опухоли обнаруживают метастазы. Если опухоль I типа локализуется, как правило, в теле и фундальном отделе желудка, то новообразования II типа могут встречаться и в антральном отделе [37]. Опухоли типа II, как и типа I, ассоциированы с гипергастринемией и развиваются из ЭХП-клеток.
НЭОЖ III типа — самый агрессивный тип, на долю которого приходится около 15—20%. Это спорадические опухоли, развитие которых не связано с желудочной секрецией и гиперплазией ЭХП-клеток. Отдаленные метастазы диагностируют у 50—100% больных. Эта опухоль обычно продуцирует 5-гидрокситриптофан и не связана с гипергастринемией [38, 39].
Технология микрочипов позволила выявить различия в экспрессии генов при различных вариантах опухоли. Так, из 270 исследованных генов статистически значимое различие установлено для мутаций CagA, MAGE — D2, MTAI, CCN2, что позволяет дифференцировать III и I типы. Доказано, что мутация гена супрессора опухоли р53 прямо коррелирует с НЭОЖ III типа и обусловливает стимуляцию пролиферации клеток [38, 39].
Большинство НЭОЖ I типа представляют собой небольшие, множественные опухоли, расположенные в теле или дне желудка и ограниченные слизистым или подслизистым слоем желудочной стенки. Поскольку большинство НЭОЖ I типа — это опухоли класса G1, метастатический риск является крайне низким, а прогноз — благоприятным. У пациентов с НЭОЖ I типа, ассоциированными с аутоиммунным гастритом, могут наблюдаться и другие аутоиммунные заболевания (сахарный диабет 1-го типа, аутоиммунный тиреоидит и первичный билиарный цирроз печени) или пернициозная анемия [24].
НЭОЖ I типа обычно протекают бессимптомно и случайно выявляются при скрининговом эндоскопическом исследовании верхних отделов желудочно-кишечного тракта. Опухоли I и II типа обнаруживают эндоскопически как полипы фундального отдела (часто множественные).
НЭОЖ II типа также небольшого размера, множественные и относительно доброкачественные. Однако в отличие от типа I они встречаются у мужчин и женщин одинаково часто. Приблизительно 30% НЭОЖ II типа на момент клинических проявлений имеют метастатическое распространение [19], а показатели выживаемости пациентов с такими НЭОЖ ниже, чем при типе I [40]. Течение большинства НЭОЖ II типа асимптомное, однако повышенная секреция желудочного сока, отмечаемая у больных с типом II, может привести к образованию пептической язвы, поэтому у таких пациентов могут наблюдаться клинические признаки язвенной болезни [41].
Контрольное обследование и прогноз
Программы контрольного обследования составляют в зависимости от типа и размеров опухоли, характера проведенного лечения, наличия рецидива. Контрольное обследование включает сбор анамнеза, осмотр, инструментальные исследования: ЭГДС, по показанию — КТ и МРТ в зависимости от клинических проявлений.
При опухоли I типа весь комплекс исследований повторяют 1 раз в 2 года, при опухоли II типа — ежегодно. В ходе ЭГДС необходима биопсия слизистой оболочки в зоне фонового ХАГ (для исключения развития аденокарциномы). Уровень гастрина исследуют у больных опухолью I и II типа.
Больным с высокодифференцированной опухолью III типа показана радикальная операция. В послеоперационном периоде проводят сцинтиграфию и исследование уровня CgA каждые 6 мес в течение 2 лет, а затем ежегодно в течение 3 лет. При метастазах опухоли контроль эффективности лечения осуществляют каждые 6 мес.
При опухоли I типа, как правило, указывают на 100% 5-летнюю выживаемость и крайне редкие летальные исходы, при опухоли II типа выживаемость составляет 60—75%, отражает уровень смертности при синдроме МЭН-I и более высокий потенциал малигнизации. При НЭОЖ III типа после радикального хирургического лечения 5-летняя выживаемость достигает 75%, а при злокачественной гастриноме IV стадии не превышает 20—38% [86].
Согласно рекомендациям NCCN [57], пациенты с небольшими ( 20 мм) должны обследоваться каждые 3—12 мес после резекции и каждые 6—12 мес в дальнейшем.
ENETS [47] рекомендует эндоскопический контроль пациентам с рецидивирующими НЭОЖ I типа каждые 12 мес, пациентам без рецидива каждые 24 мес. Ежегодная ЭГДС рекомендована больным с НЭОЖ II типа. Дальнейшее обследование пациентов с НЭОЖ III типа, перенесших гастрэктомию, проводят так же, как и после аналогичной операции при аденокарциноме желудка.
Таким образом, НЭОЖ представлены широким спектром новообразований, включающих и очень медленно прогрессирующие, и рано метастазирующие. Наблюдается значительное увеличение частоты встречаемости НЭОЖ. В соответствии с гистологическими критериями НЭОЖ делятся на 3 типа. Лечение каждого больного должно быть строго индивидуальным и проводиться командой специалистов разного профиля. При выборе способа лечения НЭОЖ следует исходить из типа опухоли, ее гистологических характеристик, локализации и степени выраженности местной инвазии, а также наличия метастазов. Личный опыт большинства хирургов ограничен небольшой группой больных, поэтому для выбора оптимального лечения необходимо опираться на результаты опубликованных исследований. Для определения оптимального способа диагностики и лечения НЭОЖ требуются дальнейшие исследования.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.
Нейроэндокринная опухоль желудка что это
МНИОИ им. П.А. Герцена – филиал ФГБУ НМИРЦ Минздрава России, Москва
Введение
Нейроэндокринные опухоли (НЭО) желудка составляют 3–6% от всех НЭО и около 2% среди всех опухолей желудка. НЭО желудка чаще встречаются у женщин (64%) [1]. Преобла-дают высокодифференцированные НЭО I типа (см. классификацию). Низкодифференцированные нейроэндокринные карциномы занимают в структуре НЭО желудка не более 6%, однако их истинная распространенность может быть недооценена из-за сложностей морфологической диагностики [2]. Длительное время НЭО желудка относили к крайне редким заболеваниям, однако в последние годы отмечена устойчивая тенденция к росту заболеваемости ими. Так, по данным National Cancer Institute, за период с 1950 по 1999 г. было зарегистрировано всего 562 случая НЭО желудка, а с 2000 по 2004 г. – уже 1043, что составило 11,7% от общего числа гастроэнтеропанкреатических НЭО [3, 4] Причины столь стремительного роста заболеваемости неизвестны. Отчасти рост числа первичных больных может быть следствием широкого внедрения эндоскопического обследования верхних отделов желудочно-кишечного тракта (ЖКТ) и иммуногистохимического исследования биопсийного материала [5]. Также высказывается мнение о роли использования ингибиторов протонной помпы в развитии карциноидов желудка I типа. Длительное (годы) применение препаратов этой группы и вызываемая ими ахлоргидрия сопровождаются выраженным повышением уровня гастрина-17, что является одним из ключевых патогенетических механизмов развития карциноидов желудка [6–8].
НЭО желудка – неоднородная группа, включающая как высокодифференцированные новоообразования, подлежащие эндоскопическому лечению и характеризующиеся благоприятным прогнозом, так и высокозлокачественные низкодифференцированные опухоли, обладающие высоким метастатическим потенциалом, характеризующиеся крайне агрессивным течением и неблагоприятным прогнозом, при которых проводят хирургическое и комбинированное лечение, как при аденокарциномах желудка. Низкая информированность врачей общей практики и онкологов общей лечебной сети о данной проблеме нередко приводит к ошибочному выбору лечебной тактики, в частности к необоснованным операциям у пациентов с карциноидами желудка I–II типов.
Классификация НЭО желудка
Впервые понятие «карциноид» было введено Обердорфером в 1907 г. для описания опухолей ЖКТ, обладающих специфической морфологической структурой, отличной от таковой у эпителиальных новообразований [9]. В 2007 г. Европейское сообщество по нейроэндокринным опухолям (European Neuroendocrine Tumor Society – ENETS) впервые предложило классификацию НЭО, в которой была использована система определения степени дифференциро-вки опухоли, аналогичная таковой для всех злокачественных новообразований ЖКТ [10, 11]. В рекомендациях 2010 г. Американский объединенный онкологический комитет (American Joint Committee on Cancer – AJCC), предложил разделить все НЭО ЖКТ по степени дифференцировки (G) в зависимости от митотического индекса и процента клеток, экспрессирующих антиген Ki-67 [12]. Именно этот подход и стал основанием для создания актуальной на сегодняшний день классификации ВОЗ для НЕО ЖКТ, в соответствии с которой выделяют НЕО G1, G2, нейроэндокринные карциномы G3 (мелко- и крупноклеточные), а также смешанные аденонейроэндокринные карциномы и гиперпластические или предопухолевые изменения [13].
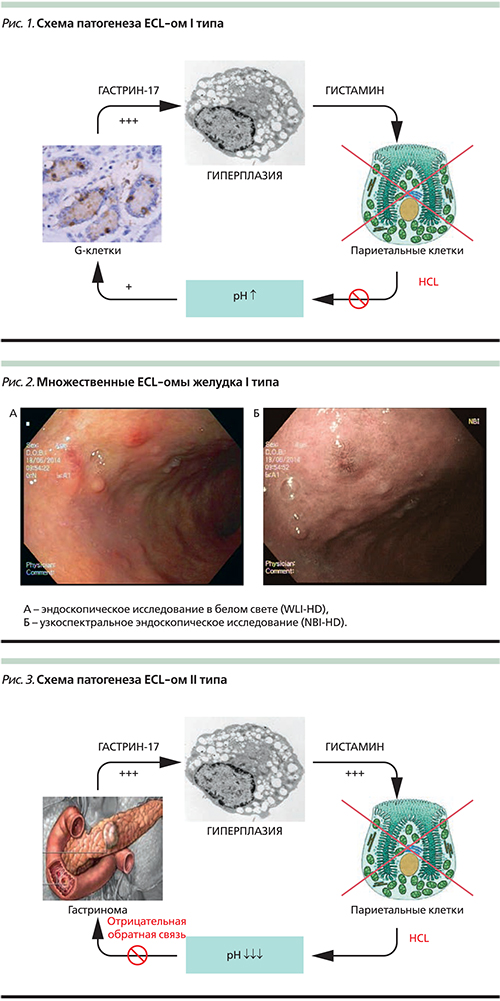
В 1993 г. итальянский патологоанатом G. Rindi предложил классификацию, подразделяющую карциноиды желудка на три основных типа. Карциноиды I типа (до 70–80% от общего числа) [14, 15] развиваются на фоне атрофического аутоиммунного гастрита, в т.ч. при пернициозной анемии [16]. При наличии данного заболевания в качестве ответа на ахлоргидрию происходит значительное повышение уровня гастрина, что в свою очередь приводит к гиперплазии нейроэндокринных клеток желудка и появлению мультифокальных карциноидных опухолей (рис. 1). В пользу данной теории свидетельствуют опыты на животных, в ходе которых было выявлено значительное повышение частоты развития НЭО желудка на фоне высоких доз ингибиторов протонной помпы [8]. По своему клеточному происхождению карциноиды I типа являются ECL-омами, т.е. опухолями из энтерохромофинноподобных (ECL) клеток. Они характеризуются множественностью зачатков, полиповидной формой роста и низким метастатическим потенциалом. Как правило, карциноиды I типа имеют высокую степень дифференцировки G1 (размеры до 1 см) и локализуются в пределах слизисто-подслизистого слоя желудка (рис. 2)
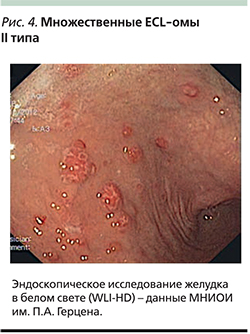
Карциноиды II типа (около 5%) также являются ECL-омами и возникают вследствие повышения уровня гастрина, но в отличие от I типа причиной гипергастринемии является функционирующая НЕО – гастринома (синдром Золингера–Элисона; рис. 3). Гастринома может возникать спорадически (до 70%) или развиваться в рамках синдрома множественной эндокринной неоплазии I типа (MEN-I) [17]. В патогенезе таких опухолей имеет значение не только гипергастринемия, но и инактивация гена MEN1. Им также свойственны множественность зачатков, полиповидная форма роста и поверхностная локализация, однако эти опухоли чаще имеют умеренную дифференцировку G2 и обладают более высоким метастатическим потенциалом (до 10%; рис. 4).
Отдельным типом НЕО желудка являются низкодифференцированные нейроэндокринные карциномы (НЭК), некоторые авторы обозначают их как 4-й тип по Rindi (рис. 6). Эта группа включает только опухоли с низкой степенью дифференцировки (G3), высоким Ki-67, не имеет связи с фоновыми состояниями и характеризуется крайне неблагоприятным прогнозом (медиана выживаемости около 12 месяцев). Различают мелкоклеточный и крупноклеточный варианты. Особые трудности возникают при попытке классифицировать опухоли с дифференцированной морфологией, но высоким митотическим индексом и Ki-67 >20%, но
Хромогранин А (ХгА) – универсальный маркер НЭО. Измерение концентрации ХгА в сыворотке крови является чувствительным, но низкоспецифичным методом диагностики и мониторинга при НЭО, в т.ч. гормонально неактивных [36, 37]. При НЭО желудка I–II типов ХгА всегда повышен, но причиной этого является не появление карциноидов, а хроническая гипергастринемия с гиперплазией нейроэндокринного аппарата желудка. Поэтому данный маркер имеет клиническое значение только при карциноидах желудка III типа. Также на корректность измерения ХгА влияет прием блокаторов протонной помпы и наличие почечной или печеночной недостаточности. В первом случае для получения корректного результата следует прекратить прием препарата перед забором крови или заменить его на блокатор Н2-гистаминовых рецепторов [38]. Мониторинг ХгА неэффективен и не должен применяться при НЭК G3 желудка.
Классический или атипичный (обусловлен гиперпродукцией гистамина) карциноидный синдром крайне редко наблюдается при НЭО желудка, главным образом при опухоли III типа [39]. В этом случае определяют суточное количество 5-ГИУК (5-гидроксииндолуксусная кислота) в моче, обладающей высокой специфичностью для диагностики и мониторинга серотонин-продуцирующих НЭО. Нормальным считается показатель 2–8 мг/сут. Клиническая значимость данного теста ограничивается возможностью ложноположительных результатов. Повышение уровня 5-ГИУК до 30 мг/сут может быть следствием синдрома мальабсорбции, употребления пищи, богатой триптофаном и серотонином, или приема ряда лекарственных препаратов (например, ацетаминофена, барбитуратов, эфедрина, никотина, кофеина и др.) [40].
Лечение
Локализованные НЭО
Выбор метода лечения НЭО зависит от их типа и степени дифференцировки. «Золотым» стандартом лечения пациентов с НЭО I и III типов является внутрипросветное эндоскопическое лечение [16, 41]. Поскольку большинство НЭО I типа имеют инвазию в пределах слизистой оболочки, наиболее часто для лечения таких больных применяются методы эндоскопической резекции слизистой оболочки или аргоноплазменной коагуляции. При полиповидных НЭО I типа оптимальным методом лечения является резекция слизистой оболочки (ЭРС) [21]. Первым этапом осуществляют формирование гидравлической подушки под опухолью с целью отделения последней от подслизистого слоя. Затем производят отсечение фрагмента слизистой оболочки с НЭО в пределах здоровых тканей с применением электрохирургического блока и диатермической петли [42]. Критерием радикальности подобного эндоскопического вмешательства является отсутствие опухолевых клеток в краях удаленного фрагмента слизистой оболочки [42]. ЭРС обеспечивает высокую степень радикализма и безрецидивное течение заболевания [22]. При множественных плоских НЭО I типа наиболее эффективным методом лечения признается эндоскопическая аргоноплазменная коагуляция с применением специализированных электрохирургических блоков и катетеров подачи аргона, вводимых в инструментальный канал эндоскопа. Такой подход обеспечивает глубокий, вплоть до собственной пластинки, сухой некроз слизистой оболочки в зоне опухоли, что позволяет достигать высокой степени радикальности вмешательства [22, 43].
При невозможности выполнения радикального эндоскопического лечения или достижения адекватного безрецидивного периода на фоне проводимого лечения рядом авторов предлагается выполнять антрумэктомию. Данное вмешательство приводит к значительному уменьшению числа гастрин-продуцирующих клеток, расположенных в антральном отделе желудка, и как следствие – снижению уровня гастрина с последующим регрессом опухолевой ткани [14, 16, 44, 45]. Показанием к применению более агрессивных методов хирургического лечения являются инвазия мышечного слоя стенки желудка [46]; размер опухоли >2 см, что значительно повышает риск регионарного метастазирования [17]; невозможность выполнения радикального эндоскопического лечения [35]; а также желудочно-кишечное кровотечение при условии невозможности выполнения адекватного эндоскопического гемостаза [47]. Вопрос о применении консервативных методов лечения при НЭО I типа, таких как прием разбавленной соляной кислоты или применение аналогов соматостатина, остается дискуссионным. Поэтому данные подходы могут быть рекомендованы только в случаях, когда проведение эндоскопического или хирургического лечения невозможно [45, 48–50].
При НЭО II типа, как и при I типе, применяют эндоскопические методы лечения, а также аналоги соматостатина, однако прогноз для таких больных в значительной степени определяется успехом лечения основного заболевания, т.е. гастриномы [16, 39, 51].
Основной метод лечения НЭО желудка III типа и низкодифференцированных НЭК G3 – это хирургическое вмешательство в объеме гастрэктомии или резекции желудка с регионарной лимфаденэктомией [48, 52, 53]. При инвазии высокодифференцированной опухоли III типа в пределах слизистой оболочки или подслизистого слоя возможно выполнение и внутрипросветного эндоскопического лечения в объеме эндоскопической резекции слизистой оболочки с диссекцией в подслизистом слое [54].
При мелкоклеточном раке желудка возможно проведение самостоятельной консервативной терапии (химиотерапия, химиолучевая терапия), поскольку результаты хирургического лечения неудовлетворительны и мало отличаются от таковых при консервативном лечении [55, 56].
Метастатические НЭО
В случае метастатических НЭО желудка хирургическое вмешательство в отношении первичного очага и отдаленных метастазов, в частности в печени, оправданно при наличии атипичного карциноидного синдрома или в случае возможности выполнения циторедукции в объеме R0 [57–59]. Более того, выполнение полной циторедукции значительно улучшает показатели общей выживаемости [57–64]. Во всех остальных случаях оптимальным методом остается консервативное лечение.
По данным исследований PROMID и CLARINET, применение аналогов соматостатина при метастатических нерезектабельных НЭО оказывает антипролиферативный эффект, увеличивая время до прогрессирования и показатели общей выживаемости независимо от гормональной активности опухоли [31, 65, 66]. На основании полученных данных терапия высокими дозами аналогов соматостатина (октреотид от 30 мг каждые 28 дней, ланреотид 120 мг каждые 28 дней) является стандартом лечения метастатических форм высокодифференцированных НЭО желудка, главным образом при III типе. В качестве второй линии терапии возможно применение таргетной терапии (эверолимус) и химиотерапии, однако эффективность подобного лечения для НЭО желудка не подтверждена серьезными исследованиями.
В случае генерализованных НЭО G3 схемой терапии первой линии является комбинация цисплатина и этапозида [67], в то время как терапия второй линии в данный момент отсутствует [31]. В проведенном недавно ретроспективном исследовании применение темозоломида и капецитабина данной группой больных позволило добиться частичного ответа от 33% участников, что требует дальнейшего изучения этой комбинации препаратов [68]. Также довольно оптимистичные предварительные результаты были получены при использовании фторурацила или капецитабина в сочетании с оксалиплатином или иринотеканом [69, 70]. В отношении применения лекарственной терапии в адъювантном режиме проведено лишь одно небольшое (n=52) исследование в группе пациентов после резекции печени, которые получали комбинацию фторурацила и стрептозотоцина. Не было отмечено никаких статистически значимых различий в показателях выживаемости между основной и контрольной группами, а также группой исторического контроля [71].
Выводы
НЭО желудка представляют собой неоднородную группу заболеваний, различающихся по клиническому течению, подходам к терапии и прогнозу. В основе правильного выбора лечебной тактики лежит определение нейроэндокринной природы опухоли и ее типа по существующим классификациям. Лечение пациентов с НЭО желудка может варьироваться от малоинвазивных эндоскопических методик (карциноиды I, II типов) до агрессивных программ комбинированного и комплексного лечения (НЭК G3), потому информированность о различиях между разными типами НЭО желудка служит ключевым фактором при выборе лечебной тактики.
Литература
1. Янкин А.В. Нейроэндокринные опухоли желудочно-кишечного тракта. Практическая онкология. 2005:6(4):227–33.
2. Modlin I.M., Lye K.D., Kidd M. A 5-decade analysis of 13,715 carcinoid tumors. Cancer. 2003;97(4):934–59.
3. Landry C.S., Brock G., Scoggins C.R., McMasters K.M., Martin R.C. 2nd. A proposed staging system for gastric carcinoid tumors based on an analysis of 1,543 patients. Ann. Surg. Oncol. 2009;16(1):51–60.
4. Mulkeen A., Cha С. Gastric carcinoid. Curr. Opin. Oncol. 2005;17(1):1–6.
5. Modlin I.M., Oberg K., Chung D.C., Jensen R.T., de Herder W.W., Thakker R.V., Caplin M., Delle Fave G., Kaltsas G.A., Krenning E.P., Moss S.F., Nilsson O., Rindi G., Salazar R., Ruszniewski P., Sundin A. Gastroenteropancreatic neuroendocrine tumours. Lancet Oncol. 2008;9(1):61–72.
6. Burkitt M.D., Pritchard D.M. Pathogenesis and management of gastric carcinoid tumours. Aliment. Pharmacol. Ther. 2006;24(9):1305–20.
7. Hodgson N., Koniaris L.G., Livingstone A.S., Franceschi D. Gastric carcinoids: a temporal increase with proton pump introduction. Surg. Endosc. 2005;19(12):1610–12.
8. Havu N. Enterochromaffin-like cell carcinoids of gastric mucosa in rats after life-long inhibition of gastric secretion. Digestion. 1986;35(Suppl 1):42–55.
9. Kloppel G. Oberndorfer and his successors: from carcinoid to neuroendocrine carcinoma. Endocr. Pathol. 2007;18(3):141–44.