Оментобурсит что это такое
Основной причиной летальных исходов при остром деструктивном панкреатите в настоящее время являются гнойно-септические осложнения. Будучи инфицирован гнойно – гнилостными микроорганизмами, некротический процесс склонен распространятся на отдаленные от своего источника отделы. Этому могут способствовать агрессивные свойства гноя, содержащего большое количество панкреатических ферментов и анатомические особенности забрюшинного пространства, допускающие сообщения между теми или иными его отделами. Развитие осложнений происходит, как правило, per continuitatem, путем расплавления брюшинного листка, отделяющего забрюшинно располагающуюся поджелудочную железу от свободной брюшной полости [1,2,5]. Исследование по лечению и применению хирургического вмешательства при гнойном оментобурсите является актуальной задачей.
Целью работы является рассмотрение проблемы диагностики и хирургической тактики при наиболее часто встречающемся гнойном осложнении деструктивного панкреатита – оментобурсите.
К сожалению, до сих пор не выработано четких единых рекомендаций относительно способов хирургического лечения гнойного оментобурсита (за исключением нескольких региональных стандартов)[6,7,8]. Практически ежегодно проблемы лечения осложнений деструктивного панкреатита обсуждаются на многочисленных конференциях и съездах, однако на настоящий момент летальность при инфицированном панкреонекрозе составляет до 70%[4,5,7]. Открытыми остаются вопросы относительно места малоинвазивных методик (пункционные методы и дренирование) в арсенале лечащего врача, сроки выполнения, показания и противопоказания к оперативным вмешательствам[4]. Проблема усугубляется тем, что рекомендуемые в литературных источниках современные методы инструментальной (МРТ, спиральная КТ, тонкоигольная пункция-аспирация под УЗ-контролем) и лабораторной (прокальцитониновый тест) диагностики практически недоступны на уровне хирургических отделений районных и небольших городских больниц.
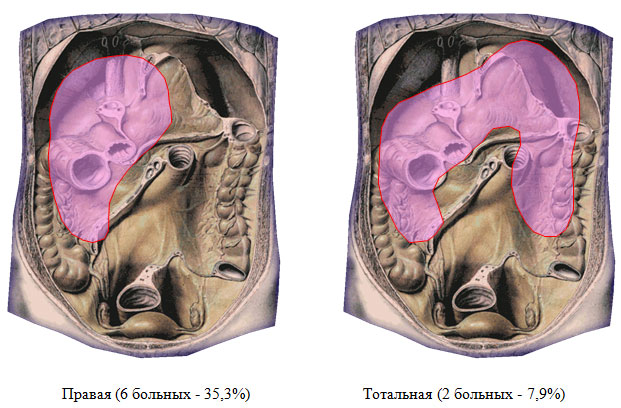
За период 2007-2011 гг. в хирургическом отделении ФГУЗ МСЧ №98 проведено лечение 37 больных деструктивным панкреатитом, в течение заболевания которых зарегистрированы гнойно-септические осложнения. При разборе хирургической анатомии присоединившихся осложнений выявлено следующее. Разрушение заднего листка брюшины над поджелудочной железой и проникновение гноя в сальниковую сумку вызывает гнойный оментобурсит (центральная локализация – 27 больных, 72,9%). Прорыв гноя через винслово отверстие приводит к образованию подпеченочного или правостороннего гнойника (6 пациентов – 16,3%), разрушение левых отделов mesocolon и желудочно-ободочной связки – к образованию левостороннего поддиафрагмального абсцесса (у 2 больных – 5,4%). Под тотальной локализацией имелось в виду абсцедирование обширных участков некроза парапанкреатической и параколярной клетчатки как по ходу восходящей, так и по ходу нисходящей ободочной кишки (2 человека – 5,4%). Области локализации панкреатогенных абсцессов приведены на рисунке 1. Проведен анализ историй болезни 27 пациентов, у которых течение деструктивного панкреатита осложнилось присоединением гнойного оментобурсита (в качестве единственного первичного гнойного очага).
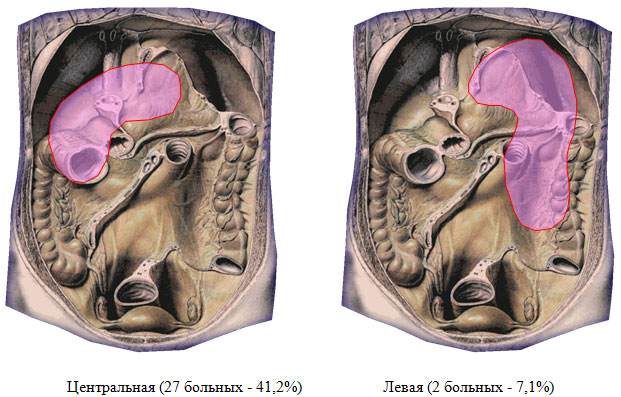
Рисунок 1. Локализация панкреатогенных абсцессов
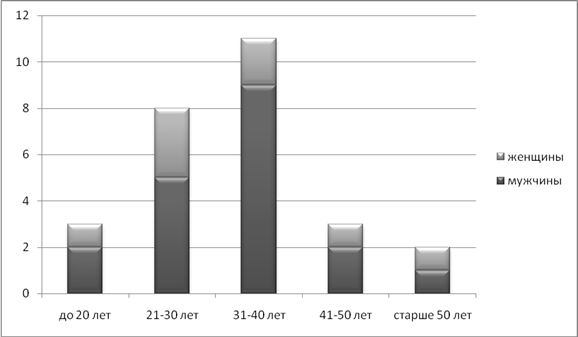
Возраст больных составил 17- 55 лет. Мужчин было 19 человек (70,4%), женщин – 8 (29,6%). Состав больных разделённых по возрастам приведён на рисунке 2.
Рисунок 2. Состав больных по полу и возрасту
Установление наличия гнойного осложнения базировалось на характерной клинической картине, данных инструментального исследования (УЗИ, КТ) и лабораторных тестах (определение активности панкреатических ферментов, прокальцитониновый тест) и являлось безусловным показанием к активной хирургической тактике.
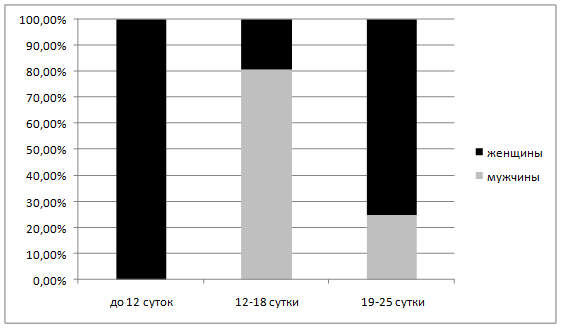
Часть исследованных больных (26 человек) подверглись оперативному лечению, выполненному на 10-15 сутки от момента начала заболевания, 3 пациентам после предварительно выполненной компьютерной томографии было произведено эхоконтролируемое дренирование сальниковой сумки. Из числа больных последней группы у 2 человек манипуляция не дала положительного результата и они были оперированы традиционным способом через 3 суток после первичного дренирования. У всех больных операция выполнялась полуоткрытым способом, предусматривающим установку трубчатых дренажей вместе с тампоном Penrose. В послеоперационном периоде больным проводилась интенсивная инфузионно-трансфузионная, антибактериальная, антисекреторная, симптоматическая терапия.
Присоединение при деструктивном панкреатите гнойно-септических осложнений является абсолютным показанием к оперативному вмешательству. Этот факт в настоящее время не вызывает сомнений, т.к. дальнейшее консервативное ведение больных с несанированными гнойными очагами бесперспективно и ведет к неблагоприятному исходу [4,9].
Рисунок 3. Сроки оперативных вмешательств у больных с гнойным оментобурситом.
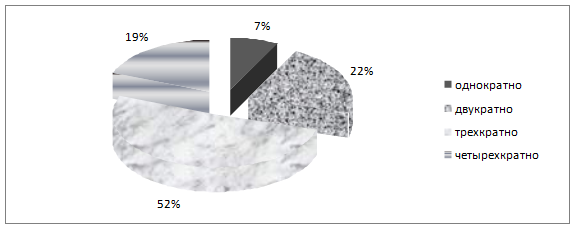
Полуоткрытый тип операций у больных с гнойным оментобурситом, завершающийся формированием оментобурсостомы предусматривает возможность многократных некр- и секвестрэктомий без риска подвергать больного повторной (пусть даже запрограммированной) лапаротомии, на что указывает большое количество авторов [3,4,5,7,9]. Однократная некрозосеквестрэктомия, как правило, не несет радикального характера и возникает необходимость в повторных санациях сальниковой сумки. В исследуемой группе однократная санация проведена у 2 (7%) человек, двухкратно – у 6 (22%), трехкратно – у 14(52%), четырехкратно – у 5 (19%) пациентов (рисунок 4).
Рисунок 4. Кратность некрсеквестрэктомий у больных с гнойным оментобурситом
Отдельно следует выделить группу из 3 больных, у которых была предпринята попытка дренирования жидкостного образования под УЗ-контролем. Во всех трех случаях попытка увенчалась успехом и сальниковая сумка была санирована через установленные дренажи. Однако в последующем течение заболевания у 2 пациентов, сопровождающееся длительным выделением гнойного экссудата (более 7-10 дней) и его объемом (более 100 мл/сут), несмотря на ежедневные санации растворами антисептиков и консервативную терапию, заставило заподозрить наличие секвестрированных очагов некроза, поддерживающих воспалительный процесс. Это было установлено при повторной КТ и больные были оперированы стандартным полуоткрытым способом.
В ходе проведённых исследований получены следующие результаты:
Работа выполнена в рамках Федеральной целевой программы ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009-2013 годы.
Рецензенты:
Сарвилина Ирина Владиславовна, д.м.н., ген. директор медицинского центра «Новомедицина», ведущий научный сотрудник ЗАО НПО «Европа-Биофарм», г. Ростов-на-Дону.
Масляков Юрий Степанович, д.м.н., профессор, зав. кафедрой «Фармокология и клиническая формакология» ГБОУ ВПО «РостГМУ» Минздрава России, г. Ростов-на-Дону.
П.Г.Кондратенко, А.А.Васильев, М.В.Конькова
Острый панкреатит: современный взгляд на проблему
П.Г.КОНДРАТЕНКО, д.м.н., профессор; А.А.ВАСИЛЬЕВ, к.м.н.; М.В.КОНЬКОВА, к.м.н.
/Донецкий государственный медицинский университет им.М.Горького, клиника госпитальной хирургии и эндоскопии/

Для инфицированного панкреонекроза характерны расплавление некротизированной ткани железы (обычно с 5–7-х суток от начала заболевания), секвестрация (с 3–4-й недели от начала заболевания), что обусловливает длительное тяжелое состояние больного.
Панкреонекроз характеризуется фазовым течением, причем каждой его фазе соответствует определенная клиническая форма.
I фаза — ферментативная — наблюдается в первые 5 суток заболевания. В этот период происходит формирование панкреонекроза различной протяженности, развитие эндотоксикоза (средняя длительность гиперферментемии составляет 5 суток), а у части пациентов — полиорганной недостаточности и эндотоксинового шока. Максимальный срок формирования панкреонекроза составляет 3 суток, в дальнейшем он, как правило, не прогрессирует. Однако при тяжелом панкреатите период формирования панкреонекроза гораздо меньше — 24–36 часов.
II фаза — реактивная (2-я неделя заболевания) — характеризуется началом асептической воспалительной реакции в очагах некроза в ПЖ и парапанкреатической клетчатке. Клинически проявляется наличием парапанкреатического инфильтрата и резорбтивной лихорадкой.
Кроме того, реактивная фаза острого деструктивного панкреатита характеризуется:
— лабораторными показателями синдрома системной воспалительной реакции: лейкоцитозом со сдвигом формулы влево, лимфопенией, увеличенной СОЭ, повышением концентрации фибриногена, С-реактивного протеина и др.;
— признаками парапанкреатического инфильтрата на сонограмме.
Мониторинг парапанкреатического инфильтрата заключается в динамическом исследовании клинико-лабораторных показателей и данных повторного ультразвукового исследования (УЗИ) (не менее 4 исследований на второй неделе заболевания).
В конце второй недели заболевания целесообразно проведение компьютерной томографии ПЖ, так как к этому сроку у подавляющего большинства пациентов наблюдается один из трех возможных исходов реактивной фазы:
— рассасывание, когда наблюдается редукция местных и общих проявлений острой воспалительной реакции;
— асептическая секвестрация панкреонекроза с исходом в кисту ПЖ: сохранение размеров парапанкреатического инфильтрата при нормализации самочувствия и стихании синдрома системной воспалительной реакции на фоне сохраняющейся гиперамилаземии;
— септическая секвестрация (развитие гнойных осложнений).
III фаза — расплавления и секвестрации (начинается с 3-й недели заболевания, может длиться несколько месяцев). Секвестры в ПЖ и в забрюшинной клетчатке начинают формироваться с 10–14-х суток от начала процесса. Возможны два варианта течения этой фазы:
— асептическое расплавление и секвестрация, или стерильный панкреонекроз, который характеризуется образованием постнекротических кист и свищей;
— септическое расплавление и секвестрация, или инфицированный панкреонекроз. О наличии у пациента гнойно-некротического парапанкреатита судят на основании инструментальных и клинико-лабораторных данных.
Одним из наиболее информативных методов неинвазивной диагностики воспаления поджелудочной железы является неотложная сонография.
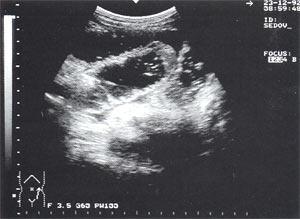
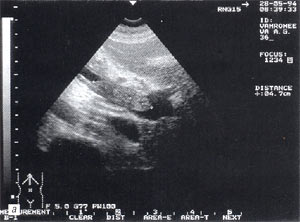
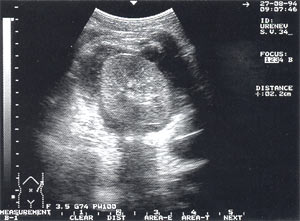
При остром отечном панкреатите поджелудочная железа увеличена в размерах, имеет “балонообразную” форму, контуры ее неровные, структура паренхимы диффузно-неоднородная, эхогенность — от умеренно повышенной до высокой. Отмечается расширение вирсунгова протока до 0,3–0,5 см (рис.1).
При всех формах ОП может выявляться воспалительная жидкость в брюшной полости в виде анэхогенных скоплений в отлогих ее участках.
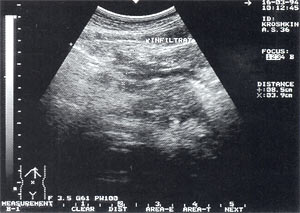
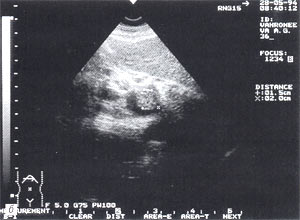
При мелкоочаговом панкреонекрозе ПЖ увеличена в размерах, отмечается неровность и нечеткость контуров за счет инфильтрации парапанкреатической зоны. Паренхима органа диффузно неоднородная, эхогенность повышена. В паренхиме выявляются гипоэхогенные очаги малых размеров (до 1 см в диаметре) с ровными контурами, расположенные диффузно, иногда сливающиеся между собой и сочетающиеся с гиперэхогенными зонами (рис.2).
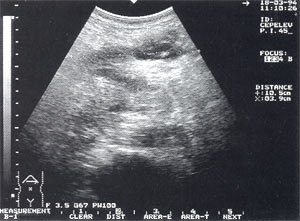
При крупноочаговом панкреонекрозе на сонограмме обнаруживаются все вышеперечисленные признаки, однако зоны деструкции более 1 см в диаметре (рис.3).
При субтотальном панкреонекрозе на фоне деструктивных изменений ПЖ отмечаются гипоэхогенные очаги, расположенные чаще в проекции “тело–хвост”, имеющие ровные контуры с наличием мелкозернистых включений. Для этой формы панкреатита характерно затухание эхо-сигнала по нижнему контуру ПЖ. При энергетическом допплеровском исследовании отмечается более выраженное, чем при отечном ОП, усиление кровотока. Кроме того, специфическими допплеровскими признаками этой формы заболевания являются деформация паренхиматозного сосудистого рисунка в зоне деструктивных изменений, а также наличие артериовенозного шунтирования.
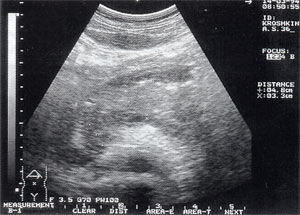
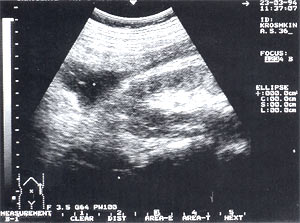
Оментобурсит сонографически определяется в виде гипоэхогенной зоны различной протяженности без четких границ, имеющей вид полосы, вытянутого овала или веретена, расположенной вдоль участка “тело–хвост” ПЖ (рис.4).
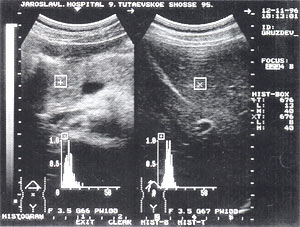
Абсцесс ПЖ или сальниковой сумки. В проекции сальниковой сумки или ПЖ сонографически определяется гипоэхогенный очаг от 3 до 5 см и более в диаметре с ровными контурами, имеющий толстые стенки и неоднородное содержимое (рис.5).
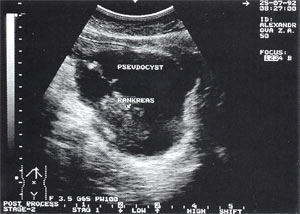
Псевдокиста лоцируется, как анэхогенное овальное или округлое образование с ровными четкими контурами, ярко очерченной капсулой, без внутренних эхоструктур. Размеры кист — от 1,5 до 12 см и более в диаметре.
Парапанкреатический инфильтрат определяется в виде неоднородного образования повышенной эхогенности в проекции ПЖ без четких контуров и границ.
Ряд авторов придерживается мнения о преимуществах компьютерной томографии (КТ) в диагностике ОП.
Список рекомендованной литературы находится в редакции.
Гнойный панкреатит
Гнойный панкреатит – это флегмонозное воспаление поджелудочной железы с формированием микро- или макроабсцессов в ее паренхиме. Является одной из самых тяжелых форм острого панкреатита. Наблюдаются изнуряющие опоясывающие боли в животе, тошнота, рвота, изжога, диарея, в тяжелых случаях – полиорганная недостаточность. Диагноз ставится на основании клинического осмотра, ультразвукового исследования, РХПГ и лапароскопии. Лечение осуществляется в условиях отделения реанимации, включает в себя инфузионную терапию, введение спазмолитиков и обезболивающих препаратов, ингибиторов протеаз, кардиотоников; при необходимости проводится хирургическое вмешательство.
Общие сведения
Гнойный панкреатит – грозное заболевание, развивающееся при сочетании нескольких этиологических факторов, приводящее к диффузному гнойному воспалительному процессу в ткани поджелудочной железы. Острый панкреатит – третье по частоте хирургическое заболевание, нуждающееся в неотложной оперативной помощи, после острого аппендицита и холецистита.
Среди всех вариантов острого воспаления поджелудочной железы гнойный панкреатит встречается у каждого десятого пациента. В целом патология поражает 0,02-0,08% населения мира ежегодно, подавляющее большинство пациентов – мужчины. Опасность заключается в высоком риске развития полиорганной недостаточности и последующего летального исхода при несвоевременной диагностике и начале лечения.
Причины
Для развития гнойного панкреатита недостаточно только попадания инфекции в паренхиму поджелудочной железы, а требуется сочетание нескольких этиологических факторов. К предрасполагающим факторам гастроэнтерологи и абдоминальные хирурги относят употребление большого количества алкоголя (алкогольный панкреатит), курение, погрешности в питании, злоупотребление некоторыми лекарственными препаратами.
Благоприятным фоном могут служить заболевания гепатобилиарной системы, приводящие к нарушению оттока желчи: холелитиаз, холангиты, кисты, стенозы и опухоли желчевыводящих протоков (билиарный панкреатит); травмы и кисты поджелудочной железы. На фоне воздействия перечисленных факторов происходит повышение давления в желчных путях, что способствует ретроградному забросу панкреатического сока в протоки поджелудочной железы.
Патогенез
В основе патогенеза лежат сосудистые нарушения и преждевременная активация панкреатических ферментов. Собственные ферменты расплавляют ткань поджелудочной железы, вызывая асептическое воспаление. Из-за аррозии стенки мелких сосудов органа возникают множественные кровоизлияния в паренхиму (геморрагический панкреатит). При наличии очага хронической инфекции (холецистит, холангит, аппендицит, тяжелые бактериальные или вирусные заболевания и др.) бактерии по желчным путям, с током крови либо по лимфатическим сосудам попадают в ткань железы, вызывая ее инфицирование.
Чаще всего воспалительный процесс принимает диффузный характер, на его фоне формируется множество микроабсцессов, с течением времени сливающихся в большие гнойные полости. При вскрытии абсцессов гной может попадать в брюшную полость и кровоток, приводя к распространению воспаления на другие органы и системы. Для гнойного панкреатита, в отличие от абсцесса поджелудочной железы, характерно диффузное воспаление, множество гнойных очагов.
Попадание гноя, продуктов распада и ферментов поджелудочной железы в кровоток и брюшную полость приводит к значительной интоксикации, нарушению работы жизненно важных внутренних органов и в итоге к полиорганной недостаточности. Если не распознать гнойный панкреатит до этого этапа, не начать интенсивную патогенетическую терапию, поражение внутренних органов может стать необратимым, что в результате приведет к летальному исходу.
Симптомы гнойного панкреатита
От начала заболевания до появления яркой клинической картины панкреатита может пройти как несколько дней, так и несколько недель. Обычно первым клиническим признаком является панкреатическая колика – возникновение острой опоясывающей боли в верхней половине живота. Боль иррадиирует в спину, лопатки, за грудину. Интенсивность боли может быть настолько сильной, что иногда приводит к потере сознания. Часто боль сопровождается упорной рвотой, которая не приносит облегчения пациенту, возникает даже после глотка воды.
Рвота провоцирует повышение внутрибрюшного давления, вызывая заброс панкреатических соков в поджелудочную железу, из-за чего интенсивность боли после рвоты повышается еще больше. Пациент часто занимает вынужденное положение на боку с подтянутыми к груди коленями. Из-за нарушения деятельности поджелудочной железы развиваются симптомы диспепсии: тошнота, отрыжка, повышенный метеоризм, диарея. Стул жидкий, содержит непереваренные частички пищи и жиры. Сочетание тяжелого диспепсического, болевого и интоксикационного синдромов приводит к возникновению беспокойства, плаксивости, иногда – к развитию панкреатогенного психоза.
При прогрессировании процесса возникает динамическая кишечная непроходимость, проявляющаяся значительным вздутием живота, рвотой застойным содержимым. При пальпации живота в верхней половине отмечается резкая болезненность, возможно появление симптомов раздражения брюшины. На коже передней брюшной стенки выступают цианотичные пятна, заметен отек жировой клетчатки в области поясницы. На первых этапах развития заболевания температура тела субфебрильная, но после присоединения инфекции и диффузного воспалительного процесса отмечается значительная гипертермия.
Осложнения
Токсическое воздействие панкреатических ферментов на костный мозг проявляется выраженной тромбоцитопенией, анемией. В результате гнойного расплавления тканей поджелудочной железы и окружающих органов могут формироваться свищи, ферментативный перитонит, гнойный плеврит; аррозия крупных сосудов приводит к профузным кровотечениям; в результате воспалительного процесса возникают тромбозы и тромбофлебиты вен порто-кавальной системы. Возможно формирование септического процесса, в котором гнойный панкреатит служит первичным очагом.
Выраженная интоксикация приводит к поражению сердца – отмечается постоянная тахикардия, артериальная гипотензия. Токсический миокардит вызывает развитие тяжелой недостаточности кровообращения. Поражение легких может сопровождаться респираторным дистресс-синдромом, дыхательной недостаточностью. Прогрессирующая полиорганная недостаточность в итоге может привести к летальному исходу.
Диагностика
При проведении перечисленных исследований будет обнаружено увеличение размеров органа за счет отека, формирование множества гнойных полостей, отек и воспалительная инфильтрация забрюшинной клетчатки вокруг железы. В сальниковой сумке может быть виден выпот. К назначению ретроградной холангиопанкреатографии нужно подходить очень осторожно – данная процедура может привести к развитию панкреонекроза. РХПГ выполняется только для исключения закупорки общего желчного протока конкрементами, как причины гнойного панкреатита, либо после стабилизации состояния пациента. По показаниям назначается эзофагогастродуоденоскопия, МСКТ органов брюшной полости.
Обязательно проводятся динамические исследования по определению уровня ферментов поджелудочной железы в крови и моче. При затруднениях в диагностике рекомендуется диагностическая лапароскопия. Показаниями к этой операции являются развитие панкреатита, гипертензия в желчных путях, подозрение на панкреонекроз. Дифференцировать гнойный панкреатит следует с другой острой хирургической патологией: холециститом, аппендицитом, прободной язвой желудка и ДПК, кишечной непроходимостью, тромбоэмболией мезентериальных сосудов.
Лечение гнойного панкреатита
Проводится высокообъемная инфузионная терапия в сочетании с форсированным диурезом для выведения из кровотока токсинов, снижения уровня ферментов поджелудочной железы, уменьшения отека органа. В состав инфузионной терапии обязательно включаются ингибиторы протеолитических ферментов (апротинин), а при снижении уровня глюкозы на фоне деструкции ткани поджелудочной железы – концентрированные растворы сахаров. Для коррекции водно-электролитных нарушений требуется введение растворов солей, кальция, магния.
Прогноз и профилактика
Прогноз гнойного панкреатита всегда очень серьезен из-за сопутствующих ему тяжелых осложнений. Даже после выздоровления такие пациенты требуют длительного наблюдения гастроэнтеролога, серьезного восстановительного лечения. Профилактика заключается в полном отказе от алкоголя и курения, соблюдении режима питания, своевременном лечении хронических заболеваний гепатобилиарной системы (холелитиаз, холецистит и др.).
Опыт применения эхографии при остром панкреатите и его осложнениях
УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5″ высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Материалы и методы
Результаты
На основе наших наблюдений выявлены следующие сонографические особенности острого панкреатита:
Изменения непосредственно в поджелудочной железе:
Рис. 1. Острый панкреатит, деструктивная форма. Увеличение размеров поджелудочной железы, нечеткость контуров, увеличение расстояния между задней стенкой желудка и поджелудочной железы.
Рис. 2. Острый панкреатит, повышение эхогенности поджелудочной железы (по сравнению с эхогенностью печени).
Изменения в брюшной полости, являющиеся косвенными признаками острого панкреатита и относящиеся к его осложнениям:
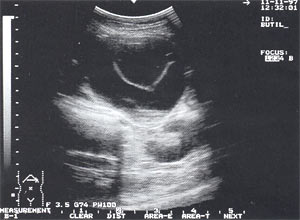
Рис. 3. Псевдокиста поджелудочной железы при остром панкреатите в виде анэхогенного образования с четкими контурами, однородной структурой, с наличием гиперэхогенных включений (детрит поджелудочной железы).
Рис. 4. Расширенные петли тонкого кишечника до 3,5 см, заполненные жидким содержимым на фоне свободной жидкости в брюшной полости.
Рис. 6. Инфильтрат в проекции большого сальника с анэхогенным включением до 4 см (абсцедирование).
Восходящий медиастенит, отмечаемый другими авторами, нами не наблюдался.
Разрывы псевдокист поджелудочной железы при ультразвуковой диагностике наблюдались у 2 больных (0,7%).
Кровоизлияние в псевдокисту поджелудочной железы с формированием организованной гематомы (рис. 9) отмечено у 1 пациента (0,35%).
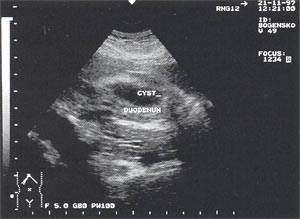
Рис. 10. Атипично расположенная псевдокиста поджелудочной железы (парадуоденально) в виде анэхогенного образования округлой формы с четкими контурами, однородной структурой, размером до 4,5 см, расположенного рядом с двенадцатиперстной кишкой.
Разрывы селезенки вследствие портальной гипертензии (нами не наблюдались).
Рис. 11. Левосторонний панкреатогенный паранефрит, визуализирующийся в виде жидкостного образования, окружающего почку со всех сторон. Поперечный срез.
Заключение
Проведенное исследование показывает, что ультразвуковая диагностика должна быть обязательным элементом диагностического алгоритма у больных острым панкреатитом. Для повышения диагностической ценности эхографии необходима определенная последовательность в выполнении ультразвукового исследования: детальный осмотр парапанкреатических тканей и самой железы; осмотр всех отделов брюшной полости на предмет свободной жидкости и инфильтратов; осмотр плевральных полостей и полости перикарда на наличие выпота; детальный осмотр внутри- и внепеченочных желчных протоков; прицельный осмотр сосудов системы воротной вены; исследование забрюшинного пространства; динамическое наблюдение (частота повторного УЗИ определяется степенью тяжести заболевания и вероятностью развития осложнений).
Для улучшения получаемых результатов УЗИ могут быть рекомендованы следующие технические приемы:
Литература
УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5″ высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.