Обследование при мастопатии, болях в молочной железе и др.
МАСТОПАТИЯ
– разнородная группа заболеваний молочной железы, возникающая, чаще всего, на фоне гормональных нарушений.
Проявляется в двух формах:
диффузная мастопатия – болезненное уплотнение ткани всей молочной железы, иногда сопровождающееся выделениями из соска (белыми, желтыми либо зеленоватыми);
узловая мастопатия – единичные или множественные узлы в молочной железе неправильной формы, с четкими границами. Диагностируются при маммографическом, ультразвуковом исследованиях и пункции узлов.
При планировании эффективного лечения мастопатии важно проведение полноценного обследования органов внутренней секреции, в том числе щитовидной железы. Такое лечение может и должен проводить только опытный гинеколог-эндокринолог.
КИСТА МОЛОЧНОЙ ЖЕЛЕЗЫ
– тонкостенная полость, содержащая жидкость. Диагностируется при маммографическом и ультразвуковом исследованиях, лечится посредством проведения пункции кистозной полости – удаления жидкости.
ГАЛАКТОЦЕЛЕ
– разновидность кисты, возникающая при кормлении грудью в связи с закупоркой млечного протока.
ГАЛАКТОРЕЯ
– выделение молока или молозива из сосков, не связанное с грудным вскармливанием. Галакторея чаще всего вызвана гиперпролактинемией (повышением в крови гормона пролактина). Причиной также может стать повышение уровня эстрогенов (женских половых гормонов).
У многих больных с незлокачественными заболеваниями наблюдаются выделения из сосков. Как правило, выделения небольшие, могут быть самого разнообразного цвета.
Особую тревогу вызывают кровянистые выделения, связанные с внутрипротоковой папилломой или раком молочной железы. С точки зрения онкологической настороженности, необходимо проводить обязательное цитологическое исследование этих выделений.
Патоморфолог может указать на наличие молозивных телец при галакторее, воспалительных изменений либо опухолевых клеток при раке.
ФИБРОАДЕНОМА
– доброкачественная опухоль, возникающая из клеток ткани молочной железы. Диагностируется при маммографическом и ультразвуковом исследованиях, для подтверждения диагноза необходима пункция опухоли.
Показанием к хирургическому удалению опухоли является ее прогрессирующее увеличение в объеме.
Разновидность фиброаденом – листовидная фиброаденома подлежит обязательному удалению, так как она может превратиться в саркому.
ЛИПОМА
– единичное, либо множественное, мягко-эластичное доброкачественное новообразование, которое формируется из жировой ткани. Чаще всего опухоли данного вида появляются в подкожно-жировой клетчатке.
Диагноз не вызывает затруднений.
Лечение, как правило, проводится при больших размерах опухоли, вызывающих косметический дефект.
ВНУТРИПРОТОКОВАЯ ПАПИЛЛОМА
– доброкачественная опухоль из клеток стенки протока, растущая внутри протока. Симптомом внутрипротоковой папилломы является выделение из соска прозрачной, «янтарной» или кровянистой жидкости. Диагностируется при специальном рентгенологическом исследовании – дуктографии и исследовании выделений под микроскопом.
Внутрипротоковая папиллома подлежит обязательному хирургическому удалению, так как из нее может развиться злокачественная опухоль.
МАСТИТ
– инфекционное либо асептическое воспаление ткани молочной железы, дифференцируется с диффузными и воспалительными формами рака.
ЖИРОВОЙ НЕКРОЗ (ОЛЕОГРАНУЛЕМА)
– вариант завершения воспалительного процесса или травмы молочной железы (иногда возникает после хирургического лечения или проведения лучевой терапии). Плотное узловое образование неправильной формы, дающее симптомы, сходные с узловыми формами рака молочной железы.
ГИНЕКОМАСТИЯ
– увеличение грудных желез у мужчин из-за гипертрофии железистой ткани.
Развитие гинекомастии связано с избытком (превышением) эстрогенов по отношению к тестостерону.
От гинекомастии необходимо отличать избыточное развитие жировой ткани в области ареолы (ложная гинекомастия).
Для подтверждения диагноза гинекомастии используются маммография и ультразвуковое исследование.
Лечение необходимо проводить с учетом патогенетического механизма развития заболевания (лечение заболеваний печени, щитовидной железы, отмена медикаментов …). Больным с прогрессивно увеличивающейся гинекомастией, неподдающейся терапии эндокринных нарушений, показано хирургическое лечение – трансареолярная мастэктомия.
РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
– злокачественная опухоль. Выделяют диффузные и узловые формы рака молочной железы.
Узловые формы рака при небольших размерах опухоли клинически похожи на любое узловое образование, чаще всего на узловую мастопатию.
Диффузные формы труднее при клинической диагностике.
К особым формам относятся маститоподобные, рожистые и отечно-инфильтративные формы.
РАК ПЕДЖЕТА
– локализуется в области ареолы и соска, по виду напоминает экзему.
При прогрессировании заболевания сосок разрушается и на его месте возникает язвенная поверхность.
Чем опасен рак молочной железы?
Если не лечить, опухоль увеличивается, прорастает в кожу и грудную стенку, поражает ближайшие лимфоузлы. В других органах (легких, печени, костях, головном мозге) могут появиться отдаленные метастазы.
Придя в кабинет врача-онколога, Вам нужно будет пройти клинический осмотр.
Сначала врач опросит Вас и уточнит необходимые данные из Вашего анамнеза – то есть из истории заболевания, в основном акцентируя внимание на факторах риска.
Затем врач проведет пальпацию, то есть ощупывание молочных желез. Во время клинического обследования врач попросит вас принять различные положения – поднять руки, положить их на плечи врачу. Это делает более доступными для пальпации грудь и подмышечную впадину. В ряде ситуаций необходимо проведение пальпации не только в положении стоя, но и лежа на кушетке.
Врач проверит состояние сосков и ареол, а также наличие выделений из сосков. При появлении выделений из сосков врач-онколог возьмет мазок этих выделений для цитологического исследования.
Врач-онколог выберет оптимальную для Вас комбинацию основных методов лучевой диагностики заболеваний молочной железы, то есть маммографии и УЗИ, оценив показания и противопоказания к каждому из них.
На повторном приеме врач-онколог сопоставит результаты лучевых методов исследования с клинической картиной и определит тактику дальнейшего наблюдения и лечения. При необходимости врач-онколог совместно с врачом-рентгенологом или врачом ультразвуковой диагностики проводит биопсию.
Тревожные симптомы
Заметили хотя бы один из вышеперечисленных признаков? Обратитесь к онкологу-маммологу. Если в Вашей поликлинике нет онколога-маммолога, обратитесь к терапевту, гинекологу или хирургу. Они проведут предварительный осмотр и дадут направление в онкологический диспансер или специализированную клинику.
Записаться на консультацию:
+7 (916) 757 80 54
Филиал №1 Клиники женского здоровья МКНЦ (г. Москва, ул. Гончарная, д. 23)
+7 (916) 757 80 05
Филиал №2 Клиники женского здоровья МКНЦ (г. Москва, Верхний Предтеченский пер., д. 8)
Филлоидная фиброаденома
Пациентка 13 лет. Самостоятельно обнаружила уплотнение в молочной железе и янтарные кровянистые выделения из соска.
Клинический осмотр: молочные железы развиты правильно, на коже левой молочной железы в верхних квадрантах – стрии (растяжки кожи), у ареолы – легкое покраснение и раздражение кожи (со слов пациентки за счет компрессов).
Пальпаторно: правая молочная железа мягкая, без особенностей; левая молочная железа плотная по всему объему. Выделения из левого соска при надавливании янтарные.
Взят мазок.
Цитология: эритроциты, макрофаги.
Молочные железы представлены железистой тканью. Слева за ареолой – полицикличное образование с неоднородной эхоструктурой, четкими, ровными контурами и анэхогенным включением до 3 см. Усилен кровоток. Размеры выходят за границы визуализации. Лимфоузлы структурные
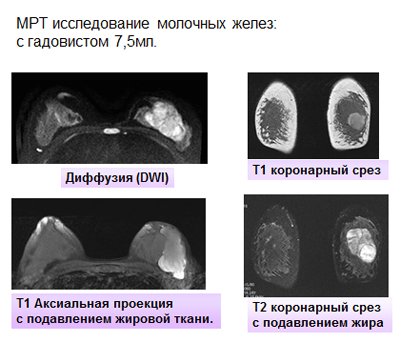
Для решения вопроса об объеме последующего оперативного лечения и активности процесса проведено МРТ исследование молочных желез в аксиальной и коронарной плоскости, в режиме 3D, а также с внутривенным введением 7,5 мл гадовиста в режиме динамического контрастного усиления. В левой молочной железе определяется объемное образование, занимающее практически всю зону железистой ткани, размером 6,6×4,6×5,2 см. Структура опухоли дольковая с множественными сосудами по междольковым перегородкам. В нижних отделах опухоли визуализируется неправильной округлой формы киста с геморрагическим содержимым размером до 3,3 см в диаметре (рис. 1)
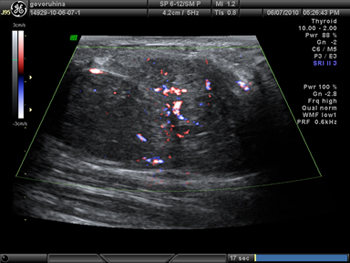
Рис. 1. Ультразвуковая картина: гипоэхогенное образование, выходящее за размер датчика, с усиленным кровотоком и полицикличными контурами.
В режиме диффузии данная зона патологически изменена. При динамическом контрастном усилении отмечается выраженное накопление контрастного препарата опухолью и капсулой кисты, а так же внутрикапсульными разрастаниями (рис. 2-3).
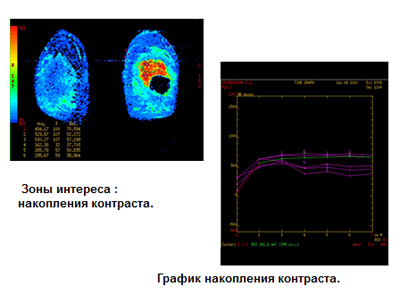
Рис. 3. График накопления контрастного вещества.
Правая молочная железа без особенностей. Лимфоузлы в аксиллярных зонах визуализируются, увеличены, структурны.
После инструментальных методов диагностики, проведена диагностическая пункция образования из нескольких мест.
Цитология: обильное скопление клеток кубического эпителия (3-х мерные структуры), оксифильные массы.
Учитывая клиническую картину, объемность опухоли, активность кровотока в ней, УЗИ, МРТ-исследование и график накопления контраста, а также результаты цитологического исследования был поставлен диагноз: «Листовидная фиброаденома с кистозным компонентом левой молочной железы».
Проведена энуклеация опухоли молочной железы.
Гистология: филлоидная опухоль (фото 1).
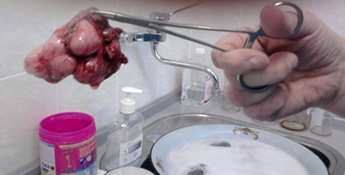
Фото 1. Макропрепарат (филлоидная фиброаденома)
При повторном обследовании пациентки через 3 месяца после оперативного вмешательства асимметрии молочной железы не наблюдается. Пальпаторно левая молочная железа без особенностей. При УЗИ выявлена рубцовая деформация тканей молочной железы в месте оперативного вмешательства (фото 2).
Интерпретация клеточного состава, особенности изменений в клетках при различных патологических процессах
Основу цитологической диагностики составляет изучение клеток, изменений в их расположении и строении. Критерии цитологической диагностики включают анализ клеточного и неклеточного состава: количество клеток, наличие клеток разного типа, их расположение в структурах или разрозненно, вид структур, размер, форма, строение клеток и ядер, наличие или отсутствие клеточного и ядерного полиморфизма и другие параметры. По характеру и степени выраженности отклонения от нормального клеточного состава судят о природе патологического процесса. По признакам, характерным для определенных тканей, судят о тканевой принадлежности опухоли. При этом учитывают фон препарата — элементы крови, бесструктурное вещество, коллоид, жир и др.
Количество клеток в мазке определено прочностью межклеточных связей и обилием стромы. Богатый клеточный состав бывает в низкодифференцированных опухолях, гемато- и лимфосаркоме, нейроэндокринных опухолях. Скудный материал и даже единичные клетки встречают, в частности, при скиррозном и дольковом раке молочной железы.
Расположение клеток. Клетки в мазке могут располагаться разрозненно или в виде структур. Для доброкачественных поражений характерно правильное, упорядоченное расположение клеток, одинаковое расстояние между ними, сходные размеры клеток и ядер, образующих структуру. Для злокачественных новообразований характерны структуры (комплексы, пучки) с неупорядоченным расположением клеток.
Размеры клеток и ядер. Размеры клеток по возможности оценивают в сравнении с размерами нормальных клеток того же типа. Размеры ядер обычно сравнивают с размером эритроцита (в норме достаточно стабильным, примерно 7 мкм). Соотношение размера ядра и цитоплазмы (ядерно-цитоплазматическое соотношение) также весьма различно в разных клетках, и при его оценке учитывают степень отклонения этого параметра от нормальной клетки того же типа.
Фон препарата часто имеет большое диагностическое значение. Фоном могут быть элементы периферической крови или воспаления, связанного с инфекцией, сопровождающего опухолевый и другие процессы, клеточный детрит, межуточное вещество. Фон препарата может иметь диагностическое значение при определении тканевой принадлежности или гистологической формы опухоли.
При реактивных и фоновых поражениях чаще всего увеличено число клеток (гиперплазия, пролиферация), размер ядер и отмечается их более интенсивная окраска (гиперхромия). Хроматин распределен сравнительно равномерно. В некоторых ядрах (особенно характерно для железистого эпителия) увеличен размер ядрышек. При некоторых состояниях изменен размер клеток и наблюдаются особенности окрашивания цитоплазмы.
Изменения в клеточном составе мазка при злокачественной опухоли характеризуются клеточным и ядерным полиморфизмом (различием характеристик разных клеток), образованием структур, отличающихся от нормальных, изменением фона препарата; для многих злокачественных опухолей характерен так называемый опухолевый диатез — реакция соединительной ткани на инвазию (прорастание опухоли).
Если количество материала достаточное, клетки сохранены, хорошо приготовлен и окрашен препарат, то можно без характеристики микроскопической картины формулировать цитологический диагноз с указанием на гистологическую форму опухоли и степень дифференцировки (низкодифференцированная аденокарцинома, плоскоклеточный рак с ороговением, фиброаденома).
Цитологическая диагностика заболеваний молочной железы
Показанием к цитологическому исследованию служат узловые образования в молочной железе, наличие выделений из соска, эрозивных или язвенных поверхностей. Выявление узловых образований возможно при пальпации, ультразвуковом исследовании, маммографии.
Особенно важно выполнять пункцию узловых образований молочной железы, в т. ч. непальпируемых, при наличии факторов риска рака, к которым относится: возраст (женщины старше 40 лет), нарушение гормонального баланса, раннее начало менструаций (раньше 12 лет) и позднее окончание (позже 50 лет), отсутствие родов и кормления ребенка, избыточная жировая клетчатка, особенно при быстром наборе веса, в сочетании с гиперплазией эпителия протоков, генетические особенности – наиболее часто предрасположенность к раку молочной железы и яичников передается по материнской линии (ген BRCA1), нарушение менструального цикла вследствие длительного лечения гормонами, особенно эстрогенами, наличия гормонально активных опухолей яичника и эндометрия, гормональная контрацепция при неправильном применении и гормональная заместительная терапии в климактерическом периоде, рентгеновское облучение.
Получение материала
Материал получают с помощью диагностической пункции – тонкоигольной аспирационной биопсии (ТАБ), отпечатков с трепанобиоптата (core biopsy) или эрозивных поверхностей, при наличии выделений из соска – сцеживания отделяемого. Возможна также интраоперационная диагностика по соскобу с ткани (или опухоли) молочной железы, удаленной во время операции.
Если предполагается использовать метод жидкостной цитологии и/или дополнительные молекулярные исследования – после ТАБ и приготовления стандартного мазка для получения клеточной суспензии иглу промывают в небольшом количестве стабилизирующего раствора, предназначенного для соответствующего исследования, в контейнере (или пробирке типа Эппендорф).
Приготовление препаратов
При получении небольшого количества жидкости (из кист, выделений из соска), препараты готовят как мазки крови: каплю выделений помещают на стекло, каплю из иглы выдувают, и с помощью специального стекла с шлифованным краем или пластикового шпателя для приготовления мазков крови делают препарат. Капля следует (тянется) за стеклом (шпателем) до образования на крае препарата “щеточки”, которой заканчивается мазок.
При наличии объемных жидкостных образований весь полученный материал помещают в пробирку и доставляют в лабораторию. При получении жидкости она должна быть полностью эвакуирована; в этом случае пункция молочной железы может быть и диагностической и лечебной процедурой. Наличие прозрачной жидкости чаще всего свидетельствует о доброкачественном процессе (кистозной полости). Мутная или кровянистая жидкость является достаточно серьезным основанием к поиску признаков опухолевого процесса. Любая полученная жидкость должна быть исследована цитологическим методом.
Жидкий материал или клеточная суспензия в контейнере (жидкостная цитология) подлежат дальнейшей обработке в лаборатории. Можно готовить “традиционные” мазки из жидкостей после их центрифугирования или стандартные тонкослойные препараты методом жидкостной цитологии. Если клеточная суспензия богата материалом, а также содержит небольшие клочки ткани, возможно приготовление из нее клеточных блоков (цитоблоки, вариант гистологического исследования).
Окрашивание можно проводить любым методом. При необходимости выполняют молекулярное исследование (проточная цитометрия, иммуноцитохимическое, молекулярно-генетическое исследования и др.).
Трактовка цитологического заключения
Цитологическое заключение о гиперплазии эпителия молочной железы (с предположительным или уверенным заключением о кисте, фиброзно-кистозной болезни или фиброаденоме) позволяет клиницисту планировать лечебную тактику.
При уверенном заключении о злокачественном процессе, установленном квалифицированными специалистами, цитологический диагноз может служить основанием для планирования лечения. При необходимости цитологический диагноз дополняется молекулярными исследованиями.
Если врач-цитолог не может судить о патологическом процессе вследствие недостаточного количества материала, некротических изменений и других причин, желательно повторить ТАБ с более тщательным выбором участка для пункции, нескольких пассов иглой в разных направлениях.
При цитологическом диагнозе дисплазии, тяжелой дисплазии, гиперплазии с атипией (или гиперплазии с атипией отдельных клеток), а также при предположительном цитологическом заключении о злокачественном процессе при небольшом количестве клеточного материала, возможно уточнение диагноза с помощью повторной пункции тонкой иглой или гистологического исследования (трепанобиопсия или секторальная резекция со срочным гистологическим исследованием).
Интеграция различных лабораторных методов
Определение рецепторов эстрогенов и прогестерона, рецепторов HER2/neu в пунктатах молочной железы – исследования, которые при раке молочной железы должны быть выполнены у каждой больной для определения лечебной тактики.
Опухоли с наличием рецепторов к эстрогенам отличаются хорошим прогнозом, ответом на гормональную терапию. Опухоли с положительной реакцией на HER2/neu и отрицательной на рецепторы эстрогенов отличаются плохим прогнозом и низкой продолжительностью жизни, однако возможен хороший ответ на таргетную терапию трастузумабом. Рак с базальноклеточным фенотипом и отрицательной реакцией на рецепторы эстрогенов характеризуется плохим прогнозом, низкой продолжительностью жизни и отсутствием ответа на терапию.
Оксифильно-клеточные опухоли щитовидной железы
Полный текст:
Аннотация
Диагностика и лечение опухолей щитовидной железы (ЩЖ) из оксифильных клеток (ОК) вызывают много споров. Мы представляем 11-летний опыт лечения 159 больных оксифильно-клеточными опухолями (ОКО), из которых было 102(64%) аденомы, 15 (9%) фолликулярных карцином, 3S (24%) папиллярных карцином и 4 (2,5%) опухоли неопределенного потенциала злокачественности. Среди фолликулярных карцином преобладали минимально инвазивные формы (11 (73%) из 15 случаев). Размер фолликулярных карцином был достоверно больше, чем аденом (36,5 и 17 мм; р
For citation:
Severskaya N.V., Ilyin A.A., Chebotareva I.V., Isayev P.A., Rumyantsev P.O., Medvedev V.S. Oxyphil-cell tumors of the thyroid. Problems of Endocrinology. 2008;54(4):21-27. (In Russ.) https://doi.org/10.14341/probl200854421-27
Оксифильно-клеточными опухолями (ОКО) щитовидной железы (ЩЖ) (синонимы: онкоцитомы, опухоли из В-клеток, клеток Асканази, Гюртле[*]) традиционно считаются опухоли фолликулярного происхождения, состоящие преимущественно из оксифильных клеток [23]. Оксифильные клетки (ОК) характеризуются наличием обильной эозинофильной зернистости цитоплазмы, в которой содержится большое количество митохондрий [22, 25]. Появление оксифилии рассматривают как феномен метаплазии клеток, возникающий при хроническом воспалении (тиреоидит) или в результате изменений митохондриальной или ядерной ДНК, приводящих к накоплению дефектных митохондрий со сниженной функцией [13, 25]. Оксифильные изменения могут происходить не только в фолликулярных, но и в парафолликулярных С-клетках ЩЖ [10]. Интересно, что Гюртле, чьим именем обычно называют ОК и состоящие из них опухоли, первым описал оксифильные изменения в С-клетках. Фолликулярные В-клетки впервые описаны Асканази, тем не менее в литературе наиболее часто фолликулярные ОКО обозначают как Гюртле-клеточные опухоли.
В 50-х годах прошлого века Американское онкологическое общество рекомендовало классифицировать все ОКО ЩЖ как злокачественные. Однако последующие исследования показали, что ОКО следует подразделять на доброкачественные и злокачественные в зависимости от наличия или отсутствия капсулярной и сосудистой инвазии [7, 14]. В классификации ВОЗ (1987 г.) выделяют Гюртле- клеточные аденомы и Гюртле-клеточный рак, который рассматривают как вариант фолликулярного рака ЩЖ. Однако впоследствии была обнаружена различная онкогенная экспрессия фолликулярных карцином из А- и В-клеток, что не позволяет объединить эти опухоли в один класс [20]. Кроме того, не определено место опухолей с оксифильной цитоплазмой, но с ядерными изменениями, характерными для папиллярной карциномы [8]. Было предложено подразделять OK-рак ЩЖ на фолликулярный и папиллярный по аналогии с опухолями из А- клеток [21]. Некоторые авторы выделяют также Гюртле-клеточную инсулярную (низкодифференцированную) карциному [3] и различные варианты строения папиллярной карциномы, включая Warthin-lake вариант с лимфоидной инфильтрацией стромы (напоминающий по строению папиллярную лимфоматозную цистаденому слюнной железы, Warthin’s tumor) и вариант из высоких клеток (tall-cell variant) [2, 5, 19].
Подобно разногласиям, существующим в классификации, нет единой концепции в отношении ведения больных с ОКО, что связано с различными представлениями об агрессивности этого вида опухолей. Одни исследователи выступают за тотальную тиреоидэктомию [1, 28], другие придерживаются дифференцированного подхода, основанного на традиционных принципах ведения больных с фолликулярными опухолями ЩЖ в зависимости от степени капсулярной и сосудистой инвазии и наличия метастазов [11, 26].
В данной статье мы представляем накопленный за 11 лет опыт по ведению 159 больных с ОКО ЩЖ.
Материалы и методы
В исследование включены 159 больных с ОКО ЩЖ, оперированных в клинике Медицинского радиологического научного центра РАМН (Обнинск) с 1994 по 2005 г. Возраст больных — от 12 до 70 лет, в среднем 38,7 ± 13,9 года (медиана 40 лет). Среди них 20 мужчин и 139 женщин (соотношение 1:7).
В анализ включены только те опухоли, в которых более 75% фолликулярных клеток обладали онкоцитарными свойствами. Диагноз Гюртле-кле- точной карциномы (ОКК) ставили на основании наличия полной инвазии капсулы и/или сосудов. Случаи пенетрации опухоли в стенку сосудов или капсулы были отнесены к разряду опухолей с неопределенным злокачественным потенциалом. Опухоли с признаками оксифилии цитоплазмы, но с ядерными изменениями, характерными для папиллярного рака, рассматривали как папиллярный рак из оксифильных клеток (ОКПР).
Следуя данным критериям, у 102 (64%) человек диагностирована оксифильно-клеточная аденома (ОКА), у 15 (9,5%) — фолликулярная ОКК (у 11 — с минимальной инвазией, у 4 — с обширной), у 4 (2,5%) — ОКО неопределенного потенциала злокачественности, у 38 (24%) — ОКПР.
Статистическую обработку результатов проводили с использованием t-теста, ANOVA, критериев Краскела—Уоллиса, Фишера. Различия считали достоверными при р 0,22).
Ультразвуковое исследование (УЗИ). Медиана и средний размер ОКК были достоверно выше по сравнению с ОКА (р 0,05) (см. таблицу).
Эхографическая картина ОКК и ОКА практически не различалась (р = 1,0). Большинство опухолей были представлены гипоэхогенным узлом (85%) правильной формы (100 и 97% соответственно), с четкими границами (85 и 81%) и ровными контурами (83 и 81%). Кальцинаты встречались соответственно у 7 и 6% больных (р — 1,0). Признаки кистозной дегенерации узла отмечены в 21 и 14% случаев (р = 0,4).
Эхографическая картина ОКПР отличалась от таковой при ОКК и ОКА. При ОКПР опухоль при УЗИ выглядела как гипоэхогенный узел неправильной формы (65%; р 0,38).
Цитологическое исследование проводили 145 пациентам (см. таблицу). 85% ОКА и 75% ОКК при цитологическом исследовании имели картину фолликулярной ОКО. При ОКК лишь у 3 (25%) больных был заподозрен рак (при гистологии у 1 — с минимальной инвазией и 2 — с обширной). Информативность цитологического исследования в диагностике ОКПР была значительно выше (чувствительность 89%). Предположение о злокачественной опухоли было также высказано у 1 больной с ОКО неопределенного потенциала злокачественности. Однако судить об истинности данного заключения не представляется возможным. Вероятность злокачественности ОКО при цитологической картине фолликулярной ОКО в данной группе составила 16,2% (16 из 99 случаев).
Большинству больных с ОКО (и = 102; 64%) хирургическое лечение проведено в объеме гемитирео- идэкгомии. Реже выполняли тиреоидэктомию (п = 49; 31%) и субтотальную резекцию (л = 8; 5%). 70 (44%) больным хирургическое лечение было дополнено удалением паратрахеальной клетчатки шеи, из них 2 также иссечением паравазальной клетчатки с одной стороны (см. таблицу). 4 пациентам с ОКПР после тиреоидэктомии проведена радиойодтерапия.
Фолликулярный рак. У 11 (73%) пациентов с ОКК была расценена как минимально инвазивная,
с прорастанием собственной капсулы во всех 11 случаях и сосудов капсулы — в 2 случаях. У 4 (27%) больных выявлена обширная инвазия в капсулу опухоли с прорастанием в окружающую ткань ЩЖ и сосуды. Размер карцином с выраженной инвазией был достоверно выше, чем минимально-инвазивных (соответственно 49,5 ± 8,8 и 29,1 ± 9,7 мм; медиана 50,5 и 33 мм; р 0,25). Поражение регионарных лимфоузлов наблюдали чаще при многофокусном поражении ЩЖ, чем при солитарной первичной опухоли (р = 0,058).
ОКА были солитарными у 62 (61%) больных. У 10 одиночная ОКА выявлена на фоне узлового коллоидного зоба. У 12 (12%) ОКА были множественными. У 11 из них множественные опухоли были выявлены уже при 1-й операции. У 1 пациентки 2-я ОКА в противоположной доле обнаружена через 2,5 года после 1-й операции.
У 20 (20%) больных с ОКА аденоме сопутствовал папиллярный рак, в котором оксифильные изменения клеток чаще отсутствовали или были незначительными (17 (85%) из 20 случаев). Среди больных с множественными ОКА папиллярный рак обнаружен у 4 (33%) из 12. У 1 пациентки на фоне множественных ОКА и папиллярной карциномы выявлен медуллярный рак ЩЖ. Из 20 больных с сочетанной патологией (ОКА и папиллярный рак) у 7 (35%) имелись множественные фокусы рака, у 4 (20%) — метастазы в регионарные лимфоузлы шеи.
Папиллярный рак был также выявлен у 2 из 4 больных с ОКО неопределенного потенциала злокачественности и у 1 (7%) из 15 пациенток с ОКК.
Множественные опухоли (первично-множественные аденомы и ОКА в сочетании с папиллярным раком) чаще встречались в старшей возрастной группе (42,9 ± 13,8 года, медиана 45) по сравнению с одиночными ОКА (35,5 ± 14,8 года, медиана 34, t-тест, р = 0,02).
У 9 оперированных больных опухоль оказалась полностью некротизирована. Все наблюдаемые случаи были расценены как аденома (не выявлены признаки сосудистой или капсулярной инвазии). У всех больных, за исключением одного, опухоль была солитарной (у одного — множественные ОКА, 1 из которых полностью некротизирована). Кроме того, некроз был выявлен у 1 больной с минимально-инвазивной ОКК, однако некроз в данном случае наблюдался лишь в центре опухоли (вероятно, в месте пункции). Локальный некроз в центре опухоли был также обнаружен у 1 больной неинкапсулированным ОКПР. В последнем случае опухоль прорастала за пределы капсулы ЩЖ до окружающей жировой клетчатки, с метастазами в регионарные лимфоузлы. Примечательно также, что во всех случаях (кроме одного), когда мы наблюдали некроз опухоли, в окружающей ткани отсутствовали признаки тиреоидита.
Контрольное обследование проведено 102 больным с ОКО через 6—126 мес после хирургического лечения (в среднем 30,03 ± 24,5 мес, медиана 24 мес), в том числе 30 пациентам после тиреоидэктомии и 72 — после операции в меньшем объеме, чем тиреоидэктомия. Среди больных с ОКПР рецидив метастазирования в паравазальные лимфоузлы шеи выявлен у 1 (3,2%) из 31 через 9 мес после тиреоидэктомии и удаления паратрахеальной и па- равазальной клетчатки. Среди пациентов с ОКА рецидив опухоли в оставшейся тиреоидной ткани выявлен у 3 (5,4%) из 56, при объеме операции меньше, чем тиреоидэктомия, — у 3 (6,4%) из 47. Однако при первично-множественных ОКА, в том случае если хирургическое лечение было проведено в объеме меньшем, чем тиреоидэктомия, рецидив опухоли в оставшейся ткани наблюдался гораздо чаще — у 3 (33%) из 9 больных.
Примечательно, что у 2 из 3 пациентов с рецидивами ОКА при 1-й операции в окружающей ткани обнаружен папиллярный рак ЩЖ, а при повторной — метастазы в лимфоузлы шеи. Ни у кого из 12 больных с ОКК и 3 с опухолью неопределенного потенциала злокачественности не выявлено ни рецидива заболевания в оставшейся ткани, ни регионарных или отдаленных метастазов.
Диагностика и лечение ОКО являются спорными вопросами в тиреоидологии. До сих пор не определено их точное место в классификации опухолей ЩЖ. Не ясно, обладают ли они большим злокачественным потенциалом по сравнению с неоксифильными аналогами, и в силу этого требуется ли более агрессивная тактика их лечения.
В нашем исследовании среди 159 оперированных за 11 лет больных большую часть ОКО составили В-клеточные аденомы. ОКК была выявлена лишь у 15 (9,4%) пациентов, ОКПР — у 38 (24%). Среди всех оперированных больных с цитологической картиной ОКО вероятность рака ЩЖ составила 16,2%, что соответствует данным аналогичных исследований.
Дифференциальная диагностика ОКК трудна, так как 75% больных имеют цитологическую картину ОКО, а эхографическая картина карцином не отличается от таковой при аденоме. Однако, к счастью, лишь меньшая часть (27%) ОКК представлена формами с выраженной инвазией. Попытка найти какие-либо дополнительные клинические признаки, позволяющие предположить природу ОКО, не принесли существенного результата. Ни пол, ни возраст больных с доброкачественными и злокачественными ОКО существенно не различались. Однако обнаружено, что размер ОКК (36,5 мм) был достоверно больше, чем ОКА (17 мм). Кроме того, отмечено, что с увеличением размера ОКК повышалась вероятность сосудистой инвазии. Подобные данные были ранее получены в других работах, что позволило некоторым исследователям предположить существование злокачественной трансформации ОКА в ОКК по мере роста опухоли, а также рассматривать минимально-инвазивные ОКК как предшественники широко-инвазивных форм [6, 16, 27]. Однако в литературе встречаются также сообщения об ОКК с выраженной инвазией с отдаленными метастазами при размере опухоли менее 1 см [27]. В нашей группе минимальный размер ОКК — 14 и 16 мм (оба случая с минимальной инвазией).
Определенную трудность вызывает диагностика фолликулярного варианта ОКПР на стадии, когда опухоль еще не проявила инвазивных свойств и ядерные изменения, характерные для папиллярного рака, минимальны [3]. На этой стадии опухоль часто расценивается морфологами как ОКА, и только возникновение в дальнейшем регионарных метастазов свидетельствует о злокачественном потенциале. Возможно, что именно эти нераспознанные случаи фолликулярного варианта ОКПР создали представление о злокачественности всех ОКО [3]. Для выявления таких трудных для диагностики случаев фолликулярного варианта ОКПР было предложено исследовать экспрессию RET/PTC [3, 8]. Однако в других работах сообщается, что экспрессия RET/PTC не специфична для папиллярного рака и может также выявляться при других заболеваниях, в том числе при ОКО ЩЖ [9]. Вероятно, потребуются дальнейшие исследования для выяснения, какой метод следует считать наиболее информативным для установления природы ОКО. На сегодняшний день этот вопрос остается открытым. Тем не менее, интересен факт столь частого сочетания ОКА с папиллярным раком (20%).
Многие исследователи отмечали, что ОКК обладают большим злокачественным потенциалом по сравнению с их неоксифильными аналогами [4, 7, 24, 29]. Однако другие авторы считают, что сама по себе оксифилия не является неблагоприятным фактором, а в прогностическом плане имеют значение другие признаки (экстратиреоидная инвазия, наличие отдаленных метастазов) [11, 12, 17, 26]. В отношении ОКПР большинство исследователей признает, что оксифилия при папиллярном раке не влияет на прогноз [5]. Исключение составляет лишь tall-cell-вариант, обладающий более агрессивным течением, высокой частотой регионарного и отдаленного метастазирования, низкой чувствительностью к радиойодтерапии и, как следствие, высокой летальностью [19, 27].
В нашем исследовании мы не получили убедительных доказательств в пользу большей агрессивности рака из оксифильных клеток. Ни у кого из больных не выявлено отдаленных метастазов. Среди 15 фолликулярных ОКК лишь в 4 (27%) случаях установлена выраженная инвазия, однако ни в одном случае не обнаружено экстратиреоидного распространения или метастазов. Среди больных ОКПР экстратиреоидная инвазия наблюдалась лишь у 10%, регионарные метастазы (преимущественно в лимфоузлы паратрахеальной клетчатки) — у 36%, что соответствует данным литературы, а также ранее полученным в нашей клинике сведениям о распространенности папиллярного рака из А- клеток.
Заслуживает внимания частота множественных ОКА (12%), а также сочетание ОКА и папиллярного рака (20%). В ранее проведенных работах сообщалось о множественных ОКО, которые, по данным разных авторов, встретились в 7,1—25% чаще у молодых пациентов [16]. Высказывалось мнение, что определенную роль в возникновении первично-множественных ОКО могут играть генетические факторы или фоновые процессы в ЩЖ, в том числе сопутствующий тиреоидит [16]. Сообщалось также о семейных случаях множественных ОКО, что предполагает наличие герминативной мутации [6]. В нашем исследовании хронический тиреоидит в окружающей ткани был выявлен у 5 (42%) из 12 больных с множественными ОКА и у 10 (67%) из 15 больных с многофокусным папиллярным раком, однако с такой же частотой тиреоидит наблюдался и при солитарных опухолях, что ставит под сомнение его роль в развитии множественных ОКО. Тем не менее интересен факт столь частого сочетания тиреоидита с ОКПР (74%). Обнаружение данной ассоциации и другими исследователями позволило предположить, что оксифилия при папиллярном раке вторична (является следствием тиреоидита) в отличие от остальных опухолей, развивающихся из первично-оксифильных клеток [16].
Интересной особенностью ОКО является нередко наблюдаемый ишемический некроз ОКО, который развивается в богатых дефектными митохондриями ОКО, вероятно, как реакция на гипоксию вследствие нарушения кровоснабжения (после пункционной биопсии или без видимых причин) [18, 21]. В нашей серии наблюдений у 9 пациентов отмечен тотальный некроз опухоли, что в значительной степени затруднило диагностику опухоли при гистологическом исследовании. Ни в одном случае тотального некроза опухоли признаков капсулярной инвазии не найдено, поэтому все эти наблюдения были расценены как аденомы. Локальный некроз (в месте пункции) был также обнаружен у 1 пациентки с минимально-инвазивной ОКК и инвазивным ОКПР. Из описанных в доступной литературе случаев некроза ОКО почти у половины больных опухоли были злокачественными [16]. Поэтому, несмотря на регрессию размеров опухоли вследствие некроза (по данным УЗИ), всем больным с цитологическим заключением ”ОКО» рекомендовалось хирургическое лечение [16]. Тем не менее, в нашей клинике наблюдаются 2 пациента с цитологическим заключением «ОКО”, у которых после аспирационной биопсии отмечено уменьшение размеров опухоли более чем на 40% (в 1 случае полная регрессия при УЗИ). Больные не были оперированы, и динамическое наблюдение за ними (в течение 2—3,5 года) не выявило признаков прогрессирования заболевания.
Выбор хирургического лечения пациентов с ОКО также вызывает много вопросов. Так, вплоть до 1983 г. большинство исследователей рассматривали все ОКО как потенциально злокачественные, требующие агрессивной хирургической тактики [15, 28]. Применение критериев капсулярной и сосудистой инвазии позволило дифференцированно подходить к выбору лечения. Большинство исследователей признало, что достаточным объемом операции при ОКА может быть гемитиреоидэктомия. В работах последних лет многие авторы также рекомендуют придерживаться этой тактики при минимально-инвазивных ОКК (не более 1 фокуса полной капсулярной и/или сосудистой инвазии), для которых характерно относительно доброкачественное течение и появление отдаленных метастазов маловероятно [27]. Однако данные рекомендации подходят только для солитарных опухолей. При множественных ОКО показана тиреоидэктомия [16]. В отношении ОКК с выраженной инвазией большинство исследователей выступают за тиреидэктомию, однако имеются работы, в которых показано, что объем операции существенно не влияет на рецидив заболевания и летальность [26].
В нашей группе большинству (69%) больных с ОКО хирургическое лечение было проведено в меньшем объеме, чем тиреоидэктомия. Из 102 пациентов, наблюдаемых после лечения (30 — после тиреоидэктомии и 72 — после операции меньшего объема), рецидив заболевания развился у 4 (у 3 — множественные ОКА в остаточной ткани после гемитиреоидэктомии и у 1 — метастазы ОКПР в регионарные лимфоузлы после тиреоидэктомии и лимфодиссекции). К сожалению, срок наблюдения (6—126 мес, медиана 24 мес) не позволяет оценить отдаленные результаты лечения. Тем не менее полученные данные свидетельствуют о необходимости предоперационной диагностики возможных первично-множественных ОКО, при которых необходима тиреоидэктомия. В случае проведения операции в меньшем объеме вероятность рецидива в оставшейся ткани достигает 33%. Трудности дифференциальной диагностики фолликулярного варианта ОКПР и ОКА диктуют необходимость длительного наблюдения за больными с ОКА с обязательным исследованием зоны регионарного лимфооттока и периодическим рентгенологическим исследованием легких.
[*]Клетки Гюртле—Асканази (К. W. Hurtle, 1860—1945, немецкий гистолог; М. Askanazy, 1865—1950, немецкий патолог). — Прим. ред.