Острый коронарный синдром (ОКС)
Симптомы острого коронарного синдрома
Основным симптомом острого коронарного синдрома является боль:
по характеру – сжимающая или давящая, нередко ощущается чувство тяжести или нехватки воздуха;
локализация (расположение) боли – за грудиной или в предсердечной области, то есть по левому краю грудины; боль отдает в левую руку, левое плечо либо в обе руки, область шеи, нижнюю челюсть, между лопаток, левую подлопаточную область;
чаще боль возникает после физической нагрузки или психоэмоционального стресса;
длительность – более 10 минут;
после приема нитроглицерина боль не проходит.
Формы острого коронарного синдрома выделяют по изменениям на электрокардиограмме (ЭКГ, метод регистрации электрической активности сердца на бумаге) – по изменению сегмента ST (отрезок кривой ЭКГ, который соответствует периоду сердечного цикла, когда оба желудочка полностью охвачены возбуждением).
Острый коронарный синдром с подъемом сегмента ST — он отражает наличие острой полной окклюзии (закупорка просвета) коронарной артерии.
Острый коронарный синдром без подъема сегмента ST – в лечении больных с этой формой заболевания тромболитики (препараты, разрушающие тромб (сгусток крови), закрывающий просвет сосуда) не используются:
инфаркт миокарда (гибель клеток участка сердечной мышцы в результате нарушения его кровоснабжения) ;
нестабильная стенокардия (вариант острой ишемии миокарда, тяжесть и продолжительность которой недостаточна для развития инфаркта миокарда).
Причины
Внезапное нарушение кровоснабжения сердечной мышцы, возникающее из-за несоответствия между снабжением миокарда кислородом и потребностью в нем, служит непосредственной причиной развития острого коронарного синдрома. Это происходит по следующим причинам:
Основной причиной ОКС является формирование нестабильной бляшки с высоким риском надрыва капсулы и формированием частично или полностью окклюзирующего тромба коронарной артерии, что определяет клиническую и электрофизиологическую картину коронарной патологии Маркером формирования нестабильной атеросклеротической бляшки является рост концентрации в сыворотке крови провоспалительных цитокинов (С-реактивный пептид).
ОКС, по клиническому течению и динамике изменений на ЭКГ, подразделяется на два подтипа: ОКС без подъема ST-сегмента на ЭКГ (ОКС-БПST) и ОКС с подъемом ST-сегмента на ЭКГ (ОКС-ПST).
ОКС-БПST — больные с наличием боли в грудной клетке, но без подъема ST-сегмента на ЭКГ.
ОКС-ПST — больные с наличием типичных болей или других неприятных ощущений (дискомфорт) в грудной клетке, стойким подъемом ST-сегмента или впервые возникшей блокадой левой ножки пучка Гиса (БЛНПГ).
Больные с подозрением на ОКС, а тем более на острый ИМ должны быть госпитализированы в специализированные стационары для идентификации диагноза, решения вопроса о тактике лечения (консервативная медикаментозная, артифициальный тромболизис, механическая реканализация, эндоваскулярная ангиопластика, хирургическое вмешательство), для мониторинга ритма сердечной деятельности и показателей центральной гемодинамики.
К факторам, способствующим возникновению острого коронарного синдрома, относятся:
Диагностика
Распознавание ОКС базируется на трех группах критериев. Первую группу составляют признаки, определяемые при расспросе и физикальном исследовании больного, вторую группу – данные инструментальных исследований и третью – результаты лабораторных тестов.
Типичными клиническими проявлениями ОКС являются ангинозная боль в покое продолжительностью более 20 мин, впервые возникшая стенокардия III функционального класса, прогрессирующая стенокардия. К атипичным проявлениям ОКС относят разнохарактерные болевые ощущения в грудной клетке, возникающие в покое, боль в эпигастрии, острые расстройства пищеварения, боль, характерную для поражения плевры, нарастающую одышку. Физикальное исследование больных с ОКС нередко не выявляет каких–либо отклонений от нормы. Его результаты важны не столько для диагностики ОКС, сколько для обнаружения признаков возможных осложнений ишемии миокарда, выявления заболеваний сердца неишемической природы и определения экстракардиальных причин жалоб больного.
Основным методом инструментальной диагностики ОКС является электрокардиография. ЭКГ больного с подозрением на ОКС, по возможности, следует сопоставлять с данными предыдущих исследований. При наличии соответствующей симптоматики для НС характерны депрессия сегмента ST не менее чем на 1 мм в двух и более смежных отведениях, а также инверсия зубца T глубиной более 1 мм в отведениях с преобладающим зубцом R. Для развивающегося ИМ c зубцом Q характерна стойкая элевация сегмента ST, для стенокардии Принцметала и развивающегося ИМ без зубца Q – преходящий подъем сегмента ST. Помимо обычной ЭКГ в покое, для диагностики ОКС и контроля эффективности лечения применяется холтеровское мониторирование электрокардиосигнала.
Из биохимических тестов, применяемых для диагностики ОКС, предпочтительным считается определение содержания в крови сердечных тропонинов T и I, повышение которого представляет собой наиболее надежный критерий некроза миокарда. Менее специфичным, но более доступным для определения в клинической практике критерием является повышение в крови уровня креатинфосфокиназы (КФК) за счет ее изофермента МВ–КФК. Увеличение содержания МВ–КФК (предпочтительно массы, а не активности) в крови более чем вдвое по сравнению с верхней границей нормальных значений при наличии характерных жалоб, изменений ЭКГ и отсутствии других причин гиперферментемии позволяет с уверенностью диагностировать ИМ.
Острый коронарный синдром без подъема сегмента ST на ЭКГ
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ММА имени И.М. Сеченова
Острый коронарный синдром – предварительный диагноз, позволяющий врачу определить неотложные лечебные и организационные мероприятия. Соответственно, огромное значение имеет разработка клинических критериев, позволяющих врачу принимать своевременные решения и выбирать оптимальное лечение, в основе которого лежат оценка риска развития осложнений и целевой подход к назначению инвазивных вмешательств. В ходе создания таких критериев все острые коронарные синдромы были разделены на сопровождающиеся и не сопровождающиеся стойким подъемом сегмента ST. В настоящее время оптимальные лечебные мероприятия, эффективность которых основана на результатах хорошо спланированных рандомизированных клинических испытаний, уже во многом разработаны. Так, при остром коронарном синдроме со стойким подъемом сегмента ST (или впервые возникшей полной блокадой левой ножки пучка Гиса), отражающим острую тотальную окклюзию одной или нескольких коронарных артерий, целью лечения является быстрое, полное и стойкое восстановление просвета коронарной артерии при помощи тромболизиса (если он не противопоказан) или первичной коронарной ангиопластики (если она технически выполнима). Эффективность указанных лечебных мероприятий доказана в целом ряде исследований.
При остром коронарном синдроме без подъема сегмента ST речь идет о пациентах с болями в грудной клетке и изменениями на ЭКГ, свидетельствующими об острой ишемии (но не обязательно о некрозе) миокарда. У таких больных часто обнаруживаются стойкая или преходящая депрессия сегмента ST, а также инверсия, уплощение или «псевдонормализация» зубцов Т. Кроме того, изменения ЭКГ при остром коронарном синдроме без подъема сегмента ST могут быть неспецифическими или вовсе отсутствовать. Наконец, в указанную категорию больных могут быть включены и некоторые пациенты с указанными выше изменениями на электрокардиограмме, но без субъективных симптомов (т.е. случаи безболевой «немой» ишемии и даже инфаркта миокарда).
В отличие от ситуаций со стойким подъемом сегмента ST существовавшие ранее предложения по тактике лечения при остром коронарном синдроме без подъема сегмента ST носили менее четкий характер. Лишь в 2000 году были опубликованы рекомендации Рабочей группы Европейского кардиологического общества по лечению острого коронарного синдрома без подъема сегмента ST. В скором времени соответствующие рекомендации будут выработаны и для врачей России.
В настоящей статье рассматривается лишь ведение больных с подозрением на острый коронарный синдром, у которых отсутствует стойкий подъем сегмента ST. При этом основное внимание уделено непосредственно диагностике и выбору терапевтической тактики.
Но предварительно считаем необходимым сделать два замечания:
Уровень А: Заключения основаны на данных, которые были получены в нескольких рандомизированных клинических исследованиях или метаанализах.
Уровень В: Заключения основаны на данных, которые были получены в единичных рандомизированных испытаниях или в нерандомизированных исследованиях.
Уровень С. Заключения основаны на согласованном мнении экспертов.
В дальнейшем изложении после каждого пункта будет указан уровень его обоснованности.
Тактика ведения больных с острым коронарным синдромом
Первичная оценка состояния больного
Первичная оценка состояния пациента с жалобами на боль в грудной клетке или другими симптомами, позволяющими заподозрить ОКС, включает в себя:
1. Тщательный сбор анамнеза. Классические характеристики ангинозных болей, равно как и типичные варианты обострения ИБС (затяжная [> 20 минут] ангинозная боль в покое, впервые возникшая тяжелая [не ниже III ФК по классификации Canadian Cardiovascular Society (CCS)] стенокардия, недавнее утяжеление стабильной стенокардии не менее чем до III ФК по CCS) хорошо известны. Однако следует отметить, что ОКС может проявляться и атипичными симптомами, в числе которых боли в грудной клетке в покое, боли в эпигастрии, внезапно возникшая диспепсия, колющие боли в груди, «плевральные» боли, а также усиление одышки. Причем частота указанных манифестаций ОКС достаточно велика. Так, по данным Multicenter Chest Pain Study (Lee T. с соавт., 1985), острая ишемия миокарда была диагностирована у 22% пациентов с острыми и колющими болями в грудной клетке, а также у 13% больных с болями, характерными для поражения плевры, и у 7% больных, у которых болевые ощущения полностью воспроизводились при пальпации. Особенно часто атипичные проявления ОКС наблюдаются у пациентов молодого (25–40 лет) и старческого (более 75 лет) возраста, а также у женщин и больных сахарным диабетом.
2. Физикальное обследование. Результаты осмотра и пальпации грудной клетки, данные аускультации сердца, а также показатели частоты сердечных сокращений и артериального давления обычно находятся в пределах нормы. Целью физикального обследования является в первую очередь исключение внесердечных причин боли в грудной клетке (плеврит, пневмоторакс, миозит, воспалительные заболевания костно–мышечного аппарата, травмы грудной клетки и др.). Кроме того, при физикальном обследовании следует выявлять заболевания сердца, не связанные с поражением коронарных артерий (перикардит, пороки сердца), а также оценить стабильность гемодинамики и тяжесть недостаточности кровообращения.
3. ЭКГ. Регистрация ЭКГ в покое является ключевым методом диагностики ОКС. В идеале следует записать ЭКГ во время болевого приступа и сравнить ее с электрокардиограммой, зарегистрированной после исчезновения болей. При повторяющихся болях для этого может быть использовано многоканальное мониторирование ЭКГ. Очень полезно также сравнить ЭКГ со «старыми» пленками (если таковые доступны), особенно при наличии признаков гипертрофии левого желудочка или перенесенного инфаркта миокарда.
Наиболее надежными электрокардиографическими признаками ОКС являются динамика сегмента ST и изменения зубца Т. Вероятность наличия ОКС наиболее велика, если соответствующая клиническая картина сочетается с депрессией сегмента ST глубиной более 1 мм в двух или более смежных отведениях. Несколько менее специфичным признаком ОКС является инверсия зубца Т, амплитуда которого превышает 1 мм, в отведениях с преобладающим зубцом R. Глубокие негативные симметричные зубцы Т в передних грудных отведениях часто свидетельствуют о выраженном проксимальном стенозе передней нисходящей ветви левой коронарной артерии. Наконец, наименее информативны неглубокая (менее 1 мм) депрессия сегмента ST и незначительная инверсия зубца Т.
Следует помнить о том, что полностью нормальная ЭКГ у больных с характерными симптомами не исключает диагноз ОКС.
Таким образом, у больных с подозрением на ОКС следует зарегистрировать ЭКГ в покое и начать длительное многоканальное мониторирование сегмента ST. Если мониторирование по каким–либо причинам невыполнимо, то необходима частая регистрация ЭКГ (уровень обоснованности: С).
Больные с подозрением на ОКС без подъема сегмента ST должны быть немедленно госпитализированы в специализированные отделения неотложной кардиологии/отделения интенсивной терапии и кардиореанимации (уровень обоснованности: С).
Исследование биохимических маркеров повреждения миокарда
«Традиционные» сердечные ферменты, а именно креатинфосфокиназа (КФК) и ее изофермент МВ КФК менее специфичны (в частности, возможны ложноположительные результаты при травме скелетных мышц). Кроме того, имеет место значительное перекрывание между нормальными и патологическими сывороточными концентрациями указанных ферментов. Наиболее специфичными и надежными маркерами некроза миокарда являются кардиальные тропонины Т и I. Следует определять концентрацию тропонинов Т и I через 6–12 часов после поступления в стационар, а также после каждого эпизода интенсивной боли в грудной клетке.
Если у больного с подозрением на ОКС без подъема сегмента ST имеет место повышенный уровень тропонина Т и/или тропонина I, то такое состояние следует расценивать, как инфаркт миокарда, и проводить соответствующее медикаментозное и/или инвазивное лечение.
Следует также учитывать, что после некроза сердечной мышцы повышение концентрации различных маркеров в сыворотке крови происходит неодновременно. Так, наиболее ранним маркером некроза миокарда является миоглобин, а концентрации МВ КФК и тропонина увеличиваются несколько позже. Кроме того, тропонины остаются повышенными в течение одной–двух недель, что затрудняет диагностику повторного некроза миокарда у больных, недавно перенесших инфаркт миокарда.
Соответственно, при подозрении на ОКС тропонины T и I должны быть определены в момент поступления в стационар и повторно измерены через 6–12 часов наблюдения, а также после каждого болевого приступа. Миоглобин и/или МВ КФК следует определять при недавнем (менее шести часов) появлении симптомов и у пациентов, недавно (менее двух недель назад) перенесших инфаркт миокарда (уровень обоснованности: С).
Начальная терапия больных с подозрением на ОКС без подъема сегмента ST
При ОКС без подъема сегмента ST в качестве начальной терапии следует назначить:
1. Ацетилсалициловую кислоту (уровень обоснованности: А);
2. Гепарин натрия и низкомолекулярные гепарины (уровень обоснованности: А и В);
3. b–блокаторы (уровень обоснованности: В);
4. При сохраняющихся или рецидивирующих болях в грудной клетке – нитраты внутрь или внутривенно (уровень обоснованности: С);
5. При наличии противопоказаний или непереносимости b–блокаторов – антагонисты кальция (уровень обоснованности: В и С).
В течение первых 8–12 часов необходимо тщательно наблюдать за состоянием больного. Предметом особого внимания должны быть:
Пациенты с острым коронарным синдромом представляют собой весьма разнородную группу больных, которые различаются по распространенности и/или тяжести атеросклеротического поражения коронарных артерий, а также по степени «тромботического» риска (т.е. риска развития инфаркта миокарда в ближайшие часы/дни). Основные факторы риска представлены в таблице 1.
Пациенты с острым коронарным синдромом представляют собой весьма разнородную группу больных, которые различаются по распространенности и/или тяжести атеросклеротического поражения коронарных артерий, а также по степени «тромботического» риска (т.е. риска развития инфаркта миокарда в ближайшие часы/дни). Основные факторы риска представлены в таблице 1.
На основании данных динамического наблюдения, ЭКГ и биохимических исследований каждый пациент должен быть отнесен к одной из двух указанных ниже категорий.
1. Пациенты с высоким риском развития инфаркта миокарда или смерти
К этой категории относятся больные, у которых имели место:
2. Пациенты с низким риском развития инфаркта миокарда или смерти
К этой категории относятся больные, у которых за время динамического наблюдения:
Дифференцированная терапия в зависимости от риска развития инфаркта миокарда или смерти
Для больных с высоким риском указанных событий может быть рекомендована следующая лечебная тактика:
1. Введение блокаторов IIb/IIIa рецепторов: абциксимаб, тирофибан или эптифибатид (уровень обоснованности: А).
2. При невозможности использования блокаторов IIb/IIIa рецепторов – внутривенное введение гепарина натрия по схеме (табл. 2) или низкомолекулярных гепаринов (уровень обоснованности: В).
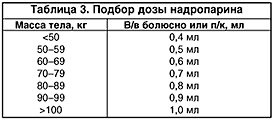
В современной практике широко используются следующие низкомолекулярные гепарины: адрепарин, дальтепарин, надропарин, тинзапарин и эноксапарин. В качестве примера остановимся подробнее на надропарине. Надропарин – низкомолекулярный гепарин, полученный из стандартного гепарина методом деполимеризации. Препарат характеризуется выраженной активностью в отношении фактора Xа и слабой активностью в отношении фактора IIа. Анти–Xа активность надропарина более выражена, чем его влияние на АЧТВ, что отличает его от гепарина натрия. Для лечения ОКС надропарин вводят п/к 2 раза в сутки в комбинации с ацетилсалициловой кислотой (до 325 мг/сут). Начальную дозу определяют из расчета 86 ЕД/кг, и ее следует вводить в/в болюсно. Затем подкожно вводят такую же дозу. Продолжительность дальнейшего лечения – 6 дней, в дозах, определяемых в зависимости от массы тела (табл. 3).
3. У больных с жизнеопасными нарушениями сердечного ритма, гемодинамической нестабильностью, развитием ОКС вскоре после инфаркта миокарда и/или наличием в анамнезе АКШ следует как можно быстрее выполнить коронароангиографию (КАГ). В процессе подготовки к КАГ следует продолжать введение гепарина. При наличии атеросклеротического повреждения, позволяющего провести реваскуляризацию, вид вмешательства выбирают с учетом особенностей повреждения и его протяженности. Принципы выбора процедуры реваскуляризации при ОКС аналогичны общим рекомендациям для данного вида лечения. Если выбрана чрескожная транслюминальная коронарная ангиопластика (ЧТКА) с установкой стента или без него, то ее можно произвести немедленно после ангиографии. В этом случае введение блокаторов IIb/IIIa рецепторов следует продолжать в течение 12 часов (для абциксимаба) или 24 часов (для тирофибана и эптифибатида). Уровень обоснованности: А.
У больных с низким риском развития инфаркта миокарда или смерти может быть рекомендована следующая тактика:
1. Прием внутрь ацетилсалициловой кислоты, b–блокаторов, возможно – нитратов и/или антагонистов кальция (уровень обоснованности: В и С).
2. Отмена низкомолекулярных гепаринов в том случае, если за время динамического наблюдения отсутствовали изменения на ЭКГ и не повышался уровень тропонина (уровень обоснованности: С).
3. Нагрузочная проба для подтверждения или установления диагноза ИБС и оценки риска неблагоприятных событий. Больным с выраженной ишемией во время стандартного нагрузочного теста (велоэргометрия или тредмил) следует выполнить КАГ с последующей реваскуляризацией. При неинформативности стандартных тестов могут быть полезны стресс–эхокардиография или нагрузочная перфузионная сцинтиграфия миокарда.
Ведение больных ОКС без подъема сегмента ST после выписки из стационара
1. Введение низкомолекулярных гепаринов в том случае, если имеют место повторные эпизоды ишемии миокарда и невозможно выполнить реваскуляризацию (уровень обоснованности: С).
2. Прием b–блокаторов (уровень обоснованности: А).
3. Широкое воздействие на факторы риска. В первую очередь – прекращение курения и нормализация липидного профиля (уровень обоснованности: А).
4. Прием ингибиторов АПФ (уровень обоснованности: А).
В настоящее время многие лечебные учреждения в России не располагают возможностями проведения вышеупомянутых диагностических и лечебных мероприятий (определение уровня тропонинов T и I, миоглобина; экстренная коронароангиография, использование блокаторов IIb/IIIa рецепторов и др.). Можно ожидать, однако, все более широкого их включения в медицинскую практику в нашей стране уже в ближайшем будущем.
Применение нитратов при нестабильной стенокардии основывается на патофизиологических предпосылках и клиническом опыте. Данные контролируемых исследований, указывающие на оптимальные дозировки и длительность их применения, отсутствуют.
Антитромботическая терапия острого коронарного синдрома без стойкого подъема сегмента ST
Cовременные контролируемые исследования и международные рекомендации Острый коронарный синдром без стойкого подъема сегмента ST на электрокардиограмме (ЭКГ) является частью такого клинического симптомокомплекса, как острый коронарный синдром (ОКС), вкл
Cовременные контролируемые исследования и международные рекомендации
Острый коронарный синдром без стойкого подъема сегмента ST на электрокардиограмме (ЭКГ) является частью такого клинического симптомокомплекса, как острый коронарный синдром (ОКС), включающий большой спектр состояний, связанных с обострением ишемической болезни сердца (ИБС), от нестабильной стенокардии и инфаркта миокарда (ИМ) без подъема сегмента ST — ИМБПST (в Европе они объединены термином ОКСБПST), до ИМ с подъемом сегмента ST (ИМСПST) (рис).
Только около 25% среди госпитализируемых в Европе и США больных с ОКС составляют пациенты с острым ИМ с подъемом сегмента ST, а приблизительно 75% — больные с нестабильной стенокардией или ИМ без подъема сегмента ST [1].
Острый коронарный синдром без стойкого подъема сегмента ST является для клинициста важным диагнозом, так как при нестабильной стенокардии и ИМБПST лечебная тактика практически не различается и направлена на устранение ишемии миокарда, предупреждение и лечение осложнений. Важность выделения данного синдрома объясняется и тем, что при нем существенно возрастает риск смерти или нефатального ИМ, который наиболее выражен в течение первых 30 дней после появления симптомов [2].
Обсуждаются пять основных причин развития острого коронарного синдрома без подъема сегмента ST [3]:
Как показывают данные ангиоскопических и ангиографических исследований, наиболее частой причиной развития данного заболевания является неокклюзирующий тромбоз на месте разрыва атеросклеротической бляшки.
Антитромбоцитарные средства (ацетилсалициловая кислота (АСК) и тиенопиридины). Лечение больных с ОКСБПST надо начинать (наряду с купированием болевого синдрома) с приема 160–325 мг (250 мг) АСК в таблетках, не покрытых кишечнорастворимой оболочкой, в сочетании с «нагрузочной» дозой (300 мг) клопидогреля (табл. 1). При использовании «нагрузочной» дозы клопидогреля в 300 мг эффективное ингибирование агрегации тромбоцитов достигается в течение от 4 до 6 ч, тогда как при назначении 75 мг препарата оно проявляется через 3–5 дней [4]. По некоторым данным, «нагрузочная» доза клопидогреля в 600 мг позволяет достичь этого эффекта в течение 2 ч [5]. Комбинацию этих препаратов Европейское общество кардиологов (ESC) рекомендует применять в течение 9–12 мес, а Американская коллегия кардиологов (АСС) и Американская ассоциация сердца (АНА) — до 9 мес [3], а затем используется одна АСК неопределенно долго (пожизненно или до появления побочных эффектов). После однократных «нагрузочных» доз АСК и клопидогреля в дальнейшем АСК назначается по 75–160 мг/сут, а клопидогрель — по 75 мг/сут. Кроме того, тиенопиридины — клопидогрель (в дозах, указанных выше) и тиклопидин (первая доза 500 мг, затем по 250 мг 2 раза в сутки, регулярный контроль за числом тромбоцитов и лейкоцитов) могут быть рекомендованы в случае непереносимости АСК: повышенная чувствительность или выраженное желудочно-кишечное расстройство. При этом надо отметить, что предпочтение отдается клопидогрелю, так как при применении этого препарата быстрее проявляется антитромботическое действие (особенно при применении «нагрузочной» дозы) и меньше побочных эффектов. Комбинация АСК и клопидогреля используется как у больных с низким риском (планируется только медикаментозное лечение), так и перед проведением коронарной ангиопластики и после нее. Для уменьшения риска возникновения кровотечений целесообразно отменить клопидогрель по крайней мере за 5 (лучше за 7) дней до выполнения операции коронарного шунтирования.
Поэтому если в первые 24–36 ч после госпитализации планируется коронароангиография, то клопидогрель не назначается до тех пор, пока не решится вопрос о целесообразности и сроках проведения КШ. В том случае, когда после коронароангиографии будет принято решение о немедленном выполнении чрескожных коронарных вмешательств (ЧКВ) (баллонная ангиопластика или стентирование коронарной артерии), «нагрузочная» доза препарата может быть дана прямо на катетеризационном столе.
Не следует применять в качестве антиагрегантов дипиридамол, сульфинпиразон (противоподагрическое средство, в больших дозах нарушающее агрегацию тромбоцитов), простациклин и его аналоги, потому что они не влияют на течение и/или прогноз ОКСБПST [3]. Говоря об антитромбоцитарных препаратах, следует отметить отсутствие данных о пользе пероральных ингибиторов тромбоцитарных гликопротеиновых рецепторов IIb/IIIa (ИГПР IIb/IIIa) у больных с ОКС без подъема сегмента ST. Не имеют преимущества перед АСК блокаторы тромбоксансинтетазы и антагонисты рецепторов тромбоксана А2 [3].
Антитромбоцитарное действие АСК связано с ингибированием циклооксигеназы-1 и в связи с этим со снижением синтеза тромбоксана А2 (ТхА2), что нарушает один из путей агрегации тромбоцитов. Максимальное уменьшение агрегации тромбоцитов достигается при уменьшении образования ТхА2 не менее чем на 90%. АСК эффективна у больных с высоким риском сердечно-сосудистых осложнений, включая нестабильную стенокардию, ИМ, хроническую стабильную стенокардию, ишемический инсульт, тогда как у лиц с низким риском их развития (здоровые индивидуумы без факторов риска сердечно-сосудистых заболеваний) ее профилактический эффект минимален. Хотя исследований по сравнению эффективности различных доз АСК у больных с ОКС без подъема сегмента ST не проводилось, представляется, что ее дозы, превышающие 80–160 мг/сут, не обладают большей эффективностью, но увеличивают риск развития кровотечений. Однако начинать лечение (первый прием) для быстрого наступления эффекта, если больной до этого не получал АСК, надо с 160–325 мг препарата (разжевать таблетку перед проглатыванием). У больных, которым уже назначали АСК, курс лечения следует продолжить.
АСК противопоказана при повышенной чувствительности к салицилатам, включая случаи бронхиальной астмы, у больных с активным кровотечением, гемофилией, кровоизлияниями в сетчатку, а также в случаях наличия потенциальных источников кровотечения (желудочно-кишечный тракт, мочеполовая система) и при тяжелой неконтролируемой артериальной гипертензии. В исследованиях по первичной профилактике сердечно-сосудистых заболеваний ее использование было связано с небольшим увеличением частоты возникновения внутричерепных кровоизлияний.
При длительном совместном применении АСК и ингибиторов ангиотензинпревращающего фермента (иАПФ), особенно у больных с тяжелой застойной хронической сердечной недостаточностью (ХСН), возможно некоторое ослабление гемодинамических эффектов иАПФ. В большинстве случаев это существенно не влияет на их клиническую эффективность. В то же время надо иметь в виду, что в этих ситуациях альтернативой иАПФ могут служить антагонисты рецепторов ангиотензина II, а АСК — клопидогрель. При назначении АСК больным с ХСН ее доза должна составлять не более 100 мг в сутки [7].
Клопидогрель и тиклопидин, относящиеся к тиенопиридиновым антиагрегантам, способны селективно угнетать АДФ-индуцированную агрегацию тромбоцитов. В отличие от АСК они не влияют на активность циклооксигеназы, продукцию тромбоксана тромбоцитами и простациклина клетками эндотелия. При приеме внутрь тиенопиридины трансформируются в печени в активные метаболиты, которые и обладают антитромбоцитарным эффектом. Их антиагрегантное действие необратимо, но при назначении «обычных» доз оно проявляется позже, чем у АСК (только через несколько дней). После отмены тиенопиридинов функция тромбоцитов восстанавливается медленно.
Тиенопиридины можно применять для вторичной профилактики ИМ, ишемического инсульта, лечения ОКСБПST, а также с целью предупреждения окклюзии коронарных стентов и шунтов. Исследование CAPRIE (Clopidogrel versus aspirin in patients at risk of a ischaemic events), в которое были включены 19 185 больных с ИМ, инсультом, стенозирующим атеросклерозом периферических артерий, получавших АСК в дозе 325 мг/сут или клопидогрель — 75 мг/сут, показало, что клопидогрель не менее эффективен, чем АСК, а вероятно, даже превосходит его в профилактике сердечно-сосудистых осложнений. Относительный риск развития ИМ, инсульта, внезапной сердечной смерти был меньше на 8,7% (p = 0,043) при использовании клопидогреля [8].
Таким образом, клопидогрель является наиболее совершенным препаратом этой группы. Этот высокоэффективный антиагрегант значительно быстрее тиклопидина проявляет антиагрегантное действие и имеет меньше побочных эффектов. Так, в ходе исследования CLASSICS [9], включавшего 1020 больных, которым проводилось стентирование коронарной артерии, была установлена большая безопасность клопидогреля по сравнению с тиклопидином. Осложнения (кровотечения, тромбоцитопения и нейтропения, другие побочные эффекты) практически в 2 раза чаще регистрировались у больных, получавших тиклопидин (9,12% по сравнению с 4,56%). По данным литературы, у 10–15% больных, получающих тиклопидин в рекомендованных дозах (по 250 мг 2 раза в сутки), развиваются побочные эффекты. Наиболее серьезными из них являются нейтропения, тромбоцитопения, агранулоцитоз, тромбоцитопеническая пурпура. Поэтому в течение первых 3 мес лечения тиклопидином рекомендуется каждые 2 нед делать анализ крови.
Необходимость совместного применения клопидогреля и АСК при ОКСБПST была доказана в ходе рандомизированного, двойного слепого, плацебо-контролируемого исследования CURE (Clopidogrel in unstable angina to prevent recurrent events) [10], в которое было включено 12 562 больных (средний возраст 64 года) из 482 медицинских центров, расположенных в 26 странах. Не позднее чем через 24 ч после появления симптомов они были разделены на две группы (6259 больных), получавших клопидогрель (сначала 300 мг, затем 75 мг 1 раз в сутки), и группу (6303 больных), получавших плацебо. Клопидогрель и плацебо в обеих группах назначались в дополнение к АСК (от 75 до 325 мг/сут). Средняя продолжительность наблюдения за больными составляла 9 мес (от 3 до 12 мес).
Антикоагулянты. Большое значение в ведении больных с ОКСБПST придается антикоагулянтам, которые оказывают существенное влияние на уменьшение прогрессирования патологического процесса и развитие осложнений. Имеются убедительные доказательства того, что эффективность НФГ у данных больных выше, чем при использовании плацебо. В то же время анализ результатов нескольких исследований по комбинированному лечению НФГ и АСК не показал его значимого преимущества по сравнению с применением только АСК [18]. Тем не менее четко прослеживается тенденция к уменьшению риска смерти и развития ИМ при ОКСБПST (на 33–56% в течение 5 дней — 12 нед) в результате совместного использования НФГ и АСК [19, 20]. Поэтому эта комбинация до сих пор рекомендуется ESC [18] и АСС/АНА [3], в качестве стандартной терапии ОКС без подъема сегмента ST (см. табл. 1).
Продолжительность лечения НФГ составляет 2–5 дней. Недостатком НФГ является непредсказуемость его антикоагулянтного действия при внутривенном введении одной и той же дозы препарата разным больным. В связи с этим необходимо осуществлять регулярный (каждые 6 ч) контроль за активированным частичным тромбиновым временем (АЧТВ), целевой уровень которого должен в 1,5–2,5 раза превышать норму (достигать приблизительно 50–70 с). Кроме того, определять АЧТВ следует через 4–6 ч после каждого изменения скорости введения препарата и при ухудшении состояния больного (рецидив болей, кровотечение, артериальная гипотензия и др.). Если дважды значения АЧТВ будут соответствовать целевому уровню, его можно контролировать через каждые 24 ч. Номограмма для коррекции скорости внутривенного введения НФГ представлена в таблице 3.
Многие годы НФГ (наряду с оральными антикоагулянтами) был основным препаратом для лечения и профилактики тромботических осложнений при различных сердечно-сосудистых заболеваниях. Однако, несмотря на высокую эффективность, НФГ имеет ряд недостатков и серьезных побочных эффектов, которые в определенной степени удалось преодолеть после создания ГНМВ.
ГНМВ получают путем различных способов (химических и ферментативных) деполимеризации НФГ, в результате чего образуются его фрагменты с более низким молекулярным весом (от 4000 до 6500 дальтон). Данные нарушения структуры гепарина приводят к изменениям в его фармакодинамике и фармакокинетике.
В отличие от НФГ, ГНМВ обладают большей активностью в ингибировании Ха-фактора свертывания и меньше влияют на IIa-фактор (тромбин). Отношение анти-Ха к анти-IIa-активности различных ГНМВ варьирует от 2:1 до 4:1 [21].
ГНМВ обладают значительно большей биодоступностью при подкожном введении, чем НФГ (соответственно 90% и 30%). К преимуществу первых перед НФГ относится также существенно большая продолжительность периода полувыведения. Все это дает им возможность вызывать устойчивую и предсказуемую гипокоагуляцию при одно- или двухразовом подкожном введении. Кроме того, применение ГНМВ в большинстве случаев не требует лабораторного мониторинга. Анализ большого клинического материала показывает, что тяжелые и фатальные кровотечения реже регистрируются при подкожном введении ГНМВ, чем при внутривенном применении НФГ [21].
Проведено более 10 рандомизированных исследований, посвященных сравнению воздействия ГНМВ и плацебо, АСК или НФГ у больных ОКСБПST. Было установлено, что эффективность ГНМВ выше, чем при приеме плацебо, а их сочетание с АСК более эффективно, чем монотерапия АСК [1]. Однако при сопоставлении различных ГНМВ (эноксапарин натрия, далтепарин натрия, надропарин кальция) с НФГ, выполненном в четырех крупных исследованиях, были получены неоднородные результаты.
Ю. А. Бунин, доктор медицинских наук, профессор
РМАПО, Москва