Облацио в кардиологии что это такое
Облацио в кардиологии что это такое
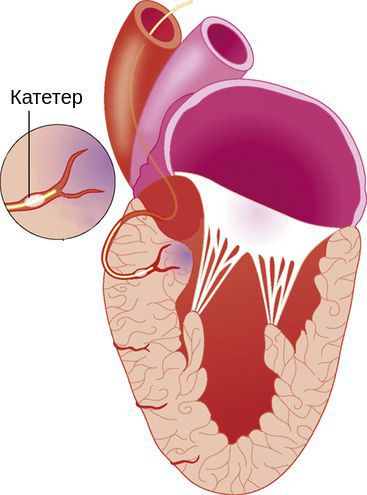
В норме регулярная работа нашего сердца поддерживается электрическими импульсами, которые генерируются группой специальных клеток. Эти клетки сформированы в компактное образование – синусовый узел, расположенный в верхней части правого предсердия [рис. 1].
При фибрилляции предсердий (мерцательной аритмии) вместо регулярного сердечного ритма в предсердиях возникают множественные электрические волны, приводящие к хаотичным сокращениям обоих предсердий с очень высокой частотой [рис. 2].
Фибрилляция предсердий (мерцательная аритмия), как правило, проявляется учащенным нерегулярным сердечным ритмом, одышкой, плохой переносимостью физических нагрузок. Нередко фибрилляции предсердий протекает бессимптомно и обнаруживается случайно при регистрации ЭКГ. Нередко у пациентов с фибрилляцией предсердий (мерцательной аритмии) обнаруживается еще один вид нарушений сердечного ритма – трепетание предсердий [ рис.3 ]. Симптомы трепетания предсердий мало отличаются от фибрилляции предсердий. Точная диагностика данных нарушений ритма и определение тактики лечения должны определяется кардиологом-аритмологом.
2. Зачем и как лечить фибрилляцию предсердий?
Лечение фибрилляции предсердий ставит своей целью:
По данным мировой медицинской статистики фибрилляция предсердий (мерцательная аритмия) – самое часто встречающаяся (1-2 % в популяции) нарушение сердечного ритма. У значительной части пациентов (до 40%) ФП носит бессимптомный характер. У этой категории больных медикаментозное антиаритмическое или немедикаментозное лечение (катетерная аблация) ФП, как правило, не проводится. Лечение этих пациентов заключается в контроле частоты сердечного ритма и назначении антикоагулянтов для профилактики тромбоэмболических осложнений. Пациентам, у которых фибрилляция предсердий сопровождается описанными выше симптомами назначают постоянную антиаритмическую терапию, направленную на профилактику рецидивов ФП. Приблизительно у одной трети среди всех больных ФП удается подобрать эффективный антиаритмический препарат или их комбинацию.
У 30% больных с симптомной, плохо переносимой фибрилляцией предсердий не удается подобрать эффективную антиаритмическую терапию, либо прием антиаритмических средств противопоказан, сопровождается развитием побочных эффектов или пациенты не хотят придерживаться тактики длительного консервативного медикаментозного лечения. Этой категории больных в соответствии с современными международными и российскими рекомендациями рекомендуется проведение катетерной аблации.
Следует подчеркнуть, что выбор вариантов лечения в каждом конкретном случае – задача кардиолога-аритмолога с учетом мнения пациента и объективных медицинских данных.
3. Катетерная и хирургическая аблация
В зависимости от формы фибрилляция предсердий (пароксизмальная, персистирующая или постоянная), наличия другой патологии со стороны сердечно-сосудистой системы и сопутствующих заболеваний применяются 3 разновидности катетерной (или хирургической) аблации:
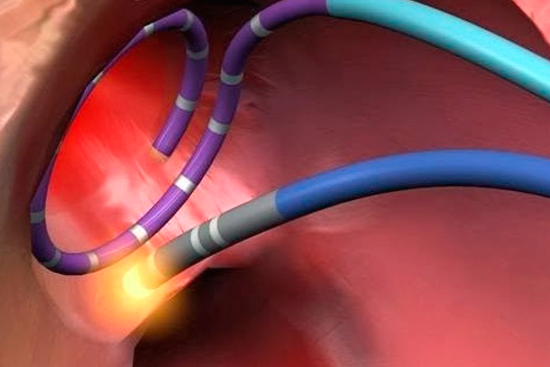
• внутрисердечная катетерная аблация – наиболее широко используемый метод немедикаментозного лечения ФП. Катетерная аблация проводится в условиях рентгеноперационной с использованием управляемых катетеров, перемещаемых в камеры сердца через сосудистые доступы (бедренные и подключичные вены). Цель катетерной аблации радикальное устранение «источников» аритмии в левом и (при трепетании предсердий) правом предсердии. В настоящее время широкое клиническое применение нашли 2 вида катетерной аблации: радиочастотная катетерная аблация и баллонная криоаблация.
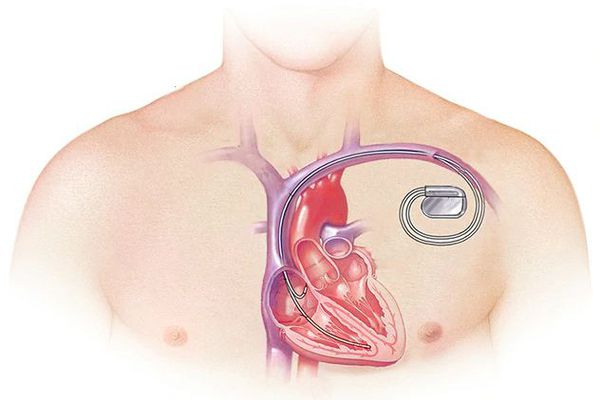
• катетерная аблация (деструкция) АВ узла – разновидность внутрисердечной катетерной аблации, которая применяется в тех случаях, когда ФП сопровождается стойко высокой частотой сердечных сокращений при невозможности медикаментозного контроля или радикального устранения ФП. Аблация АВ узла проводится только после имплантации искусственного водителя ритма (кардиостимулятора).
4. Радиочастотная или баллонная криоаблация?
Как это работает?
Видео 1. Баллонная криоаблация
Эффективность и безопасность
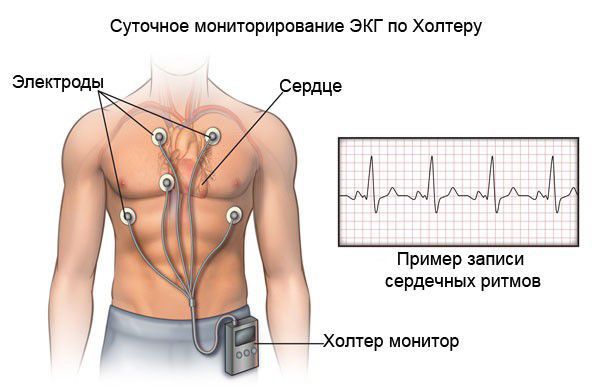
Общепринятым определением эффективности катетерной аблации при ФП считается отсутствие любых предсердных аритмий после аблации без применения антиаритмических средств. Контроль за эффективностью осуществляется клинически (самоконтроль пациентов) или с использованием систем длительной регистрации ЭКГ (ХМ ЭКГ или специальные имплантируемые регистраторы сердечного ритма).
Одним из основных факторов, определяющих эффективность катетерных аблаций при ФП является длительность эпизодов фибрилляции. В тех случаях когда приступы аритмии не превышают нескольких часов или дней (т.н. пароксизмальная форма) и, как правило, закачиваются самостоятельно, оперативное лечение максимально эффективно. В сравнительных исследованиях (международное исследование «Fire and Ice») рецидивов ФП в течение первого года не было у 65% больных как после радиочастотной, так и после баллонной криоаблации. При этом, есть наблюдения, что у лиц без сопутствующей кардиальной патологии эффективность баллонной криоаблации может достигать 80-90%.
У пациентов с персистирующей формой ФП, т.е. с аритмией длительностью более 7 дней, а также требующей для восстановления синусового ритма проведения медикаментозной или электрической кардиоверсии, ожидаемая эффективность катетерных аблаций – около 50-60%.
Если после катетерной аблации ФП рецидивирует с прежней частотой и длительностью, оправданным является проведение повторного вмешательства.
Осложнения при катетерной аблации ФП могут проявляться в виде повреждения сосудов в месте пункции, перфорации стенки сердца с развитием тампонады, образование тромбов в полости сердца и тромбоэмболическими осложнениями, термическим повреждением пищевода, развитием пареза диафрагмального нерва и рядом других. Применение современных высокотехнологичных методов контроля во время внутрисердечных вмешательств, достаточный опыт и квалификация врачей позволяет выполнять данные вмешательства эффективно и без значительного риска развития осложнений. Вместе с тем, необходимо четко осознавать, что решение о проведении интервенционного лечения ФП должен принимать врач с достаточным опытом лечения подобной категории больных, объективно учитывая аргументы «за и против».
5. Катетерная аблация ФП в отделе клинической электрофизиологии и рентгенхирургии нарушений ритма
Интервенционная аритмология – одно из основных направлений в научной и клинической работе отдела клинической электрофизиологии с момента его основания в 1990 г. Почти 20 лет насчитывает опыт лечения различных нарушений сердечного ритма с использованием технологии катетерных аблаций.
С 2012 года в отделе был внедрен метод катетерных аблаций при ФП. Сегодня приоритетным методом, используемым в клинической практике отдела клинической электрофизиологии при немедикаментозном лечении ФП является метод баллонной криоаблации. Этот выбор основан на том, что криоаблация при ФП не уступает по эффективности радиочастотной, являясь при этом наиболее безопасным методом интервенционного лечения ФП, что было доказано при анализе многолетнего опыта ведущих мировых центров в лечении ФП.
Специалисты отдела клинической электрофизиологии проводят полноценное предоперационное обследование пациентов, выполняют интервенционное вмешательство и обеспечивают амбулаторное наблюдение за всеми пациентами в течение не менее 1 года после катетерной криоаблации ФП. В тех случаях, когда у пациентов имеются сложные сопутствующие нарушения сердечного ритма применяется комплексное (одномоментное) интервенционное лечение, либо т.н. «гибридная терапия», сочетающая катетерное вмешательство и последующее медикаментозное лечение. В случае рецидива ФП может быть выполнена повторная баллонная криоаблация или радиочастотная катетерная аблация.
Радиочастотная абляция сердца
Радиочастотная абляция сердца
Изобретение и активное внедрение в повсеместную практику малоинвазивных вмешательств с максимальным эффектом – это основной путь развития современной медицины. Именно к таким операциям и относится радиочастотная катетерная абляция.
РЧА – это методика лечения нарушений сердечного ритма, путем проведения физической деструкции очага патологического возбуждения или участков анормального проведения импульса.
Эта операция позволила отказаться от сложных хирургических вмешательств на открытом сердце при лечении множества видов аритмий, в том числе и устойчивых к медикаментозной терапии.
Показания к операции
Радиочастотная катетерная абляция сердца является вариантом выбора при лечении аритмий у пациентов молодого возраста, так как позволяет в относительно короткие сроки не только улучшить самочувствие пациента и качество его жизни, но и уменьшить риски внезапной сердечной смерти и потери трудоспособности.
Патологии, при которых врачи настоятельно рекомендуют проведение РЧА сердца:
РЧА может при жизненной необходимости проводиться даже детям без врожденных пороков развития сердца, начиная с раннего возраста. В этом случае показаниями к назначению операции РЧА будет развитие тахизависимой кардиопатии со снижением насосной функции сердца и отсутствием должного эффекта после применения всех групп антиаритмических препаратов.
Стоит отметить, что при ряде аритмических нарушений радиочастотная абляция сердца рекомендуется и том в случае, если пациент не желает принимать антиаритмические средства пожизненно или плохо их переносит.
Цель операции
Цели, преследуемые при выполнении РЧА сердца, всегда направлены на устранение причины аритмогенеза – патологического проводящего пути или аномально активного участка миокарда. Для этого при абляции сердца выполняется точечное разрушение неправильно функционирующего участка проводящей системы сердца, что может иметь два различных эффекта, каждый из которых оптимален при своей группе патологий сердца. Так при лечении предсердных тахикардий с аномалиями AV-проведения методикой выбора является полная или частичная радиочастотная абляция атриовентрикулярного соединения. В то же время в случае желудочковой тахикардии или наличия обходных путей проведения РЧА будет направлено на разрушение самого патологического участка сердца.
Проведение радиочастотной катетерной абляции сердца позволяет избежать ряда негативных последствий жизни с аритмией, таких как:
Виды РЧА
Так как принцип действия катетерной абляции заключается в разрушении небольшого участка, то все разновидности данной процедуры отличаются по физическому фактору, вызывающему деструкцию:
Однако эффективность, управляемость деструкции и особенности выполнения для этих методик неодинаковы. Сейчас чаще всего применяется именно РЧА, так как именно по этой методике наработано наибольшее количество положительных результатов. Тогда как, например, от абляции постоянным электрическим током большинство кардиохирургов отходят в пользу РЧА сердца и других методик.
Подготовка к операции, необходимые анализы и обследования
Перед операцией при общении с кардиохирургом, который будет проводить радиочастотную абляцию сердца, необходимо четко озвучить список лекарственных препаратов, принимаемых пациентом, и их дозировки. Также важно предоставить врачу информацию о наличии имплантированного кардиостимулятора, аллергических реакций или непереносимости на медикаменты, если они имеют место.
В список обязательных диагностических процедур перед проведением абляции сердца включаются следующие:
Так же при наличии сопутствующей патологии, кроме рутинных методов, могут потребоваться дополнительные анализы и диагностических процедуры. Например, больным с ИБС может быть назначена липидограмма, а пациентам с сахарным диабетом – исследование уровня гликированного гемоглобина. Важно учитывать, что многие пациенты с аритмиями получают антикоагулянтную терапию, поэтому к вышеуказанному может быть добавлено и исследование МНО.
Рекомендуется накануне перед РЧА (не менее 12 часов) не принимать пищу и воду.
Методика проведения операции
При проведении радиочастотной абляции не требуется общая анестезия, поэтому пациенту лишь обезболивают место введения катетерного электрода, а также назначают седативные препараты. Уже в операционной обеспечивается стабильный венозный доступ: он понадобится для введения контрастных веществ, антиаритмиков или других лекарственных средств, необходимость в которых может возникнуть в ходе РЧА сердца.
Главные инструменты бригады электрофизиологов и кардиохирургов – гибкие катетерные электроды. Они вводятся через крупный сосуд, преимущественно доступ проводится через бедренную артерию. Не исключаются и другие варианты введения электродов, например, через подключичную вену или другие сосуды. Радиочастотная абляция выполняется под контролем рентгеноскопии, поэтому пациенту не стоит бояться, что кардиохирурги действуют вслепую.
Обычно операция РЧА проводится в два этапа:
В случае, когда патология (например, фибрилляция предсердий) требует разрушения атриовентрикулярного соединения, то добавляется еще один этап – имплантация кардиостимулятора, так как при такой абляции сердца полностью прекращается проведение импульсов от тканей предсердий к миокарду желудочков.
Электрофизиологическое исследование является составлением своеобразной карты сердца, на которой будут отражаться участки, где происходит патологическое проведение или образование электрических импульсов. Производится эта процедура путем введения специфического контраста и электрической стимуляции участков сердца. Во время этой процедуры обычно индуцируются нарушения ритмичности работы сердца, но в условиях операционной эти аритмии не несут угрозы пациенту.
По завершению картирования кардиохирурги вводят через тот же доступ абляционный электрод и приступают к собственно проведению РЧА сердца. Катетерный абляционный электрод устанавливают в проекции патологического участка и точечным воздействием радиочастотных волн производят его разрушение. При наличии крупного очага или нескольких аномальных зон в тканях сердца их деструкция может быть выполнена в ходе одной операции или потребуется повторное проведение РЧА позднее.
После процедуры РЧА при наличии показаний может производиться установка и программирование кардиостимулятора.
Так как во время проведения абляции сердца пациент находится в сознании, то это иногда сопряжено с некоторым дискомфортом. Поэтому при появлении любых неприятных ощущений желательно сообщать врачу. В то же время не стоит бояться этого вмешательства, ведь практически все манипуляции с электродами для больного безболезненны.
Количество времени, затрачиваемое на проведение радиочастотной абляции, колеблется в диапазоне от 3 до 7 часов.
Описание послеоперационного периода и реабилитации
Одним из наиболее значимых преимуществ РЧА по сравнению с операциями на открытом сердце – является малая травматичность и быстрое восстановление. В то время как больной после стернотомии будет ощущать боль в области грудины, месяцами носить специальный бандаж, а также ограничивать свои нагрузки, пациент после РЧА уже через пару недель сможет вернуться к своему обычному ритму жизни, который уже не будет обременен аритмией.
Непосредственно из операционной пациент переводится в отделение интенсивной терапии, где и проводит первые сутки после РЧА. Здесь проводится постоянный контроль за сердечным ритмом и артериальным давлением. Для предупреждения кровотечения из места введения абляционного катетера рекомендуется лежать в первые 4-5 часов после операции.
При отсутствии осложнений покинуть клинику, в которой проводилась абляция сердца, пациент сможет уже на следующий день.
Возможные осложнения при РЧА
Такое вмешательство, как абляция сердца, имеет очень низкий риск возникновения серьезных осложнений, но не исключает их совсем. Наиболее часто пациенты сталкиваются с возникновением гематомы в месте введения электродов, однако они обычно не требуют какого-либо специфического лечения и в течение нескольких недель проходят самостоятельно.
Реже встречаются более серьезные осложнения:
Риск смерти при проведении данной операции обычно составляет около 0,2% и менее.
Результативность после операции РЧА будет зависеть от типа аритмии, анатомических особенностей сердца пациента и наличия сопутствующей патологии внутренних органов в целом и сердца в частности. Процент успешных РЧА колеблется в пределах от 75% до 95%, например, при лечении суправентрикулярных аритмий он составляет около 96%. Частота осложнений при выполнении абляции сердца встречается не чаще, чем в 1,5-2%.
Иногда после удачно проведенной первой операции РЧА со временем формируются новые аномальные участки, что связано с особенностями электрофизиологии сердца конкретного пациента, в таких клинических ситуациях также может потребоваться повторная абляция.
В подавляющем большинстве случаев отзывы пациентов о качестве жизни после РЧА положительные. Они могут заниматься теми делами, доступ к которым ранее был закрыт из-за риска возникновения аритмии. Пациенты могут заниматься спортом, женщины фертильного возраста безопасно выносить и даже самостоятельно родить ребенка. Существенным плюсом является и то, что при ряде патологий после РЧА сердца не требуется продолжать постоянный прием медикаментов.
Выполнение радиочастотной абляции требует высокотехнологичного оборудования и наличия квалифицированных специалистов, поэтому еще не проводится повсеместно. Обычно клиники располагающие данными ресурсами есть в крупных городах, а в Санкт-Петербурге и Москве их даже несколько.
Стоимость радиочастотной абляции сердца рассчитывается индивидуально для каждого пациента и может значительно варьировать из-за разных объемов вмешательства, необходимости имплантации стимулятора, а также уровня клиники, в которой проводится операция. Средняя цена составляет от 150 тыс. руб.
Следует отметить, что в РФ существуют квоты на бесплатное проведение РЧА сердца.
Что такое кардиомиопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кузнецова Т. Н., кардиолога со стажем в 26 лет.
Определение болезни. Причины заболевания
Пусковым механизмом возникновения кардиомиопатии поначалу считали процесс воспаления в сердце, который мог быть спровоцирован вирусными, бактериальными и аутоиммунными повреждениями клеток. Исходя из этой теории, назначение антибиотиков, противовирусных и противовоспалительных препаратов должно было привести к регрессии повреждения и восстановлению функции сердца. Однако практика это не подтвердила.
Риск развития кардиомиопатий повышен у лиц с отягощённой наследственностью, а также после перенесённых острых инфекционных заболеваний. Для появления вторичных кардиомиопатий важно наличие системных аутоиммунных заболеваний, эндокринной патологии (сахарный диабет, тиреотоксикоз) и токсических факторов.
Первичные кардиомиопатии чаще выявляют в детском и молодом возрасте, вторичные же возможны в любом возрасте.
Симптомы кардиомиопатии
Специфических, характерных только для кардиомиопатии симптомов не существует. Именно эта особенность и затрудняет раннюю диагностику заболевания. Кардиомиопатия длительно протекает бессимптомно или малосимптомно, в развёрнутой стадии похожа по клинике на проявления ишемической болезни сердца, различных пороков сердца.
Первыми жалобами, с которыми пациенты обращаются к врачу, являются:
Патогенез кардиомиопатии
За последние годы благодаря возможностям генетики было установлено, что причиной многих кардиомиопатий являются генетические мутации, которые приводят к выработке дефектных белков кардиомиоцита. От того, какой белок рабочей клетки миокарда (кардиомиоцита) изменился, зависит развитие определённого вида кардиомиопатии.
Подобные изменения бывают также при наследственных нарушениях обмена веществ и лизосомальных болезнях накопления (редких заболеваниях, при которых нарушается функция внутриклеточных органелл лизосом). Из-за врождённой нехватки ферментов, перерабатывающих углеводсодержащие продукты, в организме накапливаются крупные молекулы гликогена, гликопротеина и др., которые повреждают организм. Таких заболеваний известно более сотни, но их распространённость невелика. Как правило, проявляются они в детском и молодом возрасте и помимо поражения сердца затрагивают практически весь организм: кости, мышцы, нервную систему, зрение и слух. Самыми изученными болезнями накопления являются гемохроматоз, болезнь Пике и болезнь Фабри.
Классификация и стадии развития кардиомиопатии
По мере накопления информации были выявлены самые распространённые типы кардиомиопатии и их семейные формы:
К редким формам кардиомиопатии относят также системные заболевания и патологические состояния, при которых возникают так называемые вторичные кардиомиопатии: диабетическая, тиреотоксическая, алкогольная, аутоиммунная и другие.
Исходя из причины развития болезни, становится ясным, что кардиомиопатии могут быть как изолированными – первичными, так и являться частью системного заболевания, т. е. быть вторичными.
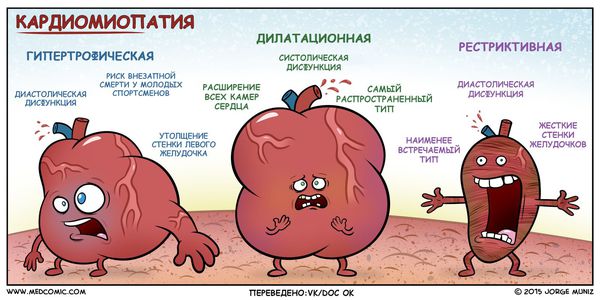
В России традиционно применяется клинико-морфологическая классификация первичных кардиомиопатий, где кардиомиопатии разделяются на:
Анатомическая классификация гипертрофической кардиомиопатии в зависимости от локализации:
I. Гипертрофия левого желудочка:
В зависимости от наличия обструкции выносного тракта левого желудочка (область между межжелудочковой перегородкой и передней створкой митрального клапана) в покое и при нагрузке выделяют два типа гипертрофической кардиомиопатии :
К тяжело выявляемым видам относится аритмогенная дисплазия правого желудочка, при которой происходят структурные изменения в строении стенки правого желудочка — замещение кардиомиоцитов фиброзно-жировой тканью и развитие аритмии.
Неклассифицируемые кардиомиопатии: некомпактный миокард, стресс-индуцированная кардиомиопатия.
Вторичные (специфические) кардиомиопатии: при имеющемся известном заболевании тяжесть поражения сердца более выражена и не соответствует причине:
Осложнения кардиомиопатии
Особенности течения кардиомиопатии представляют угрозу для жизни. Болезнь может дебютировать сразу внезапной смертью или жизнеугрожающими аритмиями : фибрилляцей желудочков, желудочковой тахикардией. Высокий риск внезапной сердечной смерти связан с такими факторами риска, как:
С утяжелением недостаточности все симптомы становятся более выраженными. Выделяют пять стадий сердечной недостаточности:
Диагностика кардиомиопатии
Особых признаков, характерных для этого заболевания, при сборе жалоб и осмотре пациента выявить не удаётся.
При клиническом осмотре обращают на себя внимание признаки сердечной недостаточности различной степени выраженности, аритмии, возможны тромбоэмболические осложнения.
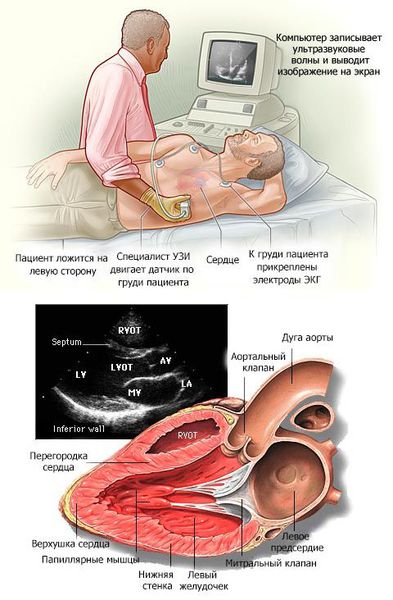
В основном кардиомиопатии выявляются при проведении эхокардиографии (ЭХОКГ) и электрокардиографии (ЭКГ). Дополнительно применяются рентгеноконтрастная вентрикулография и магнитно-резонансная томография (МРТ) с контрастированием гадолинием.
В современной кардиологии всё больше распространяются новые методы визуализации сердца и сосудов — например, магнитно-резонансная томография (МРТ). Но её недостатком является дороговизна оборудования и малая доступность методики из-за отсутствия качественного оборудовании и специалистов.
На стандартной ЭКГ также могут быть зарегистрированы изменения в виде признаков гипертрофии миокарда левого желудочка, а также признаки его перегрузки и различные нарушения ритма сердца.
При холтеровском мониторировании ЭКГ также фиксируются нарушения ритма и проводимости практически в 100 % случаях. Выявление таких нарушении ритма сказывается на подборе базисной терапии кардиомиопатии.
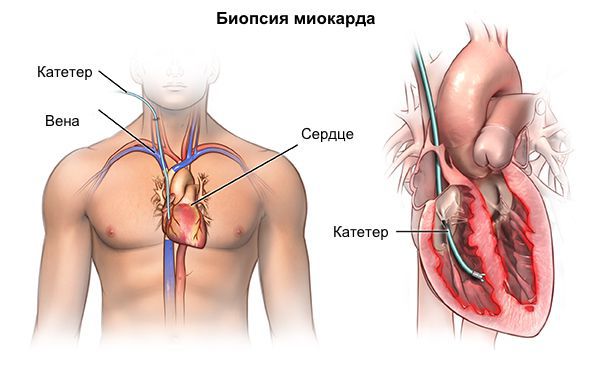
В особых случаях для уточнения диагноза редких форм кардиомиопатии (например, при амилоидозе) возможна прижизненная биопсия миокарда. Методика инвазивная, потенциально опасная для пациента, требует использования уникального комплекса аппаратуры и высочайшей квалификации специалистов, что возможно только в нескольких научных кардиологических центрах РФ.
Из лабораторных методов диагностики помимо стандартных анализов крови (клинического и биохимического), необходимо отметить ДНК-диагностику. Она является «золотым стандартом» при подозрении на кардиомиопатию согласно мировым (европейским и американским) руководствам. Этот подход на данный момент является практически единственным, который применим для раннего выявления и прогнозирования риска развития семейных форм кардиомиопатии. В России такой уровень диагностики возможен в единичных лабораториях и является дорогостоящей процедурой из-за своей уникальности.
Лечение кардиомиопатии
По современным представлениям стратегия лечения пациента определяется в процессе разделения больных на категории в зависимости от типа кардиомиопатии.
Все больные с выявленной кардиомиопатией, независимо от течения заболевания (в том числе и бессимптомные), нуждаются в динамическом наблюдении. Кратность наблюдения и объём обследований определяются индивидуально. В обязательный перечень входят стандартные анализы (клинический и биохимический анализ крови), ЭКГ, ЭХОКГ и холтеровское мониторирование ЭКГ.
Лечебная тактика зависит от множества факторов и подбирается индивидуально. При этом учитываются анатомические особенности — обструкция выносного тракта левого желудочка, растяжение полостей сердца, наличие клапанной патологи, стадия сердечной недостаточности и также сопутствующие заболевания. Необходимо выявлять факторы, повышающие риск внезапной смерти и жизнеугрожающих аритмий [15]
При дилатационной кардиомиопатии необходимо лечить причину развития растяжения полостей сердца, если это возможно. В медикаментозной терапии сердечной недостаточности применяют все стандартные группы лекарств:
Помимо лекарств в ряде случаев прибегают к хирургическим методам лечения кардиомиопатии.
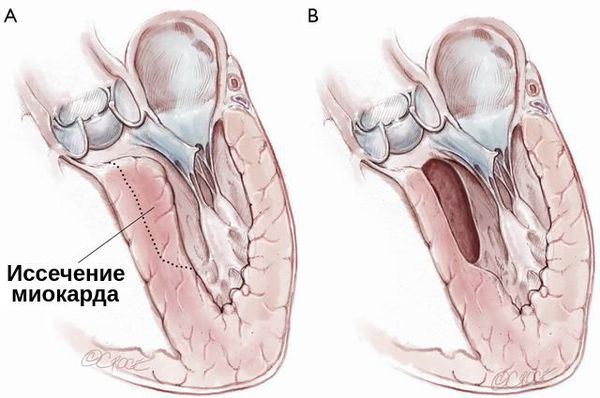
При гипертрофической кардиомиопатии применяется септальная миэктомия — иссечение миокарда, расположенного в основании межжелудочковой перегородки. Она может быть дополнена и вмешательством на изменённом митральном клапане: вальвулопластикой, протезированием митрального клапана и коррекцией кольца митрального клапана.
При тяжёлой обструктивной гипертрофической кардиомиопатии рассматривается проведение операции — иссечения части сердечной мышцы или более щадящая методика — чрескожная транслюминальная алкогольная абляция. При ней через катетер вводится до 3 мл 96 % спирта в зону максимальной гипертрофии миокарда и вызывается его инфаркт. Из-за этого мышца уменьшается в размере, исчезает препятствие (обструкция) току крови через митральное кольцо. Далее проводится установка кардиостимулятора для синхронизации работы всех отделов сердца. Эта процедура проводится кардиохирургами в специализированных отделениях.
Прогноз. Профилактика
Прогноз при гипертрофической кардиомиопатии также неблагоприятный, но смертность не такая высокая — в первый год умирают 1 % заболевших, чаще от внезапной смерти, обусловленной факторами риска (наследственностью, тахикардией, предшествующим обмороками, понижением давления).
При рестриктивной кардиомиопатии прогноз неблагоприятный, так как заболевание часто находят уже на поздней стадии развития. Лечение только симптоматическое и поддерживающее.
Для человека с выявленной кардиомиопатии частота посещений и обследований устанавливается индивидуально.