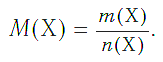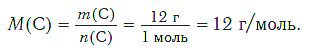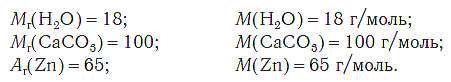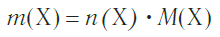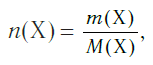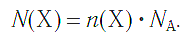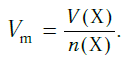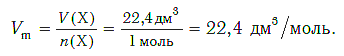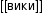Объем в чем измеряется химия
Урок 9. Молярная масса и молярный объем
В уроке 9 «Молярная масса и молярный объем» из курса «Химия для чайников» выясним, что подразумевается под молярной массой и молярным объемом; приведем формулы для их вычисления. Напоминаю, что в прошлом уроке «Химическое количество вещества и моль» мы выяснили, что такое химическое количество вещества; рассмотрели моль в качестве единицы количества вещества, а также познакомились с постоянной Авогадро.
Молярная масса
Вы знаете, что одинаковое химическое количество любых веществ содержит одно и то же число структурных единиц. Но у каждого вещества его структурная единица имеет собственную массу. Поэтому и массы одинаковых химических количеств различных веществ тоже будут различны.
Молярная масса — это масса порции вещества химическим количеством 1 моль.
В Международной системе единиц молярная масса выражается в кг/моль. В химии чаще используется дольная единица — г/моль.
Определим молярную массу углерода. Масса углерода химическим количеством 1 моль равна 0,012 кг, или 12 г. Отсюда:
Молярная масса любого вещества, если она выражена в г/моль, численно равна его относительной молекулярной (формульной) массе.
На рисунке 47 показаны образцы веществ (H2O, CaCO3, Zn), химическое количество которых одно и то же — 1 моль. Как видите, массы разных веществ химическим количеством 1 моль различны.
Молярная масса является важной характеристикой каждого отдельного вещества. Она отражает зависимость между массой и химическим количеством вещества. Зная одну из этих величин, можно определить вторую — массу по химическому количеству:
и, наоборот, химическое количество по массе:
а также число структурных единиц:
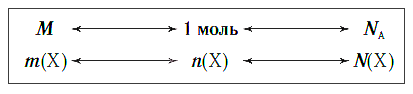
Взаимосвязь между этими тремя характеристиками вещества в любом его агрегатном состоянии можно выразить простой схемой:
Молярный объем
Подобно молярной массе, молярный объем газа равен отношению объема данного газообразного вещества V(Х) к его химическому количеству n(Х) :
Так как объем газа зависит от температуры и давления, то при проведении различных расчетов берутся обычно объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимаются температура 0 °С и давление 101,325 кПа.
Установлено, что при нормальных условиях отношение объема любой порции газа к химическому количеству газа есть величина постоянная и равная 22,4 дм 3 /моль. Другими словами, молярный объем любого газа при нормальных условиях:
Пример 1. Вычислите химическое количество SiO2, масса которого равна 240 г.
Пример 2. Определите массу серной кислоты H2SO4, химическое количество которой 2,5 моль.
Пример 3. Сколько молекул CO2 и сколько атомов кислорода содержится в углекислом газе массой 110 г?
Пример 4. Какой объем занимает кислород химическим количеством 5 моль при нормальных условиях?
Краткие выводы урока:
Надеюсь урок 9 «Молярная масса и молярный объем» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Данный урок был заключительным в главе «Основные химические понятия».
Молярный объем

Всего получено оценок: 193.
Всего получено оценок: 193.
При изучении химических веществ важными понятиями являются такие величины, как молярная масса, плотность вещества, молярный объем. Так, что же такое молярный объем, и в чем его отличие для веществ в разном агрегатном состоянии?
Молярный объем: общая информация
Чтобы вычислить молярный объем химического вещества необходимо молярную массу этого вещества разделить на его плотность. Таким образом, молярный объем вычисляется по формуле:
где Vm – молярный объем вещества, М – молярная масса, p – плотность. В Международной системе СИ эта величина измеряется в кубический метр на моль (м 3 /моль).
Молярный объем газообразных веществ отличается от веществ, находящихся в жидком и твердом состоянии тем, что газообразный элемент количеством 1 моль всегда занимает одинаковый объем (если соблюдены одинаковые параметры).
Объем газа зависит от температуры и давления, поэтому при расчетах следует брать объем газа при нормальных условиях. Нормальными условиями считается температура 0 градусов и давление 101,325 кПа.
Молярный объем 1 моля газа при нормальных условиях всегда одинаков и равен 22,41 дм 3 /моль. Этот объем называется молярным объемом идеального газа. То есть, в 1 моле любого газа (кислород, водород, воздух) объем равен 22,41 дм 3 /м.
Молярный объем при нормальных условиях можно вывести, используя уравнение состояния для идеального газа, которое называется уравнением Клайперона-Менделеева:
где R – универсальная газовая постоянная, R=8.314 Дж/моль*К=0,0821 л*атм/моль К
Объем одного моля газа V=RT/P=8.314*273.15/101.325=22.413 л/моль, где Т и Р – значение температуры (К) и давления при нормальных условиях.
Закон Авогадро
В 1811 году А. Авогадро выдвинул гипотезу, что в равных объемах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковой число молекул. Позже гипотеза подтвердилась и стала законом, носящим имя великого итальянского ученого.
Закон становится понятен, если вспомнить, что в газообразном виде расстояние между частицами несопоставимо больше, чем размеры самих частиц.
Таким образом, из закона Авогадро можно сделать следующие выводы:
Следствие из закона Авогадро и понятие молярного объема основаны на том, что моль любого вещества содержит одинаковое число частиц (для газов – молекул), равное постоянной Авогадро.
Чтобы узнать число молей растворенного вещества содержится в одном литре раствора, необходимо определить молярную концентрацию вещества по формуле c=n/V, где n – количество растворенного вещества, выражаемое в молях, V – объем раствора, выражаемый в литрах С – молярность.
Что мы узнали?
В школьной программе по химии 8 класса изучается тема «Молярный объем». В одном моле газа всегда содержится одинаковый объем, равный 22,41 кубический метр/моль. Этот объем называется молярным объемом газа.
Определение молярного объема при химических реакциях
Молярный объем — что это такое в химии
Молярный объем V m — является отношением объема вещества к его количеству, численно равен объему одного моля вещества.
Термин «молярный объем» применим по отношению к простым веществам, химическим соединениям и смесям. Величина зависит от следующих факторов:
Молярный объем вычисляют по формуле:
Молярный объем является характеристикой плотности упаковки молекул в рассматриваемом веществе. В случае простых веществ в некоторых ситуациях допустимо использовать понятие атомного объема.
Исходя из того, что объем газа определяется температурой и давлением, в процессе расчетов принято использовать объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимают:
Молярный объем какого-либо газа при нормальных условиях:
Молярный объем смеси
Молярный объем смеси:
Молярный объем газов
Закон Авогадро: одинаковые количества газов при одинаковых условиях занимают одинаковый объем.
Молярный объем идеального газа вычисляют с помощью формулы, которая является выводом из уравнения состояния идеального газа.
Молярный объем идеального газа:
где T — является термодинамической температурой;
R — универсальная газовая постоянная.
Молярный объем кристаллов
Объем V я элементарной ячейки кристалла вычисляют с помощью характеристик кристаллической структуры, которые определяют на основании результатов рентгеноструктурного анализа.
Зависимость между объемом ячейки и молярным объемом:
где Z — определяет, сколько формульных единиц в элементарной ячейке.
Значения молярного объема химических элементов
Вычисление химического количества газа по его объему
Объем газа можно рассчитать по его химическому количеству. В этом случае необходимо преобразовать формулу молярного объема путем выражения из нее V :
Таким образом, объем газа равен произведению его химического количества на молярный объем. Продемонстрировать данное утверждение можно на примере. Допустим, что необходимо определить объем (н. у.) метана с химическим количеством 1,5 моль. Используя уравнение, записанное ранее, проведем вычисления:
При известном объеме газообразного вещества можно определить химическое количество рассматриваемого газа. В этом случае следует выразить из уравнения молярного объема n:
Определение объема веществ при химических реакциях
Перед тем, как приступить к расчетам объема веществ, следует ввести понятие плотности. Данный показатель определяется отношением массы вещества к его объему. Плотность измеряют в к г / м 3 (или г/л, г/мл). В случае газообразных веществ плотность принимает очень маленькие значения. Упростить расчеты химических реакций можно, если рассматривать отношение плотностей газов.
Относительной плотностью газа В по газу А называют величину, равную отношению плотностей рассматриваемых веществ или отношению молярных масс этих газов.
Данный параметр обозначают D A ( B ) и определяют по формуле:
В связи с тем, что в расчете относительной плотности используют величины одинаковой размерности, данный параметр является безразмерной величиной. Определить относительную плотность газообразных веществ по некому газу можно с помощью отношения молярных масс этих газов. Например, относительная плотность кислорода по водороду составляет:
Согласно закону Авогадро, в равных объемах различных газов, которые существуют при одинаковых температурах и давлениях, содержится одно и то же количество молекул. Данная гипотеза была представлена в 1811 году в Турине профессором физики Амедео Авогадро.
Подтверждение теория нашла во множестве экспериментальных опытах. Закон получил название закона Авогадро и стал в дальнейшем количественной основой современной химии. Закон Авогадро в точности реализуем в случае идеального газа. С увеличением разреженности газообразного вещества повышается точность расчетов по этому закону применительно к данному реальному газу.
Первое следствие из закона Авогадро: один моль (одинаковое количество молей) любого газа при одинаковых условиях занимает одинаковый объем.
Исходя из закона Авогадро, одинаковое число молекул какого-либо газа занимает при одинаковых условиях один и тот же объем. Наряду с тем, 1 моль какого-то вещества включает в себя (согласно определению) одинаковое количество частиц (к примеру, молекул). Таким образом, при определенных температуре и давлении 1 моль любого вещества в газообразном состоянии занимает один и тот же объем.
Если условия соответствуют нормальным, то есть температура равна 0 °C (273,15 К), и давление составляет 101,325 кПа, объем 1 моль газа соответствует 22,413 962(13) л. Данная физическая константа является молярным объемом идеального газа и обозначается Vm.
Вычислить молярный объем при температуре и давлении, отличных от нормальных условий, можно с помощью уравнения Клапейрона:
Второе следствие из закона Авогадро: молярная масса первого газа равна произведению молярной массы второго газа на относительную плотность первого газа ко второму.
Как найти объемные отношения газов в смеси
В процессе вычисления объемных отношений газов, участвующих в химических реакциях, используют закон Гей-Люссака (химический закон объемных отношений). В англоязычной литературе данный закон можно встретить под названием закона Шарля.
Закон Гей-Люссака — закон, демонстрирующий пропорциональную зависимость между объемом газообразного вещества и абсолютной температурой при постоянном давлении (то есть в изобарном процессе).
Закон получил название в честь французского физика и химика Жозефа Луи Гей-Люссака.
Математическое выражение закона Гей-Люссака:
В том случае, когда известно состояние газа при постоянном давлении и двух разных температурах, закон допустимо записывать таким образом:
По итогам химических реакций атомы не исчезают и не возникают. В результате таких процессов происходит их перегруппировка. Количество атомов до реакции и после ее протекания не меняется, что отличает их от молекул. Данное условие учитывают, расставляя стехиометрические коэффициенты в уравнениях химических реакций.
Коэффициенты в уравнениях реакций демонстрируют числа объемов газов, которые реагируют и образовываются. К примеру, 2 объема водорода и 1 объем кислорода дают 2 объема пара воды:
2 H 2 + O 2 = 2 H 2 O
V ( Н 2 ) : V ( N 2 ) : V ( N H 3 ) = 3 : 2 : 1
С другой стороны, данные соотношения справедливы лишь в случае веществ, которые участвуют в одной и той же химической реакции. Когда реагент принимает участие в двух параллельных реакциях, его химические количества в данных процессах не связаны и могут принимать любые значения.
n — количество газа.
Выразить молярный объем газов можно в л/моль:
В данной таблице использованы следующие обозначения:
Молярный объём
Моля́рный объём — объём одного моля вещества, величина, получающаяся от деления молярной массы на плотность. Характеризует плотность упаковки молекул.
Значение NA = 6,022…×10 23 называется числом Авогадро в честь итальянского химика Амедео Авогадро. Это универсальная постоянная для мельчайших частиц любого вещества.
Именно такое количество молекул содержит 1 моль кислорода О2, такое же количество атомов в 1 моле железа (Fe), молекул в 1 моле воды H2O и т. д.
Значения молярного объёма химических элементов
| Группа | I A | II A | III B | IV B | V B | VI B | VII B | VIII B | VIII B | VIII B | I B | II B | III A | IV A | V A | VI A | VII A | VIII A |
| Период | ||||||||||||||||||
| 1 | H 14,1 | He 31,8 | ||||||||||||||||
| 2 | Li 13,1 | Be 5 | B 4,6 | C 5,3 | N 17,3 | O 14 | F 17,1 | Ne 16,8 | ||||||||||
| 3 | Na 23,7 | Mg 14 | Al 10 | Si 12,1 | P 17 | S 15,5 | Cl 18,7 | Ar 24,2 | ||||||||||
| 4 | K 45,3 | Ca 29,9 | Sc 15 | Ti 10,6 | V 8,35 | Cr 7,23 | Mn 7,39 | Fe 7,1 | Co 6,7 | Ni 6,6 | Cu 7,1 | Zn 9,2 | Ga 11,8 | Ge 13,6 | As 13,1 | Se 16,5 | Br 23,5 | Kr 32,2 |
| 5 | Rb 55,9 | Sr 33,7 | Y 19,8 | Zr 14,1 | Nb 10,8 | Mo 9,4 | Tc 8,5 | Ru 8,3 | Rh 8,3 | Pd 8,9 | Ag 10,3 | Cd 13,1 | In 15,7 | Sn 16,3 | Sb 18,4 | Te 20,5 | I 25,7 | Xe 42,9 |
| 6 | Cs 70 | Ba 39 | * | Hf 13,6 | Ta 10,9 | W 9,53 | Re 8,85 | Os 8,43 | Ir 8,54 | Pt 9,1 | Au 10,2 | Hg 14,8 | Tl 17,2 | Pb 18,3 | Bi 21,3 | Po 22,7 | At н/д | Rn н/д |
| 7 | Fr н/д | Ra 45 | ** | Rf н/д | Db н/д | Sg н/д | Bh н/д | Hs н/д | Mt н/д | Ds н/д | Rg н/д | Cn н/д | Uut н/д | Fl н/д | Uup н/д | Lv н/д | Uus н/д | Uuo н/д |
| Лантаноиды | * | La 22,5 | Ce 21 | Pr 20,8 | Nd 20,6 | Pm 19,96 | Sm 19,9 | Eu 28,9 | Gd 19,9 | Tb 19,2 | Dy 19 | Ho 18,7 | Er 18,4 | Tm 18,1 | Yb 24,8 | Lu 17,8 | ||
| Актиноиды | ** | Ac 22,54 | Th 19,8 | Pa 15 | U 12,5 | Np 21,1 | Pu 12,12 | Am 20,8 | Cm 18,28 | Bk н/д | Cf н/д | Es н/д | Fm н/д | Md н/д | No н/д | Lr н/д |
См. также
Примечания
Полезное
Смотреть что такое «Молярный объём» в других словарях:
молярный объём — molio tūris statusas T sritis fizika atitikmenys: angl. gram molecular volume; molal volume; molar volume vok. Molvolumen, n rus. мольный объём, m; молярный объём, m pranc. volume molaire, m … Fizikos terminų žodynas
молярный объём газа — dujų molio tūris statusas T sritis fizika atitikmenys: angl. gas molar volume vok. molares Gasvolumen, n rus. мольный объём газа, m; молярный объём газа, m pranc. volume molaire de gaz, m … Fizikos terminų žodynas
Объём — У этого термина существуют и другие значения, см. Объём (значения). Объём Размерность L3 Единицы измерения СИ … Википедия
Молярный объем — Молярный объём объём одного моля вещества, величина, получающаяся от деления молярной массы на плотность. Характеризует плотность упаковки молекул. Согласно закону Авогадро, для любого газа при нормальных условиях эта величина имеет универсальное … Википедия
мольный объём — molio tūris statusas T sritis fizika atitikmenys: angl. gram molecular volume; molal volume; molar volume vok. Molvolumen, n rus. мольный объём, m; молярный объём, m pranc. volume molaire, m … Fizikos terminų žodynas
мольный объём газа — dujų molio tūris statusas T sritis fizika atitikmenys: angl. gas molar volume vok. molares Gasvolumen, n rus. мольный объём газа, m; молярный объём газа, m pranc. volume molaire de gaz, m … Fizikos terminų žodynas
Число Авогадро — Число Авогадро, константа Авогадро физическая константа, численно равная количеству специфицированных структурных единиц (атомов, молекул, ионов, электронов или любых других частиц) в 1 моле вещества. Определяется как количество атомов в 12 … Википедия
Уравнение Ван-дер-Ваальса — Уравнение состояния Стат … Википедия
Объём
Объём — количественная характеристика пространства, занимаемого телом или веществом. Объём тела или вместимость сосуда определяется его формой и линейными размерами. С понятием объёма тесно связано понятие вместимость, то есть объём внутреннего пространства сосуда, упаковочного ящика и т. п. Синонимом вместимости частично является ёмкость, но словом ёмкость обозначают также сосуды и качественную характеристику конденсаторов.
Принятые единицы измерения — в СИ и производных от неё — кубический метр, кубический сантиметр, литр (кубический дециметр) и т. д. Внесистемные — галлон, баррель.
Слово «объём» также используют в переносном значении для обозначения общего количества или текущей величины. Например, «объём спроса», «объём памяти», «объём работ». В изобразительном искусстве объёмом называется иллюзорная передача пространственных характеристик изображаемого предмета художественными методами.
Содержание
Вычисление объёма
Математически
В общем случае математически объём тела вычисляется по следующей интегральной формуле:

где 
Для ряда тел с простой формой более удобным является использование специальных формул. Например, объём куба с длиной стороны, равной a, равен 
Через плотность
Объём находится по формуле:
Единицы объёма жидкости
Английские внесистемные
Американские внесистемные
Античные внесистемные
Древнееврейские
Русские внесистемные
Единицы сыпучих веществ
Английские внесистемные
Русские внесистемные
Молярный объём
Vm — величина, равная отношению объёма V системы (тела) к её количеству вещества n:
Молярный объем для газов при нормальных условиях: Vm = 22,4 л/моль
Прочие единицы измерения
Примечания
Литература
Полезное
Смотреть что такое «Объём» в других словарях:
объём — объём, а … Русский орфографический словарь
объём — объём … Словарь употребления буквы Ё
объём — объём/ … Морфемно-орфографический словарь
объём — сущ., м., употр. сравн. часто Морфология: (нет) чего? объёма, чему? объёму, (вижу) что? объём, чем? объёмом, о чём? об объёме; мн. что? объёмы, (нет) чего? объёмов, чему? объёмам, (вижу) что? объёмы, чем? объёмами, о чём? об объёмах 1. В… … Толковый словарь Дмитриева
объём — а; м. 1. Величина чего л. в длину, высоту и ширину, измеряемая в кубических единицах. О. геометрического тела. О. куба, цилиндра. О. здания. О. полтора кубометра. В объёме (в трёх измерениях; объёмно). 2. Содержание чего л. с точки зрения… … Энциклопедический словарь
объём — объём, объёмы, объёма, объёмов, объёму, объёмам, объём, объёмы, объёмом, объёмами, объёме, объёмах (Источник: «Полная акцентуированная парадигма по А. А. Зализняку») … Формы слов
ОБЪЁМ — ОБЪЁМ, а, муж. 1. Величина чего н. в длину, высоту и ширину, измеряемая в кубических единицах. О. пирамиды. О. здания. 2. Вообще величина, количество. Большой о. работ. О. информации. О. знаний. | прил. объёмный, ая, ое (к 1 знач.). Объёмное… … Толковый словарь Ожегова
объём — ОБЪЁМ1, а, м Величина или вместимость предмета, определяемая произведением длины, высоты и ширины и измеряемая в кубических единицах. Объем бассейна в новой школе составляет 300 кубических метров. ОБЪЁМ2, а, м Количество или величина чего л.… … Толковый словарь русских существительных
ОБЪЁМ — ОБЪЁМ, мера части пространства, занимаемого телом. Единицей измерения служит объём единичного куба … Современная энциклопедия
объ — объ. Пишется вм. (об) перед е, ю, я, напр. объехать, объявить.Примечание. Вм. этой приставки и следующей за ней буквы и пишется обы, напр. обыграть. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
объ… — Пишется вместо об… перед е, ю, я, напр. объехать, объявить. Примечание. вместо этой приставки и следующей за ней буквы и пишется обы, напр. обыграть. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова