Нейтропения у взрослых после химиотерапии что это
Инфекционные осложнения, лейкопения и нейтропения
Инфекционные осложнения, лейкопения и нейтропения
Инфекции вызываются ростом различных микроорганизмов, например, бактерий, вирусов или грибов, внутри человеческого организма. Инфекции могут начинаться в любом органе, но наиболее часто они возникают в тех частях организма, которые тесно соприкасаются с внешней средой, например в коже, слизистых оболочках пищеварительного тракта (полость рта, пищевод, кишечник), дыхательных путей (гортань, трахея, бронхи, легкие) и органах мочеполовой системы. В норме организм защищен от большинства возбудителей инфекционных заболеваний иммунной системой, которая способна эффективно уничтожать микроорганизмы.
Однако в период проведения противоопухолевой терапии возможно нарушение функционирования иммунной системы – такие методы лечения, как лучевая терапия, химиотерапия, а также некоторые «таргетные» препараты способны повреждать костный мозг, в котором образуются клетки, необходимые для функционирования иммунной системы – лейкоциты. Выделяют множество форм лейкоцитов, к наиболее важным из них относятся нейтрофилы – клетки, играющие главную роль в сопротивляемости организма при «столкновении» с возбудителями бактериальных инфекций. Плохое питание, недостаток сна и стресс также ослабляют иммунную систему.
Степень выраженности угнетения функции иммунной системы отражает количество нейтрофилов в крови. В норме их количество превышает 2,0*10^9 клеток на 1 литр крови (также можно встретить обозначение 2000 клеток на 1 мкл) Снижение их количества обозначают термином «нейтропения». В зависимости от выраженности нейтропении выделяют следующие степени её тяжести:
К характерным симптомам инфекции относятся: лихорадка (повышение температуры до 38 oC и выше), появление кашля или боли в горле, диарея, боль в ушах или в области пазух носа, кожная сыпь, появление боли при мочеиспускании или изменение цвета мочи, выделения из половых путей и т.д. Обязательно проконсультируйтесь со своим лечащим врачом в случае возникновения вышеперечисленных симптомов.
Стоит учитывать, что прием некоторых лекарственных препаратов, например нестероидных противовоспалительных средств, таких, как парацетамол, аспирин, ибупрофен, а также глюкокортикостероидов (дексаметазон, метилпреднизолон, преднизолон и т.д.) может снижать температуру тела и маскировать другие симптомы инфекции. Это может привести к тяжелым последствиям, обязательно сообщите вашему лечащему врачу, если вы принимали или принимаете постоянно эти или другие препараты с аналогичным механизмом действия.
Для диагностики нейтропении используется общий (клинический) анализ крови, кровь для анализа забирается из пальца или из вены. В случае, если подозревается развитие инфекции, в зависимости от её клинической картины проводятся дополнительные методы обследования, например, анализ мочи, кала, рентгенография легких, УЗИ брюшной полости и т.д.
Инфекционные осложнения и «фебрильная» нейтропения у онкологических пациентов являются опасными и потенциально жизнеугрожающими осложнениями. Пациентам, получающим противоопухолевое лечение, рекомендуется регулярно (например, 1 раз в неделю) контролировать показатели общего анализа крови, рекомендуется всегда иметь при себе антибактериальные препараты. Обратитесь к врачу за получением дополнительной информации.
Что я могу сделать для того, чтобы предотвратить развитие инфекции?
Ваш лечащий врач даст вам рекомендации по необходимым мерам предосторожности в процессе лечения, например следующие:
Лечение и профилактика нейтропении
В случае, если нейтропения в процессе лечения развивается снова и снова, или в процессе проведения терапии отмечалось развитие инфекционных осложнений Ваш врач может принять решение о снижении (редукции) доз противоопухолевых препаратов. Уменьшение дозы противоопухолевых препаратов снижает их негативное влияние на процессы кроветворения и во многих случаях позволяет предотвратить развитие нейтропении.
В клиническую практику внедрены также т.н. «гранулоцитарные колониестимулирующие факторы (Г-КСФ)», например филграстим, пэг-филграстим и т.д. Г-КСФ способствует процессам образования клеток иммунной системы в костном мозге.
Как правило, Г-КСФ вводятся через 24-72 часа после химиотерапии подкожно или внутривенно. Их применение позволяет эффективно поддерживать количество нейтрофилов и лейкоцитов в крови и проводить более агрессивную химиотерапию. Большинство пациентов делают себе эти уколы самостоятельно, наиболее удобным является введение под кожу живота. В сети Интернет опубликовано множество обучающих материалов по технике их выполнения (например). Обсудите со своим лечащим врачом целесообразность применения Г-КСФ в вашем индивидуальном случае.
ВНИМАНИЕ! Инфекционные осложнения, возникающие в ходе проведения противоопухолевого лечения, могут представлять собой непосредственную угрозу для жизни. Не занимайтесь самолечением, обратитесь к врачу.
Нейтропения у взрослых после химиотерапии что это
ФГБУ “Онкологический научный центр им. Н.Н. Блохина” РАМН, Москва
Одним из наиболее частых и опасных побочных эффектов цитостатической терапии
является нейтропения. Цитостатики, действуя на быстроделящиеся клетки, затрагивают и систему кроветворения. Циркулирующие нейтрофилы живут в среднем 6–9 часов, и система гемопоэза постоянно вырабатывает около 50 млн этих клеток в 1 минуту для замещения выбывших. Снижение
продукции нейтрофилов после воздействия химиопрепаратов приводит к быстрому уменьшению содержания этих клеток в периферической крови, что повышает риск развития инфекционных осложнений.
Длительная нейтропения зачастую не позволяет проводить химиотерапию (ХТ) в запланированные сроки, заставляет редуцировать дозы цитостатиков, что в свою очередь снижает эффективность противоопухолевого лечения. Кроме того, инфекционные осложнения на фоне нейтропении в
отсутствие адекватной терапии характеризуются стремительным течением и высокой летальностью. В связи с этим существует необходимость тщательной оценки миелотоксического потенциала современных режимов химиотерапии и выявления групп больных с высоким риском развития нейтропении, которым требуется профилактическое назначение колониестимулирующих факторов (КСФ).
Повышенный риск развития инфекции на фоне нейтропении обусловил выделение симптомокомплекса
“фебрильная нейтропения” (ФН). Согласно руководству NCCN (National Comprehensive Cancer Network) [1], ФН характеризуется повышением температуры в ротовой полости выше 38,5 °С при однократном измерении или выше 38,0 °С при двух последовательных измерениях в течение 2 часов при абсолютном числе нейтрофилов (АЧН) в крови менее 0,5 × 109/л или ожидаемом снижении 10 дней или ФН
после ХТ; вовлечение в опухолевый процесс костного мозга; лучевая терапия в анамнезе; недавно перенесенное оперативное вмешательство; наличие раневого процесса; плохой соматический статус пациента; нарушение функции печени и почек; пневмония; присоединившаяся грибковая инфекция.
Риск развития инфекционных осложнений у больных нейтропенией обусловлен не только уменьшением АЧН, но и нарушением функциональных свойств нейтрофилов (ослабление хемотаксиса и фагоцитоза; нарушение экзогенной продукции ростовых факторов, таких как интерлейкин-1,
интерлейкин-3, гранулоцитарно-макрофагального КСФ, Г-КСФ; изменение активности ферментов; снижение образования активных форм кислорода).
Оценка риска развития ФН должна проводиться перед каждым курсом ХТ. Если пациент в течение предыдущего цикла ХТ перенес эпизод ФН или дозолимитирующей нейтропенической инфекции и проводимая ХТ направлена на выздоровление, проведение последующих курсов ХТ в прежних дозах влечет за собой “высокий риск” развития ФН. В таких случаях необходимо рассмотреть вопрос об использовании КСФ. Если пациент перенес эпизод ФН, несмотря на использование КСФ, NCCN рекомендует провести редукцию доз химиопрепаратов во время последующих циклов или изменить
режим ХТ.
Эти рекомендации основаны на результатах крупных рандомизированных исследований, показавших, что риск развития ФН может быть значи-тельно снижен благодаря проведению первичной профилактики с использованием КСФ.
Vogel и соавт. [4] в двойном слепом рандомизированном плацебо-контролируемом многоцентровом
исследовании установили, что при первом и всех последующих циклах ХТ профилактическое назначение КСФ (пегилированный филграстим) значительно снижает риск развития ФН при режимах ХТ, которые прежде ассоциировались с “высоким риском” этого осложнения. В исследование
были включены больные РМЖ, получавшие доцетаксел 100 мг/м2 каждые 3 недели. Пациентки были распределены в 2 группы: 1-я группа (465 жен-щин) получала инъекции плацебо; 2-я группа (463 женщины) – пегфилграстим подкожно (вводился через 24 часа после завершения цикла ХТ). В группе
плацебо частота развития ФН составила 17 %, в группе пегфилграстима – 1 %. Потребность в госпитализации уменьшилась с 14 до 1%, а в использовании внутривенной антибактериальной терапии (АБТ) – с 10 до 2 % (p 50·× 109/л Граноген следует немедленно отменять.
Успех лечения ФН во многом зависит от раннего распознавания возможной инфекции и раннего начала терапии. Нейтропения значительно ослабляет иммунный ответ организма, что не позволяет развиваться характерным клиническим проявлениям инфекции, затрудняя ее клиническую диагностику у онкологических больных. Гипертермия у пациентов с нейтропенией часто бывает единственным
признаком инфекционного процесса.
Согласно клиническим рекомендациям ESMO, необходимо проводить тщательные первичный осмотр и
обследование на выявление возможных очагов инфекции [8]:
1. Наличие длительно стоящего центрального венозного катетера.
2. Симптомы и признаки наличия инфекции дыхательной системы, сердечно-сосудистой системы,
желудочно-кишечного тракта, кожных покровов, мочеполовой системы, центральной нервной системы.
3. Данные о предшествующих положительных результатах микробиологического анализа.
4. Рутинные лабораторные и инструментальные исследования:
• общий и биохимический анализы крови, коагулограмма, С-реактивный белок;
• посев крови (минимум 2 раза), включая посев из центрального венозного катетера; микроскопическое исследование и посев мочи;
• микроскопическое исследование мокроты и ее посев;
• микроскопическое исследование кала и его посев (при диарее);
• исследование очагов инфекции на коже (аспират, биопсия, мазок);
• рентгенография органов грудной клетки.
5. Дальнейшие исследования (при длительной и глубокой нейтропении): компьютерная томография органов грудной клетки (если лихорадка сохраняется, несмотря на адекватную АБТ, более 72 часов).
Немедленный подсчет формулы крови для установления числа нейтрофилов параллельно с другими исследованиями, представленными выше, имеют ключевое значение для определения необходимости начала ранней терапии ФН.
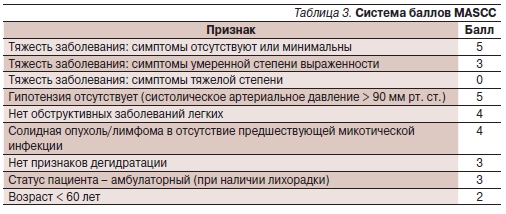
Международной ассоциацией поддерживающей терапии при раке (MASCC) разработан прогностический индекс [9, 10]. Он позволяет быстро оценивать риск осложнений – до того, как станет известно содержание нейтрофилов в крови пациента. Эффективность данного метода подтверждена во многих проспективных исследованиях.
Критерии индекса MASCC представлены в табл. 3.
Показателем “низкого риска” осложнений является сумма баллов > 21. Частота серьезных осложнений при этом не превышает 6 %, а смертность – 1 %. При сумме баллов
1. Crawford J, Althaus D, et al. National Comprehensive Cancer Network. Myeloid growth factors clinical practice guidelines in oncology. J Nat Compreh Cancer Network 2005;3:540–55.
2. ASCO Recommendations for the use of hematopoietic colony-stimulating factors: evidencebased,
clinical practice guidelines. J Clin Oncol 1994;12:2471–250.
3. Zielinski CC, Awada A, Cameron DA, et al. The impact of new European Organisation for Research and Treatment of Cancer guidelines on the use of granulocyte colony-stimulating factor on the management of breast cancer patients. Eur J Cancer 2008;44: 353–65.
4. Vogel CL, Wojtukiewicz MZ, Carroll RR, et al. First and subsequent cycle use of pegfilgrastim prevents febrile neutropenia in patients with breast cancer: a multicenter, double-blind, placebo-controlled phase III study. J Clin Oncol2005;23:1178–84.
5. Timmer-Bonte JN, de Boo TM, Smith HJ, et al. Prevention of chemotherapyinduced febrile neutropenia by prophylactic antibiotics plus or minus granulocyte colony-stimulating factor in small cell lung cancer: a Dutch randomized phase III study. J Clin Oncol 2005;23:7974–84.
6. Yoshida M, Ohno R. Antimicrobial prophylaxis in febrile neutropenia. Clin Infect Dis 2004;39 (1):65–7.
7. Cullen M, Steven N, Billingham L, et al. Antibacterial prophylaxis after chemotherapy for solid tumours and lymphomas. N Engl J Med 2005;353:988–98.
8. Минимальные клинические рекомендации Европейского общества медицинской онкологии (ESMO). М., 2010. C. 375–91.
9. Klastersky J, Paesmans M, Rubenstein E B et al. The Multinational Association for Supportive Care in Cancer risk index: a multinational scoring system for identifying low-risk febrile neutropenic cancer patients. J Clin Oncol 2000; 18:3038–51.
10. Innes H, Lim SL, Hall A, et al. Management of febrile neutropenia in solid tumours and lymphomas
using the Multinational Association for Supportive Care in Cancer (MASCC) risk index: feasibility and safety in routine clinical practice. Supp Care Cancer 2008;16:485–491.
11. Vidal L, Paul M, Ben Dor I, et al. Oral versus intravenous antibiotic treatment for febrile neutropenia
in cancer patients: a systematic review and meta-analysis of randomized trials. J Antimicrob Chemother 2004;54:29–37.
12. Kovacs J, Masour H. Evolving health effects of Pneumocystis: one hundred years of progress of diagnosis and treatment. JAMA 2009;301:2578–85.
13. 13 Wolf H-H, Leithauser M, Maschmeyer G, et al. Central venous catheter-related infections in hematology and oncology. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol 2008;87:863–76.
14. Raad I, Kassar R, Dany G, et al. Management of the catheter in documented catheterrelated coagulase-negative staphylococcal bacteremia: remove or retain? Clin Infect Dis 2009;49:1187–194.
15. Kim SH, Kang CI, Kim HB, et al. Outcomes of hickman catheter salvage in febrile neutropenic cancer patients with Staphylococcus aureus bacteremia. Infect Control Hosp Epidemiol 2003;24:897–904.
16. Walsh TJ, Teppler H, Donowitz GR, et al. Caspofungin versus liposomal amphotericin B for empirical antifungal therapy in patients with persistent fever and neutropenia. N Engl J Med 2004;351:1391–402.
17. Herbrecht R, Denning DW, Patterson TF, et al. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N Engl J Med 2002;347:408–15.
18. Dockrell DH. Salvage therapy for invasive aspergillosis. J Antimicrob Chemother 2008;61:41–4.
19. Schmutzhard E, Williams KJ, Vukmirovits G, et al. A randomised comparison of meropenem with cefotaxime or ceftriaxone for the treatment of bacterial meningitis in adults. Meropenem Meningitis Study Group. J Antimicrob Chemother 1995;36:85–97.
Нейтропения
Нейтрофилы – это самая многочисленная группа гранулоцитов, основной функцией которых является фагоцитоз (уничтожение) патогенной флоры в организме человека.
Нейтропения – это уменьшение количества нейтрофилов в крови, что приводит к риску возникновения бактериальных и грибковых инфекций.
В здоровом состоянии защиту иммунных «границ» предоставляют зрелые сегментоядерные нейтрофилы. Помогают «контролировать» ситуацию и более молодые – палочкоядерные нейтрофилы, но их намного меньше (это хорошо видно по результату анализа крови, где в норме зрелых нейтрофилов насчитывается от 42-72%, а молодых всего от 1-6%).
Но, в случае возникновения тех или других заболеваний, соотношение всех видов нейтрофилов (сегментоядерных, палочкоядерных, миелоцитов, метамиелоцитов) резко нарушается, что приводит к патологическому повышению нейтрофилов или их уменьшению (нейтропении).
При этом количество нейтрофилов в крови человека — не стабильно, в отличие от других клеточных групп лейкоцитарной формулы. На созревание, развитие и нормальное соотношения данных гранулоцитов, влияют не только врожденные, приобретенные патологии, но и резкое эмоциональное потрясение, стресс нарушение рациона питания и т.д.
Нейтропения у детей должна быть тщательным образом исследована, чтобы предотвратить как тяжелые патологии, так и радикальное лечение без серьезных на то причин.
Классификация степеней тяжести нейтропении:
Если уровень нейтрофилов критически снижается – это приводит к развитию инфекции в кишечнике, во рту, вызывая тем самым расстройство пищеварительной системы, гингивиты, стоматиты, грибковые поражения кожи и т.д.
Тяжелая нейтропения при наличии онкопатологии крайне неблагоприятно влияет на работу иммунной системы, приводя к прогрессирующим воспалениям и инфекциям, вплоть до летального исхода.
Этиология
Нейтрофилы развиваются в костном мозге в течение 15 дней, находятся в кровеносном русле около 8 часов, составляют подавляющую клеточную часть лейкоцитарной формулы и при обнаружении «вредителей» тут же отправляются на их ликвидацию.
Основные причины нейтропении, которые нарушают данный физиологический процесс:
Нейтропения у детей, также может развиться в связи с нарушением работы поджелудочной железы и заторможенным умственным развитием (синдром Швахмана-Даймонда-Оски).
Нейтропения разделяется на:
Острая нейтропения развивается стремительно на фоне быстрого потребления/разрушения нейтрофилов, хроническая — из-за сокращения выработки гранулоцитов или же избыточной селезеночной секреции.
Первичная нейтропения связанная с внутренними нарушениями (врожденные патологии, идиопатическая нейтропения, циклическая нейтропения, доброкачественная этническая), вторичная — обусловлена влиянием внешних факторов на созревание и развитие клеток костного мозга.
Вторичная нейтропения
Вторичная нейтропения чаще всего развивается вследствие:
Вторичная нейтропения провоцирует патологии:
В случае с вторичной нейтропенией лечить нужно не «анализ» крови, а пациента с конкретными симптоматическими проявлениями.
Первичную и вторичную нейтропению стоит различать, так как в первом случае понижение уровня нейтрофилов – это единственное проявление, тогда как вторичные развиваются на основе инфекций, системных аутоиммунных патологий и онко неоплазий.
Клинические проявления
В большинстве случае нейтропения протекает без каких-либо признаков. Симптомы снижения нейтрофилов обычно возникают только тогда, если развилась вторичная нейтропения, на фоне тех или других патологий.
Общая симптоматика нейтропении:
В результате резкого понижения гранулоцитов, также может развиться фебрильная нейтропения. Это лихорадочное состояние отягощенное тахикардией, тремором, ознобом, повышением АД, вплоть до развития сердечно-сосудистого коллапса.
Фебрильная нейтропения обычно развивается вследствие онкопатологий, воздействия лучевой или химиотерапии, в виде гиперергической реакции организма на токсические влияния (цитостатиков, распад здоровых и онкоклеток).
Может проявляться и на фоне тяжелого инфекционного процесса, который провоцируют стафилококки, стрептококки, клостридии, реже грибки и вирусы. В более редких случаях фебрильная нейтропения может развиться на основе первичной аутоиммунной нейтропении.
Диагностика
Диагностика может быть плановой, внеплановой (при наличии специфической симптоматики), а также может проводиться при наличии каких-либо подозрений у лечащего врача (необычные или часто повторяющиеся инфекции).
Плановое исследование крови у детей до 1 года проводится 1 раз в 3 месяца, после года – 1 раз в 6 месяцев (включая взрослых).
Если диагностика засвидетельствовала понижение нейтрофилов в крови, дополнительно должно быть назначено:
Далее проводится оценка динамики показателей лейкоцитарной формулы (после перенесенных инфекций, между ними, после выздоровления), включая СОЭ (скорость оседания эритроцитов), цветовой показатель и т.д.
Определение причины нейтропении может включать такие диагностические манипуляции:
В случае тяжелой нейтропении в острой форме — комплексная диагностика должна быть выполнена максимально оперативно.
Если рассматривается врожденная патология, диагностика включает молекулярно-генетическое исследование нейтропении.
По одному анализу крови, который показал низкий уровень гранулоцитов, невозможно поставить окончательный диагноза. Так как это единственные клетки крови, концентрация которых может меняться ежедневно, ввиду короткой «жизни» в кровяном русле (6-8 часов).
Для точного подтверждения состояния пациента, анализ крови нужно повторить с небольшим интервалом времени (время сдачи анализов устанавливает врач).
Лечение
Интермиттирующая нейтропения обычно проходит без симптомов и тяжелых инфекционных осложнений, поэтому в терапевтическом лечении не нуждается. Особенно в том случае, если пациент тщательно соблюдает правила личной гигиены, употребляет в пищу продукты, которые прошли термическую обработку (блюда из сырой рыбы, мясо с кровью при нейтропении нельзя), пользуется перчатками во время уборки, защищает кожу от длительного воздействия солнца.
При вторичной нейтропении лечение направлено, в первую очередь, на ликвидацию основного заболевания, которое и повлекло за собой патологическое снижение гранулоцитов.
В «Клинике Спиженко» лечение нейтропении проводится с учетом причины возникновения и клинических симптомов и может включать:
Включая лечение ассоциированных состояний (язвы, стоматит, гингивит) с помощью полосканий солевым раствором ротовой полости, применения антисептиков (хлоргексидина), нистатина, клотримазола, флуконазола (при кандидозах).
При острых поражениях слизистых, дополнительно назначается диета (с преобладанием в рационе жидкой пищи) и местное обезболивание. Если снижение нейтрофилов произошло в результате приема лекарственных средств, выход из ситуации – прекратить их использование и перейти на альтернативное лечение.
Включая анальгетики (Ибупрофен, Индометацин, Амидопирин, Ацетилсалициловая кислота, Фенилбутазон).
Лечение фебрильной нейтропении
Фебрильная нейтропения требует незамедлительного медицинского вмешательства (в течение 1 часа!).
При нейтропенической лихорадке назначается:
Основа современного антибактериального лечения ФН (фебрильной нейтропении) — бета-лактамные антибиотики.
В «Клинике Спиженко» вы сможете пройти комплексное исследование нейтропении, установить точную причину и получить наиболее корректное лечение (при необходимости).
Нейтропения – это не «приговор», но и не повод оставлять данную ситуацию без компетентного медицинского внимания.
Заполните всего три поля
и наш специалист Вам перезвонит!
Ваши данные успешно отправлены! Ожидайте нашего звонка.
Фебрильная нейтропения у онкологических больных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Российский онкологический научный центр им. Н.Н. Блохина РАМН
О нкологические больные являются группой риска в отношении развития инфекционных заболеваний. Гнойно–воспалительные осложнения у них развиваются значительно чаще, чем у пациентов, не страдающих опухолевыми заболеваниями. Риск возникновения инфекции зависит от нозологической формы онкологического заболевания и ряда предрасполагающих факторов.
Больные гемобластозами, получающие иммуносупрессивную терапию, перенесшие трансплантацию костного мозга и имеющие глубокую и длительную гранулоцитопению, а также дефект системы фагоцитоза и нарушения клеточного и/или гуморального иммунитета, имеют наибольший риск развития инфекционных осложнений [3,4,6,7].
Больные солидными опухолями в основном не имеют выраженной иммуносупрессии. Однако они также предрасположены к инфекции вследствие обструкции естественных пассажей (бронхиальные пути, мочевыводящий тракт, желчные пути, желудочно–кишечный тракт), повреждения анатомических барьеров (поверхности кожи и слизистых) в результате химиотерапии или лучевой терапии, дисфункции ЦНС, а также наличия катетеров, шунтов, протезов и пр. [8].
Гранулоцитопения вследствие цитостатической терапии у больных солидными опухолями, как правило, является непродолжительной и не сопровождается развитием серьезных инфекционных осложнений в отличие от больных гемобластозами. Несмотря на то, что глубина и длительность нейтропении является наиболее важным фактором в отношении развития инфекций (чем длительнее и глубже нейтропения, тем выше риск инфекции), тем не менее немаловажное значение имеют интенсивность режимов цитостатической терапии и сопутствующие заболевания (табл. 1 и 2). Совокупность факторов, обусловливающих риск возникновения инфекции, позволяет отнести больного в группу «высокого» или «низкого» риска развития инфекции [4,5 ].
Под нейтропенией подразумевается количество нейтрофилов ниже 500 клеток /мм 3 или менее 1000 кл/мм 3 с ожидаемым их снижением ниже 500 кл/мм 3 [4].
Классически инфекции подразделяются на три стандартных группы: микробиологически подтвержденная инфекция с или без инфекций кровотока, клинически подтвержденная инфекция и лихорадка неясного генеза (FUO) [4,5].
Клинически подтвержденной считается инфекция даже в том случае, если из найденного очага инфекции микробиологического подтверждения получено не было, что встречается в 20–30% случаев фебрильных эпизодов у больных гемобластозами в состоянии нейтропении. Микробиологически подтвержденная инфекция встречается более, чем в 30% случаев ФН. При этом бактериемия обнаруживается в трети случаев и в 88% случаев вызывается единственным микроорганизмом, чаще (78%) грамположительными кокками [1,4].
На основании анализа 1049 эпизодов нейтропении у больных гемабластозами (EORTC– IATCG) было установлено, что основными очагами инфекции являются инфекции кровотока (34%), инфекции ротовой полости и гортаноглотки (22%), респираторного тракта (в основном пневмонии – 13%, при этом синуситы составили только (1%), кожи и мягких тканей (13%), ЖКТ (7%), инфекции внутрисосудистых катетеров и флебиты (5%), мочевыводящей системы (3%), прочие – 2%. Очаг инфекции не был найден в 56% случаев [4]. Представленные данные в целом соответствуют результатам, полученным в клинике РОНЦ им. Н.Н.Блохина РАМН при анализе 260 случаев ФН у детей, больных острыми миело– и лимфобластными лейкозами (табл. 3) [1].
Лихорадка развивается у большинства пациентов, страдающих гемобластозами, и может быть связана с основным заболеванием или быть следствием цитостатической терапии.
Показанием для начала антибиотикотерапии у больных с нейтропенией согласно рекомендациям Общества, изучающего инфекции у иммунодепрессивных больных (Consensus Guidelines of the Immunocompromised Host Society (IHS), является температура во рту свыше 38,5°С, измеренная однократно, или свыше 38°C, измеренная двукратно или более раз за период более 12 часов. Рабочий комитет Общества инфекционных заболеваний Америки (Working Committee of Infectious Diseases Society of America) считает, что достаточно однократного повышения оральной температуры свыше 38,3°С или повышения температуры свыше 38°С двукратно за одночасовой период. Следует помнить, что в условиях нейтропении классические признаки воспаления могут отсутствовать и лихорадка является единственным признаком инфекционного процесса. Однако неинфекционная лихорадка может быть не связана с инфекций, а быть следствием наличия злокачественной опухоли, химиотерапии, реакцией на переливание крови, антибиотикотерапию, колониестимулирующие факторы или проявлением аллергии. Однако у больных в состоянии нейтропении лихорадка чаще всего бывает признаком инфекции. Иногда инфекция (например, вызванная Clostridium septicum) может развиться и в отсутствие лихорадки вследствие иммунологического дефицита [4].
У больных с ФН группы высокого риска инфекции, имеющих глубокую длительную нейтропению, эмпирическая антимикробная терапия показана при первых признаках инфекции или при повышении температуры, согласно описанным выше критериям. До разработки концепции эмпирической антибиотикотерапии инфекция в присутствии геморрагического синдрома или без него была причиной смерти 50–80% больных лейкозами и 50% больных солидными опухолями в состоянии нейтропении [4,5].
Выбор антимикробных агентов должен быть основан на знании чувствительности наиболее вероятных возбудителей инфекции у этой категории больных. Учитываться должны также и местные эпидемиологические факторы [1,8].
Перед началом терапии ФН следует определить пациента в группу высокого или низкого риска инфекции, а также понять необходимость включения ванкомицина в первоначальную терапию.
Показаниями для назначения ванкомицина являются наличие большого количества метициллинрезистентных стафилококков или пенициллинрезистентных стрептококков или энтерококков в конкретном стационаре, клинически подтвержденная катетер–ассоциированная инфекция или тяжелые мукозиты. Монотерапия ванкомицином не проводится.
Для лечения ФН взрослым больным с низким риском инфекции показана пероральная терапия ципрофлоксацином в комбинации с амоксициллин/клавулановой кислотой. В случае невозможности пероральной терапии больному следует назначить монотерапию цефалоспоринами 3–4 поколений (цефтазидим или цефепим) или карбапенемами. Комбинированная терапия у этой группы пациентов проводится с использованием цефтриаксона и амикацина [4,5].
У больных с высоким риском инфекции может быть назначена монотерапия одним из следующих препаратов: цефепим или цефтазидим, имипенем или меропенем. При назначениии комбинаций используют аминогликозиды (амикацин) плюс антипсевдомонадные пенициллины (пиперациллин/тазобактам), или цефалоспорины (цефепим или цефтазидим) или карбапенемы (меропенем). При показаниях к назначению ванкомицина его следует комбинировать с цефепимом или цефтазидимом с (или без) аминогликозидами, или карбапенемами с (или без) аминогликозидами или антипсевдомонадными пенициллинами с аминогликозидами (табл. 4) [4,9,10].
При наличии эзофагитов необходимо добавление ацикловира (HSV инфекция). При наличии инфильтратов в легких показано эмпирическое назначение амфотерицина Б. При подозрении на инфицирование Pneumocystis carinii следует назначать сульфаметоксазол/триметоприм (TMP–SMX). Азолы (флуконазол) используются профилактически в тяжелых случаях у иммунодефицитных больных. Так, флуконазол (400 мг/день) предотвращал инфекцию, вызванную Candida albicans, C.tropicalis, но не C.krusei и C.glabrata [4,10].
Оценка эффекта терапии через 3 суток
А. Лихорадка отсутствует
– При оценке эффекта терапии через 3–5 дней в случае негативных бактериологических анализов, нормализации температуры и повышения числа нейтрофилов выше 500/мм 3 не следует продолжать введение антибиотиков широкого спектра дольше 5– 7 дней, так как это может привести к суперинфекции резистентными или оппортунистическими микроорганизмами. При клинически или микробиологически доказанной инфекции антибиотикотерапию следует продолжить.
В отношении прекращения антибактериальной терапии с исчезновением лихорадки мнения экспертов расходятся: предлагается или прекратить антибиотикотерапию (с последующим возобновлением в случае рецидива лихорадки), или продолжать антибактериальную терапию до соответствующего повышения числа нейтрофилов.
Б. Лихорадка сохраняется
– Если при сохранении лихорадки состояние пациента остается стабильным, то выбранная схема антибактериальной терапии сохраняется до 5–7 дня. При повышении числа нейтрофилов свыше 500 кл/мм 3 антибиотикотерапия прекращается или продолжается при наличии клинически или микробиологически подтвержденной инфекции. При числе нейтрофилов ниже 500 кл/мм 3 при клинически подтвержденной инфекции или лихорадке неясного генеза следует эмпирически добавлять ванкомицин, аминогликозиды и/или амфотерицин Б. При наличии микробиологически подтвержденной инфекции – изменение терапии согласно результатам антибиотикограммы.
– Если состояние больного при существующей лихорадке не стабильно, то при клинически доказанной инфекции или лихорадке неясного генеза следует добавлять ванкомицин, аминогликозиды и/или амфотерицин Б. При наличии микробиологически подтвержденной инфекции следует менять или добавлять в схемы антибиотики исходя из результатов антибиотикограммы [5,6,9].
В проведенном нами исследовании при лечении 260 эпизодов ФН у детей больных острым лимфобластным лейкозом (ОЛЛ) и острым миелобластным лейкозом (ОМЛ) активность полусинтетических пенициллинов, цефалоспоринов и карбапенемов составила соответственно 63%, 57% и 60% для больных ОЛЛ и несколько ниже – 40%, 31%, 33% для больных ОМЛ [1]. Среди больных, не ответивших на терапию, дополнительное назначение ванкомицина было эффективно у 28% и 52% больных ОЛЛ и ОМЛ. Использование амфотерицина Б в качестве третьей линии терапии было эффективно почти у всех оставшихся больных (табл. 5).
При лечении ФН, особенно в группе больных высокого риска инфекции, следует помнить о возможном инфицировании герпес–вирусами, респираторными вирусами, вирусами гепатитов. Должны быть проведены соответствующие исследования с последующей терапией [1]. При исследовании уровня инфицированности вирусами Эпштейн–Барра и герпес–вирусом 6 типа, а также ЦМВ у детей с острыми лейкозами было установлено, что 100% детей инфицированы ВЭБ и ГВ–6 типа. 76% детей имели повышенные или высокие титры антител, 24% детей имели выраженные клинические симптомы вирусной инфекции. Лечение ганцикловиром было эффективно во всех случаях. Инфицированность ЦМВ составила 5% [1,11].
Если при лечении больных с ФН одновременно используются препараты с одинаковой токсичностью в отношении почек, то кумулятивная токсичность будет превосходить токсичность каждого из используемых препаратов. Поэтому для лечения следует использовать высокоочищенные и наименее токсичные препараты. Так, применение хроматографически очищенного ванкомицина является наиболее целесообразным. Амикацин является наиболее активным среди прочих аминогликозидов, нетилмицин – менее нефротоксичным. Гентамицин, сизомицин, тобрамицин почти потеряли свою активность во многих клиниках. Использование качественного амфотерицина Б позволит снизить общий токсический эффект комбинаций.
В течение последних двух десятилетий большое внимание уделяется гемопоэтическим цитокинам – гранулоцитарному и гранулоцитарно–макрофагальному колониестимулирующим факторам (G–CSF и GM–CSF), которые применяются с целью укорочения длительности нейтропении у онкологических больных с высоким риском инфекции. Оба фактора широко используются онкологами в следующих случаях: при первичной профилактике в течение первого курса химиотерапии для предотвращения инфекционных осложнений, связанных с нейтропенией, если риск фебрильной нейтропении выше 40%; для вторичной профилактики в течение последующих курсов химиотерапии при наличии фебрильной нейтропении в течение первого курса химиотерапии с целью уменьшения числа инфекционных осложнений и сохранения нужной интенсивности химиотерапии; после трансплантации стволовых клеток костного мозга с целью усиления гемопоэза. Полезность назначения гемопоэтических факторов была подтверждена многочисленными исследованиями [2,4,9].
Таким образом, проблема лечения ФН онкологических больных требует тщательного контроля со стороны как онкологов, так и клинических микробиологов. Тщательный микробиологический мониторинг позволит применять рациональную антимикробную терапию в этой группе больных.
1. Методические рекомендации «Профилактика и лечение фебрильных нейтропений у детей с острыми лейкозами». Иванова Л.Ф., Багирова Н.С., Дмитриева Н.В. Утв. МЗ РФ 2002г. Москва. РОНЦ им. Н.Н.Блохина РАМН.
2. American Society Clin Oncol Recommmendations for the Use of Hematopoietic Colony–Stimulating Factors: evidance–based clinical practice guidelines. J Clin Oncol 1994; 12: 2471–508
3. Bodey et al. Quantitative relationships between circulating leukocytes and infection in patients with acute leukemia. Ann Intern Med 1966, 61,328.
4. Glauser MP and Pizzo PA «Management of Infections in Immunocompromised Patients». W.B.Saunders Comp Ltd. 2000, 473p.
5. Hughes WT et al. «2002 Guidelines for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer». CID 2002, 34 (15 March).
6. Finberg RW, Talcott JA. Fever and neutropenia. How to use a new treatment strategy. N.Eng J Med.1999, 341,362–363.
7. Pizzo PA Fever in immunosuppressed patients. N Eng J Med 1999, 341, 893–900
8. Scevola D. La profilassi antibiotica nella practica chirurgica e medica, Ed.Micom, 1998, 128p.
9. The textbook of Febrile Neutripenia. Ed:Rolston K.V.I. and Rubienstein E.B. 2001, Martin Dunitz. 341p.
10. Viscoli C. The evolution of the empirical management of fever and neutropenia in cancer patients. J Antimicrob Chemother, 1998, 41 (Suppl D), 65–80.WOOd MJ.