Немногочисленные очаги глиоза что это
Глиоз
Общие сведения
Глиоз головного мозга представляет собой патологический процесс, проявляющийся замещением нейронов глиальными элементами. Глиоз не является самостоятельным заболеванием, скорее это защитная реакция на гибель нейронов, то есть вторичный процесс. При этом, процесс разрушения нейронов стимулирует заполнение глиальными клетками образовавшихся пустот, что приводит к изменению количественного соотношение элементов нервной ткани.
Ткань мозга состоит из совокупности нейронов, эпендимальной мембраны и глиальных клеток. В норме глиальная ткань ответственна за трофическую/секреторную функции и обмен веществ в клетках мозга, а также выполняет функцию защиты нейронов. На ее долю приходится около 40% от общей массы мозга. Разрастание глиальных клеток образует очаги глиоза в белом веществе головного мозга, которые в зависимости от этиологии первичного заболевания могут иметь очаговый/диффузный характер. Располагаться очаги глиоза могут в любой области (структурах) головного мозга. И чем в большем объеме образуются глии, тем менее эффективно функционирует ЦНС. При большом разрастании глии может образовываться кистозно-глиозный атрофированный участок ткани головного мозга. Чем в большем объеме в белом веществе образуются глии — тем хуже работает вся нервная система. Образуется кистозно-глиозно-атрофический участок.
Статистических данных о встречаемости различных видов глиоза нет. Можно лишь отметить, что наиболее часто встречаются супратенториальные очаги глиоза.
Супратенториальные очаги —что это такое? Супратенториальные — это очаги глиоза сосудистого происхождения. Различные патологические процессы в сосудах головного мозга (тромбоз, фиброз, некроз), вызывающие расстройство процесса кровообращения способствуют образованию мелких гипер/гипертензивных участков, которые сопровождаются такими расстройствами как плохая координация, головокружения, изменение почерка.
Единичные очаги глиоза
Для очагового глиоза характерны единичные четко ограниченные островки в белом веществе, размер и расположение которых определяется причинами гибели нейронов. Встречаются у лиц любого возраста и, может быть, как проявлением естественных возрастных дегенеративных процессов в тканях мозга, ишемии церебральных структур, локального воспалительного процесса, хронической гипертонии, процесса демиелинизации, так и следствием травм в родах у младенцев. Обычно единичные (ограниченные очаги) глиоза головного мозга являются случайной находкой на КТ/МРТ, поскольку в большинстве случаев они клинически не проявляются и дискомфорта не приносят, за исключением их локализации в лобной доле, где расположены центры, ассоциирующиеся с чувствами и ощущениями, что может проявляться появлением галлюцинаций. Единичный глиоз головного мозга не склонен к разрастанию.
Множественные очаги глиоза
Появление множественных очагов глиоза обусловлено травмами и острыми/хроническими нарушения кровообращения мозга, то есть, сосудистого генеза. По мере развития патологии/заболевания, взывающих гибель нейронов происходит увеличение как количества, так и размера измененных участков. Возникают преимущественно на фоне выраженного атеросклероза, инсульта, инфаркта мозга, при сдавлении сосудов мозга и в результате возрастных изменений. Множественные очаги глиоза в своем большинстве усиливают клиническую симптоматику основного заболевания и вызывают нарушение функции ЦНС.
Патогенез
Патогенез формирования участков глиоза чрезвычайно разнообразный и определяется непосредственно заболеванием, лежащим в основе этого патологического процесса.
Классификация
В основе классификации — характер разрастания глиальных клеток и их локализация.
По морфологическим признакам выделяются:
По локализации патологического процесса выделяют:
По количественному признаку выделяют единичные и множественные очаги глиоза. Гистологически выделяют гиподенсные (без определенной структуры, не поддаются окрашиванию) и гиперинтенсивные (четко структурированы, хорошо окрашиваются) участки глиоза.
По характеру процесса/распространенности выделяют:
Причины
В основе патологического процесса замещения нейронов клетками нейроглии могут лежать самые разнообразные причины:
Симптомы
Клиническая симптоматика варьирует в широких пределах, и определяется преимущественно симптоматикой основного заболевания, вызвавшего глиоз. Как правило, единичные очаги глиоза небольшого размера специфической нейро-симптоматики не дают и обнаруживаются случайно при обследовании головного мозга на МРТ. В тоже время, множественные (обширные) очаги глиоза практически всегда манифестируют нейро-симптоматикой в виде:
Клинические симптомы во многом определяются локализацией очага глиоза:
Локализация очагов глиоза в лобных долях чаще обусловлена возрастными изменениями. Принято считать, что, если заболеваний, способных вызывать гибель нейронов и размножение глиальных клеток не выявлено, то такой процесс следует считать первичной патологией, развивающейся по мере старения организма и манифестирующего нарушением концентрации, внимания, памяти, расстройствами мелкой моторики, замедлением реакций.
Анализы и диагностика
В основе диагностики — методы визуализации (МРТ/КТ) головного мозга. Эти методы позволяют определить:
На снимке ниже показаны множественные очаги глиоза.
МРТ позволяет установить не только факт наличия участков глиозных изменений, но и выявить причину. Снимки МРТ дают четкое представление о наличии зон в мозге, которые не получают достаточного питания из-за нарушения проходимости сосудов атеросклеротическими бляшками; позволяют определить воспалительные процессы, участки гематомы, выявить новообразования. Это в определенной степени позволяет устранить провоцирующий фактор и выработать тактику минимизации рисков дальнейшего распространения процесса.
Лечение
Поскольку замещение нейронов очагами глиоза является необратимым процессом, то соответственно, патологический процесс не лечится. Основным направлением терапевтического воздействия является лечение основного заболевания, провоцирующего этот процесс (гипертоническая болезнь, сахарный диабет, атеросклероз, посттравматические осложнения и др.).
В тоже время, при выраженной нейро-симптоматике, рекомендуется назначение лекарственных средств (индивидуально в зависимости от симптомов), направленных на улучшение проводимости нервных волокон, укрепление стенок кровеносных сосудов и улучшение их эластичности, повышение активности мозга и улучшение когнитивных функций.
С целью оптимизации метаболизма головного мозга/мозгового кровообращения назначаются Инстенон, Кавинтон, Галидор, Трентал. Эффективно назначение ноотропов, усиливающих устойчивость ЦНС к действию неблагоприятных факторов (Ноотропил, Пирацетам, Фезам, Семакс, Глицин). Показаны лекарственные средства, купирующие процесс агрегации тромбоцитов и укрепляющие стенки сосудов (Аскорутин, Тромбо АСС, Плавикс, Тиклид, Курантил, витаминные комплексы).
С целью нормализации кратковременной памяти, ориентации в пространстве, купирования поведенческих расстройств может назначаться экстракт листьев Гинкго билоба или Танакан. Для улучшения внимания/памяти пациентам с когнитивными расстройствами, в основе которых сосудистая церебральная патология показано введение в больших дозах таких препаратов как Церебролизин, Кортексин. При нейроинфекциях назначаются антибактериальные препараты/противовирусные препараты в зависимости от патогена, вызвавшего нейроинфекцию. При выраженных головных болях — анальгетики (Кетанов, Анальгин и др.)
Пациенты должны постоянно контролировать массу тела/АД, соблюдать низкокалорийную витаминизированную диету, делать оздоровительную гимнастику, поддерживать двигательную/интеллектуальную активность (чтение, заучивание стихотворений, просмотр телевизионных передач, общение с друзьями/близкими, прослушивание музыки, изучение языков и др.).
PsyAndNeuro.ru
Взаимодействие нейрон-глия в патогенезе эпилепсии
Со времен Гиппократа эпилепсия являлась устрашающей болезнью, которая также ассоциировалась с одержимостью. Однако с момента появления электроэнцефалографии (ЭЭГ) в 1929 году данное заболевание обрело патофизиологическое объяснение в виде появления гиперсинхронных импульсов очага нейронов в центральной нервной системе (ЦНС). Согласно современному международному стандарту, для того, чтобы поставить диагноз эпилепсии, требуется наличие как минимум 2 эпизодов неспровоцированных судорог с интервалом более 24 часов, или 1 эпизода вместе с вероятностью дальнейших припадков, рассчитываемой по риску рецидива после двух неспровоцированных припадков, происходящих в течение следующих 10 лет, или верифицированный диагноз эпилептического синдрома.
Открытие фенобарбитала в 1912 году стало отправной точкой в лечении эпилепсии: препарат был эффективен у 2/3 больных. Однако оставшаяся треть оставалась резистентной к лечению, что дало повод исследовать патогенез эпилепсии: изучение гиперсинхронности и изменений в активности нейронов. Активность нейронов регулируется нейромедиаторами, их обменом, биохимией и связью с ионными каналами. Были попытки привязать эпилепсию к поломке определенного гена, однако в основном заболевание является полигенным.
Были описаны различные биологические изменения в ЦНС, участвующие при эпилептогенезе: глиоз, избыточное воспаление, нарушение проницаемости гематоэнцефалического барьера (ГЭБ), нейродегенерация, аберрантный нейрогенез, аксональная и дендритная пластичность, изменения в нейрональной цепи, структурно-функциональные изменения рецепторов ионных каналов, реорганизация экстрацеллюлярного матрикса и др. Однако надо понимать, что ранее исследователи изучали в основном нейрональную активность и вклад нейронов в эпилептогенез. Далее мы более подробно обсудим некоторые из этих факторов, обсуждая вклад глии и ее влияния на нейроны в процессе патогенеза припадков.
Глиоз
Плотная фиброзная ткань глии, которая образуется в ответ на повреждение ЦНС, называется глиозным рубцом или глиозом. Данный рубец является одним из основных признаков хронической очаговой эпилепсии. При глиозе астроциты и микроглия приобретают патологический вид: гипертрофия клеток и их отростков, увеличение экспрессии белков (виментин, GFAP, CD68), увеличение клеточной пролиферации, а также формирование вязкого межклеточного вещества, богатого хондроитинсульфатом. Такая изменённая глия может влиять на окружающие ее клетки, выбрасывая в пространство цитокины, хемокины, ростовые факторы. До определённого момента такая реакция является адаптационной, однако в дальнейшем воспаление приводит к разрушению нервной ткани.
Вопрос о том, является ли глиоз причиной судорог, остается спорным. Лучшим доказательством связи между глиозом и эпилепсией являются исследования, в которых глиоз был спровоцирован делецией гена интегрина β1 в астроцитах. У животных, подвергшихся эксперименту, были отмечены спонтанные рецидивирующие припадки. Более того астроцит-специфическая делеция гена туберозного склероза Tsc1 вызывает дезорганизацию нервной ткани в виде астроглиоза, что также сопровождается припадками. При болезни Александера, одним из основных симптомов которой являются судороги, присутствует мутация гена GFAP в астроцитах. Данные примеры объясняются тем, что пораженные астроциты в недостаточном количестве вырабатывают глутаматные транспортеры, что ведет к эксайтотоксичности, гибели нейронов и припадкам. Однако есть исследования, не подтверждающие связи глиоза и эпилепсии. К примеру, в одном исследовании резецировали ткани пациентов с очаговой кортикальной дисплазией, где не было найдено глиоза в участках неповрежденной эпилептогенной коры.
Во всяком случае, роль глиоза в патогенезе эпилепсии остается значимой.
Ионный и водный гомеостаз
Активность нейронов зависит от работы Na + и К + каналов. Так как межклеточное вещество (МКВ) в головном мозге очень мало по объему, данные каналы не допускают чрезмерного тока ионов и жидкости в него. Так, например, регуляция калия в МКВ регулируется Na/K-АТФазой, которая обеспечивает отток избыточного калия из МКВ в астроциты.
Предполагают, что нарушения в работе калиевого буфера могут приводить к припадкам. Доказать это можно исследованиями, где потеря гена K ir 4.1, ответственного за экспрессию калиевых каналов, приводила к приобретенной эпилепсии у животных.
Также стоит вспомнить хлор и его ингибирующее действие на рецепторы ГАМК типа А. За транспорт хлора ответственны 2 транспортера: Na/K/Cl и K/Cl. Потеря функции последнего тесно связана с возникновением эпилепсии у людей. Глутамат является одним из факторов влияния на экспрессию и функцию данного транспортера. Избыточное количество глутамата, выделяющегося во время припадка, активирует NMDA рецепторы, что приводит к дефосфорилированию и уменьшению экспрессии K/Cl насоса. При этом отток хлора из клетки уменьшается, что приводит к гипервозбудимости ГАМК рецептора. Тут стоить отметить, что астроциты играют важную роль в регуляции количества глутамата: при повреждении астроцитов повышенное количество глутамата и дизрегуляция ГАМК рецептора приведет к судорогам.
Также активность нейронов связана с током жидкости, который обеспечен белками аквапоринами (АКП). АКП4 экспрессируется на поверхности отростков астроцитов, которые находятся непосредственно у кровеносных сосудов. Изменения в экспрессии данного гена наблюдались в исследованиях у животных, и людей. Также полагают, что АКП4 связан с обменом калия воздействуя на K ir 4.1.
Нейромедиаторы
Увеличенное количество внеклеточного глутамата является маркером эпилептически пораженной ткани и причиной судорог.
Одна из важнейших функций астроцитов в ЦНС – удаление излишек глутамата из МКВ, что обеспечивается двумя Na-зависимыми транспортерами (ЕААТ1 и ЕААТ2). При попадании глутамата в клетку происходит его деградация при помощи дегидрогеназы в альфа-кетоглутарат, вступая затем в цикл Кребса и обеспечивая клетку энергией. Оставшаяся превалирующая часть глутамата при помощи глутамин-синтетазы превращается в глутамин. Далее глутамин выделяется в МКВ, где захватывается нейронами и вступает в глутамат-глутаминовый цикл. В возбужденных нейронах глутамат из данного цикла пакуется в везикулы для дальнейшего выброса, в то время как в ГАМК-ергических тормозных нейронах глутамат переводится в ГАМК. При глиозе астроцитов данная физиологическая цепочка становится патологической, что было продемонстрировано на мышиной модели вирус-индуцированного астроглиоза. В пораженных астроцитах уменьшилось количество глутамин-синтетазы, что уменьшало поставку глутамина для тормозных ГАМК-ергических нейронов, что привело к гипервозбудимости нейронов. В итоге возникали эпилептогенные очаги и припадки.
Последние исследования действительно показывают, что роль глии в патогенезе эпилепсии важна. Однако остается еще множество вопросов, как именно происходит взаимодействие глии и нейронов, и что является первичным: возникновение эпилептогенного очага при разрушенной глии, или разрушенная глия вследствие эпилептогенных нейронов.
Данный перевод является обзорным. Для получения более углубленной информации рекомендуется перейти к оригиналу:
Источник: Patel, D. C., Tewari, B. P., Chaunsali, L., & Sontheimer, H. (2019). Neuron–glia interactions in the pathophysiology of epilepsy. Nature Reviews Neuroscience. doi:10.1038/s41583-019-0126-4
Дифференциальная диагностика поражений белого вещества головного мозга при магнитно-резонансной томографии
Врач МРТ
Воронцова Жанна Ватиславовна
Дифференциально-диагностический ряд заболеваний белого вещества является очень длинным. Выявленные с помощью МРТ очаги могут отражать нормальные возрастные изменения, но большинство очагов в белом веществе возникают в течение жизни и в результате гипоксии и ишемии.
ПРИ КАКИХ БОЛЕЗНЯХ ВОЗНИКАЮТ ОЧАГИ
В БЕЛОМ ВЕЩЕСТВЕ?
Очаговые изменения сосудистого генеза
Воспалительные заболевания
Заболевания инфекционной природы
Интоксикации и метаболические расстройства
Травматические процессы
Врожденные заболевания
Могут наблюдаться в норме
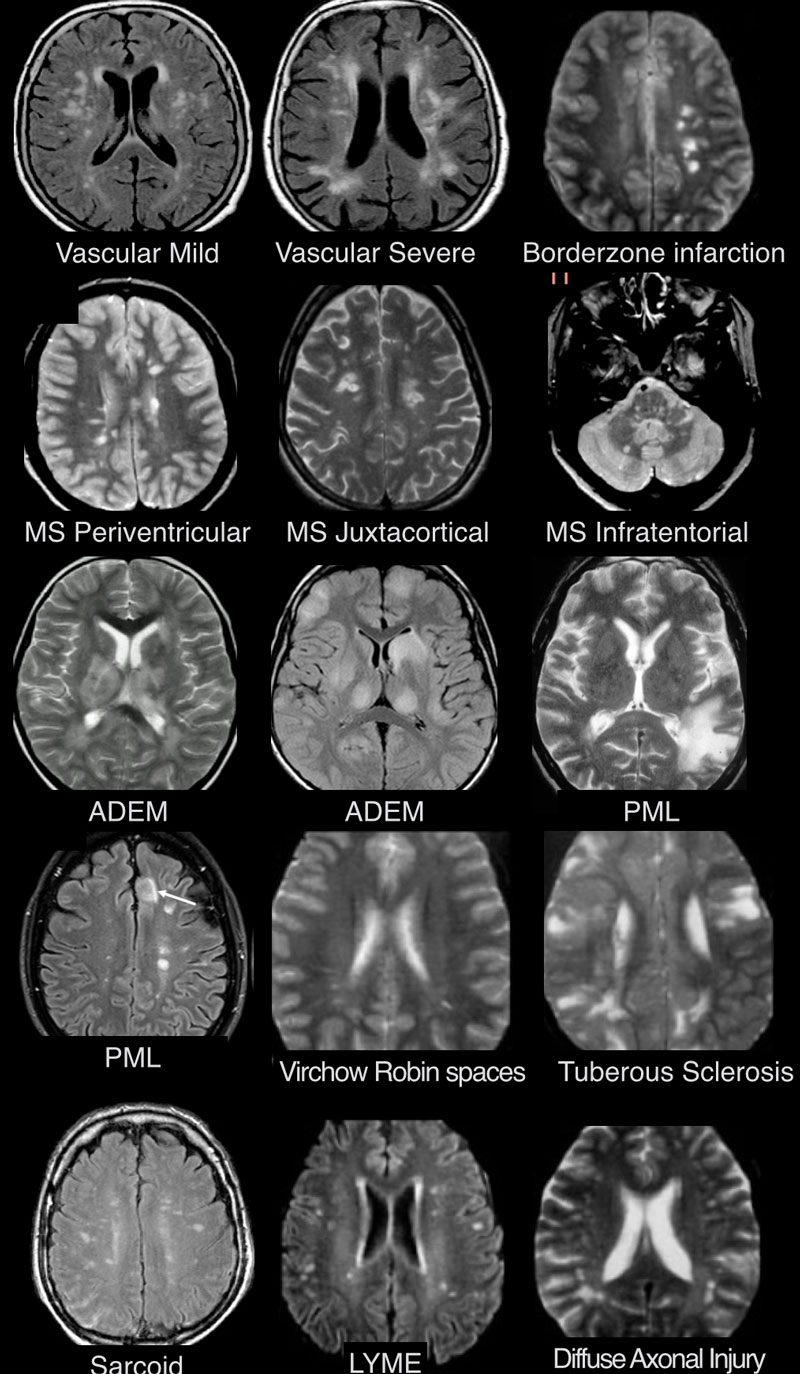
МРТ ГОЛОВНОГО МОЗГА: МНОЖЕСТВЕННЫЕ ОЧАГОВЫЕ ИЗМЕНЕНИЯ
На изображениях определяются множественные точечные и «пятнистые» очаги (некоторые из них будут рассмотрены более детально).
Рассеянный склероз — хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга, характеризующееся многоочаговостью поражения белого вещества центральной нервной системы, ремиттирующе-прогредиентным течением, вариабельностью неврологических симптомов и преимущественным поражением лиц молодого возраста (подробнее с диагностическими критериями указанного заболевания Вы можете ознакомится в статье «Современные критерии диагностики рассеянного склероза», опубликованной на нашем сайте).
Острые нарушения мозгового кровообращения:
Острый диссеминированный энцефаломиелит (ОДЭМ)
Саркоидоз головного мозга
Прогрессирующая мультфокальная лейкоэнцефалопатия (ПМЛ)
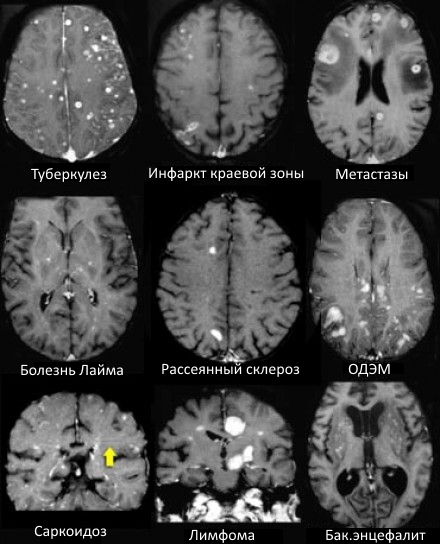
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА МНОЖЕСТВЕННЫХ ОЧАГОВ, УСИЛИВАЮЩИХСЯ ПРИ КОНТРАСТИРОВАНИИ
На МР-томограммах продемонстрированы множественные патологические зоны, накапливающие контрастное веществ (некоторые из них описаны далее подробнее).
Острые нарушения мозгового кровобращения
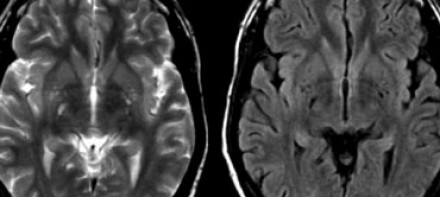
ПЕРИВАСКУЛЯРНЫЕ ПРОСТРАНСТВА ВИРХОВА-РОБИНА
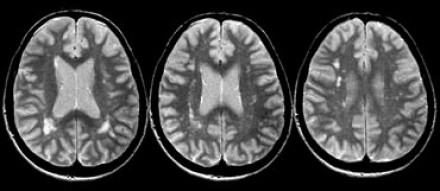
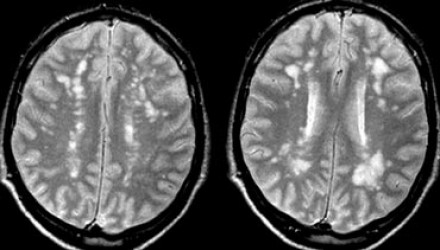
Слева на Т2-взвешенной томограмме видны множественные очаги высокой интенсивности в области базальных ганглиев. Справа в режиме FLAIR сигнал от них подавляется, и они выглядят темными. На всех остальных последовательностях они характеризуются такими же характеристиками сигнала, как ликвор (в частности, гипоинтенсивным сигналом на Т1 ВИ). Такая интенсивность сигнала в сочетании с локализацией описанного процесса являются типичными признаками пространств Вирхова-Робина (они же криблюры).
Пространства Вирхова-Робина окружают пенетрирующие лептоменингеальные сосуды, содержат ликвор. Их типичной локализацией считается область базальных ганглиев, характерно также расположение вблизи передней комиссуры и в центре мозгового ствола. На МРТ сигнал от пространств Вирхова-Робина на всех последовательностях аналогичен сигналу от ликвора. В режиме FLAIR и на томограммах, взвешенных по протонной плотности, они дают гипоинтенсивный сигнал в отличие от очагов иного характера. Пространства Вирхова-Робина имеют небольшие размеры, за исключением передней комиссуры, где периваскулярные пространства могут быть больше.
На МР-томограмме можно обнаружить как расширенные периваскулярные пространства Вирхова-Робина, так и диффузные гиперинтенсивные участки в белом веществе. Данная МР-томограмма превосходно иллюстрирует различия между пространствами Вирхова-Робина и поражениями белого вещества. В данном случае изменения выражены в значительной степени; для их описания иногда используется термин «ситовидное состояние» (etat crible).
Пространства Вирхова-Робина увеличиваются с возрастом, а также при гипертонической болезни в результате атрофического процесса в окружающей ткани мозга.
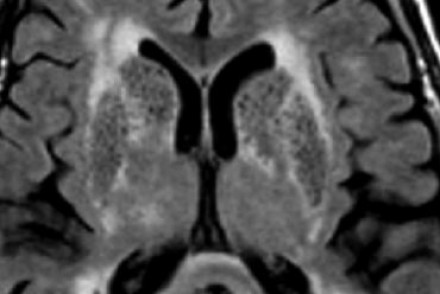
НОРМАЛЬНЫЕ ВОЗРАСТНЫЕ ИЗМЕНЕНИЯ
БЕЛОГО ВЕЩЕСТВА НА МРТ
К ожидаемым возрастным изменениям относятся:
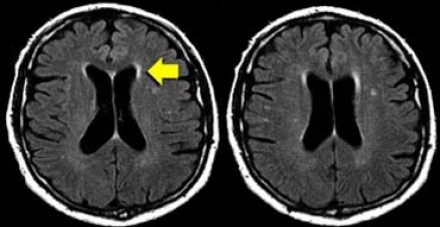
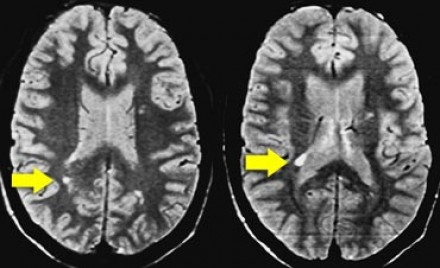
Перивентрикулярные «шапочки» представляют собой области, дающие гиперинтенсивный сигнал, расположенные вокруг передних и задних рогов боковых желудочков, обусловленные побледнением миелина и расширением периваскулярных пространств. Перивентрикулярные «полосы» или «ободки» это тонкие участки линейной формы, расположенные параллельно телам боковых желудочков, обусловленные субэпендимальным глиозом.
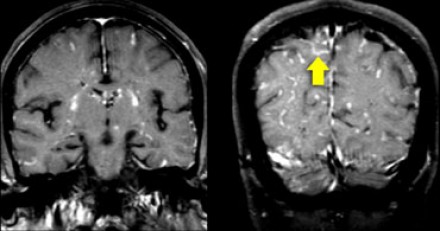
На магнитно-резонансных томограммах продемонстрирована нормальная возрастная картина: расширение борозд, перивентрикулярные «шапочки» (желтая стрелка), «полосы» и точечные очажки в глубоком белом веществе.
Клиническое значение возрастных изменений мозга недостаточно хорошо освещено. Тем не менее, имеется связь между очагами и некоторыми факторами риска возникновения цереброваскулярных расстройств. Одним из самых значительных факторов риска является гипертония, особенно, у пожилых людей.
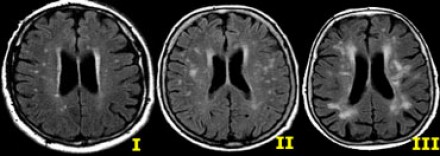
Степень вовлечения белого вещества в соответствии со шкалой Fazekas:
ДИСЦИРКУЛЯТОРНАЯ ЭНЦЕФАЛОПАТИЯ НА МРТ
Очаговые изменения белого вещества сосудистого генеза — самая частая МРТ-находка у пациентов пожилого возраста. Они возникают в связи с нарушениями циркуляции крови по мелким сосудам, что является причиной хронических гипоксических/дистрофических процессов в мозговой ткани.
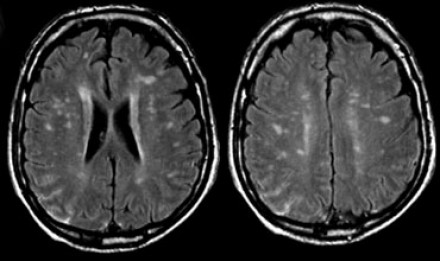
На серии МР-томограмм: множественные гиперинтенсивные участки в белом веществе головного мозга у пациента, страдающего гипертонической болезнью.
На МР-томограммах, представленных выше, визуализируются нарушения МР-сигнала в глубоких отделах больших полушарий. Важно отметить, что они не являются юкставентрикулярными, юкстакортикальными и не локализуются в области мозолистого тела. В отличие от рассеянного склероза, они не затрагивают желудочки мозга или кору. Учитывая, что вероятность развития гипоксически-ишемических поражений априори выше, можно сделать заключение о том, что представленные очаги, вероятнее, имеют сосудистое происхождение.
Только при наличии клинической симптоматики, непосредственно указывающей на воспалительное, инфекционное или иное заболевание, а также токсическую энцефалопатию, становится возможным рассматривать очаговые изменения белого вещества в связи с этими состояниями. Подозрение на рассеянный склероз у пациента с подобными нарушениями на МРТ, но без клинических признаков, признается необоснованным.
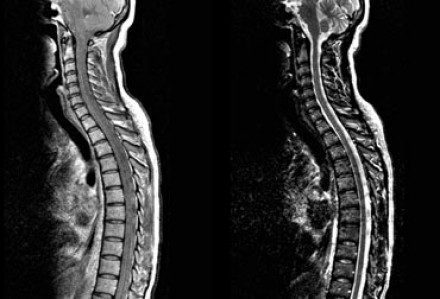
На представленных МР-томограммах патологических участков в спинном мозге не выявлено.
У пациентов, страдающих васкулитами или ишемическими заболеваниями, спинной мозг обычно не изменен, в то время как у пациентов с рассеянным склерозом в более чем 90% случаев обнаруживаются патологические нарушения в спинном мозге. Если дифференциальная диагностика очагов сосудистого характера и рассеянного склероза затруднительна, например, у пожилых пациентов с подозрением на РС, может быть полезна МРТ спинного мозга.
Вернемся снова к первому случаю: на МР-томограммах выявлены очаговые изменения, и сейчас они гораздо более очевидны. Имеет место распространенное вовлечение глубоких отделов полушарий, однако дугообразные волокна и мозолистое тело остаются интактными. Нарушения ишемического характера в белом веществе могут проявляться как лакунарные инфаркты, инфаркты пограничной зоны или диффузные гиперинтенсивные зоны в глубоком белом веществе.
Лакунарные инфаркты возникают в результате склероза артериол или мелких пенетерирующих медуллярных артерий. Инфаркты пограничной зоны возникают в результате атеросклероза более крупных сосудов, например, при каротидной обструкции или вследствие гипоперфузии.
Структурные нарушения артерий головного мозга по типу атеросклероза наблюдаются у 50% пациентов старше 50 лет. Они также могут обнаруживаться и у пациентов с нормальным артериальным давлением, однако более характерны для гипертоников.
САРКОИДОЗ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
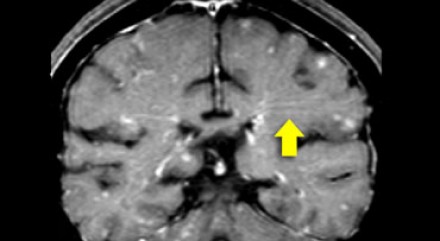
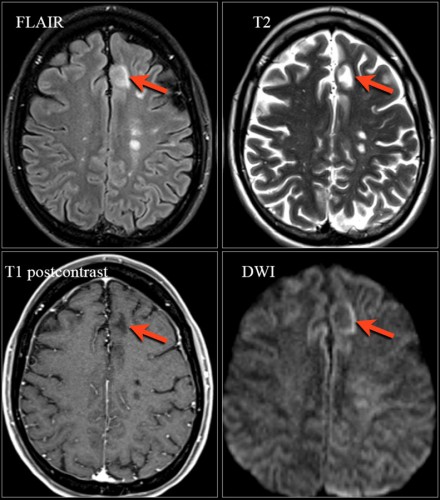
На Т1 взвешенных томограммах с контрастным усилением препаратами гадолиния, выполненных этому же пациенту, что и в предыдущем случае, визуализируются точечные участки накопления контраста в базальных ядрах. Подобные участки наблюдаются при саркоидозе, а также могут быть обнаружены при системной красной волчанке и других васкулитах. Типичным для саркоидоза в этом случае считается лептоменингеальное контрастное усиление (желтая стрелка), которое происходит в результате гранулематозного воспаления мягкой и паутинной оболочки.
Еще одним типичным проявлением в этом же случае является линейное контрастное усиление (желтая стрелка). Оно возникает в результате воспаления вокруг пространств Вирхова-Робина, а также считается одной из форм лептоменингеального контрастного усиления. Таким образом объясняется, почему при саркоидозе патологические зоны имеют схожее распределение с рассеянным склерозом: в пространствах Вирхова-Робина проходят мелкие пенетрирующие вены, которые поражаются при РС.
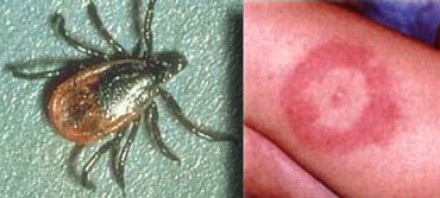
БОЛЕЗНЬ ЛАЙМА (БОРРЕЛИОЗ)
На фотографии справа: типичный вид сыпи на коже, возникающей при укусе клеща (слева) — переносчика спирохет.
Болезнь Лайма, или боррелиоз, вызывают спирохеты (Borrelia Burgdorferi), переносчиком инфекции являются клещи, заражение происходит трансмиссивным путем (при присасывании клеща). В первую очередь при боррелиозе на возникает кожная сыпь. Через несколько месяцев спирохеты могут инфицировать ЦНС, в результате чего появляются патологические участки в белом веществе, напоминающие таковые при рассеянном склерозе. Клинически болезнь Лайма проявляется острой симптоматикой со стороны ЦНС (в том числе, парезами и параличами), а в некоторых случаях может возникать поперечный миелит.
Ключевой признак болезни Лайма — это наличие мелких очажков размером 2-3 мм, симулирующих картину рассеянного склероза, у пациента с кожной сыпью и гриппоподобным синдромом. К другим признакам относится гиперинтенсивный сигнал от спинного мозга и контрастное усиление седьмой пары черепно-мозговых нервов (корневая входная зона).
ПРОГРЕССИРУЮЩАЯ МУЛЬТИФОКАЛЬНАЯ ЛЕЙКОЭНЦЕФАЛОПАТИЯ, ОБУСЛОВЛЕННАЯ ПРИЕМОМ НАТАЛИЗУМАБА
Относительно редкий, но в то же время серьезный побочный эффект приема этого препарата — повышение риска развития ПМЛ. Диагноз ПМЛ основывается на клинических проявлениях, обнаружении ДНК вируса в ЦНС (в частности, в цереброспинальной жидкости), и на данных методов визуализации, в частности, МРТ.
По сравнению с пациентами, у которых ПМЛ обусловлен другими причинами, например, ВИЧ, изменения на МРТ при ПМЛ, связанной с приемом натализумаба, могут быть описаны как однородные и с наличием флюктуации.
Ключевые диагностические признаки при этой форме ПМЛ:
На МРТ видны признаки ПМЛ, обусловленной приемом натализумаба. Изображения любезно предоставлены Bénédicte Quivron, Ла-Лувьер, Бельгия.
Дифференциальная диагностика между прогрессирующим РС и ПМЛ, обусловленной приемом натализумаба, может быть достаточно сложной. Для натализумаб-ассоциированной ПМЛ характерны следующие нарушения:
Дифференциальная диагностика РС и ПМЛ