Некомпактный миокард что это такое
Синдром некомпактного миокарда (НМ) левого желудочка (ЛЖ), или губчатая кардиомиопатия, является редкой и малоизученной врожденной кардиомиопатией, которая характеризуется нарушением эндомиокардиального морфогенеза, гипертрофией миокарда ЛЖ, его чрезмерной трабекуляцией и образованием широких межтрабекулярных пространств. Первое сообщение о НМ появилось в литературе в 1986 году. В нашей стране заболевание впервые описано в 1998 году. По данным различных авторов распространенность НМ варьирует от 0,05 до 0,24 % [4]. Некомпактность ЛЖ может иметь место у людей различных возрастных групп, от 1 месяца до 71 года, но преимущественно встречается у лиц молодого возраста. Это может быть связано с тем, что, большинство пациентов с развернутой клинической картиной заболевания умирает, не дожив до среднего возраста или даже до совершеннолетия [2]. Причина возникновения НМ ЛЖ – несовершенный эмбриогенез, в результате которого нарушается нормальное развитие миокарда. Первичный миокард состоит из неплотно связанной сети переплетенных между собой волокон, разделенных глубокими карманами, сообщающимися с полостью ЛЖ. В период с 5-й по 8-ю неделю эмбрионального развития эта рыхлая сеть волокон постепенно становится компактной [5]. Процесс начинается с эпикарда и идет к эндокарду, от основания сердца к его верхушке. В то же время развивается коронарное кровообращение и межтрабекулярные карманы превращаются в капилляры. В норме массивные мышечные трабекулы могут встречаться в правом желудочке, наличие их в левом желудочке считается патологией. Нормальный вариант повышенной трабекулярности правого желудочка очень трудно отличить от патологического некомпактного миокарда, поэтому вопрос об изменении правого желудочка до сих пор остается спорным. В большинстве случаев губчатая кардиомиопатия поражает левый желудочек, хотя в литературе встречаются описания как изолированного поражения правого желудочка, так и сочетанного поражения [1]. У 44 % лиц с НМ наблюдают передающиеся из поколения в поколение проявления этой патологии, что свидетельствует о её наследственном характере. В клинической картине наиболее часто встречается триада: сердечная недостаточность (СН) (73 %), желудочковые и наджелудочковые нарушения ритма (41 %) и тромбоэмболические осложнения (33 %). Диагностика НМ основана, прежде всего, на данных эхокардиографии (ЭХОКГ). Всем больным с губчатым миокардом показана антикоагулянтная терапия. Также может понадобиться антиаритмическая терапия и имплантация кардиовертера-дефибриллятора. При прогрессирующей сердечной недостаточности спасти таких больных может только трансплантация сердца [3]. Прогноз заболевания неблагоприятный. Больные погибают от декомпенсации кровообращения, рефрактерной к терапии аритмии, тромбоэмболии легочной артерии или внезапно.
Приводим клиническое наблюдение пациента с некомпактным миокардом левого желудочка. Больной Ф. 37 лет 21.10.15 г. обратился в Оренбургскую клиническую больницу № 2 в жалобами на одышку при незначительной физической нагрузке, подъеме на 1-2 этаж, слабость, перебои, замирание в работе сердца, повышение АД до 140\90 мм. рт. ст., снижение толерантности к физической нагрузке. Из анамнеза заболевания известно, что при прохождении профосмотра 5 лет назад, на ЭКГ выявили изменения в виде: полной блокады левой ножки пучка Гиса (ПБЛНПГ). Наблюдался у кардиолога по месту жительства c ДЗ: Дилатационная кардиомиопатия, вторичная. Спортивное сердце. Ухудшение в течение последнего года. С июня 2014 г., стал отмечать снижение толерантности к физической нагрузке. Одышка стала возникать при меньшей нагрузке, перебои в работе сердца. До июня 2014 г., продолжал занимался активным спортом (тяжелая атлетика), принимал белковые препараты, энергетики. Обратился к кардиологу по месту жительства, направлен в стационар. Стационарное лечение в отделении городской клинической больницы № 1 с ДЗ: Вторичная дилатационная кардиомиопатия. Спортивное сердце. ПБЛНПГ. Постоянная форма мерцательной аритмии. Принимал: диувер, дигоксин, бисопролол, хартил, амоксициллин, кларитромицин. Состояние без особой положительной динамики. В последующем наблюдался у кардиолога. Проводилось обследование: общий анализ крови, общий анализ мочи, определение в крови уровня глюкозы, креатинина, билирубина, холестерина, АлАт, АсАТ, триглицеридов, МНО, АЧТВ – патологии не было выявлено. Неоднократно проводилось электрокардиография. При поступлении: фибрилляция предсердий с ЧЖС 41-150 в мин(91 в мин) тахисистолическая форма. ЭОС влево. Полная блокада л. н. п. Гиса. При выписке: фибрилляция предсердий с ЧЖС 65-150 в мин (83 в мин) нормосистолическая форма, в остальном без динамики.
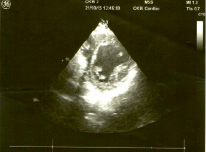
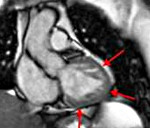
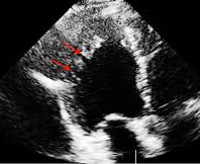
Сразу при поступлении было проведено ЭХОКГ (рисунок), где были выявлены признаки наличия некомпактного миокарда.
ЭХОКГ больного Ф., 37 лет 21.10.15 г.
Отмечается некомпактность миокарда в области боковой стенки левого желудочка. Толщина боковой стенки 18 мм, имеется четкое разграничение на компактный и некомпактный слои, толщина некомпактного слоя 12 мм, толщина компактного слоя 6 мм в диастолу. В систолу при исследовании по короткой оси общая толщина стенки 31 мм, толщина компактного слоя 6 мм, толщина некомпактного слоя 25 мм. Соотношение некомпактного и компактного слоев в систолу в месте максимального утолщения 25/6 = 4,1. Соотношение истинного миокарда к толщине всей стенки на уровне верхушки 6/31 = 0,19, т.е. меньше 0,2, что соответствует тяжелой степени некомпактности. Дилатация всех полостей сердца. Снижена глобальная сократимость левого желудочка (ФВ – 48 %). Незначительно изменена структура стенок аорты, створок митрального клапанов. Митральная и трикуспидальная регургитации. Легочная гипертензия (44 мм. рт. ст.).
Проводилось мониторирование ЭКГ: средняя ЧСС днем 108 в минуту (минимально 71 уд/мин, максимально 178 уд/мин), ночью 74 в минуту (минимально 66 уд/мин, максимально 104 уд/мин). Циркадный индекс 146 %.В пределах возрастной нормы. Фибрилляция – трепетание предсердий общей длительностью 22:36:58, с ЧЖС от 66 до 178 уд\мин в течении всего наблюдения. Полная блокада л. н. п. Гиса. Желудочковая экстрасистолия 3 кл по RYAN. В течение суток наблюдалось удлинение корригированного QT –интервала свыше 450 мс в течение 21 час 48 мин.
Больному был выставлен диагноз: Кардиомиопатия обусловленная некомпактным миокардом (губчатым). Сложные нарушения ритма и проводимости: Фибрилляция предсердий тахи-нормосистолическая форма. Желудочковая экстрасистолия 3 кл по RYAN. Полная блокада л. н. п. Гиса. СН IIА. ФК III.
Пациент получал лечение: режим, диета, карведилол, варфарин, престариум А, верошпирон. На фоне проводимого лечение самочувствие больного улучшилось и он был выписан под наблюдения кардиолога по месту жительства.
Таким образом, у нашего пациента был выявлен НМ ЛЖ. Симптомы этого заболевания неспецифичны и иногда проявляются только с возрастом, в связи с чем, его редко диагностируют и часто неадекватно проводят лечение. В то же время неблагоприятный прогноз и высокая летальность при синдроме некомпактности миокарда определяют необходимость его распознавания на ранних стадиях и дифференцированного подхода к лечению в зависимости от тяжести состояния больного с использованием современных методов как консервативного, так и хирургического лечения.
Некомпактный миокард левого желудочка — тип кардиомиопатии, который характеризуется гипертрофией мышечных волокон указанной локализации, их чрезмерной трабекулярностью, образованием глубоких межтрабекулярных пространств. Пациенты жалуются на одышку, быструю утомляемость, нарушения ритма, головную боль, отеки ног. Диагностика основывается на инструментальных методах: Эхо-КГ, ЭКГ, МРТ, ПЭТ-КТ. Тактика лечения зависит от тяжести патологии, включает в себя медикаментозные и хирургические методики, направленные на коррекцию сердечной недостаточности, предупреждение опасных аритмических, тромбоэмболических осложнений.
МКБ-10
Общие сведения
Некомпактный, или губчатый, миокард левого желудочка (НЛМЖ) — диагноз, относительно недавно введенный в клиническую практику в связи с улучшением методов исследования сердца. Является редко встречающимся заболеванием, наблюдается примерно у 0,015% взрослых людей, в 18% случаев имеет наследственный характер. Специалисты отмечают, что реальные цифры могут существенно превышать официальные данные из-за выраженной гиподиагностики сердечно-сосудистых патологий. Аномалия строения чаще диагностируется у мужчин — 56-82%. У детей составляет до 10% обнаруживаемых болезней миокарда, занимает третье место по частоте после гипертрофической и дилатационной кардиомиопатии. У больных младше 18 лет около половины наблюдений является следствием генетического дефекта.
Причины НМЛЖ
Причинные факторы патологии остаются недостаточно изученными, однако существуют определенные закономерности, свидетельствующие о ее наследственном характере. Например, аномалия строения кардиальной мышцы нередко встречается у представителей нескольких поколений одной семьи, как у мужчин, так и у женщин всех возрастов. Существуют зарегистрированные случаи, не вписывающиеся в эту концепцию. С учетом этого обстоятельства были разработаны две теории развития некомпактного миокарда левого желудочка:
Патогенез
В механизме развития заболевания ведущую роль играют три основных компонента: недостаточная функция сердца, нарушения ритма, повышенный риск тромбоэмболии. Некомпактный миокард представляет собой слой кардиомиоцитов с нарушенной структурной организацией, что не позволяет ему сокращаться так же эффективно, как здоровым участкам сердечной мышцы. Чем больше аномальных мышечных волокон – тем ярче выражены признаки кардиальной недостаточности. Патологическая архитектоника ткани создает условия для расстройства микроциркуляции крови и ишемии левого желудочка. Уменьшение функциональной активности органа может быть как систолическим, так и диастолическим по рестриктивному типу, что связано с повышенной трабекулярностью.
Нарушения сердечного ритма провоцируются анатомической неоднородностью миокарда – некомпактный, рыхлый слой сменяется слоем с более плотной структурой. Это негативно влияет на распространение электрического импульса по мышечным волокнам и может приводить к развитию желудочковых аритмий. На фоне сниженной насосной функции сердца, наличия обширных полостей между дополнительными трабекулами неритмичные сокращения создают предпосылки для изменения реологических свойств крови и тромбообразования.
Классификация
Некомпактный миокард определяют как первичную структурную и функциональную патологию сердечной мышцы, развивающуюся при отсутствии заболеваний, способных вызвать нарушение строения тканей: артериальной гипертензии, дисфункции венечных сосудов, клапанной системы. Аномалию, локализованную в левом желудочке, систематизируют по наличию либо отсутствию сопутствующих изменений строения сердца:
Симптомы НМЛЖ
Заболевание имеет чрезвычайно разнообразную клиническую картину, выраженность которой во многом зависит от степени гипертрофического процесса. Обычно симптомы проявляются у детей и подростков, однако манифестация возможна и в зрелом возрасте. Пациенты отмечают нарастающие симптомы сердечной недостаточности, прежде всего – появление одышки. Учащение дыхания вначале выявляется при активной физической активности, затем – при легкой нагрузке, в терминальных стадиях — в покое. Застойные явления в сосудах легких провоцируют затруднения дыхания в положении лежа, ночные приступы кашля, иногда с примесью крови.
При выраженной гипофункции кардиомиоцитов могут наблюдаться отеки и синюшность нижних конечностей. У ряда больных обнаруживается слабость, быстрая утомляемость, спутанность сознания, нарушение сна, уменьшение диуреза, особенно в дневное время. Развитие аритмии добавляет к клинической картине ощущение сердцебиения, перебоев в работе органа, тахикардию или выраженную брадикардию, боль за грудиной, головокружение, иногда – потери сознания. Некомпактный миокард нередко сочетается с нейромышечными патологиями, что проявляется снижением тонуса скелетной мускулатуры, нарушением походки, постепенной утратой физических навыков (ходьба, способность сидеть, держать голову).
Осложнения
Диагностика
Симптомы некомпактного миокарда достаточно неспецифичны, поэтому на первое место в обнаружении патологии выходят инструментальные методы. На первичном приеме кардиолог или терапевт может заподозрить наличие аномального строения сердца по сочетанию признаков сердечной недостаточности и аритмического синдрома. Специалист уточняет семейный анамнез, чтобы выявить возможную наследственную предрасположенность. Из дополнительных методов обследования используются:
Дифференциальный диагноз проводят с опухолями сердца, другими видами кардиомиопатий, добавочными хордами, трабекулами, ишемической болезнью, амилоидозом, инфарктом миокарда, кардиогенным шоком, кардиогенным дистресс-синдромом. Как причины развития одышки необходимо исключить хронические обструктивные заболевания легких (ХОБЛ, бронхиальную астму, эмфизему легких), пневмонию.
Лечение НМЛЖ
При отсутствии симптоматики, нарушений ритма, уменьшения фракции выброса левого желудочка проведение специализированной терапии не показано. Необходим контроль над состоянием в динамике, плановые осмотры у кардиолога не реже 1 раза в 6 месяцев. При выраженных проявлениях патологии необходима коррекция состояния, предупреждение опасных осложнений. Существуют две основные линии лечения некомпактного миокарда левого желудочка:
Прогноз и профилактика
Долгосрочный прогноз зависит от распространенности аномалии, возраста пациента, наличия сопутствующих заболеваний. Смертность в течение 7 лет с момента постановки диагноза достигает 24%. При своевременном обращении к специалистам, комплексном полноценном лечении возможна коррекция недостаточной функции сердца, аритмических проявлений. Из-за преимущественно наследственной этиологии некомпактного миокарда специфическая профилактика отсутствует. Общие превентивные мероприятия включают ведение здорового образа жизни, достаточную физическую активность, правильное питание, снижение психоэмоциональных нагрузок.
Некомпактный миокард
Некомпактный миокард левого желудочка (синонимы: губчатый миокард, эмбриональный миокард, персистирующие синусоиды) — генетически детерминированная кардиомиопатия, которая характеризуется патологической трабекулярностью миокарда левого желудочка в результате нарушения нормального эмбриогенеза сердца с формированием двух слоев миокарда: толстого некомпактного (эндокардиального) и тонкого нормального (компактного, эпикардиального).
Код по МКБ-11
BC44 Noncompaction cardiomyopathy
Историческая справка
Первые упоминания губчатого миокарда описаны американским хирургом Самуэлем Беллетом в 1932 году: в миокарде левого желудочка новорожденного с цианотическим врожденным пороком сердца отмечались глубокие лакуны и трабекулы, выявленные при аутопсии. Далее, лишь с развитием и внедрением эхокардиографии (далее ЭхоКГ), в 1984 году немецкие ученые Рольф Энгбердинг и Франц Бендер описали наличие синусоид миокарда у пациента, характерные лишь для эмбрионального этапа развития сердца. В 1990 году детский кардиолог и американский профессор кафедры педиатрии вместе с соавторами предложил термин «изолированная некомпактность миокарда левого желудочка». Учитывая все большее внедрение в практику ЭхоКГ, описывалось множество случаев данной нозологии, и в 1995 году Всемирная организация здравоохранения включила данное заболевание в группу неклассифицируемых кардиомиопатий. Затем, в 2006 году, Американская ассоциация сердца отнесла данную патологию к первичным генетическим кардиомиопатиям. С 2008 года заболевание включено в группу неклассифицируемых кардиомиопатий согласно классификации Европейского общества кардиологов.
Эпидемиология
Распространенность заболевания среди взрослого населения составляет 0,014%. Встречается: у 0,01-0,27% всех взрослых пациентов, направленных на ЭхоКГ; у 3% больных из 960 с признаками ХСН; у 100 пациентов из 36933, перенесших ЭхоКГ (в период с 1994-2006 гг). По данным разных ученых, заболевание чаще встречается у мужчин (56–82 %). В детской практике из всех случаев кардиомиопатий некомпактный миокард встречается в 9,2%, занимая третье место после гипертрофической КМП и дилатационной КМП.
Эмбриональное развитие миокарда
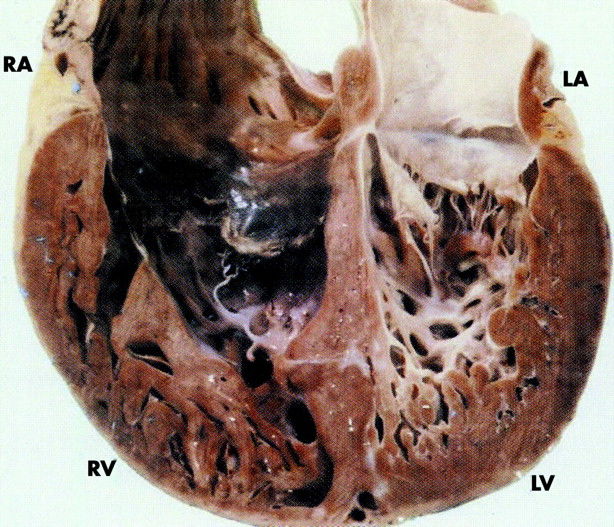
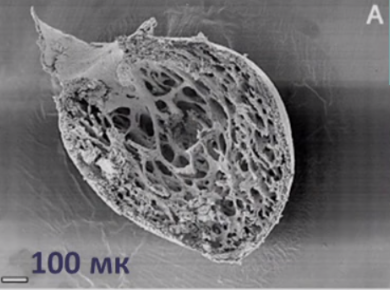
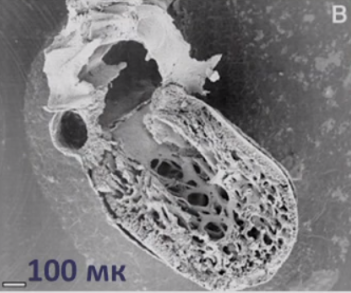
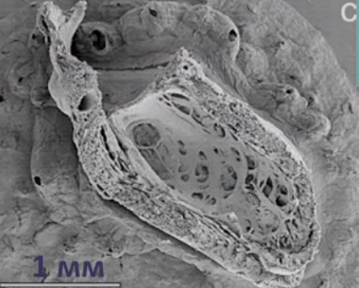
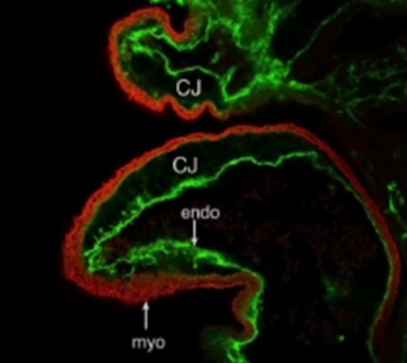
Для наиболее точного понимания механизма образования некомпактного слоя миокарда обратимся к эмбриологии. Миокард развивается из миоэпикардиальной пластинки спланхнотома мезодермы, представляя собой сеть волокон, разделенных широкими полостями. С 5-й недели эмбрионального развития происходит уплотнение сети волокон, сужение межтрабекулярных лакун, формируется коронарный кровоток, происходит процесс уменьшения межтрабекулярных пространств до размеров капилляров. Миокард «компануется» от основания к верхушке, от эпикарда к эндокарду (рис. 1, 2, 3, 4). При нарушении данного процесса, чаще всего в результате генетической мутации в генах, кодирующих белок таффазин, альфадистробеверин, гетерозиготные мутации в генах, кодирующих MYH7, ACTC, TNNT2, в сердце остаются зоны некомпактного миокарда с глубокими межтрабекулярными пространствами.
Классификация
Большинство ученых выделяют следующие формы некомпактного миокарда:
– изолированный;
– в сочетании с врожденными пороками сердца;
– в сочетании с нейромышечными заболеваниями (метаболическая миопатия, синдром Barth, синдром Roifman, синдром Ohtahara, синдром Noonan, мышечная дистрофия Emery–Dreifuss, мышечная дистрофия Becker, синдром Melnick–Needles).
По форме возникновения:
– спорадическая;
– семейная (30%).
По анатомическим формам выделяют:
– левожелудочковая;
– правожелудочковая;
– бивентрикулярная.
По морфологическим типам:
– лакунарный;
– губчатый;
– смешанный.
По степени некомпактности миокарда (по отношению толщины слоя некомпактного миокарда к толщине всей стенки сердца на уровне верхушки левого желудочка):
– мягкая (0,33–0,26)
– умеренная (0,25–0,20)
– тяжелая (менее 0,2)
Патогенез и клиника
Патогенез складывается из сердечной недостаточности, синдрома нарушений ритма, тромбоэмболического синдрома.
Сердечная недостаточность выходит на ведущее место в клинике данного заболевания. Из-за нарушенной архитектоники строения миокарда происходит нарушение его сократительной способности. При тяжелой степени некомпактности клиническая картина данного синдрома наиболее выражена с преобладанием недостаточности по обоим кругам кровообращения и с выраженным снижением общей сократительной способности миокарда. Как правило, у некоторых пациентов клиника заболевания может манифестировать в результате запуска воспалительного процесса в миокарде, а в ряде случаев, при благоприятном течении, некомпактный миокард можно выявить впервые у лиц пожилого возраста. В клинической картине заболевания на первое место может выходить болевой синдром, который выражается приступами стенокардии. Это объясняется большей потребностью в кислороде некомпактного слоя миокарда, который не кровоснабжается основными ветвями коронарных артерий, а кровоснабжение его происходит непосредственно из полости левого желудочка.
Синдром нарушений ритма проявляется чаще всего желудочковыми нарушениями ритма — более чем в половине случаев (экстрасистолия, нередко и высоких градаций). В четверти случаев наблюдается фибрилляция предсердий. Также, вследствие эндомиокардиального фиброза с захватом проводящей системы сердца наблюдаются нарушения проводимости по типу АВ, СА-блокад.
Конечно же, нарушение глобальной систолической функции, наличие нарушений ритма сердца, а в частности фибрилляции предсердий, наличие глубоких лакун предрасполагает к образованию тромбов в полости левого желудочка, а отсюда и тромбоэмболических осложнений (кардиоэмболические инсульты, ТИА, мезентериальный тромбоз).
Диагностика
Клиника при данном заболевании неспецифична, она может маскировать и дебют ИБС, и прочие кардиомиопатии. В данном случае нам помогает ЭхоКГ и МРТ с контрастированием гадолинием, помимо стандартной ЭКГ и суточного мониторирования ЭКГ.
Выделяют следующие эхокардиографические критерии некомпактного миокарда:
Так же проводится оценка всех стандартных параметров при ЭхоКГ (размеры полостей, наличие изменений сократительной способности, клапанная недостаточность, оценка фракции выброса).
МРТ проводится с контрастным усилением редкоземельного металла гадолиния, оценивается: ФВ ЛЖ, индексированная масса миокарда (компактного, некомпактного); число некомпактных сегментов; критерий некомпактности (чувствительность 86%, специфичность 99%: соотношение компактного и некомпактного слоя миокарда в диастолу более 1:2); индекс ремоделирования левого желудочка.
И, конечно же, не стоит забывать о генетическом картировании и биопсии миокарда.
Принципы и тактика лечения.
Пациентам с бессимптомным течением специфической терапии не требуется, им нужно лишь динамическое наблюдение у врача кардиолога. При наличии клиники лечение должно складываться из следующих составляющих: стандартная терапия ХСН; назначение антикоагулянтной терапии при необходимости (снижение ФВ, ТЭ в анамнезе, тромбоз полостей сердца); назначение, при необходимости, антиаритмической терапии; назначение иммуносупрессивной терапии при доказанности аутоиммунного повреждения миокарда. Так же, в отдельных случаях, могут рассматриваться варианты установки ЭКС (при наличии блокад высоких градаций с эпизодами синкопе); установки кардиовертера-дефибриллятора (при плохом терапевтическом ответе на антиаритмики); трансплантации сердца.
Некомпактный миокард что это такое
ФГБУ «Объединенная больница с поликлиникой» Управления делами Президента РФ, Москва, Россия
ФГБУ «Центральная государственная медицинская академия» Управления делами Президента РФ, Москва, Россия
ГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Москва, Россия; ФГБНУ «Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний», Кемерово, Россия
Некомпактный миокард левого желудочка
Журнал: Архив патологии. 2018;80(4): 47-53
Гайсёнок О. В., Курносов П. А., Бернс С. A. Некомпактный миокард левого желудочка. Архив патологии. 2018;80(4):47-53.
Gaisenok O V, Kurnosov P A, Berns S A. Left ventricular noncompaction. Arkhiv Patologii. 2018;80(4):47-53.
https://doi.org/10.17116/patol201880447
ФГБУ «Объединенная больница с поликлиникой» Управления делами Президента РФ, Москва, Россия
Представлен обзор литературы по некомпактному миокарду левого желудочка (некомпактная кардиомиопатия). Подробно отражены исторические аспекты, эпидемиология, этиология, патофизиология, особенности клинической картины, диагностики, лечения и прогноза данной патологии.
ФГБУ «Объединенная больница с поликлиникой» Управления делами Президента РФ, Москва, Россия
ФГБУ «Центральная государственная медицинская академия» Управления делами Президента РФ, Москва, Россия
ГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Москва, Россия; ФГБНУ «Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний», Кемерово, Россия
Определение. Исторические аспекты. Некомпактная кардиомиопатия (некомпактный миокард левого желудочка — НМЛЖ), «губчатый» миокард, left ventricular non-compaction) — аномалия строения сердца, заключающаяся в наличии 2-слойной структуры миокарда, состоящей из внутреннего выстланного эндотелием некомпактного, или трабекулярного, слоя и лежащего под ним компактного слоя. НМЛЖ — одна из редких первичных кардиомиопатий, для которой характерно чрезмерное развитие трабекул с формированием глубоких ниш, сообщающихся с полостью левого желудочка (ЛЖ), но не с коронарными артериями [1, 2].
Как правило, под некомпактной кардиомиопатией подразумевается патология ЛЖ сердца. Правый желудочек сердца также может быть некомпактным, однако он более трабекулярен в норме, в связи с чем диагностика некомпактного миокарда правого желудочка затруднена [3]. НМЛЖ — генетически обусловленное поражение миокарда, манифестирующее сердечной недостаточностью (СН), нарушениями ритма, тромбоэмболиями и внезапной сердечной смертью (ВСС). В качестве отдельной нозологической формы НМЛЖ выделили относительно недавно, согласно классификации Европейского общества кардиологов, эта нозология относится к рубрике неклассифицируемых кардиомиопатий.
В историческом аспекте первое упоминание о НМЛЖ относится к 1926 г. R. Grant [4], который описал патологию строения миокарда, назвав ее губчатым миокардом. Однако с позиций клинической значимости эту патологию впервые упомянули в 1975 г. J. Dusek и соавт. [5]. Первое описание НМЛЖ появилось в литературе в 1986 г. В нем сообщалось, чтоу 33-летней женщины сохранились «желудочковые синусы», характерные для сердца во внутриутробном периоде, наличие которых сопровождалось тяжелой кардиомиопатией и летальным исходом, что подтвердилось на аутопсии [6]. В 1990 г. описано уже 8 случаев синдрома НМЛЖ, было дано определение этого заболевания и введена аббревиатура LVNC (left ventricular noncompaction) [7]. Большинство исследователей [2, 8, 9] расценивают НМЛЖ как врожденное состояние, возникающее на 2-м месяце эмбриогенеза, однако некоторые полагают, что существует возможность его формирования и в постнатальном периоде [10—13]. Следует признать, что, несмотря на достаточно большое количество публикаций, НМЛЖ по-прежнему остается патологией, мало известной клиницистам [14].
Эпидемиология и классификация
По данным M. Ritter и соавт. [1], распространенность заболевания среди взрослой популяции составила 0,045%, однако истинные цифры могли быть выше. R. Engberding и соавт. [8] приводят данные различных исследователей о количестве наблюдений пациентов с НМЛЖ, гендерных характеристиках, возрасте, сроках наблюдения, доминирующих клинических симптомах. Наибольшее число случаев (86 наблюдений) представлено C. Stöllberger [14]. По данным разных исследователей [1, 8, 9], заболевание чаще встречается у мужчин — 56—82%. В педиатрической практике удельный вес патологии составляет 9,2% от всех случаев диагностированных кардиомиопатий, занимая третье место после гипертрофической кардиомиопатии (ГКМП) и дилатационной кардиомиопатии [16].
Распространенность заболевания в детской популяции, по данным C. Lilje и соавт. [17], составила 1,26%. Возможно, в ближайшие годы будет создан сводный регистр, что позволит более точно характеризовать эпидемиологию этой редкой кардиомиопатии.
Большинство исследователей выделяют следующие формы НМЛЖ:
в сочетании с врожденными пороками сердца,
в сочетании с нейромышечными заболеваниями (метаболическая миопатия, синдром Barth, синдром Roifman, синдром Ohtahara, синдром Noonan, мышечная дистрофия Emery—Dreifuss, мышечная дистрофия Becker, синдром Melnick—Needles).
Среди врожденных пороков сердца наиболее часто НМЛЖ ассоциирован с дефектами межпредсердной перегородки (ДМПП), врожденным стенозом легочной артерии, дефектами межжелудочковой перегородки (ДМЖП), реже — с аномалией Эбштейна, врожденными пороками аортального клапана (подклапанный стеноз, двустворчатый клапан, клапанный стеноз), клапанным стенозом легочной артерии, тетрадой Фалло [17].
В 2013 г. World Heart Federation (Всемирная федерация сердца) предложила классификацию кардиомиопатий — MOGE (S), описывающую пять признаков заболевания: морфологическую или морфофункциональную характеристику (M), пораженные органы (O), характер наследования болезни (G), ее этиологию с детальным описанием генетического дефекта либо другой причины (E) и в качестве необязательного, опционального, фактора — функциональный статус больного (S) с указанием стадии хронической сердечной недостаточности (ACC/AHA) и функционального класса (NYHA) [18]. По сути эта классификация объединила классификацию (2006) American Heart Association, которая учитывала в первую очередь генетическую природу заболевания, а затем его морфологическую характеристику [19] и классификацию ESC (2008), основанную в первую очередь на морфофункциональной характеристике заболевания с последующим делением на наследственные или ненаследственные подклассы [20].
Этиология и патофизиология
Считают, что причина возникновения НМЛЖ — несовершенный эмбриогенез, в результате которого нарушается нормальное развитие миокарда. Первичный миокард состоит из неплотно связанной сети переплетенных между собой волокон, разделенных глубокими карманами, сообщающимися с полостью ЛЖ. В период с 5-й по 8-ю неделю эмбрионального развития эта рыхлая сеть волокон постепенно становится компактной. Процесс начинается с эпикарда и идет к эндокарду, от основания сердца к его верхушке. В то же время развивается коронарное кровообращение и межтрабекулярные карманы превращаются в капилляры. Различные сроки нарушения эмбрионального морфогенеза определяют объем некомпактного («губчатого») миокарда в пределах желудочков. Значительная трабекуляция — нормальная характеристика миокарда во внутриутробном периоде. Наличие «губчатого» миокарда у взрослых считают результатом недостаточного обратного развитиядетских трабекул [21]. Некомпактность Л.Ж. встречается в возрастных группах от 1 мес до 71 года, но чаще возникает в молодом возрасте. Описаны как клинические случаи постнатального формирования НМЛЖ [12, 22—24], так и случаи исчезновения этого заболевания [25, 26].
Несмотря на то что причиной развития заболевания с фенотипом НМЛЖ служит нарушение уплотнения миокарда, непосредственные механизмы его возникновения до сих пор остаются неизученными. Существует предположение, что некоторые кардиомиопатии являются лишь различными последствиями вариаций в развитии миокарда, обусловленных генетическими мутациями, нарушением на разных этапах экспрессии одной или нескольких групп генов. Так, некомпактный миокард определяется фенотипом, морфологической экспрессией различных лежащих в основе заболеваний [27]. Встречаются как спорадические формы заболевания, так и семейные случаи. Описаны два типа наследования: аутосомно-доминантный и сцепленный с полом (до 44% наблюдений) [28]. Синдром НМЛЖ, тип 1 наследуется по аутосомно-доминантному типу. При этом типе наблюдается как изолированный синдром НМЛЖ, так и его сочетание с пороками сердца. Чаще всего встречаются ДМПП, изолированный или множественные ДМЖП, стеноз легочных артерий, однако описаны и некоторые другие виды пороков. Причиной этого заболевания являются мутации в гене дистробревина, который расположен в локусе 18q12.1—q12.2 [29, 30].
НМЛЖ, тип 2, как правило, наследуется по аутосомно-доминантному типу, не наблюдается сочетания НМЛЖ с пороками сердца. Ген, ответственный за это заболевание, в настоящее время не известен, однако картирован локус 11p15, сцепленный с НМЛЖ [29, 31].
Х-сцепленный тип НМЛЖ наследуется по Х-сцепленному рецессивному типу. Женщины могут являться носительницами мутантного гена, при этом у них существует 50% вероятность передать ген, несущий мутацию, сыновьям. Все дочери женщин-носительниц окажутся здоровыми, но половина из них также будут являться носительницами мутантного гена.
Изолированный НМЛЖ (т.е. при отсутствии других патологических изменений сердца) связан с мутацией в гене G4.5 в Xq28, которую также регистрируют при синдроме Барта — рецессивном наследственном заболевании, сцепленном с хромосомой Х. Он манифестирует в детском возрасте триадой симптомов: дилатационной кардиомиопатией, нейтропенией и скелетной миопатией [32]. Ген G4.5 кодирует группу белков тафазинов, функция которых до сих пор остается малоизученной [33]. Заболевание генетически неоднородно — при неизолированной НМЛЖ мутации могут происходить и в гене α-дистробревина [34].
Данные аутопсии и морфологических исследований эксплантированного сердца у больных с НМЛЖ подтверждают существование анатомических изменений, обнаруженных при жизни [35]. При гистологическом исследовании в толще эндокардиального слоя и трабекул определяют фокальные участки ишемического некроза, которые отсутствуют в эпикардиальном слое. Характерны участки интерстициального фиброза различной степени выраженности. Нередко имеются морфологические признаки хронического миокардита.
Обнаруженные изменения позволяют предположить возможные механизмы возникновения нарушений ритма и прогрессирующей недостаточности ЛЖ, характерной для НМЛЖ. Межтрабекулярные карманы получают кровь прямо из полости ЛЖ, но эпикардиальный и эндокардиальные слои миокарда, включая трабекулы, зависят от коронарного кровоснабжения. Постепенно развивающиеся микроциркуляторные нарушения в многочисленных трабекулах приводят к несоответствию массы миокарда количеству обеспечивающих ее капилляров. Кроме того, утолщенный миокард может создавать дополнительную компрессию интрамурального коронарного русла. В конечном итоге оба процесса приводят к уменьшению субэндокардиальной перфузии, несмотря на отсутствие обструкции в венечных артериях. Снижение коронарного резерва регистрируют у пациентов с НМЛЖ при позитронно-эмиссионной томографии сердца. Прогрессирующая ишемия и фиброз могут привести к ухудшению систолической функции и создать субстрат для возникновения нарушений ритма. Выраженная трабекулярность способствует возникновению диастолической дисфункции. Рестриктивные изменения регистрируют у 35% взрослых пациентов с НМЛЖ.
Особенности клинической картины
Заболевание может дебютировать как в неонатальном периоде, так и в более позднем возрасте. Клиническое течение заболевания — от асимптоматичного до быстро развивающейся СН. У пациентов с НМЛЖ могут возникать нарушения ритма, симптомы недостаточности ЛЖ, тромбоэмболия [36—38]. В детском возрасте также описаны цианоз, плохая прибавка массы тела и дисморфические признаки. Достаточно большое число случаев НМЛЖ диагностируют при обследовании семей больных НМЛЖ или как случайную находку при рутинном обследовании сердца. Частота возникновения тромбоэмболических осложнений достаточно высока и составляет 24%. Считают, что тромбоэмболии возникают вследствие застоя крови в межтрабекулярных карманах. Чаще всего больные жалуются на сердцебиение, синкопальные состояния, загрудинную боль стенокардического характера [39]. Практически у всех больных (97%) регистрируются патологические изменения на ЭКГ, самыми распространенными из которых являются полная блокада левой ножки пучка Гиса (44%), а также желудочковые и наджелудочковые аритмии [40].
До сих пор остается неясным, может ли НМЛЖ дебютировать с ВСС. Это заболевание достаточно редко обнаруживают при аутопсии пациентов, умерших внезапно, что может быть связано с низкой осведомленностью врачей о такой болезни. Существует предположение, что на долю НМЛЖ приходится некоторая часть смертей, приписываемых миокардитам или ВСС у людей с морфологически неизмененным сердцем. Так, в исследованиях Е. Oeschlin и соавт. [33] у 14 из 34 больных выявлена желудочковая тахикардия типа «пируэт», 4 пациентам имплантирован кардиовертер-дефибриллятор. Доказано также, что синдром Вольфа–Паркинсона–Уайта (преимущественно тип В) при НМЛЖ значительно чаще встречается у детей, чем у взрослых.
Диагностика
Ремоделирование сердца у пациентов с НМЛЖ происходит неодинаково: возможны изменения по дилатационному типу, гипертрофическому, рестриктивному, а также по смешанному типу, когда присутствуют признаки как дилатации полостей сердца, так и гипертрофии стенок сердца [35, 41, 42]. К тому же сама «некомпактность» миокарда представляет собой спектр морфологических признаков — от мелких трабекул до выраженного некомпактного слоя миокарда [43]. Подобная гетерогенность заболевания влечет за собой сложность выработки универсальных диагностических критериев.
Диагноз НМЛЖ ставят по результатам эхокардиографии (ЭхоКГ), магнитно-резонансной томографии (МРТ) или ангиографии Л.Ж. При ЭхоКГ «губчатость» ЛЖ представлена трабекулами, которыепо плотности соответствуют плотности миокарда и движутся синхронно с миокардом ЛЖво время его сокращений [2]. Возможность получать четырехмерное изображение сердца значительно упрощает визуализацию избыточной трабекулярности.
При диагностике НМЛЖ большое внимание уделяют такому методу исследования, как МРТ сердца. Это связано с тем, что в отличие от ЭхоКГ МРТ сердца не ограничена акустическим окном и имеет дополнительные преимущества для визуализации очерченных полей миокардиального фиброза в случае контрастирования парамагнетиком гадолинием. Несмотря на это, главным и наиболее доступным методом обследования остается 2D-ЭхоКГ, которая позволяет определить локализацию и структуру поражения стенки Л.Ж. Проблемой разработки ультразвуковых критериев диагностики некомпактного миокарда занимаются с начала 90-х годов и даже в 1990 г. были предложены различные ультразвуковые критерии «губчатого» миокарда ЛЖ [7], однако на сегодняшний день не существует единого алгоритма в постановке диагноза. Трабекулярность миокарда повышена и при других кардиомиопатиях, поэтому эхокардиографическая диагностика НМЛЖ требует высокой квалификации врача.
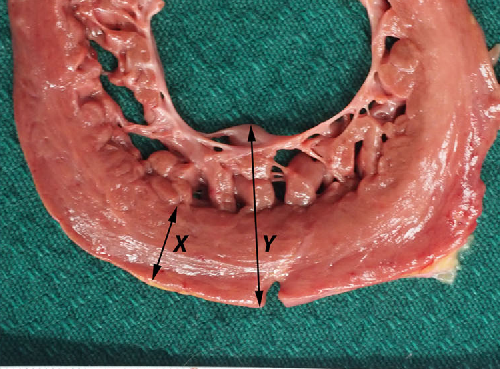
Диагностические критерии предложены T. Chin и соавт.: НМЛЖ определяется как соотношение X/Y ≤0,5, где Х – расстояние от эпикарда до межтрабекулярных пространств, а Y – расстояние от эпикарда до максимально выступающей трабекулы. Эти критерии рассматриваются в отношении трабекулы, располагающейся в области верхушки ЛЖ из парастернальной позиции по короткой оси, а также верхушечной позиции. Толщина свободной стенки ЛЖ измеряется в конце диастолы [7].
C. Stöllberger и J. Finsterer [14] рекомендуют использовать следующие диагностические критерии: более трех выступающих в полость ЛЖ трабекул по направлению от верхушки к папиллярным мышцам, видимых на одном изображении сердца; межтрабекулярные пространства, свободно сообщающиеся с полостью ЛЖ, визуализируются с помощью цветового допплеровского картирования (ЦДК). C. Lilje и соавт. [17] предложили количественные критерии для определения степени некомпактности миокарда по соотношению слоя «плотного» истинного миокарда к толщине всей стенки сердца на уровне верхушки ЛЖ: 0,33—0,26 — «мягкая» некомпактность; 0,25—0,2 — умеренная; менее 0,2 — тяжелая.
Наиболее развернутые диагностические критерии предложили R. Jenni и соавт. [9]:
1. Соотношение N/C более 2, где N — некомпактный слой миокарда, C — компактный слой миокарда. Двуслойная структура миокарда с истонченным компактным и утолщенным некомпактным слоем, выявляемая из парастернальной позиции по короткой оси.
2. Отсутствие других сопутствующих аномалий сердца.
3. Наличие многочисленных, чрезмерно выступающих в полость ЛЖ трабекул с глубокими межтрабекулярными пространствами.
4. Сообщающиеся с полостью ЛЖ межтрабекулярные пространства, выявляемые с помощью ЦДК.
Наиболее распространенными критериями из всех являются критерии, предложенные К. Chine (1990) и R. Jenni и соавт. [9]. Каждое учреждение самостоятельно решает, какие из предложенных диагностических критериев «губчатого» миокарда использовать и на каком методе диагностики остановиться.
Существующие критерии имеют различные недостатки и не учитывают возрастные, половые и расовые особенности в популяции. Согласно ультразвуковым критериям, двуслойный миокард, состоящий из трабекулярного и компактного слоев, является патогномоничным признаком некомпактного миокарда. Вместе с тем все больше исследователей предполагают возможность выявления трабекулярного миокарда в норме как во взрослой, так и в детской популяции [44].
Возможно повышение эффективности оценки трабекулярности (отношения трабекулярного слоя к компактному) ЛЖ при использовании модифицированной методики (2005), объединившей преимущества двух методов [45]:
1. Все измерения проводятся в позднюю диастолу — момент, когда граница между слоями достоверно различима.
2. Измерение отношения трабекулярного слоя (NC) к компактному слою ©.
3. Измерение проводятся в каждом трабекулярном сегменте согласно 16-сегментарной модели ЛЖ.
4. 3-й базальный сегмент, а также 9-й и 12-й; средние сегменты оцениваются в четырех- и пятикамерной позициях, остальные сегменты оцениваются в парастернальной позиции по короткой оси ЛЖ на уровне верхушки (апикальные сегменты), головок папиллярных мышц (средние сегменты) и митрального клапана (базальные сегменты).
МРТ — альтернатива ЭхоКГ в диагностике некомпактного миокарда. К достоинствам МРТ следует отнести меньшую зависимость результатов исследования от мастерства врача, возможность точной оценки всех сегментов миокарда, в том числе верхушки ЛЖ, а также правого желудочка. Недостатками являются ограничение всеобщей доступности этого метода и дороговизна. Использование внутривенных контрастных веществ для ультразвукового исследования позволяет улучшить визуализацию и облегчить определение границ эндокарда.
НМЛЖ наследуется по аутосомно-доминантному типу и может манифестировать с вероятностью до 50% у любого родственника первой степени родства, носителя генной мутации. Именно поэтому обследование членов семей больных НМЛЖ считают обязательным. Поиск мутаций в гене TAZ молекулярно-генетическими методами у больных, а также выявление гетерозиготного носительства у родственников пациента способны улучшить диагностику. Необходимо помнить, что семьям, в которых наблюдались случаи синдрома НЛМЖ, рекомендуется медико-генетическое консультирование.
Дифференциальную диагностику НЛМЖ проводят с гипертрофической кардиомиопатией, фиброэластозом, эндомиокардиальным фиброзом, миокардитом, тромбозомполости и локальной гипертрофией стенки ЛЖ, опухолями сердца, атрезией легочной артерии, синдромом Бланда—Уайта—Гарланда, добавочными хордами и трабекулами [15].
Лечение и прогноз
Основа терапевтической тактики у больных с «губчатым» миокардом — профилактика и лечение трех основных клинических проявлений: СН, аритмий и эмболических осложнений. В работе M. Toyono и соавт. [46] показано, что применение β-адреноблокатора карведилола улучшает диастолическую и систолическую функцию ЛЖ у больных с НМЛЖ, уменьшает степень гипертрофии и выраженность трабекулярности, что повышает прогноз и качество жизни больных. В то же время применение β-адреноблокатора бисопролола может иметь определенные преимущества: с одной стороны, как эффективного препарата при лечении и профилактике нарушений сердечного ритма [47, 48], с другой — как эффективного препарата в отношении лечения СН и профилактики ее осложнений, что подтверждено в крупных рандомизированных исследованиях [49, 50]. Некоторым больнымрекомендуется пересадка сердца, пациентам со «злокачественными» нарушениями ритма показана имплантация кардиовертера-дефибриллятора [51]. Максимальное количество таких пациентов, включенных в группы долгосрочного анализа, по данным литературы, не превышает 4 [51]. Также имеются сообщения о случаях лечения с применением методики сердечной ресинхронизирующей терапии (СРТ) у детей. K. Saito и соавт. [52] приводят пример успешного применения СРТ у 3-летней пациентки с изолированной формой НМЛЖ и узким комплексом QRS в сроки наблюдения до 2 лет.
Что касается антитромботической терапии у данной категории пациентов, далеко не у всех из них однозначным выбором являются антикоагулянты, так как нет проспективных исследований, которые продемонстрировали бы преимущества антикоагулянтной терапии и ее безопасность у пациентов с НМЛЖ, что порождает неопределенность в обсуждении данного вопроса и принятии окончательного решения в назначении антитромботической терапии [53]. Так, в одном из последних зарубежных исследований больных с некомпактной кардиомиопатией в соответствии с показаниями лишь 28,6% пациентов получали антикоагулянтную терапию [53], а в другом — большинство получали антиагреганты [54]. В то же время можно констатировать, что снижение фракции выброса ЛЖ, тромбоз полостей сердца, фибрилляция предсердий, эпизоды тромбоэмболии в анамнезе являются однозначными показаниями к назначению длительной антикоагулянтной терапии у данной категории пациентов [55].
Больным с различными видами аритмий, которые могут быть причиной ВСС и эмболических осложнений, необходимо ежегодно проводить холтеровское мониторирование, электрокардиографию, назначать антиаритмическую терапию, а при показаниях — имплантацию кардиовертера-дефибриллятора.
Прогноз пациентов с НМЛЖ зависит от объема пораженных сегментов, общей сократительной способности миокарда, времени возникновения и скорости нарастания симптомов С.Н. По данным I. Jedlinsky и соавт. [57], летальность больных с НМЛЖ в течение 6 лет была на уровне 50%. Из 34 больных, наблюдаемых в исследовании E. Oechslin и соавт. [33] на протяжении 44 мес, умерли 12 (у 6 больных диагностирована ВСС, у 4 — терминальная СН), 4 пациентам произведена трансплантация сердца, 4 установлен кардиовертер-дефибриллятор. По данным C. Lilje и соавт. [17], в детской популяции за 12 мес наблюдения летальность больных с НМЛЖ составила 17,1%. М. Ritter и соавт. [1] отметили, что из 17 пациентов умерли 8 (47%), 2 была произведена трансплантация сердца. Особенно негативный прогноз наблюдали у пациентов с фракцией выброса ЛЖ менее 35%.
Заключение
Хочется отметить, что изолированный «губчатый» миокард ЛЖ — редко встречаемое заболевание, приводящее к развитию С.Н. Поскольку существуют клинически здоровые лица, у которых выявляется характерная картина «губчатого» миокарда, по-видимому, эта патология становится предрасполагающей к развитию хронической СН при наличии дополнительных факторов (интоксикация, предельная физическая нагрузка и др.). Очевидно, описываемое состояние встречается чаще, чем выявляется, причем нередко эта патология не диагностируется в качестве причины смерти, а в статистике смертности скрывается за острой СН или другими заболеваниями. При своевременном выявлении НМЛЖ больные нуждаются в более тщательном диспансерном наблюдении и своевременном начале лечения. Возможно, молодые люди с повышенной трабекуляризацией ЛЖ также требуют особого внимания, поскольку с течением времени у них могут появляться признаки «губчатого» миокарда.
Авторы заявляют об отсутствии конфликта интересов.