Небиволол или метопролол что лучше
Две стороны одной медали. Бета-блокаторы: Нобелевская премия или сердечная блокада
Стимулирует сердечную деятельность выброс адреналина. Именно он учащает пульс, повышает давление и ускоряет ритм сердца и сосудов. Замедляется сердечная деятельность от дефицита подгоняющего его вещества. Пульс становится реже, давление снижается, от монотонного неторопливого постукивания сердца клонит ко сну. Такой отдых нашему мотору необходим как воздух: он позволяет накопить силы для следующего броска. Сегодня речь пойдёт о бета-блокаторах – лекарствах, которые, заботливо помогают сердцу отдыхать.
Таблетки, заслоняющие сердце от стресса
Группа препаратов, дающих сердцу полноценный отдых, заметно выделяется среди своего окружения, потому как все названия их заканчиваются на «лол». В основе их действия лежит снижение активности симпатической нервной системы, ответственной за яркую эмоциональную окраску стрессовых проявлений: гнева, тревоги, волнения и даже печали. Уменьшая их воздействие на сердце, мы даём ему возможность сокращаться реже, с меньшей силой и не так волноваться из-за недостатка кислорода. Волшебным образом исчезают приступы стенокардии и нарушения ритма, а риск внезапной смерти по вине сердца сводится к минимуму.
Рецепторы, на которые воздействует адреналин и подобные ему возбуждающие вещества (β1) находятся также в сосудистой стенке. Их блокада снимает напряжение сосудистой стенки, виновника повышения артериального давления, и дает сосудам передышку для восстановления сил.
Достояние Нобеля
Первый бета-блокатор – протеналол, синтезированный в 1962 году, не прошел этап экспериментальных исследований из-за возникновения случаев рака у мышей. А вот пропроналол, полученный в 1964 году, превзошел все ожидания. Американские ученые J. Black, G. Elion, G. Hutchings в 1988 году за разработку и обоснование механизма действия лекарств этой группы получили Нобелевскую премию.
На первых порах лекарство было задумано для лечения аритмии, и его способность снижать давление считалась второстепенной. Время показало, что важно и то, и другое.
Последнее поколение бета-блокаторов – небиволол – получен в 2001 году. К предыдущим свойствам таблетки добавился сосудорасширяющий эффект за счет выработки собственного оксида азота.
Сегодня в лечении мы применяем максимум 5 бета-блокаторов: метопролол, бисопролол, карведилол, бетаксалол, небиволол. Одни из них нормализуют цифры давления, другие – лечат стенокардию, третьи – нарушения сердечного ритма. Каждое новое поколение препаратов на порядок лучше предыдущих.
На что действуют бета-блокаторы
Назначают бета-блокаторы при:
Лекарства входят в комплексное лечение похмельного синдрома за счет их способности уменьшать проявления адреналинового выброса.
Как найти свою таблетку
К счастью, выбор препарата – искусство врача. В противном случае, вся польза от его применения сводится к нулю. Врач выбирает препарат, дозу (с учетом пульса и давления), кратность приема и его длительность.
Где таится опасность от приема бета-блокаторов
Две стороны одной медали. При правильном приеме лекарств – волшебство исцеления (достойное Нобелевской премии). Шаг в сторону – и волшебство улетучивается. Где найти ту дозу лекарства, от которой зависит равновесие? Пожалуй, на приеме у врача.
Бета-адреноблокаторы III поколения в лечении сердечно-сосудистых заболеваний
Современную кардиологию невозможно представить без препаратов группы бета-адреноблокаторов, которых в настоящее время известно более 30 наименований.
Современную кардиологию невозможно представить без препаратов группы бета-адреноблокаторов, которых в настоящее время известно более 30 наименований. Необходимость включения бета-адреноблокаторов в программу лечения сердечно-сосудистых заболеваний (ССЗ) очевидна: за последние 50 лет кардиологической клинической практики бета-адреноблокаторы заняли прочные позиции в профилактике осложнений и в фармакотерапии артериальной гипертонии (АГ), ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН), метаболическом синдроме (МС), а также при некоторых формах тахиаритмий. Традиционно в неосложненных случаях медикаментозное лечение АГ начинают с бета-адреноблокаторов и диуретиков, снижающих риск развития инфаркта миокарда (ИМ), нарушения мозгового кровообращения и внезапной кардиогенной смерти.
Концепция опосредованного действия лекарственных средств через рецепторы тканей различных органов была предложена N.?Langly в 1905 г., а в 1906 г. H.?Dale подтвердил ее в практике.
В 90-е годы было установлено, что бета-адренорецепторы подразделяются на три подтипа:
Способность блокировать влияние медиаторов на бета1-адренорецепторы миокарда и ослабление влияния катехоламинов на мембранную аденилатциклазу кардиомиоцитов с уменьшением образования циклического аденозинмонофосфата (цАМФ) определяют основные кардиотерапевтические эффекты бета-адреноблокаторов.
Антиишемический эффект бета-адреноблокаторов объясняется снижением потребности миокарда в кислороде, вследствие уменьшения частоты сердечных сокращений (ЧСС) и силы сердечных сокращений, возникающих при блокировании бета-адренорецепторов миокарда.
Бета-блокаторы одновременно обеспечивают улучшение перфузии миокарда за счет уменьшения конечного диастолического давления в левом желудочке (ЛЖ) и увеличения градиента давления, определяющего коронарную перфузию во время диастолы, длительность которой увеличивается в результате урежения ритма сердечной деятельности.
Антиаритмическое действие бета-адреноблокаторов, основанное на их способности уменьшать адренергическое влияние на сердце, приводит к:
Бета-адреноблокаторы повышают порог возникновения фибрилляции желудочков у больных острым ИМ и могут рассматриваться как средства профилактики фатальных аритмий в остром периоде ИМ.
Гипотензивное действие бета-адреноблокаторов обусловлено:
Препараты из группы бета-адреноблокаторов отличаются по наличию или отсутствию кардиоселективности, внутренней симпатической активности, мембраностабилизирующим, вазодилятирующим свойствам, растворимости в липидах и воде, влиянию на агрегацию тромбоцитов, а также по продолжительности действия.
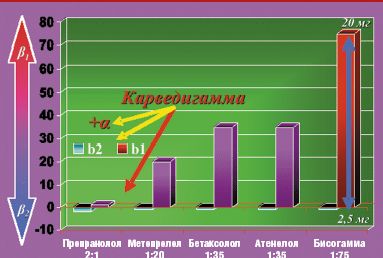
Влияние на бета2-адренорецепторы определяет значительную часть побочных эффектов и противопоказаний к их применению (бронхоспазм, сужение периферических сосудов). Особенностью кардиоселективных бета-адреноблокаторов по сравнению с неселективными является большое сродство к бета1-рецепторам сердца, чем к бета2-адренорецепторам. Поэтому при использовании в небольших и средних дозах эти препараты оказывают менее выраженное влияние на гладкую мускулатуру бронхов и периферических артерий. Следует учитывать, что степень кардиоселективности неодинакова у различных препаратов. Индекс ci/бета1 к ci/бета2, характеризующий степень кардиоселективности, составляет 1,8:1 для неселективного пропранолола, 1:35 — для атенолола и бетаксолола, 1:20 — для метопролола, 1:75 — для бисопролола (Бисогамма). Однако следует помнить, что селективность дозозависима, она снижается с повышением дозы препарата (рис. 1).
В настоящее время клиницисты выделяют три поколения препаратов с бета-блокирующим эффектом.
I поколение — неселективные бета1- и бета2-адреноблокаторы (пропранолол, надолол), которые наряду с отрицательными ино-, хроно- и дромотропными эффектами обладают способностью повышать тонус гладкой мускулатуры бронхов, сосудистой стенки, миометрия, что существенно ограничивает их использование в клинической практике.
II поколение — кардиоселективные бета1-адреноблокаторы (метопролол, бисопролол), благодаря высокой селективности в отношении бета1-адренорецепторов миокарда обладают более благоприятной переносимостью при длительном применении и убедительной доказательной базой долгосрочного прогноза жизни при лечении АГ, ИБС и ХСН.
В середине 1980-х годов на мировом фармацевтическом рынке появились бета-адреноблокаторы III поколения с низкой селективностью к бета1, 2-адренорецепторам, но с сочетанной блокадой альфа-адренорецепторов.
Препараты III поколения — целипролол, буциндолол, карведилол (его дженерический аналог с брендовым названием Карведигамма®) обладают дополнительными вазодилятирующими свойствами за счет блокады альфа-адренорецепторов, без внутренней симпатомиметической активности.
В 1982–1983 годах в научной медицинской литературе появились первые сообщения о клиническом опыте применения карведилола при лечении ССЗ.
Ряд авторов выявили протективное действие бета-адреноблокаторов III поколения на клеточные мембраны. Это объясняется, во-первых, ингибированием процессов перекисного окисления липидов (ПОЛ) мембран и антиоксидантным действием бета-блокаторов и, во-вторых, снижением влияния катехоламинов на бета-рецепторы. Некоторые авторы связывают мембранстабилизирующее действие бета-блокаторов с изменением проводимости натрия через них и ингибированием ПОЛ.
Указанные дополнительные свойства расширяют перспективы применения данных лекарственных средств, поскольку нивелируют характерное для первых двух поколений отрицательное влияние на сократительную функцию миокарда, углеводный и липидный обмен и в то же время обеспечивают улучшение перфузии тканей, позитивное влияние на показатели гемостаза и уровень оксидативных процессов в организме.
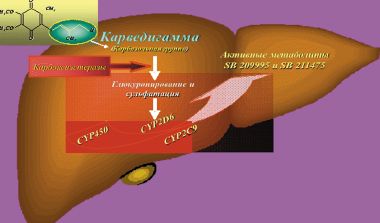
Карведилол метаболизируется в печени (глюкуронирование и сульфатация) с помощью ферментной системы цитохрома Р450, с использованием семейства ферментов — CYP2D6 и CYP2C9. Антиоксидантное действие карведилола и его метаболитов обусловлено наличием в молекулах карбазольной группы (рис. 2).
Метаболиты карведилола — SB 211475, SB 209995 угнетают ПОЛ в 40–100 раз активнее, чем сам препарат, а витамин Е — примерно в 1000 раз.
Применение карведилола (Карведигаммы®) при лечении ИБС
Согласно результатам целого ряда завершенных многоцентровых исследований, бета-адреноблокаторы оказывают выраженный антиишемический эффект. Необходимо отметить, что антиишемическая активность бета-адреноблокаторов соизмерима с активностью антагонистов кальция и нитратов, но, в отличие от этих групп, бета-адреноблокаторы не только улучшают качество, но и увеличивают продолжительность жизни пациентов с ИБС. Согласно результатам метаанализа 27 многоцентровых исследований, в которых приняло участие более 27 тыс. человек, селективные бета-адреноблокаторы без внутренней симпатомиметической активности у больных с острым коронарным синдромом в анамнезе снижают риск развития повторного ИМ и смертность от инфаркта на 20% [1].
Однако не только селективные бета-адреноблокаторы положительно влияют на характер течения и прогноз у пациентов с ИБС. Неселективный бета-адреноблокатор карведилол также продемонстрировал очень хорошую эффективность у больных со стабильной стенокардией. Высокая антиишемическая эффективность данного препарата объясняется наличием дополнительной альфа1-блокирующей активности, способствующей дилятации коронарных сосудов и коллатералей постстенотической области, а значит — улучшению перфузии миокарда. Кроме того, карведилол обладает доказанным антиоксидантным эффектом, связанным с захватом свободных радикалов, высвобождающихся в период ишемии, что обусловливает его дополнительное кардиопротекторное действие. Одновременно карведилол блокирует апоптоз (программируемая смерть) кардиомиоцитов в зоне ишемии, сохраняя объем функционирующего миокарда. Как было показано, метаболит карведилола (ВМ 910228) обладает меньшим бета-блокирующим эффектом, но является активным антиоксидантом, блокируя перекисное окисление липидов, «отлавливая» активные свободные радикалы OH–. Этот дериват сохраняет инотропный ответ кардиомиоцитов на Ca++, внутриклеточная концентрация которого в кардиомиоците регулируется Ca++-насосом саркоплазматического ретикулума. Поэтому карведилол оказывается более эффективным в лечении ишемии миокарда через ингибирование повреждающего действия свободных радикалов на липиды мембран субклеточных структур кардиомиоцитов [2].
Благодаря этим уникальным фармакологическим свойствам, карведилол может превосходить традиционные бета1-селективные адреноблокаторы в плане улучшения перфузии миокарда и способствовать сохранению систолической функции у больных ИБС. Как показано Das Gupta et al., у больных с дисфункцией ЛЖ и сердечной недостаточностью, развившейся вследствие ИБС, монотерапия карведилолом снижала давление наполнения, а также увеличивала фракцию выброса (ФВ) ЛЖ и улучшала показатели гемодинамики, при этом не сопровождаясь развитием брадикардии [3].
Согласно результатам клинических исследований у больных хронической стабильной стенокардией, карведилол снижает ЧСС в покое и при физической нагрузке, а также увеличивает ФВ в покое. Сравнительное исследование карведилола и верапамила, в котором принимало участие 313 пациентов, показало, что, по сравнению с верапамилом, карведилол в большей степени уменьшает ЧСС, систолическое АД и произведение ЧСС ´ АД при максимально переносимой физической нагрузке. Более того, карведилол обладает более благоприятным профилем переносимости [4].
Важно, что карведилол, по-видимому, более эффективен при лечении стенокардии, чем обычные бета1-адреноблокаторы. Так, в ходе 3-месячного рандомизированного многоцентрового двойного слепого исследования карведилол напрямую сравнивали с метопрололом у 364 пациентов со стабильной хронической стенокардией. Они принимали карведилол по 25–50 мг два раза в сутки или метопролол по 50–100 мг два раза в сутки [5]. В то время как оба препарата продемонстрировали хорошее антиангинальное и противоишемическое действие, карведилол более значительно увеличивал время до депрессии сегмента ST на 1 мм при физической нагрузке, чем метопролол. Переносимость карведилола была очень хорошей, и, что важно, при увеличении дозы карведилола не произошло заметных изменений типов нежелательных явлений.
Примечательно, что карведилол, не обладающий, в отличие от других бета-адреноблокаторов, кардиодепрессивным действием, улучшает качество и продолжительность жизни пациентов с острым ИМ (CHAPS) [6] и постинфарктной ишемической дисфункцией ЛЖ (CAPRICORN) [7]. Многообещающие данные были получены в ходе исследования Carvedilol Heart Attack Pilot Study (CHAPS) — пилотного исследования влияния карведилола на развитие ИМ. Это было первое рандомизированное исследование, в котором сравнивали карведилол с плацебо у 151 больного после острого ИМ. Лечение начинали в течение 24 часов с момента появления болей в грудной клетке, а дозу препарата увеличивали до 25 мг два раза в сутки. Главными конечными точками исследования были функция ЛЖ и безопасность препарата. Больных наблюдали в течение 6 месяцев с момента начала заболевания. Согласно полученным данным, частота развития серьезных кардиальных событий уменьшилась на 49%.
Полученные в ходе исследования CHAPS эхографические данные 49 пациентов со сниженной ФВ ЛЖ (
А. М. Шилов*, доктор медицинских наук, профессор
М. В. Мельник*, доктор медицинских наук, профессор
А. Ш. Авшалумов**
*ММА им. И. М. Сеченова, Москва
**Клиника Московского института кибернетической медицины, Москва
Обзор таблеток от повышенного давления нового поколения
Частое повышение показателей артериального давления (АД) – причина развития серьезных заболеваний (инсульт, инфаркт миокарда и пр.). Гипертоническая болезнь в России диагностируется у каждого третьего человека преклонного возраста. Для борьбы с гипертонией многим пациентам приходится принимать препараты на протяжении всей жизни, чтобы исключить осложнения.
Современные фармакологические компании предлагают большой выбор лекарственных средств, эффективных при гипертонии. Если не знаете, как выбрать таблетки от повышенного давления, ознакомьтесь с рейтингом, представленным ниже. В ТОП вошли лучшие медикаменты с учетом эффективности, стоимости и отзывов.
Классификация препаратов от повышенного давления
Причины гипертонии
Когда нужно вызвать врача на дом при повышении давления?
Общепринятые показатели АД – 120/80. Параметры могут незначительно варьировать в зависимости от времени суток, физической активности и возраста человека.
Таблица – Показатели артериального давления и рекомендации
Небиволол – b–адреноблокатор третьего поколения в лечении сердечно–сосудистых заболеваний
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Блокаторы b–адренергических рецепторов используются при лечении различных сердечно–сосудистых заболеваний в течение более 45 лет. Первый b–адреноблокатор (b–АБ) дихлоризопротеренол был создан в конце 50–х годов ХХ века, однако из–за выраженной внутренней симпатомиметической активности (ВСА) он оказался непригодным для клинического применения. В 1964 г. опубликованы первые сообщения о применении b–АБ без ВСА пропранолола при лечении стенокардии напряжения и артериальной гипертензии (АГ). Руководителем исследований, которые привели в начале 60–х годов прошлого века к созданию первых b–АБ, был J. W. Black, в 1988 г. удостоенный Нобелевской премии за свои работы в этой области.
За прошедшие десятилетия созданы несколько десятков препаратов со свойствами b–АБ, из которых лишь около 10 выдержали испытание временем. Первые b–АБ (пропранолол и др.) были неселективными, т.е. блокировали как b1–адренорецепторы сердца, так и b2–адренорецепторы сосудов и бронхов. В 70–е годы прошлого века появились кардиоселективные, или, по современной терминологии, b1–селективные блокаторы атенолол и метопролол, которые гораздо лучше переносились, чем пропранолол, и потому получили название b–АБ второго поколения. Позже были синтезированы b–АБ с особыми полезными свойствами, которых не было у препаратов первого и второго поколений. Эти препараты были названы M. Bristow и соавт. [1,2] b–АБ третьего поколения (табл. 1).
Не все b–АБ первого, второго и третьего поколений выдержали испытание временем. Ненужными оказались окспренолол и пиндолол, как препараты, не оказывающего кардиопротективного действия у больных, перенесших инфаркт миокарда, из–за наличия ВСА. Ненужными оказалось большинство гидрофильных b–АБ, поскольку в отличие от липофильных препаратов без ВСА они также не оказывали кардиопротективного действия. После отрицательных результатов рандомизированного плацебо–контролируемого исследования BEST с фармацевтического рынка был отозван гидрофильный b–АБ с сосудорасширяющим действием буциндолол, который M. Bristow отнес к третьему поколению b–АБ. В результате в настоящее время лишь два из b–АБ третьего поколения доказали свое несомненное превосходство над препаратами первого и второго поколения, одним из которых является суперселективный b–АБ с вазодилатирующими свойствами небиволол (Небилет).
Классификация b–адреноблокаторов
b–АБ представляют собой весьма неоднородную по своим фармакологическим эффектам группу лекарственных препаратов, единственным общим свойством которых является конкурентный антагонизм в отношении b1–адренергических рецепторов.
Наряду с блокадой b1–адренергических рецепторов b–АБ могут блокировать или не блокировать b2–адренорецепторы. В первом случае говорят о неселективных b–АБ, во втором – о b1–селективных препаратах.
Строго говоря, в настоящее время различают не два, а по меньшей мере, три подтипа b–адренергических рецепторов – b1, b2 и b3. b3–адренорецепторы обнаружены в миокарде, эндотелиальных клетках сосудов и коричневой жировой ткани (табл. 2). В миокарде b3–адренорецепторы опосредуют отрицательное инотропное действие катехоламинов. В сосудистой стенке через b3–адренорецепторы реализуется сосудорасширяющее действие катехоламинов, опосредованное высвобождаемым из эндотелия оксидом азота и циклическим гуанозинмонофосфатом в гладкомышечных клетках.
b3–адренорецепторы, которые располагаются на мембранах адипоцитов (жировых клеток), опосредуют стимулирующее действие катехоламинов на липолиз и термогенез. По некоторых данным, гипофункция b3–адренорецепторов, связанная с мутацией гена, ответственного за их синтез, сочетается с патологическим ожирением и ранним развитием сахарного диабета 2 типа. В эксперименте продемонстрирована высокая эффективность агонистов b3–адренергических рецепторов при лечении ожирения.
Из применяемых в клинической практике b–АБ лишь о пропранололе и пиндололе известно, что они одновременно блокируют не только b1– и b2–, но и b3–адренергические рецепторы. Поэтому пропранолол и пиндолол – менее всего подходят для лечения сердечно–сосудистых заболеваний у больных с ожирением, поскольку вызывают нежелательные эффекты, связанные с торможением активности как b2–, так и b3–адренергических рецепторов.
Помимо b1–селективности (или кардиоселективности, как называли это свойство раньше), b–АБ различаются по наличию или отсутствию ВСА, липофильности, вазодилатирующего, мембраностабилизирующего, антиагрегантного действия и т. д.
Общепринятой классификации b–АБ не существует. Препараты, применяемые для длительной терапии АГ, удобно разделить на следующие группы в зависимости от наличия или отсутствия вазодилатирующих свойств и b1–адреноселективности:
1. b–АБ без вазодилатирующих свойств:
а) неселективные (пропранолол, надолол, окспренолол, соталол, тимолол и др.);
б) b1–селективные (атенолол, бетаксолол, бисопролол, метопролол и др.).
2. b–АБ с вазодилатирующими свойствами:
а) неселективные (карведилол, лабетолол, пиндолол, буциндолол и др.);
б) b1–селективные (небиволол, целипролол и др.) [3–6].
Клиническое значение
вазодилатирующих свойств
и липофильности b–адреноблокаторов
У большинства больных АГ общее периферическое сосудистое сопротивление (ОПСС), как известно, повышено. ОПСС повышено также у многих больных хронической сердечной недостаточностью (ХСН), обусловленной систолической дисфункцией левого желудочка (ЛЖ). Поэтому при прочих равных условиях для длительной терапии этих заболеваний явно предпочтительнее применение b–АБ с вазодилатирующими свойствами. Следует, правда, учитывать, что механизмы сосудорасширяющего действия различных «вазодилатирующих» b–АБ неодинаковы.
Вазодилатация может быть обусловлена четырьмя основными механизмами (по отдельности и в комбинации друг с другом): 1) выраженной ВСА в отношении b2–адренорецепторов сосудов (как, например, у пиндолола и целипролола); 2) a1– и (или) a2–адренорецепторов (как у карведилола и лабетолола); 3) высвобождением из эндотелиальных клеток оксида азота, обладающего вазодилатирующими свойствами (как у небиволола); и 4) прямым сосудорасширяющим действием [4,5].
У некоторых «вазодилатирующих» b–АБ механизм сосудорасширяющего действия, как правило, сложный. Так, предполагают, что в основе вазодилатации, вызываемой лабетололом, лежит не только блокада a1–адренорецепторов, но и некоторая ВСА в отношении b2–адренорецепторов. Вазодилатирующее действие буциндолола связывают с a1–адреноблокадой и прямым сосудорасширяющим действием.
У некоторых «вазодилатирующих» b–АБ механизм сосудорасширяющего действия, как правило, сложный. Так, предполагают, что в основе вазодилатации, вызываемой лабетололом, лежит не только блокада a1–адренорецепторов, но и некоторая ВСА в отношении b2–адренорецепторов. Вазодилатирующее действие буциндолола связывают с a1–адреноблокадой, прямым сосудорасширяющим действием и отчасти ВСА.
Установлено, что сосудорасширяющее действие суперселективного b–АБ небиволола, речь о котором пойдет ниже, связано с влиянием препарата на систему L–аргинин–оксид азота в эндотелии сосудов. В исследованиях на животных, здоровых лицах и больных с АГ показано, что небиволол увеличивает экспрессию гена, ответственного за синтез нитрооксид–синтетазы, что ведет к увеличению образования и высвобождения оксида азота из эндотелиальных клеток. Клеточные механизмы сосудорасширяющего действия небиволола, однако, не до конца изучены. Предполагается несколько механизмов активации небивололом системы L–аргинин–оксид азота в эндотелии сосудов – через стимуляцию b2– или b3–адренорецепторов сосудов, через стимуляцию серотониновых рецепторов типа 5–HT1A или через взаимодействие с механизмами, опосредуемыми эстрогеновыми рецепторами [7–9].
Небиволол как вещество с антиоксидантными свойствами, по–видимому, также уменьшает инактивацию оксида азота свободными радикалами. В результате уменьшения деградации оксида азота увеличивается его доступность [9,10].
Механизм сосудорасширяющего действия «вазодилатирующих» b–АБ имеет клиническое значение. Так, есть основания предполагать, что «вазодилатирующие» b–АБ с выраженной ВСА в отношении b2–адренорецепторов (пиндолол, целипролол и др.) не оказывают кардиопротективного действия. Поэтому их применение менее предпочтительно или даже опасно у больных с высоким риском, например, у больных ХСН или больных, перенесших инфаркт миокарда.
Опыт применения пиндолола у больных, перенесших инфаркт миокарда, дают основание усомниться в наличии кардиопротективного действия у «вазодилатирующих» b–АБ, сосудорасширяющее действие которых связано с ВСА в отношении b2–адренорецепторов (т.е. у пиндолола, буциндолола и целипролола). Это объясняют тем, что b–АБ с ВСА могут оказывать стимулирующее действие на сердце, поскольку в условиях пониженной активности симпатико–адреналовой системы (например, ночью) они действуют, как агонисты b–адренорецепторов. У больных ИБС вызываемое блокаторами с ВСА увеличение ЧСС в ночное время может спровоцировать развитие приступа стенокардии. Поэтому блокаторы с ВСА не рекомендуется использовать для длительной терапии у больных, перенесших инфаркт миокарда.
К сожалению, клиническая эффективность b–АБ с вазодилатирующими свойствами недостаточно изучена в длительных контролируемых исследованиях. В частности, до сих пор неизвестно, все ли они обладают кардиопротективным действием, которое, судя по результатам рандомизированных исследований, присуще таким b–АБ без вазодилатирующих свойств, как пропранолол, тимолол, метопролол и др. [11].
Из «вазодилатирующих» b–АБ без ВСА в отношении b2–адренорецепторов наиболее хорошо изучена эффективность и безопасность лишь карведилола, небиволола, а также буциндолола и целипролола. В нескольких рандомизированных плацебо–контролируемых исследованиях оценивалось влияние этих b–АБ с вазодилатирующими свойствами на течение и исходы ХСН.
По сводным данным трех рандомизированных плацебо–контролируемых исследований, добавление карведилола снижает смертность больных ХСН в среднем на 41%.
Кардиопротективный эффект небиволола у больных ХСН, обусловленной систолической дисфункцией ЛЖ, был продемонстрирован в рандомизированном плацебо–контролируемом исследовании SENIORS (см. ниже).
С другой стороны, третий «вазодилатирующий» b–АБ буциндолол оказался неэффективным при ХСН, несмотря на то, что, по сводным данным четырех небольших исследований, добавление буциндолола недостоверно снижает смертность больных ХСН (в среднем на 17%). Дело в том, что летом 1999 г. было преждевременно прекращено крупное рандомизированное плацебо–контролируемое исследование BEST (Beta–blocker Evaluation Survival Trial) после того, как была обнаружена недостаточная эффективность буциндолола у больных тяжелой ХСН (IV функционального класса или с фракцией выброса ЛЖ меньше 20%) и повышенная смертность в подгруппе негров с ХСН (в среднем на 17%; р>0,05).
В небольшом рандомизированном плацебо–контролируемом исследовании CELICARD четвертый «вазодилатирующий» b–АБ целипролол не оказывал существенного влияния на функциональный класс больных ХСН и показатели, а также не улучшал выживаемости [12–14].
Эти данные дают основание усомниться как в наличии у буциндолола и целипролола кардиопротективного действия, так и в том, что все b–АБ могут в одинаковой мере использоваться при лечении больных ХСН, а возможно, и больных с АГ.
Общими свойствами b–АБ с кардиопротективным действием, таких как пропранолол, тимолол, бисопролол, метопролол, карведилол и небиволол, являются липофильность и отсутствие ВСА независимо от b1–селективности. Учитывая, что в отличие от «кардиопротективных» b–АБ буциндолол и целипролол обладают гидрофильными свойствами и ВСА, можно предполагать, что для лечения не только инфаркта миокарда и ХСН, но и АГ следует использовать лишь липофильные b–АБ, не обладающие ВСА.
Данные о степени липофильности отдельных b–АБ противоречивы, что объясняется различиями в методах ее определения [3,6,16–18]. Тем не менее небиволол, вне всякого сомнения, входит в число b–АБ с наибольшей липофильностью, с которой связывают кардиопротективное действие b–АБ.
Клиническое значение b1–селективности b–адреноблокаторов
Из b–АБ без вазодилатирующих свойств и ВСА для длительной терапии АГ и ХСН наиболее подходят b1–селективные препараты.
b1–селективные препараты, по определению, оказывают минимальное влияние на b2–адренорецепторы, опосредующие в основном полезные эффекты катехоламинов на сосуды (вазодилатация), бронхи (бронходилатация), печень (усиление гликогенолиза и глюконеогенеза), поджелудочную железу (секреция инсулина) и липиды (расщепление триглицеридов до свободных жирных кислот) [3, 5, 6] (табл. 2).
В частности, b1–селективные препараты в меньшей степени, чем неселективные b–АБ, влияют на ОПСС, поскольку не блокируют b2–адренорецепторы, которые опосредуют дилатацию артерий и артериол. Между тем известно, что ОПСС повышено у большинства больных с АГ и ХСН и потому дальнейшее его повышение под влиянием b–АБ особенно нежелательно, так как создает дополнительную посленагрузку на ЛЖ.
Кроме того, при лечении b1–селективными блокаторами вазоконстрикторная реакция на катехоламины выражена слабее, чем при лечении неселективными препаратами. Эта вазоконстрикторная реакция на катехоламины, иногда проявляющаяся резким подъемом АД, наблюдается при психоэмоциональном стрессе, курении сигарет, употреблении кофеина (с кофе или чаем), гипогликемии (у больных сахарным диабетом), а также после внезапной отмены клонидина и других агонистов центральных a2–адренорецепторов.
b1–селективные адреноблокаторы более безопасны у больных хроническим обструктивным заболеванием легких (ХОБЛ) и в меньшей степени ухудшают метаболизм глюкозы и липидный состав крови, чем неселективные b–АБ. К тому же есть мнение, что антигипертензивное действие b1–селективных препаратов несколько более выражено, чем действие неселективных b–АБ [3].
b–АБ, блокируя b2–адренорецепторы b–клеток поджелудочной железы, уменьшают секрецию инсулина, что сопровождается повышением базальных уровней глюкозы. По некоторым наблюдениям, b–АБ, как и тиазидные диуретики, увеличивают риск развития сахарного диабета у предрасположенных больных [5,6,19]. Поэтому b–АБ (в особенности неселективные) не рекомендуется использовать в качестве антигипертензивных препаратов первого ряда у больных с предрасположенностью к развитию сахарного диабета.
Мобилизация глюкозы из печени в ответ на гипогликемию опосредуется в основном b2–адренорецепторами. Поэтому гипогликемические реакции на введение инсулина или прием пероральных антидиабетических средств у больных сахарным диабетом при лечении b1–селективными блокаторами встречаются гораздо реже, чем при лечении неселективными препаратами.
Поэтому применение b1–селективных адреноблокаторов более безопасно при лечении АГ и ХСН у больных ХОБЛ, облитерирующим атеросклерозом артерий нижних конечностей, сахарным диабетом 1 и 2 типа и гипертриглицеридемией.
Чем выше b1–селективность b–блокатора, тем незначительнее его влияние на эффекты катехоламинов, опосредуемые b2–адренорецепторами. Поэтому такое важное клиническое значение имеет степень b1–селективности b–АБ.
Исследования in vitro с тканями животных показали, что из имеющихся в настоящее время b–АБ наибольшей b1–селективностью (в сравнении с b2–адренорецепторами) обладает небиволол (табл. 3).
У атенолола, бетаксолола, метопролола и целипролола b1–селективность умеренная. Так, по данным литературы [20], индекс b1–селективности у небиволола составляет 1:300, у целипролола – 1:72, у бетаксолола – 1:35–40, у метопролола – 1:25–80 и у атенолола – 1:15–35. Небольшая b1–селективность ацебутолола и карведилола (7:1), по–видимому, не имеет клинического значения при назначении терапевтических доз препаратов.
Недавно опубликованы результаты исследования b1–селективности небиволола, бисопролола и карведилола in vitro с тканями сердца человека. В целом они согласуются с результатами, полученными на тканях животных, и свидетельствуют о том, что небиволол – наиболее b1–селективный из доступных в настоящее время b–АБ. Его b1–селективность составляет 1:22–46, что примерно в 3,5 раз выше, чем у бисопролола (1:6–16) [21,22].
Таким образом, по b1–селективности небиволол превосходит все другие доступные b1–адреноблокаторы, и потому его иногда называют суперселективным b–АБ.
Небиволол, как суперселективный b1–адреноблокатор, оказывает наименьшее влияние на бронхи, сосуды и печень, а также на метаболизм глюкозы и липидов по сравнению с менее b1–селективными препаратами, такими, например, как атенолол и метопролол. По этой причине он гораздо лучше переносится при длительном применении, чем другие b1–адреноблокаторы. Это продемонстрировано в нескольких сравнительных исследованиях [6,7,23–26].
Суперселективный b1–адреноблокатор, каким является небиволол, оказывает минимальное влияние не только на b2–адренорецепторы, но и на b3–адренорецепторы, опосредующие, в частности, эндотелий–зависимую вазодилатацию в ответ на катехоламины (в том числе в кавернозных телах полового члена), а также липолиз и термогенез в коричневой жировой ткани [5,27] (табл. 2). В результате небиволол (в отличие от атенолола и метопролола) не вызывает эректильной дисфункции у мужчин с АГ и не способствует увеличению веса. Поэтому он может считаться b–АБ первого ряда для длительного лечения сексуально активных мужчин, а также больных с метаболическим синдромом и сахарным диабетом 2 типа, не говоря уже о больных ХОБЛ. Следовательно, небиволол является липофильным суперселективным b1–адреноблокатором без ВСА, который оказывает минимальное влияние на функциональную активность не только на b2–, но и на b3–адренорецепторов.
Таким образом, небиволол обладает пятью клинически значимыми свойствами, которые выделяют его среди доступных в настоящее время b–АБ: сверхвысокая b1–селективность, сосудорасширяющее действие, высокая липофильность, отсутствие ВСА и, по–видимому, отсутствие влияния на b3–адренорецепторы. Ни один другой b–АБ не обладает всеми этими свойствами в совокупности.
Терапевтическое
применение небиволола
Благодаря своим разнообразным фармакологическим свойствам b–АБ широко используются при лечении АГ, стабильной стенокардии напряжения, а также в качестве средства для вторичной профилактики после инфаркта миокарда. Некоторые из b–АБ наряду с ингибиторами АПФ в настоящее время составляют основу медикаментозной терапии ХСН, обусловленной систолической дисфункцией левого желудочка. По всем этим показаниям применяется также небиволол (Небилет). Липофильный суперселективный b1–адреноблокатор с вазодилатирующими свойствами, но без ВСА небиволол имеет ряд клинически важных преимуществ перед другими b–АБ. Он переносится гораздо лучше, чем другие b1–адреноблокаторы, поскольку в меньшей степени вызывает нежелательные гемодинамические и метаболические нарушения, а также не оказывает существенного влияния на бронхиальную проходимость и эректильную функцию. Кроме того, это один из немногих b–АБ, применение которых не только безопасно, но и полезно у больных систолической дисфункцией ЛЖ (фракция выброса меньше 35–40%). В результате невиболол имеет значительно меньше ограничений для клинического использования, чем многие другие b–АБ.
Небиволол в лечении
артериальной гипертензии
Длительное лечение АГ – основное показание для назначения b–АБ вообще и небиволола (Небилета), в частности. В современных рекомендациях по лечению АГ b–АБ (наряду с диуретиками, ингибиторами АПФ, антагонистами кальция и блокаторами АТ1–ангиотензиновых рецепторов) рассматриваются как один из основных классов антигипертензивных средств, которые пригодны для длительного лечения как в качестве монотерапии, так и в комбинации с другими препаратами. Блокаторы b–адренорецепторов являются препаратами выбора для длительного лечения АГ у больных ИБС, особенно после перенесенного инфаркта миокарда.
Среди современных b–АБ небиволол выделяется тем, что сочетает высокую антигипертензивную эффективность, благоприятное влияние на нарушения центральной и внутрисердечной гемодинамики и превосходную переносимость.
Антигипертензивная эффективность и безопасность небиволола при мягкой и умеренной формах гипертонической болезни изучалась в нескольких контролируемых исследованиях в сравнении с плацебо и другими антигипертензивными препаратами [8,9].
Так, в рандомизированном плацебо–контролируемом исследовании показано, что антигипертензивный эффект небиволола увеличивается в диапазоне от 2,5 до 10 мг/сут., причем не было существенных различий в антигипертензивной эффективности 5 мг и 10 мг небиволола в сутки [8,28]. Это позволило считать оптимальной дозой небиволола – 5 мг/сут. В этой дозе небиволол снижает систолическое АД в среднем на 11–27 мм рт.ст. и диастолическое АД – на 12–18 мм рт.ст. Лишь у пожилых людей и больных почечной недостаточностью начальная доза препарата составляет 2,5 мг/сут. и в дальнейшем может быть повышена до 5 мг/сут.
В многоцентровых рандомизированных исследованиях показано, что монотерапия небивололом (5 мг/сут.) позволяет получить хороший клинический эффект (снижение диастолического АД ниже 90 мм рт.ст.) у 59–100% больных с мягкой и умеренной формами гипертонической болезни. Антигипертензивный эффект препарата обнаруживается уже через 2 недели после начала терапии и нарастает к концу 4 недели терапии. Антигипертензивный эффект небиволола не ослабевает после 12 месяцев терапии, т.е. при длительном применении толерантности к препарату не развивается. Внезапная отмена небиволола не приводит к возникновению рикошетной гипертензии. В течение 1 месяца после прекращения терапии небивололом АД постепенно повышается, однако не достигает исходных значений [8,9,28].
Небиволол одинаково эффективен у больных как среднего, так и пожилого возраста. Его антигипертензивная эффективность не зависит от наличия или отсутствия сахарного диабета или гипертрофии ЛЖ, а также массы тела больного, курения и злоупотребления алкоголем [8].
При недостаточной антигипертензивной эффективности небиволол, как и другие b–АБ, комбинируют с антагонистами кальция дигидропиридинового ряда. Установлена также аддитивность антигипертензивных эффектов небиволола и тиазидного диуретика гидрохлортиазида. В то же время не обнаружено усиления антигипертензивного действия небиволола при добавлении ингибитора АПФ эналаприла [9].
Важным достоинством небиволола является его способность при приеме один раз в сутки эффективно и равномерно снижать АД на протяжении 24 часов, не изменяя естественного суточного ритма колебаний АД и предотвращая подъем АД в ранние утренние часы [28–31].
Как известно, для объективной оценки длительности и равномерности антигипертензивного эффекта лекарственных препаратов длительного действия в 1988 г. Управлением по контролю за качеством пищевых продуктов и лекарственных препаратов США (Food and Drugs Administration – FDA) был использован особый показатель – отношение остаточного (конечного) эффекта к наибольшему (пиковому) эффекту. Остаточный эффект (ОЭ) – это степень снижения АД в конце междозового интервала (т.е. через 24 ч после приема препарата – при назначении антигипертензивных препаратов, принимаемых 1 раз в сутки). Наибольший эффект (НЭ) – это степень снижения АД на максимуме действия данного препарата. Величина как ОЭ, так и НЭ рассчитывается с поправкой на эффект плацебо. Считается, что величина отношения ОЭ/НЭ для новых антигипертензивных препаратов должна быть не менее 50% (или 0,50).
По мнению P. Meredith [32], в идеале величина отношения ОЭ/НЭ должна превышать 60%. Чем ближе величина отношения ОЭ/НЭ к 100% (или 1,00), тем равномернее антигипертензивное действие препарата в течение суток, а значит, меньше вариабельность АД, которая, как известно, является одним из факторов риска развития сердечно–сосудистых осложнений.
Средние значения отношения ОЭ/НЭ для диастолического АД у небиволола в дозе 5 мг/сут. составляют 84–89% [28,29,33].
Это означает, что через 24 часа после приема небиволола сохраняется до 90% его антигипертензивной эффективности, и свидетельствует об отсутствии существенных колебаний в антигипертензивной эффективности препарата на протяжении суток. Отношение ОЭ/НЭ у небиволола – одно из самых высоких среди современных антигипертензивных препаратов и сравнимо с величиной отношения ОЭ/НЭ или превосходит его у таких антигипертензивных препаратов длительного действия, как b–АБ бетаксолол, антагонисты кальция амлодипин и лацидипин, ингибиторы АПФ лизиноприл и трандолаприл или блокаторы АТ1–ангиотензиновых рецепторов кандесартан и тельмисартан.
Следовательно, небиволол вполне удовлетворяет требованиям, которые FDA предъявляет к современным антигипертензивным препаратам длительного действия.
Антигипертензивная эффективность и переносимость небивололола сравнивались с таковыми других b1–адреноблокаторов, таких как атенолол, бисопролол и метопролол [9]. В большинстве сравнительных исследований длительностью от 4 до 24 недель небиволол назначался в суточной дозе 5 мг, атенолол – 50–100 мг, бисопролол – 5 мг и метопролол – 100 мг. Выраженность антигипертензивного действия небиволола, судя по степени снижения систолического и диастолического АД и доле больных, ответивших на терапию, не отличалась от других изучавшихся b1–адреноблокаторов.
Нельзя не отметить, что переносимость небиволола было значительно лучше, чем у других селективных b1–адреноблокаторов. В среднем при лечении небивололом побочные эффекты отмечались в 1,5 раза реже, а побочные эффекты, связанные с приемом препаратов, почти в 3 раза реже, чем при лечении атенололом, бисопрололом и метопрололом (8,2 и 20,4% соответственно).
Превосходная переносимость небиволола при АГ объясняется как его b1–суперселективностью, так и дополнительным сосудорасширяющим действием, опосредуемым оксидом азота.
В нескольких рандомизированных исследованиях двойным слепым методом сравнивали эффективность небиволола с антигипертензивными препаратами других классов [8,9,25,29,33,34]. Установлено, что по антигипертензивной эффективности небиволол (5 мг/сут.) вполне сравним с ингибиторами АПФ эналаприлом (10 мг/сут.) и лизиноприлом (20 мг/сут.), антагонистами кальция амлодипином (5–10 мг/сут.) и нифедипином–ретард (40 мг/сут.) и блокатором АТ1–ангиотензиновых рецепторов лозартаном (50 мг/сут.). Нормализация АД с одинаковой частотой достигалась среди больных, леченных небивололом, и больных, получавших другие антигипертензивные препараты (37–91% против 42–87%).
При длительном назначении небиволол вызывает обратное развитие гипертрофии ЛЖ у больных АГ, причем в этом отношении он не уступает блокатору АТ1–ангиотензиновых рецепторов телмисартану. У больных с АГ небиволол улучшает диастолическую функцию ЛЖ и увеличивает ударный объем сердца, не вызывая при этом (в отличие от атенолола) уменьшения сердечного выброса [9,26,31,34].
У больных АГ небиволол значительно уменьшает ОПСС, причем это уменьшение значительно больше, чем вызываемое бисопрололом, при одинаковой степени снижения АД. Небиволол, по–видимому, вызывает обратное развитие эндотелиальной дисфункции, которая встречается не только при АГ, но и при сахарном диабете и гиперхолестеринемии. Кроме того, он уменьшает податливость стенки аорты и крупных артерий, которая, по современных представлениям, сочетается с неблагоприятным прогнозом у больных с АГ [8,9,34].
У больных с АГ и нарушенной толерантностью к глюкозе чувствительность тканей к инсулину значительно снижается при лечении атенололом, но не изменяется при лечении небивололом по сравнению с плацебо. В другом исследовании у больных АГ, но без резистентности к инсулину небиволол (но не метопролол) значительно повышал чувствительность к инсулину. У больных сахарным диабетом 2 типа он не влияет на контроль за гликемией, но уменьшают экскрецию альбуминов с мочой. Небиволол не оказывает существенного влияния на липидный состав крови [9,26,31,34 ].
Все это позволяет использовать небиволол для лечения АГ у гораздо большего числа больных с сопутствующими заболеваниями, чем многие другие b–АБ.
Небиволол в лечении хронической
сердечной недостаточности
ХСН, обусловленная систолической дисфункцией ЛЖ, долгое время считалась противопоказанием для назначения b–АБ. В 70–е годы прошлого века появились первые сообщения о том, что b–АБ не только безопасны при ХСН, но и могут улучшать ее течение и исходы. В 90–е годы было выполнено несколько рандомизированных плацебо–контролируемых исследований, в которых было показано, что некоторые b–АБ, а именно бисопролол, карведилол и метопролол способны улучшать выживаемость больных ХСН, обусловленной систолической дисфункцией ЛЖ, а также уменьшать их потребность в госпитализации. Общими свойствами трех b–АБ с доказанной эффективностью являются липофильность и отсутствие ВСА [13].
Высокая липофильность небиволола, его сосудорасширяющее действие и отсутствие ВСА делает перспективным его применение при лечении больных с ХСН. Кроме того, данные небольших исследований указывают на то, что небиволол улучшает показатели систолической и диастолической функций ЛЖ у больных с дилатационной кардиомиопатией и, в том числе, достоверно увеличивает его фракцию выброса. В частности, в рандомизированном плацебо–контролируемом исследовании ENECA [35] показано, что у пожилых больных ХСН, обусловленной систолической дисфункцией ЛЖ, после 8 месяцев лечения небивололом (до 10 мг/сут.) фракция выброса ЛЖ достоверно увеличивается с 25,4 до 31,9%. Частота побочных эффектов при назначении небиволола и плацебо была практически одинаковой, что свидетельствует о превосходной переносимости b–АБ у пожилых больных с ХСН, обусловленной систолической дисфункцией ЛЖ.
Недавно было завершено крупное рандомизированное плацебо–контролируемое исследование, в котором оценивались эффективность и безопасность небиволола при ХСН у пожилых больных с различной фракцией выброса ЛЖ. Это – исследование SENIORS (Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors heart failure), в котором участвовали 2128 больных в возрасте 70 лет и старше [36,37]. Систолическая дисфункция ЛЖ (фракция выброса 35% или меньше) была у 65% больных. Первичными конечными точками были общее число случаев смерти или госпитализации в связи с сердечно–сосудистыми причинами. Начальная доза небиволола составляла 1,25 мг/сут.; при переносимости ее в течение 16 недель повышали до 10 мг/сут. Длительность наблюдения составила в среднем 21 мес. Средняя доза небиволола составила 7,7 мг/сут.
Полученные в исследовании SENIORS данные свидетельствуют о том, что небиволол достоверно уменьшает общее число случаев смерти или госпитализаций в связи с сердечно–сосудистыми причинами (в среднем на 14% по сравнению с плацебо). Общая смертность снизилась под влиянием небиволола в среднем на 12% (р=0,21), а сердечно–сосудистая смертность – на 16% (р=0,17).
Дальнейший анализ результатов исследования SENIORS показал, что небиволол был особенно эффективным в подгруппе больных моложе 75 лет и с фракцией выброса ЛЖ не более 35% – уменьшение общего числа случаев смерти или госпитализаций в связи с сердечно–сосудистыми причинами в среднем на 27%. В этой подгруппе общая смертность снизилась под влиянием небиволола в среднем на 38%, т. е. небиволол был сравним по эффективности с бисопрололом, карведилолом и метопрололом, эффективность и безопасность которых были установлены именно у больных с систолической дисфункцией ЛЖ преимущественно не старше 60–65 лет.
Таким образом, небиволол может считаться b–АБ первого ряда для длительного лечения ХСН у больных с систолической дисфункцией ЛЖ наряду с бисопрололом, карведилолом и метопрололом.
При дальнейшем анализе результатов исследования SENIORS обнаружено, что поддерживающая доза небиволола имеет важное значение в его влиянии на исходы ХСН [9]. Так, в подгруппе больных, у которых поддерживающая доза небиволола составляла 10 мг/сут. (а это 68% получавших небиволол и 80% получавших плацебо), b–АБ уменьшал общее число случаев смерти или госпитализаций в связи с сердечно–сосудистыми причинами в среднем на 27% (по сравнению с плацебо; р
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.