Зеленящие стрептококки
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику. Под наименованием «Зеленящие стрептококки или S.viridans» прячется целая группа микроорганизмов, относящихся к альфа-зеленящим стрептококкам семейства Streptococcaceae.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Под наименованием «Зеленящие стрептококки или S.viridans» прячется целая группа микроорганизмов, относящихся к альфа-зеленящим стрептококкам семейства Streptococcaceae. Эта группа является очень важным компонентом в составе нормально микрофлоры полости рта, слизистых оболочек дыхательных путей, пищеварительного тракта и половых органов. Поэтому обнаружив следующих ее представителей (S.gordonii, S.oralis, S. mutants, S.sanguis и S.salivarius) в посеве из полости рта, не надо немедленно начинать это лечить – этим вы только навредите организму, выбив из его состава важный компонент его нормальной микрофлоры.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
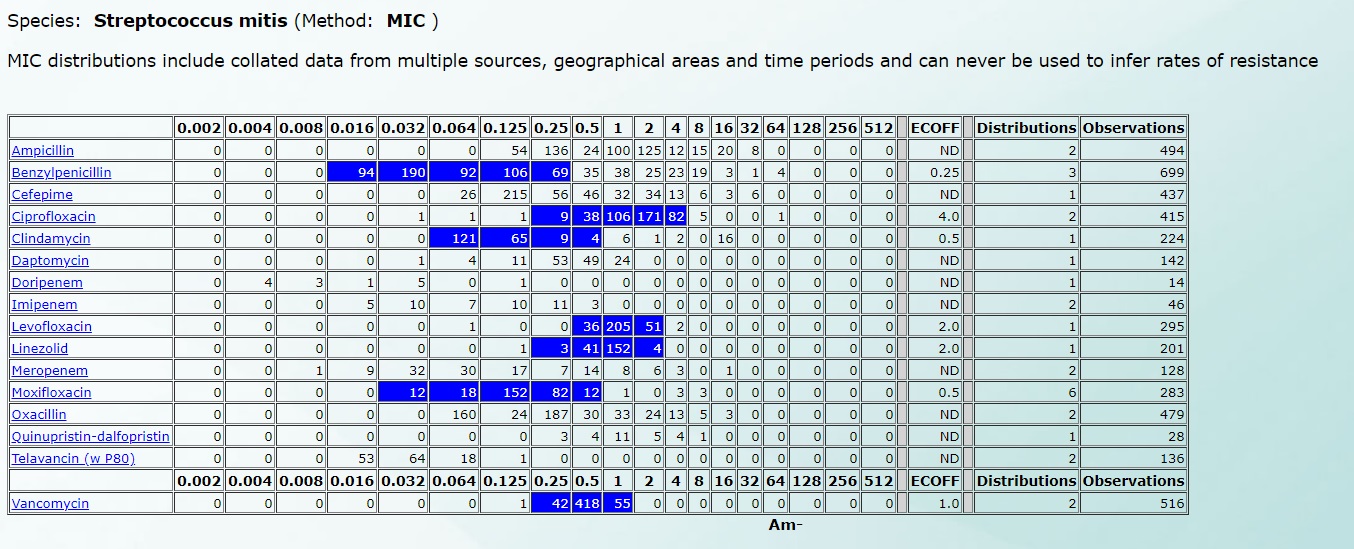
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
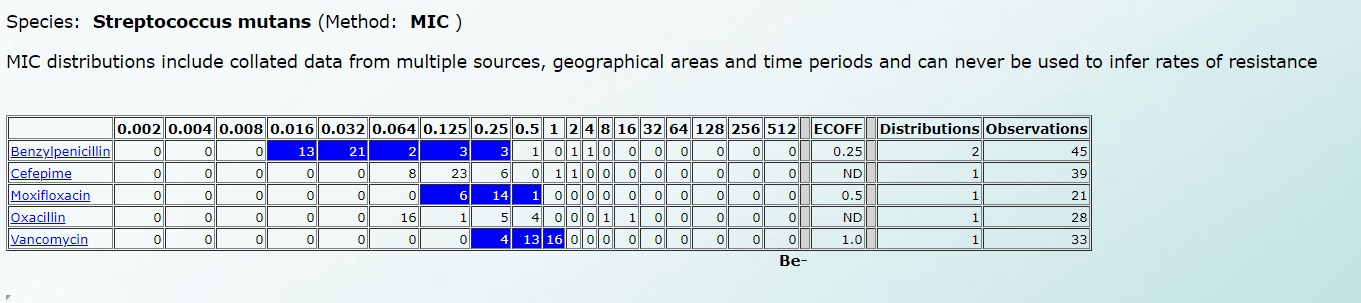
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
Стрептококки: чем опасны, как выявлять и лечить
Род бактерий, относящихся к условно патогенной микрофлоре. Носителями различных стрептококков являются практически все люди, включая младенцев. В норме активность микробов подавляет иммунитет. При ослаблении его защиты или получении извне большой заражающей дозы развиваются стрептококковые инфекции: воспалительные заболевания, поражающие слизистые дыхательных путей, ткани внутренних органов, зубы или оболочки мозга. Стрептококки очень устойчивы к факторам внешней среды, способны вырабатывать резистентность к антибактериальным препаратам.
Что такое стрептококки
Род Streptococcus объединяет разнообразные грамположительные микроорганизмы, способные размножаться в анаэробных условиях. Бактерии имеют шаровидную форму, их оболочки чрезвычайно устойчивы к агрессии внешней среды. В высушенных образцах биологических материалов стрептококки сохраняются жизнеспособными более года. Погибают при кипячении, химические дезинфицирующие препараты убивают их в течение 20 минут. По этой причине поверхностного антисептирования часто бывает недостаточно.
Источник распространения стрептококков — носители: зараженные или больные люди. В большой концентрации инфекция содержится на поверхности слизистых оболочек, в жидкостных выделениях: гное, экссудате, слюне. Микробы передаются от человека к человеку воздушно-капельным путем при чихании или кашле. В отличие от вирусов стрептококки разлетаются на относительно небольшое расстояние от источника: в радиусе не более трех метров. Высокая устойчивость бактерий во внешней среде определяет также алиментарный путь заражения: через грязные руки, продукты питания. Стрептококки длительное время сохраняются в молоке, мясных и морепродуктах, которые являются для этой группы инфекций питательную среду.
При размножении в организме человека стрептококки провоцируют интенсивные воспалительные реакции:
микробы группы А чаще поражают слизистые носа, ротовой полости, гортани, бронхов и легких, слухового аппарата, кожи, становятся возбудителями синуситов, тонзиллита, кариеса, ангины, пневмонии, дерматитов, рожи, скарлатины, осложнения ран и ожогов;
стрептококки группы В обычно провоцируют воспаления тканей мочевыделительной системы, суставных структур, соединительной ткани, вызывают цистит, адрекситы, инфекционные нефриты, ревматические процессы, послеродовые осложнения у женщин, эти микробы могут передаваться при половых контактах.
Развитию стрептококковых инфекций способствуют различные системные патологии и повреждения тканей. В том числе: сахарный диабет, злокачественные опухоли, иммунодефицитные, послеоперационные состояния, гиповитаминозы, открытые раны.
Признаки инфицирования
Распространенные симптомы стрептококковых инфекций:
повышение местной или общей температуры тела;
зуд, жжение, сухость в области гортани;
отечность и покраснение миндалин, образование желтого или сероватого налета на слизистых;
заложенность носа с последующими густыми выделениями зеленоватого или желтого цвета;
резкая боль и заложенность слухового прохода, серозные выделения с примесью гноя.
У большинства людей природная высокая склонность к заражению стрептококками. При передаче того или иного вида инфекции воспаляются так называемые входные ворота. Возникают ларингит, фарингит, ангина, отит. При распространении микробов из очагов заражения страдают нижние дыхательные пути, мозг, почки, кишечник и другие органы. К инфекциям вторичной формы можно отнести процессы с включением аутоиммунных механизмов: ревматоидный артрит, стрептококковый васкулит, гломерулонефрит.
Стрептококки — частые провокаторы токсических и некротических осложнений, в том числе тяжелой лихорадки, абсцессов и сепсиса.
Диагностика и лечение стрептококковых инфекций
Специфическая диагностика патогенов требует проведения бактериологического анализа соскобов слизистых, образцов слюны, мочи, мокроты, гнойного отделяемого и других биоматериалов. Кроме того, часто бывает необходимо тестирование крови на антитела к стрептококкам. Лабораторные исследования устанавливают вид возбудителя болезни в течение 20–30 минут.
Кроме этиологических анализов при различных патологиях требуется диагностика общего состояния поражениях органов: обследование у отоларинголога, проведение УЗИ, флюорографии и некоторых других.
Тактику лечения подбирают с учетом выявленных нарушений и устойчивости микробов к медикаментам. Терапию проводят врачи различных профилей: гинекологи, терапевты, пульмонологи, дерматологи. Для подавления активности инфекционной микрофлоры больным назначают курс антибиотиков. Против стрептококков эффективны Азитромицин, Эритромицин,препараты из ряда фторхинолонов: Ципрофлоксацин, Левофлоксацин. Покупать и применять медикаменты важно по назначению врача. Самодеятельность в этом вопросе приводит к развитию суперинфекций. Терапию дополняют также иммуномодулирующими средствами.
Предотвратить развитие стрептококковых заболеваний помогают санитарные меры, закаливание, использование антисептических средств.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Авторизуйтесьчтобы оставлять комментарии
Возрастные ограничения 18+
Лицензия на осуществление фармацевтической деятельности ЛО-77-02-011246 от 17.11.2020 Скачать.
Стафилококк
О заболевании
При выращивании в чашке Петри с кровяным агаром колонии золотистого стафилококка имеют характерный золотисто-желтый цвет, отсюда и соответствующее название. Этот микроорганизм чрезвычайно распространен, им колонизировано около четверти населения планеты.
Обычно он распространяется в носовой полости, паховой области, подмышках и других частях кожи, но в большинстве случаев является нормальной частью кожной флоры человека и не вызывает никаких проблем.
Однако при увеличении количества бактерий на коже, они начинают проникать в глубокие слои кожи через микротрещины и могут привести к кожным инфекциям и абсцессам.
Патологические процессы могут затрагивать не только различные внутренние органы, такие как печень, почки, селезенка, головной мозг, но и мышцы, кости и суставы, что ведет к крайне плачевным последствиям, поэтому при подозрении на наличие инфекции, следует немедленно обратиться к доктору.
Виды стафилококковых инфекций
Выделяют несколько наиболее распространенных видов стафилококков:
Чаще всего эта инфекция поражает верхние дыхательные пути, вызывая гнойную ангину, фарингит, тонзиллит, бронхит и другие воспалительные заболевания. Данные бактерии очень устойчивы и трудно поддаются терапии.
Данный микроорганизм чрезвычайно устойчив почти ко всем видам антибиотиков пенициллинового ряда, антисептикам, высоким температурам, активным прямым солнечным лучам. Он вызывает различные поражения кожи, такие как экзема, абсцесс, фурункулы, поражения желудочно-кишечного тракта, верхних дыхательных путей, слизистых оболочек, в худшем случае приводит к токсическому шоку.
Этот микроорганизм обитает на поверхности кожи и слизистых любого здорового человека и не несет никакого вреда. Но, если эта бактерия попадает в кровь человека с ослабленным иммунитетом, что чаще всего происходит при хирургических операциях, использовании неправильно обработанных инструментов, катетеров, происходит заражение крови, что ведет к воспалению внутренней оболочки сердца.
Несмотря на то, что этот вид наименее опасный, при заражении он приводит к общей интоксикации организма, вследствие выделения опасных токсинов и ферментов в процессе своей жизнедеятельности. Данные микроорганизмы часто становятся возбудителями воспаления уретры и мочевого пузыря. Преимущественно это характерно для женщин в силу анатомических особенностей строения их мочеполовой системы. При отсутствии лечения цистит влечет за собой воспаление почек и проблемы с зачатием ребенка.
Симптомы и формы стафилококка у взрослых и детей
Симптомы, которые ощущает больной, сильно разнятся в зависимости от способа и места инфицирования и состояния иммунитета. Но можно выделить ряд наиболее характерных признаков:
● нагноение порезов, отечность, гнойные высыпания на коже и слизистых, зуд и покраснение глаз;
● отсутствие обоняния и носового дыхания;
● першение в горле, болезненность при глотании, сухой кашель;
● тошнота, рвота, общее ослабленное состояние;
● сильные головные боли, приступы эпилепсии, сильная одышка;
● болезненные ощущения в суставах.
Одной из самых распространенных форм стафилококков у взрослых людей является его бессимптомное носительство. Здоровый человек не ощущает каких-либо признаков заболевания до тех пор, пока не появится провоцирующий фактор, который даст толчок развитию болезни.
Для женщин наиболее опасен сапрофитная форма, способная привести к возникновению цистита. Это связано с тем, что уретра женщин располагается очень близко к влагалищу, из-за чего велика вероятность попадания патогенной микрофлоры, в том числе и палочки стафилококка, в уретральный канал, а затем и в мочевой пузырь, вызывая его воспаление.
Так как маленькие дети не обладают окрепшей иммунной системой, риск развития инфекции у ребенка достаточно велик. Причем привести к серьезным осложнениям у детей могут даже те виды стафилококка, которые во взрослом возрасте практически не вызывают проблем. Особенную опасность представляет стафилококк у детей в возрасте до года, так как он с легкостью, в кратчайшие сроки способен распространиться по организму и привести к серьезным последствиям вплоть до летального исхода.
Причины возникновения
Наиболее часто бактерия попадает в организм человека через ранки и микротрещины на коже. Инфекция, проникнув через рану, начинает размножаться в крови, распространяясь по организму и поражая легкие, сердце, мозг, печень, почки, суставы.
При стафилококке заболевания могут быть самые различные такие, как пневмония, менингит, остеомиелит, эндокардит, сепсис и многие другие.
Заражение инфекцией стафилококк может произойти следующими способами:
● Контактно-бытовым путем при использовании личных предметов больного;
● Воздушно-капельным при близком общении с зараженным;
● Фекально-оральным на грязных фруктах, овощах и других продуктах питания, грязных посуде и руках;
● Вертикальным при прохождении ребенка через родовые пути зараженной матери при родах.
● Нередко инфицирование происходит во время хирургического вмешательства через медицинский инструментарий и во время проведения различных манипуляций.
Диагностика
Диагностировать наличие инфекции может только врач по результатам проведенного анализа на стафилококк.
Стоит помнить, что проведение анализа рекомендуется только, если присутствуют симптомы болезни. Наличие бактерии в биологическом материале может означать то, что человек является ее носителем, что само по себе является нормой.
Для анализа осуществляется забор материала из области, где предположительно развивается инфекция. Чтобы обнаружить патологический процесс проводятся несколько тестов, чтобы отследить динамику размножения бактерий. Если их число стремительно увеличивается, можно диагностировать наличие стафилококковой инфекции. Также дополнительный анализ позволит определить конкретный вид инфекции, чтобы доктор смог подобрать персональную схему лечения.
Лечение
Лечение стафилококка может проводиться хирургическим способом при наличии гнойного поражения в области заражения. Также может потребоваться удалить инфицированный имплант, катетер и пр.
В качестве консервативного лечения стафилококка применяют антибиотики, антибактериальные средства в сочетании с иммуномодулирующей терапией. Препараты подбираются с учетом устойчивости стафилококка к большому ряду медикаментов. Большую эффективность показало применение бриллиантового зеленого раствора для обработки зараженных ран.
Какие анализы необходимо сдать
В первую очередь, для определения наличия инфекции сдается анализ на стафилококк.
Также перед тем как начать лечение с применением антибиотиков, требуется сдать анализ на резистентность к этим медикаментам.
К какому врачу обращаться
Запущенными случаями заболевания занимается инфекционисту.
Но если у вас только появились подозрения и вы хотите получить точный диагноз, для начала вам следует обратиться к терапевту, с детьми – к педиатру. Доктор проведет диагностику и на основании полученных результатов выпишет вам направление к необходимому врачу.
Профилактика стафилококка
Как предотвратить заболевание
Чтобы предотвратить распространение стафилококка в организме и последующее развитие болезни, необходимо укреплять иммунитет. Для этого рекомендуется вести здоровый образ жизни, заниматься физической активностью, правильно питаться, соблюдая баланс витаминов и всех необходимых микроэлементов, потреблять достаточное количество воды.
Крепкий иммунитет сдержит активность патогенного микроорганизма в пределах безопасной нормы.
Стафилококк: что это, симптомы, причины, лечение
Связанные услуги
Что это такое?
Стафилококки — род анаэробных шарообразных бактерий, которые вызывают пневмонию, эндокардит, ряд инфекций кожи, остеомиелит, менингит, септический артрит, синдром токсического шока и другие заболевания. Бактерии постоянно обитают на кожных покровах здорового человека, его носоглотке и ротоглотке. Инфицирование происходит при снижении иммунитета.
Особенно подвержены стафилококковой инфекции новорожденные дети и кормящие женщины, пациенты со сниженным иммунитетом, в том числе болеющие гриппом, опухолями, лейкемией, хроническими лёгочными недугами, пребывающие на диализе, инъекционные наркоманы, люди с трансплантатами и протезами, с открытыми ранами, ожогами, хирургическими разрезами.
Чаще всего стафилококки передаются воздушно-капельным или контактным путём.
Наиболее патогенен для человека золотистый стафилококк, приводящий к воспалительным процессам и нагноению практически всех органов человека. «Золотистым» он называется из-за образования золотистого пигмента. Однако это не единственный вид бактерий. Помимо него, у пациентов встречаются:
Симптомы инфицирования
Симптоматика широко варьируется в зависимости от поражённого органа, иммунитета пациента, его возраста. Бывают случаи бессимптомной бактериемии, когда микроорганизмы обнаруживаются в крови, но не доставляют беспокойства и не влияют на функционирование органов.
Однако наиболее распространённые симптомы могут включать в себя:
Поскольку стафилококки могут поразить любой орган, симптомы тоже могут различаться.
Причины развития стафилококковой инфекции
Главная причина развития заболевания — снижение иммунитета из-за стресса, болезней, неправильного питания, авитаминоза или приёма лекарственных препаратов. Падение иммунитета, в том числе сезонное, может спровоцировать размножение бактерий и последующее инфицирование.
Есть и другие причины:
Младенцы инфицируются из-за патологий во время беременности и родов, к примеру, длительного безводного периода, недоношенности, несоблюдения гигиены.
Из-за особенностей способов передачи стафилококковую бактериемию сравнительно легко предотвратить, соблюдая базовые требования по гигиене, не взаимодействуя с чужими личными вещами, соблюдая рекомендации врача и избегая — по возможности — тесного общения с инфицированными.
Диагностика и лечение
Диагностика заболевания включает в себя:
Могут понадобиться исследования, касающиеся конкретного затронутого инфекцией органа.
Лечение — антибиотикотерапия с подбором лекарства под конкретный возбудитель. Это важно, поскольку среди бактерий стафилококкового рода встречаются резистентные к стандартным лекарствам, требующие особого подхода. Очень важно не «назначать» себе антибиотики самостоятельно — это чрезвычайно сильные и опасные лекарственные средства, прописать которые может только дерматолог.
Дополнительно могут назначаться средства для симптоматического лечения, например, мази для обработки гнойников и язв, жаропонижающие средства.
Стафилококк mitis что это
ФГБУ «НИИ детских инфекций ФМБА», Санкт-Петербург
Введение
Золотистый стафилококк (Staphy-lococcus aureus) – наиболее частый патоген человека, вызывающий различные гнойные процессы: инфекции кожи и мягких тканей (ИКМТ), остеомиелиты, пневмонии, бактериемии. Кроме того, S. aureus является представителем нормальной микробиоты человека, считается, что он встречается у 30–60% человеческой популяции и бессимптомно колонизирует слизистые крыльев носа, крылья носа, подмышечные впадины, пах, подколенную область. Как известно, внедрение первых β-лактамов почти полностью решало проблему стафилококковых инфекций, связанных с хирургическим вмешательством. Однако у стафилококков достаточно быстро появилась устойчивость к пенициллину за счет приобретения плазмидной β-лактамазы.
В 1960-х гг. вскоре после внедрения в практику пенициллиназостабильных β-лактамов (метициллин) были описаны первые S. aureus, устойчивые к этим антибиотикам (Methicillin-resistant Staphylococcus aureus, MRSA) [1]. Достаточно быстро было установлено, что устойчивость к метициллину является маркером устойчивости ко всем β-лактамам, известным в то время. Впервые появившись в Англии, MRSA теперь циркулируют на всей планете. По количеству летальных исходов MRSA лидируют среди других мультирезистентных бактерий; так, в последнем (2013) опубликованном отчете CDC morrigan сообщается, что в США от инфекций, обусловленных мультирезистентными бактериями, погибают около 23 тыс. американцев в год, из них 11 тыс. приходится на MRSA [2]. Долгое время MRSA считался исключительно госпитальной инфекцией, но с 1990-х гг. стали описывать случаи тяжелых инфекций среди людей, не связанных с учреждениями здравоохранения (внебольничные MRSA) [3]. Позже, в середине 2000-х, появились MRSA, ассоциированные с инфекциями у животных, которые могут передаваться и человеку. Основным препаратом для лечения MRSA-инфекций длительное время оставались гликопептиды, однако в середине 1990-х впервые были описаны изоляты со сниженной чувствительностью к ванкомицину [4], а с 2002 г. – абсолютно резистентные фенотипы [5]. Появление изолятов, устойчивых к гликопептидам, послужило стимулом для разработки и внедрения новых антибиотиков и даже принципиально новых классов препаратов: оксазолидинонов, глицилциклинов, липопептидов, цефалоспоринов с анти-MRSA-активностью. Однако уже описаны клинические изоляты, проявляющие устойчивость и к этим антибиотикам. Биологические особенности основных генотипов MRSA кратко представлены в табл. 1.
Распространение и молекулярная эпидемиология MRSA в мире
Для MRSA характерна высокая степень клональности популяции; так, можно выделить всего несколько групп клонов, распространных на обширных географических территориях и наиболее клинически значимых. На сегодняшний день мультилокусное сиквенс-типирование (MLST – Multi-Locus Sequence Typing) рассматривается как основной метод оценки генетического родства бактерий и стафилококков в частности. Идентифицированный клон называется сиквенс-типом (ST, sequence type) [8]. Например, первый клон MRSA – ST250 «archaic clone», был изначально распространен на территории Западной Европы. Наиболее успешные клоны, пандемично распространенные по всему миру, относятся к ST8 и ST239. Клон ST8, вариант USA300, был впервые описан как внебольничный MRSA, появившийся на территории США.
В 1970–1980 гг. MRSA стали абсолютным лидером в структуре внутригоспитальных инфекций. Тем не менее частота регистрации случаев таких инфекций в разных странах колеблется в очень широком диапазоне. На рисунке представлены данные Европейской системы по надзору за распространением резистентности (European Antimicrobial Resistance Surveillance Network – EARS-Net), где показана доля выявляемых MRSA в разных странах за 2013 г. [9]. В таких странах, как Румыния, Италия, Греция, Португалия, Мальта, частота выявления MRSA очень высока (35–65%), напротив, в скандинавских странах эта доля не превышает 5%.
В Африке доля MRSA колеблется в пределах 25–50%, а в некоторых странах не достигает 20%. Можно выделить три доминирующих клона – ST88 «African clone» (превалирует), ST80 и ST239, все они отличаются высокой долей устойчивости к ко-тримоксазолу и тетрациклинам [10].
Азия – один из неблагоприятных регионов, где соотношение CA-MRSA и HA-MRSA составляет 25 и 75%. Особенно неблагоприятна ситуация в Корее, Шри-Ланке и Вьетнаме. Вместе с тем в некоторых странах отмечается появление и распространение клонов со сниженной чувствительностью к гликопептидам. На территории всего азиатского региона циркулирует ST239, который является ведущим нозокомиальным патогеном. Среди CA-MRSA преобладают клоны ST8, ST30, ST59, ST22, ST772 и ST72 [11].
Лидерами по распространению MRSA являются страны Латинской и Южной Америки, где частота выделения HA-MRSA колеблется от 30 до 90% и CA-MRSA – от 15 до 80%. Первая вспышка CA-MRSA-инфекции произошла в 2002 г. среди заключенных в тюрьмах Уругвая. Было госпитализировано более 1000 человек, из них 12 погибли. Среди HA-MRSA превалируют клоны ST239 (вариант «Brazilian»), ST247, ST5 (вариант «New-York/Japan») и ST8; среди внебольничных – ST5 (вариант «Pediatric»), ST100 («Argentinian pediatric clone»), ST8 («USA300») [12].
В Австралии инфекции, вызванные MRSA, не превышают 30%, но остро стоит проблема CA-MRSA, с 2000-х гг. периодически описываются вспышки в местах повышенной скученности людей. К числу основных клонов CA-MRSA относятся ST93, ST75, ST30, ST1, ST45, ST78 и ST5 [13].
С 1979 по 2000 г. сообщения о выделении MRSA от животных были скорее исключением, чем обычным явлением. В 2005 г. был описан тяжелый случай развития MRSA-инфекции у 6-месячного ребенка, жившего на ферме в Нидерландах. Проведенные генетические исследования показали, что выделенный от пациентки изолят принадлежал к новому на тот момент клону, ST398, более того, у животных, обитающих на той ферме также был выявлен этот клон. Так, появился новый эпидемиологический кластер – MRSA ветеринарной линии (LA-MRSA), проявляющий устойчивость к многим группам препаратов (тетрациклины, макролиды, ко-тримоксазол, фторхинолоны). Некоторыми исследователями высказывается предположение, согласно которому клон ST398 в большей степени ассоциирован с поражениями верхних дыхательных путей [14].
В связи с крайне высокой значимостью негативных клинических факторов, ассоциированных с MRSA, в США, Австралии и ряде стран Европы были приняты жесткие противоэпидемические меры по сдерживанию этой инфекции, что способствовало существенному снижению распространения MRSA [15]. В частности, в Европе удалось снизить частоту выделения c 24% в 2005 г. до 16% в 2013-м (см. рисунок).
Проблема снижения чувствительности к гликопептидам
В 1997 г. в Японии был выделен первый VISA-изолят (Mu50), имеющий МПК ванкомицина 8 мкг/мл [4]. Mu50 был выделен из инфицированной кардиохирургической раны 4-месячного пациента, при этом терапия ванкомицином не давала положительных результатов. Другой изолят, Mu3, выделенный через год в том же госпитале также на фоне неудачи лечения имел МПК ванкомицина 4 мкг/мл, отличался нестабильностью свойств, вследствие чего он был отнесен к категории hVISA. За прошедшее десятилетие сообщения о изолятах со сниженной чувствительностью появлялись по всему миру. За последнее время в ряде регионов в популяции MRSA наблюдают сдвиг МПК в сторону больших значений («MIC creep» – «сползание МПК»): с этим феноменом, возможно, связано возрастание числа случаев клинических неудач ванкомицина [16, 17]. Однако такой сдвиг МПК наблюдается не во всех регионах мира, в некоторых работах МПК ванкомицина на протяжении длительного периода времени в одном стационаре или географическом регионе сохраняется на одном уровне [18–20]. Экстраполируя данные о чувствительности к ванкомицину с клинической точки зрения, стоит сказать, что уже при МПК=2 мкг/мл вероятность неудачной терапии ванкомицином резко возрастает [21, 22]. Несколько позже были описаны изоляты MRSA, проявляющие высокую степень устойчивости к гликопептидам.
В 2002 г. в Мичигане (США) был описан первый клинический изолят ванкомицинустойчивого S. aureus (VRSA-1). У этого изолята был обнаружен мобильный генетический элемент, полученный от ванкомицинрезистентного энтерококка [23]. С 2002 по 2009 г. в США было выявлено 11 изолятов VRSA: 7 – из Мичигана (VRSA-1, VRSA-5-10), изоляты из Пенсильвании (VRSA-2), Нью-Йорка (VRSA-3), а также из Индии и Ирана. По всему миру к 2013 г. всего было описано 33 клинических изолята VRSA [24–26]. Очевидно, что подобные фенотипы не распространяются и элиминируют из стафилококковой популяции.
Проблема MRSA в России
В России ситуацию с распространением MRSA, c одной стороны, нельзя оценить в силу отсутствия централизованной системы по сбору данных о циркуляции госпитальных и внегоспитальных патогенов, с другой – имеющиеся исследования показывают крайнюю неравномерность их распространения. Так, частота встречаемости MRSA может колебаться от 0 до 80% в зависимости от стационара и географического региона. Анализ популяционной структуры MRSA еще раз подчеркивает ее высокую клональность. Другая особенность – в России циркулируют только HA-MRSA. Изолят CA-MRSA, несущий токсин PVL, был обнаружен только в одном случае во Владивостоке [27]. Среди HA-MRSA доминируют два клона – ST8 и ST239, при этом первый превалирует [28, 29]. Проведенные авторами исследования показывают, что среди изолятов ST239 преобладают фенотипы с устойчивостью более чем к трем не-β-лактамным антибиотикам. Кроме того, ST239 встречается только среди больных инвазивными формами стафилококковых инфекций. Клон ST8, напротив, более гетерогенен по спектру антибиотикоустойчивости, а также может встречаться среди носителей. В работах О.А. Дмитренко было показано, что эти клоны циркулируют на территории России с 1990-х гг. [30]. По нашим данным, в Санкт-Петербурге и Москве с 2011 г. стал регистрироваться не характерный для России клон ST228, который характеризуется множеством различных детерминант устойчивости к не-β-лактамам, а также сниженной чувствительностью к новому цефалоспорину – цефтаролину. Помимо вышеперечисленных клонов гораздо реже, но встречаются ST1, ST5 и ST22.
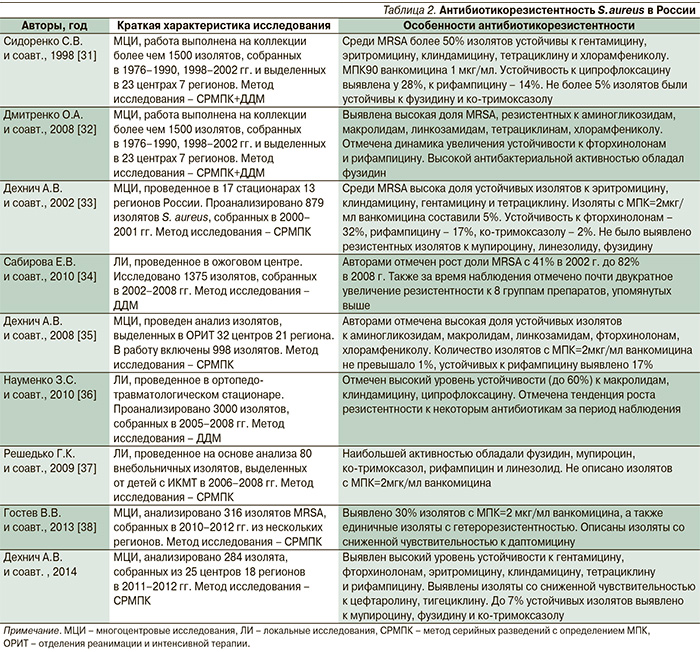
В табл. 2 представлены результаты проведенных в России многоцентровых и локальных исследований по изучению антибиотикорезистентности S. aureus. Отдельного внимания заслуживает чувствительность к ванкомицину. Во многих исследованиях с применением дискодиффузионного метода (ДДМ) оценки чувствительности, проведенных в России, не было описано ни одного случая выявления VRSA-фенотипа. Другой вопрос – это изоляты MRSA со сниженной чувствительностью к ванкомицину (hVISA и VISA). К сожалению, определение МПК в России проводят лишь единичные лаборатории, а поскольку определение снижения чувствительности и выявление hVISA/VISA изолятов возможно только этими методами (хотя и не всегда точно), данных о рассматриваемых фенотипах практически нет. Как уже отмечено ранее, в некоторых странах наблюдается «MIC creep»-эффект для ванкомицина, в какой-то степени на основе анализа имеющихся исследований можно заключить, что такой процесс происходит и в России. Например, в работах начала 2000-х гг. доля изолятов с МПК ванкомицина 2 мкг/мл составляла не боле 5%, а к 2013 г. возросла до 30% (табл. 2). Раннее исследование, проведенное авторами, также показало, что единичные изоляты проявляют hVISA-фенотип. Все эти факты свидетельствуют о том, что использование ванкомицина в клинической практике для лечения MRSA-инфекций необходимо проводить под строгим наблюдением и постоянным мониторингом чувствительности исследуемой культуры только методами количественной оценки.
Диагностика инфекций, вызываемых MRSA, детекция метициллинрезистентности
В современную диагностику инфекций, вызываемых MRSA, как и в другие области микробиологической диагностики, происходит постепенное внедрение молекулярных методов. На сегодняшний день существуют коммерческие тест-системы, основанные в основном на ПЦР, позволяющие выявлять MRSA непосредственно в биологических образцах, не выделяя чистую культуру возбудителя. Шире всего молекулярные методы применяются при диагностике бактериемии (сепсиса) и при скрининге на носительство MRSA, т.е. в тех ситуациях, когда скорость ответа имеет существенное значение. В случае бактериемии (сепсиса) быстрый ответ необходим для принятия решения об антибактериальной терапии, а в случае скрининга – для принятия решения о необходимости изоляции пациента. Скрининг на носительство широко распространен в Европе и США, где это исследование применяется в системе инфекционного контроля для предотвращения импорта MRSA в стационары.
При всей перспективности молекулярной диагностики классические методы вряд ли утратят свое значение в обозримом будущем. Если классическая микробиологическая диагностика инфекций, вызываемых MRSA, ничем не отличается от диагностики других стафилококковых инфекций, то детекция метициллинрезистентности имеет некоторые особенности. Прежде всего метициллин уже давно не применяется не только в клинической медицине, но и в лабораторной диагностике. На протяжении многих лет метициллинрезистентность выявляли ДДМ-использованием диска с оксациллином. Однако сравнительно недавно было показано, что использование диска с цефокситином обеспечивает большую чувствительность и специфичность детекции метициллинрезистентности. На основании этих данных CLSI и EUCAST рекомендуют использовать для детекции метициллинрезистентности только диски с цефокситином. Здесь же уместно еще раз напомнить, что, согласно рекомендациям CLSI и EUCAST, оценивать чувствительность стафилококков к другим β-лактамам, кроме цефтаролина и цефтобипрола, нецелесообразно из-за высокой вероятности получения ложной чувствительности. Для прогноза чувствительности к β-лактамам необходимо использовать результаты, получаемые при оценке чувствительности культуры к цефокситину.
Гораздо более серьезную проблему из-за невозможности использовать ДДМ представляет определение чувствительности стафилококков к ванкомицину (выявление фенотипов VISA и hVISA). Молекулярные тесты также отсутствуют, поскольку точный механизм формирования устойчивости не известен. Для выявления снижения чувствительности необходимо использовать фенотипические методы определения МПК в серийных разведениях или разные варианты эпсилометрических тестов. Однако перечисленные методы недостаточно стандартизованы и не обладают необходимой специфичностью и чувствительностью. Наиболее достоверным методом служит популяционный анализ (PAP), требующий для своей постановки специальной аппаратуры [39]. Естественно, что такой метод достаточно трудоемок и может быть выполнен только в специализированных референс-лабораториях. В отличие от детекции hVISA/VISA фенотип VRSA легко можно определять даже ДДМ.
Лечение инфекций, вызываемых MRSA
Наиболее детальные рекомендации по тактике терапии MRSA-инфекций изложены в двух обновляемых протоколах: Американского общества инфекционистов – IDSA (Infectious Diseases Society of America) [40] и Британского общества по микробной химиотерапии BSAC (British Society for Antimicrobial Chemotherapy) [41]. Описываемые ниже возможности лечения MRSA-инфекций основаны на этих протоколах.
Традиционными средствами лечения MRSA-инфекций считаются гликопептиды, из них в настоящее время в Российской Федерации доступен только ванкомицин. Применение ванкомицина разрешено при MRSA-инфекциях практически любой локализации, несмотря на то что его эффективность далеко не во всех случаях подтверждена контролируемыми клиническими испытаниями. Столь широкий спектр показаний к применению ванкомицина связан с тем, что препарат зарегистрирован в годы, когда требования к доказательности эффективности были минимальными. В связи с появлением штаммов MRSA со сниженной чувствительностью к ванкомицину роль этого антибиотика в этиотропной терапии пересматривается.
Прежде всего это касается режимов дозирования антибиотика, наиболее современные рекомендации по этому вопросу приведены в консенсусном документе, принятом рядом профессиональных сообществ [42]. Основу этих рекомендаций составляют клинические наблюдения, а также анализ фармакокинетических и фармакодинамических закономерностей. Показано, что предиктором эффективности ванкомицина является отношение площади под фармакокинетической кривой ванкомицина (area under the curve – AUC) к минимальной подавляющей концентрации (minimal inhibitory concentration – MIC) антибиотика в отношении возбудителя. Высокая вероятность клинического и бактериологического эффекта отмечается при значении AUC/MIC≥400. Обеспечить эту величину удается в отношении бактерий с МПК ванкомицина 1,0 мкг/мл при разовой дозе антибиотика 5–20 мг/кг, вводимой с интервалом 8–12 часов. При МПК ванкомицина в отношении возбудителя более 1,0 мкг/мл для лечения рекомендуется использовать альтернативные препараты.
Важным моментом правильного клинического применения ванкомицина служит учет того факта, что при лечении инфекций, вызванных метициллинчувствительными стафилококками, антибиотик по эффективности существенно уступает β-лактамам. Этот факт исключает возможность эмпирического применения ванкомицина при стафилококковых инфекциях без подтверждения метициллинрезистентности.
Перечень разрешенных показаний к ванкомицину и анти-MRSA-препаратам, альтернативным ванкомицину, приведен в табл. 3. Очевидно, что для альтернативных препаратов перечень показаний весьма ограничен, т.к. по современным требованиям разрешение на применение по каждому показанию может быть получено только при наличии положительных результатов контролируемых клинических испытаний. Однако на практике эти препараты применяются гораздо шире (назначение «off label»), что имеет крайне важное значение для накопления новых клинических данных и последующего расширения официальных показаний. Следует также указать, что возможности применения этих антибиотиков при MSSA-инфекциях гораздо шире. В некоторых ситуациях для лечения MRSA-инфекций применяют ко-тримоксазол, рифампицин и клиндамицин.
Бактериемии делят на осложненные и осложненные, последние определяют как развившиеся на фоне эндокардита или при наличии имплантированных устройств. Основу терапии составляют ванкомицин и даптомицин, при неосложненных формах достаточной считается 2-недельная длительность применения, при осложненных – 4–6 недель. Обсуждается вопрос о дозах даптомицина. Разрешенная доза составляет 6,0 мг/кг/сут, высказывается предположения о необходимости использовать при эндокардите дозы до 10,0 мг/кг/сут. Целесообразность использования комбинаций ванкомицина с аминогликозидами или рифампицином не доказана.
Наиболее широкие возможности существуют для лечения ИКМТ, по этому показанию можно применять все анти-MRSA-антибиотики. Оборотная сторона медали доступности многих препаратов – это сложность выбора наиболее эффективного. В клинических испытаниях при ИКМТ эффективность новых антибиотиков, как правило, сравнивают с ванкомицином (проверка гипотезы не меньшей эффективности – «non-inferiority»). Результат подавляющего большинства таких испытаний – это отсутствие достоверных различий между ванкомицином и новыми препаратами. Исключение составляет демонстрация определенных преимуществ цефтаролина перед комбинацией ванкомицина и азтреонама при оценке результата на ранних стадиях инфекции [43]. При выборе терапии ИКМТ важно помнить, что адекватный дренаж при легких формах вполне достаточен для получения максимального эффекта, а при средне-тяжелых формах эффективны доксициклин, ко-тримоксазол или клиндамицин. Среди MRSA, циркулирующих в Российской Федерации, отмечают низкую частоту ассоциированной устойчивости к ко-тримоксазолу (2% по критериям EUCAST); частота устойчивости к тетрациклинам и клиндамицину существенно выше – 52 и 45% соответственно. Для лечения поверхностных инфекций кожи и мягких тканей возможно также использование топических препаратов – мупироцина, фузидина [44].
Ни один из новых препаратов не рекомендован для лечения интраабдоминальных MRSA-инфекций. Тигециклин, разрешенный по этому показанию при MSSA-инфекциях, на практике применяют и при MRSA- инфекциях.
Лечение нозокомиальной пневмонии, в т.ч. и вентиляторассоциированной, – один из немногих случаев, в котором показано достоверное преимущество линезолида перед ванкомицином. Даптомицин при легочных инфекциях практически неэффективен, поскольку ингибируется легочным сурфактантом [45].
При инфекциях мочевыводящих путей ни один из новых антибиотиков не показан, рекомендуется использовать нитрофурантоин или ко-тримоксазол, при осложненных формах – ванкомицин и даптомицин. Концентрации линезолида и тигециклина не достигают терапевтических значений в моче, соответственно, их использование нецелесообразно [46].
Новые антибиотики также не рекомендованы для лечения инфекций ЦНС; базовым препаратом считается ванкомицин, некоторые эксперты рекомендуют его комбинацию с рифампицином. Несмотря на отсутствие официальных показаний, имеется положительный опыт применения при менингитах и других инфекциях ЦНС линезолида и даптомицина.
Помимо существующих высокоэффективных антибиотиков в настоящее время в клиническую практику внедряются новые препараты, активные в отношении MRSA, VISA, VRSA. К их числу относятся тедизолид (Tedizolid), далбаванцин (Dalbavancin) и телаванцин (Telavancin). Тедизолид – бактериостатический антибиотик группы оксазолидинонов второго поколения, механизм его действия – нарушение сборки бактериального рибосомального комплекса, что приводит к нарушению биосинтеза белка клетки. Основной особенностью тедизолида считается преодоление резистентности к линезолиду. Препарат ориентирован на терапию ИКМТ у взрослых (FDA, 2014), также ведутся клинические испытания по поводу возможности использования тедизолида для лечения нозокомиальных пневмоний [47, 48]. Далбаванцин – дериват гликопептидов, относится ко второму поколению липогликопептидов, одобрен FDA в 2014 г. для лечения ИКМТ. Этот антибиотик, аналогичный ванкомицину, нарушает биосинтез клеточной стенки бактерии [49]. Телаванцин – парентеральный липогликопептид, нарушает биосинтез клеточной стенки, одобрен в 2009 г. для лечения стафилококковых ИКМТ, внутрибольничных пневмоний и вентиляторассоциированных пневмоний [50].
Еще два препарата с анти-MRSA-активностью, рекомендованные для лечения ИКМТ, которые заслуживают внимания, – это оритаванцин (Oritavancin) группы гликопептидов [51] и хинупристин/дальфопристин (Quinupristin/dalfopristin) группы стрептограминов [52]. Проведенные клинические испытания, а также исследования чувствительности in vitro показывают высокую эффективность этих антибиотиков в отношении MRSA. К сожалению, все вышеописанные препараты пока не зарегистрированы на территории России, а стоимость лечения ими крайне высока даже в Европе и США.
Заключение
До сих пор MRSA по количеству летальных исходов и экономических затрат на лечение входит в одну тройку с такими инфекционными заболеваниями человека, как туберкулез и СПИД. Однако понимание механизмов распространения и соблюдения крайне жестких превентивных мер (по принципу «search and destroy» – «найти и уничтожить») по сдерживанию MRSA привели к значительному снижению уровня этой инфекции в Европе и США. Такой опыт, безусловно, необходимо внедрять и в нашей стране. Если в первой половине 2000-х гг. практически не было препаратов (кроме, ванкомицина) для лечения MRSA, то в настоящее время существует много альтернатив, и при условии проведения рациональной антимикробной химиотерапии можно добиться высокой эффективности лечения и свести проблему MRSA к минимуму. Более того, уже не одно десятилетие ведутся разработки по созданию стафилококковой вакцины, внедрение которой, возможно, способствовало бы снижению риска развития внутрибольничных MRSA-инфекций.
Литература
Об авторах / Для корреспонденции
В.В. Гостев – ФГБУ «НИИ детских инфекций ФМБА», Санкт-Петербург
С.В. Сидоренко – ФГБУ «НИИ детских инфекций ФМБА», Санкт-Петербург