Спр что это физиологии
Выделяют несколько последовательных этапов запуска и осуществления мышечного сокращения.
1. Потенциал действия распространяется вдоль двигательного нервного волокна до его окончаний на мышечных волокнах.
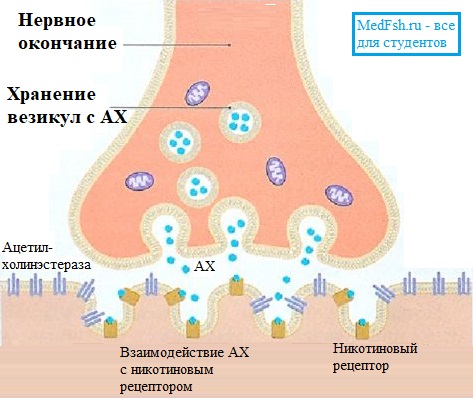
2. Каждое нервное окончание секретирует небольшое количество нейромедиатора ацетилхолина.
3. Ацетилхолин действует на ограниченную область мембраны мышечного волокна, открывая многочисленные управляемые ацетилхолином каналы, проходящие сквозь белковые молекулы, встроенные в мембрану.
4. Открытие управляемых ацетилхолином каналов позволяет большому количеству ионов натрия диффундировать внутрь мышечного волокна, что ведет к возникновению на мембране потенциала действия.
5. Потенциал действия проводится вдоль мембраны мышечного волокна так же, как и по мембране нервного волокна.
6. Потенциал действия деполяризует мышечную мембрану, и большая часть возникающего при этом электричества течет через центр мышечного волокна. Это ведет к выделению из саркоплазматического ретикулума большого количества ионов кальция, которые в нем хранятся.
7. Ионы кальция инициируют силы сцепления между актиновыми и миозиновыми нитями, вызывающие скольжение их относительно друг друга, что и составляет основу процесса сокращения мыщц.
8. Спустя долю секунды с помощью кальциевого насоса в мембране саркоплазматического ретикулума ионы кальция закачиваются обратно и сохраняются в ретикулуме до прихода нового потенциала действия. Удаление ионов кальция от миофибрилл ведет к прекращению мышечного сокращения.
Далее мы обсудим молекулярные механизмы этого процесса.
Молекулярные механизмы мышечного сокращения
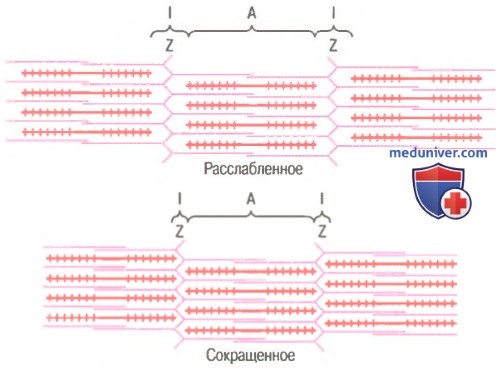
Механизм скольжения нитей для мышечного сокращения. На рисунке показан основной механизм мышечного сокращения. Показано расслабленное состояние саркомера (вверху) и сокращенное состояние (внизу). В расслабленном состоянии концы актиновых нитей, отходящие от двух последовательных Z-дисков, лишь незначительно перекрываются. Наоборот, в сокращенном состоянии актиновые нити втягиваются внутрь между миозиновыми так сильно, что их концы максимально перекрывают друг друга. При этом Z-диски притягиваются актиновыми нитями к концам миозиновых. Таким образом, мышечное сокращение осуществляется путем механизма скольжения нитей.
Что заставляет нити актина скользить внутрь среди нитей миозина? Это связано с действием сил, генерируемых при взаимодействии поперечных мостиков, исходящих от нитей миозина, с нитями актина. В условиях покоя эти силы не проявляются, однако распространение потенциала действия вдоль мышечного волокна приводит к выделению из саркоплазматическо-го ретикулума большого количества ионов кальция, которые быстро окружают миофи-бриллы. В свою очередь, ионы кальция активируют силы взаимодействия между нитями актина и миозина, в результате начинается сокращение. Для осуществления процесса сокращения необходима энергия. Ее источником являются высокоэнергетические связи молекулы АТФ, которая разрушается до АДФ с высвобождением энергии. В следующих разделах мы приведем известные детали молекулярных процессов сокращения.
Молекулярные особенности сократительных нитей
Миозиновая нить. Она состоит из множества молекул миозина, молекулярная масса каждой составляет около 480000. На рисунке показана отдельная молекула; и также — объединение многих молекул миозина в миозиновую нить, а также взаимодействие одной стороны этой нити с концами двух актиновых нитей.
В состав молекулы миозина входят 6 полипептидных цепей: 2 тяжелые цепи с молекулярной массой около 200000 каждая и 4 легкие цепи с молекулярной массой около 20000 каждая. Две тяжелые цепи спирально закручиваются вокруг друг друга, формируя двойную спираль, которую называют миозиновым хвостом. С одного конца обе цепи изгибаются в противоположных направлениях, формируя глобулярную полипептидную структуру, называемую миозиновой головкой. Таким образом, на одном конце двойной спирали молекулы миозина образуются 2 свободные головки; 4 легкие цепи также включены в состав миозиновой головки (по 2 в каждой). Они помогают регулировать функцию головки во время мышечного сокращения.
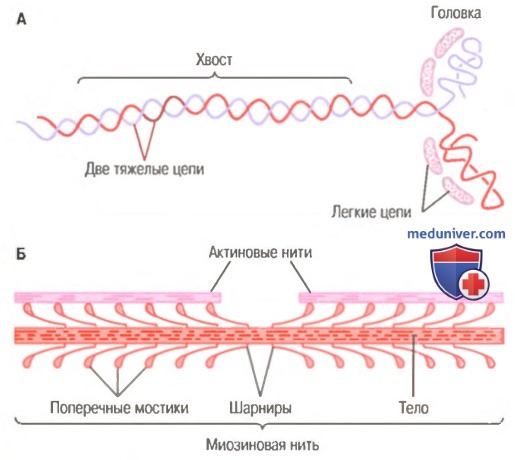
Б. Объединение многих молекул миозина в одну миозиновую нить.
Показаны также тысячи миозиновых поперечных мостиков и взаимодействие их головок с прилежащими актиновыми нитями.
Миозиновая нить состоит из 200 или более отдельных молекул миозина. Видно, что хвосты молекул миозина объединяются, формируя тело нити, а многочисленные головки молекул выдаются наружу по сторонам тела. Кроме того, наряду с головкой в сторону выступает часть хвоста каждой миозиновой молекулы, образуя плечОу которое выдвигает головку наружу от тела, как показано на рисунке. Выступающие плечи и головки вместе называют поперечными мостиками. Каждый поперечный мостик может сгибаться в двух точках, называемых шарнирами. Один из них расположен в месте, где плечо отходит от тела миозиновой нити, а другой — где головка крепится к плечу. Движение плеча позволяет головке или выдвигаться далеко наружу от тела миозиновой нити, или приближаться к телу. В свою очередь, повороты головки участвуют в процессе сокращения, что обсуждается в следующих разделах.
Общая длина каждой миозиновой нити остается постоянной и равна почти 1,6 мкм. В самом центре миозиновой нити на протяжении 0,2 мкм поперечных мостиков нет, поскольку снабженные шарнирами плечи отходят в стороны от центра.
Сама миозиновая нить сплетена таким образом, что каждая последующая пара поперечных мостиков смещена в продольном направлении относительно предыдущей на 120°, что обеспечивает распределение поперечных мостиков во всех направлениях вокруг нити.
АТФ-азная активность миозиновой головки. Есть и другая особенность миозиновой головки, необходимая для мышечного сокращения: миозиновая головка функционирует как фермент АТФ-аза. Как объясняется далее, это свойство позволяет головке расщеплять АТФ и использовать энергию расщепления высокоэнергетической связи для процесса сокращения.
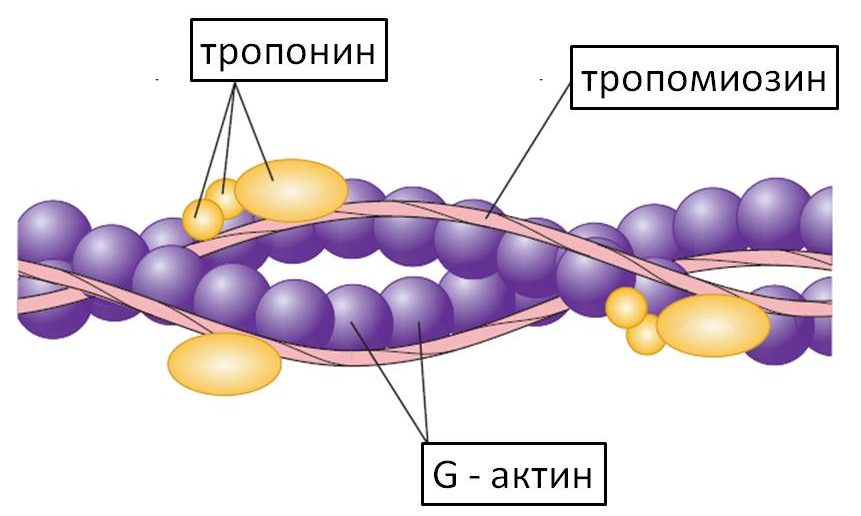
Актиновая нить. Актиновая нить состоит из трех белковых компонентов: актина, тропомиозина и тропонина.
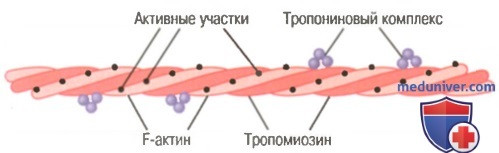
К одному концу каждой молекулы тропомиозина прикреплен тропониновый комплекс, который запускает сокращение.
Основой актиновой нити являются две цепи белковой молекулы F-актина. Обе цепи закручиваются в спираль так же, как и молекула миозина.
Каждая цепь двойной спирали F-актина состоит из полимеризованных молекул G-актина с молекулярной массой около 42000. К каждой молекуле G-актина прикреплена 1 молекула АДФ. Полагают, что эти молекулы АДФ являются активными участками на актиновых нитях, с которыми взаимодействуют поперечные мостики миозиновых нитей, обеспечивая мышечное сокращение. Активные участки на обеих цепях F-актина двойной спирали расположены со смещением таким образом, что вдоль всей поверхности актиновой нити встречается один активный участок примерно через каждые 2,7 нм.
Длина каждой актиновой нити — около 1 мкм. Основания актиновых нитей прочно встроены в Z-диски; концы этих нитей выступают в обоих направлениях, располагаясь в пространствах между миозиновыми молекулами.
Молекулы тропомиозина. Актиновая нить также содержит другой белок — тропомиозин. Каждая молекула тропомиозина имеет молекулярную массу 70000 и длину 40 нм. Эти молекулы спирально оплетают спираль из F-актина. В состоянии покоя молекулы тропомиозина располагаются поверх активных участков актиновых нитей, препятствуя их взаимодействию с миозиновыми нитями, лежащему в основе сокращения.
Тропонин и его роль в мышечном сокращении. По ходу молекул тропомиозина к ним периодически прикреплены другие белковые молекулы, называемые тропонином. Они представляют собой комплексы трех слабосвязанных белковых субъединиц, каждая из которых играет специфическую роль в регуляции мышечного сокращения. Одна из субъединиц (тропонин I) имеет высокое сродство к актину, другая (тропонин Т) — к тропомиозину, третья (тропонин С) — к ионам кальция. Считают, что этот комплекс прикрепляет тропомиозин к актину. Высокое сродство тропонина к ионам кальция, как полагают, инициирует процесс сокращения, о чем говорится в следующей статье.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Башкирский государственный медицинский университет
Нормальная физиология
Теория
Синапс. Физиология мышечных волокон
Синапс — это специфическое место контакта двух возбудимых систем (клеток) для передачи возбуждения.
«synapsis» — «соприкосновение, соединение, застежка»
По способу передачи сигналов:
По виду медиатора: холинэргические и др.
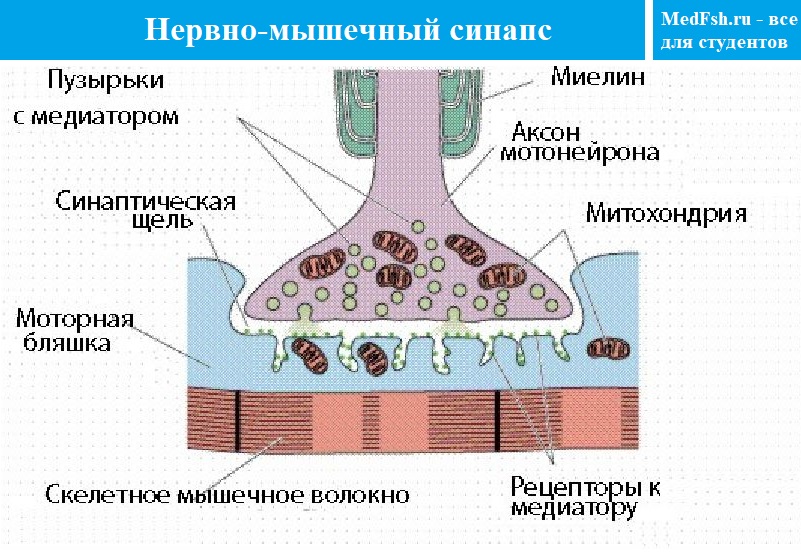
Нервно-мышечный синапс (НМС) — химический, передача с помощью медиатора ацетилхолина.
Синонимы к слову НМС:
В нервно-мышечном синапсе медиатор — ацетилхолин (АХ).
АХ синтезируется из холина и уксусной кислоты (ацетил-коэнзима А) с помощью фермента холинэстеразы. Эти вещества перемещаются из тела нейрона по аксону к пресинаптической мембране. Здесь в пузырьках происходит окончательное образование АХ.
3 фракции медиатора:
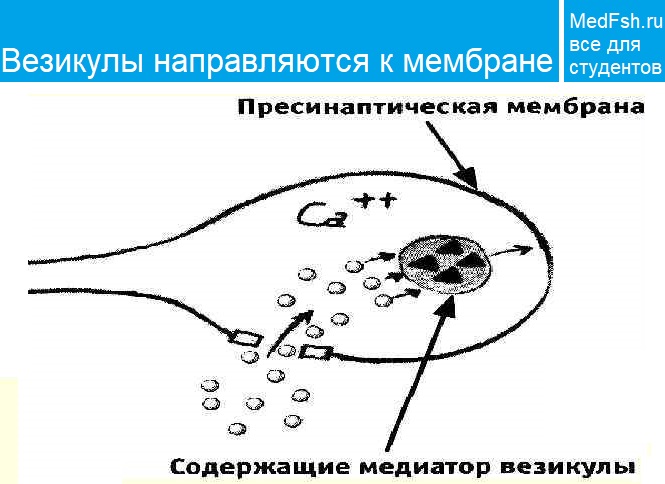
Механизм синаптической передачи
1 этап
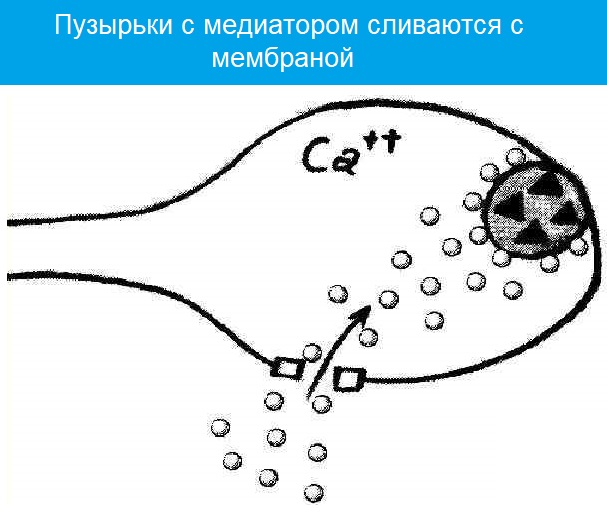
2 этап
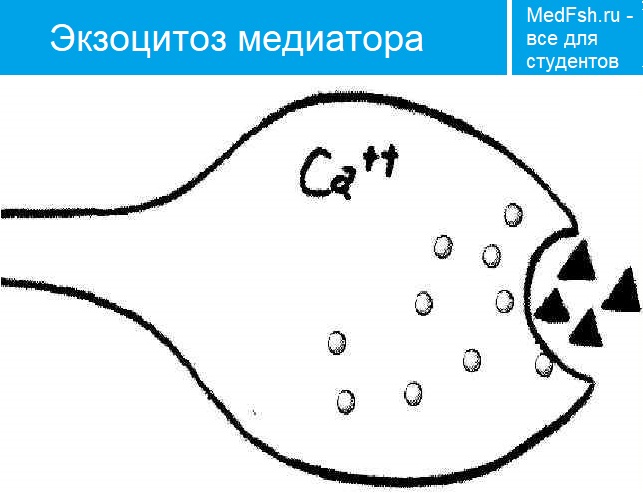
3 этап
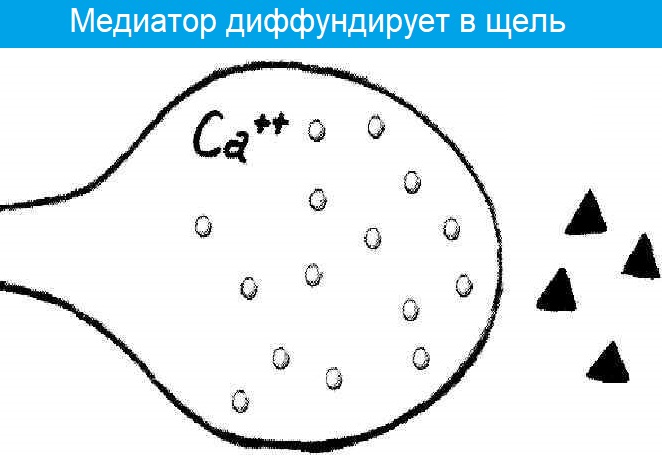
4 этап
Они связаны между собой так называемыми белками экзоцитоза.
5 этап
6 этап
Квант медиатора — количество молекул, содержащихся в одной везикуле.
На 1 ПД выбрасывается 100 квантов АХ.
6 этап
7 этап
8 этап
9 этап
10 этап
На постсинаптической мембране возникает потенциал концевой пластинки (ПКП). Он является аналогом локального ответа (ЛО).
События в синапсе :
На самой постсинаптической мембране ПД возникнуть не может, так как здесь отсутствуют потенциалзависимые каналы, они являются хемозависимыми!
Достигнув пороговой величины, то есть КУД, ПКП возбуждает соседнюю (внесинаптическую) мембрану мышечного волокна за счет местных круговых токов.
Особенности проведения возбуждения в нервно-мышечном синапсе
Одностороннее проведение возбуждения — только в направлении от пресинаптического окончания к постсинаптической мембране.
Суммация возбуждения соседних постсинаптических мембран.
Синаптическая задержка — замедление в проведении импульса от нейрона к мышце составляет 0,5-1 мс. Это время затрачивается на секрецию медиатора, его диффузию к постсинаптической мембране, взаимодействие с рецептором, формирование ПКП, их суммацию.
Низкая лабильность — она составляет 100-150 имп/с для сигнала, что в 5-6 раз ниже лабильности нервного волокна.
Чувствительность к действию лекарственных веществ, ядов, БАВ, выполняющих роль медиатора.
Утомляемость химических синапсов — выражается в ухудшении проводимости вплоть до блокады в синапсе при длительном функционировании синапса. Главная причина утомляемости — исчерпание запасов медиатора в пресинаптическом окончании.
Законы проведения возбуждения по нервам:
В зависимости от скорости проведения возбуждения нервные волокна подразделяются на 3 группы: A, B, C. В группе A выделяют 4 подгруппы: альфа, бетта, гамма и сигма.
Физиология мышечных волокон
Физиологические свойства скелетных мышц:
Физические свойства скелетных мышц:
Режимы сокращения:
Изотонический режим — сокращение мышцы происходит с изменением ее длины без изменения напряжения (тонуса) (напр.: сокращение мышц языка).
Изометрический режим — длина постоянная, увеличивается степень мышечного напряжения (тонуса) (напр.: при поднятии непосильного груза).
Ауксотонический режим — одновременно изменяется длина и напряжение мышцы (характерен для обычных двигательных актов).
Механизм сокращения поперечно-полосатых мышц
Миозиновые волокна соединены в толстый пучок, от которого в торону актиновых нитей отходят поперечные мостики. У каждого мостика выделяют шейку и головку.
Нить актина располагается в виде 2 скрученных ниток бус. На ней имеются актиновые центры.
Тропомиозин в виде спиралей оплетает поверхность актина, закрывая в покое ее центры. Одна молекула тропомиозина контактирует с 7 молекулами актина.
Тропонин образует утолщение на конце каждой нити тропомиозина.
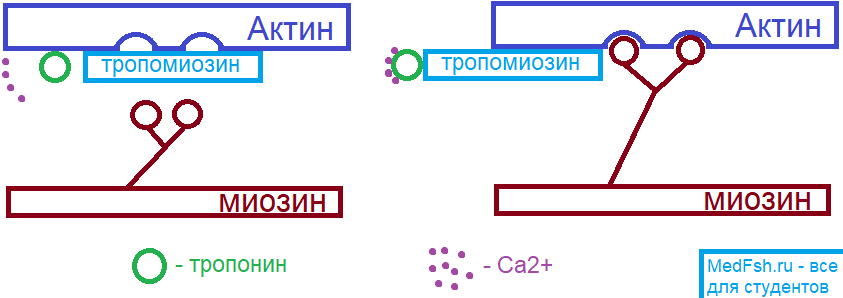
Под влиянием возникшего в мышечном волокне ПД из саркоплазматического ретикулума (СПР — депо Ca2+) высвобождаются ионы Ca. Кальций связывается с тропонином, который смещает тропомиозиновый стержень, что приводит к открытию актиновых центров.
В результате, к актиновым центрам присоединяются головки поперечных миозиновых мостиков.
Эти постики совершают «гребущие движения», в результате чего нити актина перемещаются этими мостиками относительно волокон миозина, происходит укорочение мышцы.
Процесс расслабления происходит в обратной последовательности с использованием энергии АТФ за счет функционирования кальциевого насоса.
При отсутствии повторного импульса ионы Ca не поступают из СПР. В результате отсутствия Ca-тропонинового комплекса, тропомиозин возвращается на свое прежнее место, блокируя актиновые центры актина. Актиновые протофибриллы легко скользят в обратном направлении благодаря эластичности мышцы, и мышца удлиняется (расслабляется).
Гладкие мышцы
Гладкие мышцы — это мышцы, формирующие слой стенок полых внутренних органов. Они построены из веретенообразных одноядерных мышечных клеток без поперечной исчерченности за счет хаотичного расположения миофибрилл.
Особенности гладких мышц:
Клетки в гладких мышцах функционально связаны между собой посредством щелевидных контактов — нексусов, которые имеют низкое электрическое сопротивление. За счет этих контактов ПД распространяется с одного мышечного волокна на другое, охватывая большие мышечные пласты, и в реакцию вовлекается вся мышца.
Гладкие мышцы способны осуществлять относительно медленные ритмические и длительные тонические сокращения.
Медленные ритмические сокращения обеспечивают перемещение содержимого органа из одной области в другую.
Длительные тонические сокращения, особенно сфинктеров полых органов, препятствуют выходу из них содержимого.
Это способность сохранять приданную им при растяжении или деформации форму. Благодаря пластичности гладкая мышца может быть полностью расслаблена как в укороченном, так и в растянутом состоянии.
Растяжение является адекватным раздражителем для гладкой мускулатуры. Сильное и резкое растяжение гладких мышц вызывает их сокращение.
Сравнительная характеристика скелетных и гладких мышц:
Кафедра физиологии
Разделы сайта
Новости
Нервно-мышечная физиология
Физиология нервов.
Центральная нервная система у человека состоит из нервных клеток, каждая из которых имеет один аксон и много дендритов. Нервные волокна делятся на: мякотные и безмякотные. Все они имеют шванновскую оболочку, а мякотные, кроме этого, покрыты еще миелиновой оболочкой между которой имеются перехваты Ранвье, в которых миелиновая оболочка отсутствует. Безмякотные волокна имееют малый диаметр, меньше 1,3 мкм, небольшую скорость распространения импульса до 2 м/сек, продолжительность ПД – 2 мсек. Мякотные возникли из безмякотных, диаметр до 25 мкм, скорость распространения возбуждения до 120 м/сек, продолжительность ПД – 0,4-0,5 мсек.
Распространение ПД по безмякотному волокну: немецкий физиолог Герман предложил теорию «местных токов», согласно которой при распространении возбуждения на мембране нервного волокна между возбужденным и невозбужденным участком возникает местный ток, который является раздражителем для невозбужденного участка. Если его величина достаточна для возникновения ПД в соседнем участке, то ПД распространяется на этот участок.
Распространение местных токов в безмякотных нервных волокнах прямопропорционально сопротивлению мембраны и обратнопропорционально сопротивлению внутри- и внеклеточной среды. Расстояние на которое распространяются местные токи будет тем больше, чем больше амплитуда ПД и чем меньше пороговый потенциал.
В мякотных волокнах возбуждение возникает при нанесении раздражения в перехватах Ранвье (теория Тасаки) и распространяется по мембране волокна сальтаторно (скачкообразно) (рис.1).

Рисунок 1. Проведение возбуждения по миелиновому нервному волокну.
При этом может охватывать не только один, но и два перехвата Ранвье, что обеспечивает надежность, а также увеличивает скорость распространения возбуждения и экономически более выгодна, так как на 1 импульс в безмякотном волокне энергия расходуется в 20 раз больше, чем в мякотном. Таким образом, скорость и расстояние, на которое распространяется возбуждение в безмякотных волокнах пропорциональна диаметру, сопротивлению мембраны и амплитуде ПД; в мякотных прямопропорциональна длине межперехватных участков, а их длина тем больше, чем больше диаметр волокна. Скорость не зависит от силы раздражения.
Теория Германа была экспериментально подтверждена.
Гельмгольц – определил скорость распространения импульса у лягушки; Бабский – определил скорость распространения импульса у человека. Эрландер и Гассер классифицировали различные нервные волокна на три группы А, В и С:
Законы проведение возбуждения по нервам.
I закон анатомо-физиологический целостности нервного волокна. Чтобы возбуждение распространялось по нервному волокну необходимо не только его морфологическая целостность, но и физиологическая непрерывность. Препараты для проводниковой анестезии нарушают физиологическую непрерывность тем, что инактивируют натриевую проницаемость в нервных волокнах.
II закон изолированного проведения возбуждения по нервному волокну. В смешанном нерве возбуждение с одного нервного волокна не передается на соседние, так как сопротивление межклеточной жидкости меньше чем сопротивление мембран соседних волокон. Этим обеспечив ается точность проведения информации в нервных волокнах к иннервируемым структурам.
III закон двухстороннее проведение возбуждения. Распространение ПД по мембране нервного волокна возможно в обе стороны, так как строение мембраны на всем протяжении одинаково. В то же время возбуждение не может возвратиться в участок, где оно возникло, так как он находится в состоянии рефрактерности.
Если второй парой электродов подействовать на поражённый участок, то возбуждение будет, т.е. ткань ещё жива.
Если снять альтератор, то ткань возвращается к исходному состоянию в обратном порядке фаз IV, III, II, I.
Парабиоз – это стойкое не распространяющееся возбуждение.
Возникают потенциалы меньшие по своей амплитуде, а дальше абортивные потенциалы, не способные распространяться: уменьшаются процессы Na-евой проницаемости, и увеличиваются процессы Na-евой инактивации.
Механизм нервно-мышечной передачи
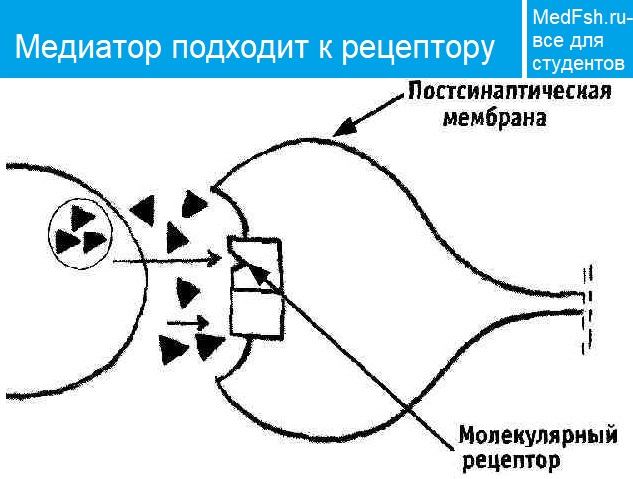
Синапсы представляют собой коммуникационные структуры, которые формируются окончанием нервного волокна и прилегающей к нему мембраной мышечного волокна (пресинаптической нервной и постсинаптической мышечной мембранами) (рис.2). 
Рис.2. Мионевральный синапс.
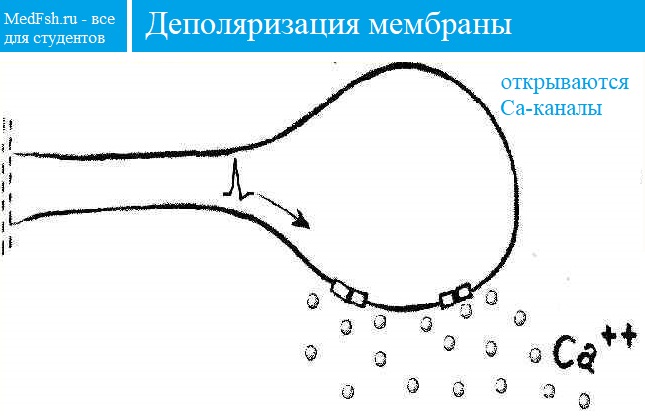
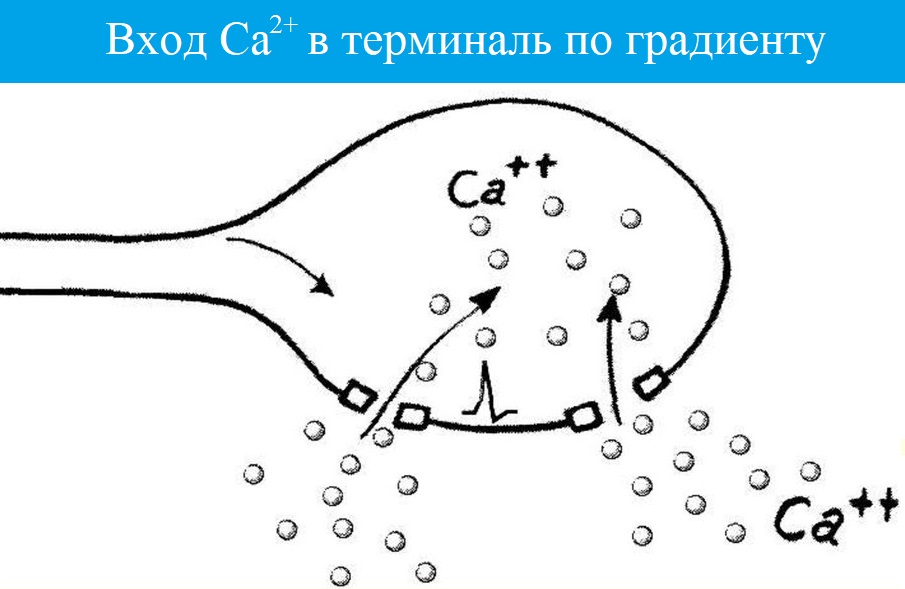
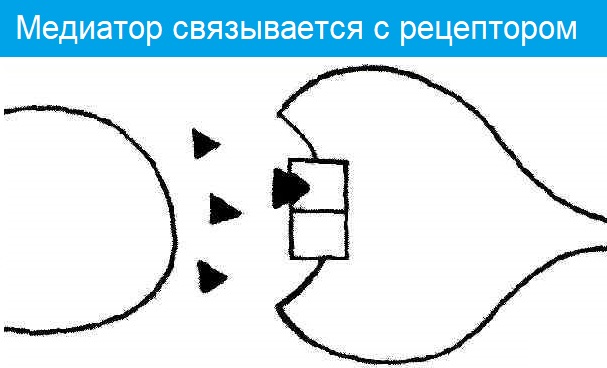
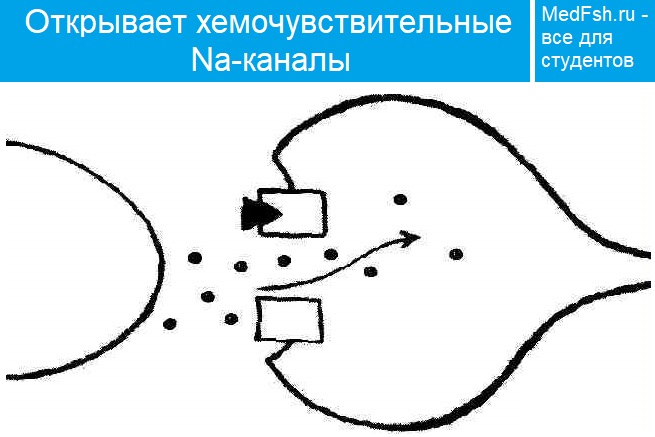
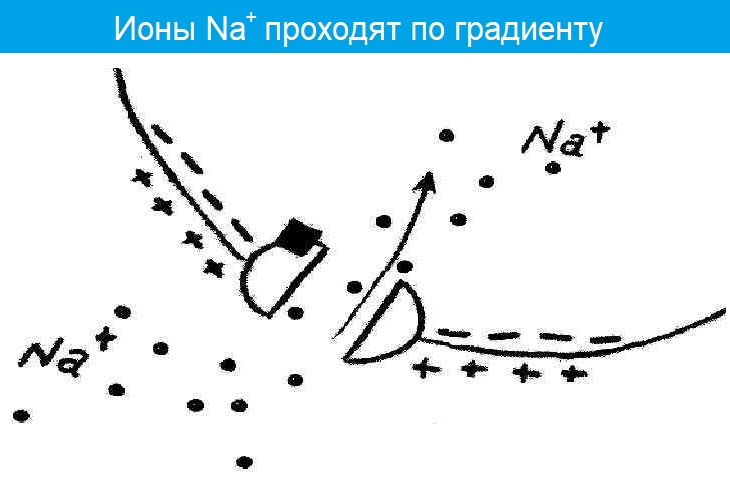
Когда нервный импульс достигает окончания аксона, на деполяризованной пресинаптической мембране открываются потенциалзависимые Са2+ каналы. Вход Са2+ в аксональное расширение (пресинаптическую мембрану) способствует высвобождению химических нейромедиаторов, находящихся в виде везикул (пузырьков) из окончания аксона. Медиаторы (в нервно-мышечном синапсе это всегда ацетилхолин) синтезируются в соме нервной клетки и путем аксонального транспорта транспортируются к окончанию аксона, где и выполняют свою роль. Медиатор диффундирует через синаптическую щель и связывается со специфическими рецепторами на постсинаптической мембране. Так как медиатором в нервно-мышечном синапсе является ацетилхолин, то рецепторы постсинаптической мембраны называют холинорецепторами. В результате этого процесса на постсинаптической мембране открываются хемочувствительные Nа+-каналы, возникает деполяризация, величина которой различна, и зависит от количества выделенного медиатора. Чаще всего возникает локальный процесс, который называют потенциалом концевой пластинки (ПКП). При повышении частоты стимуляции нервного волокна, усиливается деполяризация пресинаптической мембраны, а, следовательно, возрастает количество выделяемого медиатора и число активированных хемочувствительных Nа+каналов на постсинаптической мембране. Таким образом, возникают ПКП, которые по амплитуде деполяризации суммируются до порогового уровня, после чего, на мембране мышечного волокна, окружающей синапс, возникает ПД, который обладает способностью к распространению вдоль мембраны мышечного волокна. Чувствительность постсинаптической мембраны регулируется активностью фермента – ацетилхолинэстеразы (АЦХ-Э), который гидролизует медиатор АЦХ на составные компоненты (ацетил и холин) и возвращает назад – в пресинаптическую бляшку для ресинтеза. Без удаления медиатора на постсинаптической мембране развивается длительная деполяризация, которая ведет к нарушению проведения возбуждения в синапсе – синаптической депрессии. Таким образом, синаптическая связь обеспечивает одностороннее проведение возбуждения с нерва на мышцу, однако на все эти процессы расходуется время (синаптичекая задержка), что приводит к низкой лабильности синапса по сравнению с нервным волокном.
Таким образом, нервно-мышечный синапс является «выгодным» местом, куда можно воздействовать фармакологическими препаратами, изменяя чувствительность рецептора, активность фермента. Эти явления будут часто встречаться в практике врача: например, при отравлении токсином ботулизма – блокируется высвобождение медиатора АЦХ (разглаживание морщин в косметической медицине), блокада холиноререпторов (курареподобными препаратами, бунгаротоксином) нарушает открытие Nа+ каналов на постсинаптической мембране. Фосфоорганические соединения (множество инсектицидов) нарушает эффективность АЦХ-Э и вызывает длительную деполяризацию постсинаптической мембраны. В клинике используют специфические блокаторы нервно-мышечного проведения: блокада холинорецепторов курареподобными препаратами, сукцинилхолином и другими конкурентными ингибиторами, вытесняющими АЦХ с холинорецептора. При заболевании миастении из-за дефицита холинорецепторов на постсинаптической мембране (из-за их аутолитического разрушения) возникает прогрессирующая мышечной слабость, вплоть до полной остановки мышечных сокращений (остановка дыхания). В этом случае используют блокаторы АЦХ-Э, что приводит к увеличению длительности связывания медиатора с меньшим количеством холинорецепторов и несколько увеличивает амплитуду деполяризации постсинаптической мембраны.
Физиология мышц.
Существует 3 типа мышечной ткани: поперечно-полосатая, сердечная, гладкая.
Скелетная мышечная ткань образует большой объем соматической мускулатуры. Содержит хорошо выраженное упорядоченное строение сократительных белков в виде поперечной исчерченности. Связей между отдельными мышечными волокнами нет. Регуляция сокращений происходит сознательно.
Сердечная мышца содержит также поперечную исчерченность, но является функциональным синцитием. Благодаря наличию пейсмекерных клеток, обладает способностью генерировать спонтанные нервные импульсы, обеспечивающие сердечные сокращения.
В гладких мышцах нет поперечной исчерченности, которая бы придавала определенные физические и физиологические свойства этой ткани. Так в отличие от скелетной, которой присуща высокая эластичность, в гладкой мышце больше выражено свойство пластичности, что обусловлено отсутствием четкой упорядоченности миофиламентов актина и миозина. В отличие от регулярной саркомерной структуры скелетных и сердечной мышц, тонкие филаменты гладких мышц присоединены к структурам в цитоплазме, называемым плотными тельцами (прикрепительными бляшками сарколеммы), состоящими из белка десмина. Гладкие мышцы бывают висцеральные (мультиунитарные) и полиэлементные (унитарные).
Висцеральные содержат мостики- щелевые контакты с низким сопротивлением электрическому току – синцитий. Висцеральные мышцы встречаются в стенках полых органов (кишечник, матка, мочеточники, мочевой пузырь).
Полиэлементные гладкие мышцы состоят из отдельных мышечных единиц без соединительных мостиков, поэтому для них характерны точные, четко дозированные сокращения, подобно скелетным. Однако, сокращения этих мышц нельзя контролировать, в отличие от скелетных (мышцы радужки глаза, цилиарного тела, семенных протоков, артерии). Благодаря своему строению (висцеральные) обладают большой пластичностью, однако при определенной предельной степени растяжения способны деполяризоваться и сокращаться (саморегуляция). Пример, давление внутри стенок мочевого пузыря мало изменяется при относительно небольшом его растяжении, если растяжение возрастает резко – происходит сокращение мышц детрузора – эвакуация мочи даже в тех случаях, когда иннервация нарушена. Полиэлементные гладкие мышцы имеют более мощную (плотную) иннервацию и слабое развитие межклеточных контактов (нексусов). Тонус этих мышц и его колебания имеют нейрогенную природу. Имеют парасимпатические и симпатические, а также метасимпатические волокна. Строение нервных окончаний в гладкой мышце отличается от строения нервно-мышечного синапса в скелетной мышцы. В гладкой мышце нет концевых пластинок и отдельных нервных окончаний. По всей длине разветвлений адренергических и холинергических нервных волокон имеются утолщения, называемые варикозами. Они содержат гранулы с медиатором, который выделяется из каждой варикозы. Клетки, лишенные непосредственных контактов с варикозами, активируются ПД, распространяющимися через нексусы на соседние клетки. По ходу следования нервного волокна мышечные клетки могут возбуждаться или тормозиться (стимуляция адренергических волокон уменьшает, а холинергических – увеличивает мышечную активность, в других, например в сосудах, норадреналин – усиливает, а ацетилхолин – уменьшает мышечный тонус. Ионная природа гладкой мышцы определяется особенностями каналов мембраны гладко-мышечной клетки. Основную роль в механизме генерации ПД играют ионы Са2+, но по этим каналам могут внутрь клетки двигаться и другие двухвалетные ионы Ва2+, Mg2+. Вход Са2+ в клетку необходим для поддержания тонуса мышц и развития сокращения, поэтому блокирование Са2+ каналов гладких мышц приводит к ограничению поступления этого иона в цитоплазму миоцитов внутренних органов и сосудов, что широко используется в практической медицине для коррекции моторной функции ЖКТ и тонуса сосудов.
Регуляция мышечных сокращений зависит от объема иннервации. Аксон спинно-мозгового (двигательного) мотонейрона ветвится на несколько терминалей (веточек), каждая из которых подходит к одному мышечному волокну. Поэтому в целостном организме, при возбуждении 1 нервного волокна сокращается группа мышц. Совокупность двигательного нейрона и мышечных волокон, которые он иннервирует называют двигательной единицей. Количество мышечных волокон, входящих в двигательную единицу, различно и зависит о функции, которую реализует каждая конкретная мышца в организме. В мышцах глаз, кисти руки, которые обеспечивают высокоточные, координированные движения, 1 двигательная единица содержит 3-5 мышечных волокон. Двигательные единицы мышц спины, бедра – состоят из нескольких сотен мышечных волокон, которые регулируются одним мотонейроном.
Вернемся к мембране мышечного волокна, на которой распространяется ПД, возникший в результате «успешного» проведения возбуждения через синапс. Продолжением мембраны мышечного волокна является саркотубулярная система, образующая поперечные инвагинации (впячивания) (Т-система поперечных трубочек). Система Т-трубочек выполняет несколько важных функций: является внутриклеточным депо ионов Са2+; сообщается с внеклеточной жидкостью и таким образом регулируется содержание Са2+ в ней; содержит потенциалчувствительные Nа+ каналы, которые дают возможность ПД распространяться как вдоль, так и вглубь мышечного волокна. Система Т-трубочек обеспечивает быстрое и согласованное возбуждение мышечной клетки, так как распространение деполяризации по Т-системе сопряжено с выходом Са2+ из цистерн саркоплазматического ретикулума, обеспечивает инициацию сокращения мышцы. Через Т-трубочки может происходить выделение продуктов обмена (например, молочной кислоты) из мышечной клетки в интерстиций (межклеточное пространство) и далее в кровь. Большой объем клетки скелетной мышцы невозможно было бы активировать быстро, если бы Са2+ поступал из внеклеточной среды. Накоплению Са2+ в саркоплазматическом ретикулуме способствует белок (кальсеквестрин), который непрочно связывает Са2+ в ретикулуме. Высвобождение Са2+ из саркоплазматического ретикулума в скелетных мышцах происходит благодаря взаимодействию Т трубочек и концевых цистерн (триада).
Ионы Са2+ попав в саркоплазму инициируют сокращение, связываясь с белком тропонином – блокатором актина в покое (рис.3).

Рисунок. 3. Механизм мышечного сокращения.
1) работу Са-АТФ-азы, (активация насоса происходит за счет неорганического фосфата, образующегося при гидролизе АТФ),
2) за счет Э происходит откачивание против градиента концентрации Са2+ назад в саркоплазматический ретикулум (активный транспорт).
3) АТФ в мышечной клетке обеспечивает работу Na+-К-АТФ-азы, обеспечивающей удаление Na+ из клетки и восстановление потенциала покоя (а, следовательно, и возбудимости) мышечной клетки.
АТФ обеспечивает процессы, как сокращения, так и расслабления. Если Са2+ не будет транспортироваться назад в СПР, то расслабление не наступит, развивается ригидность мышцы (при трупном окоченении), или в живом организме – при посттетанической контрактуре – накопление Са2+ в саркоплазме инициирует длительное мышечное сокращение вне поступления ПД через синапс на мембрану мышечного волокна.
Гладкая мышца содержит также тропомиозин, но не имеет тропонина, соотношение актина к миозину 14-16 к 1, сравните в скелетных соотношение актина к миозину 2 к 1. Гладкая мышца имеет щелевые контакты – это мостики, соединяющие мембраны соседних клеток. Регуляция сократительной активности гладких мышц происходит благодаря связыванию Са2+ с кальмодулином, активирующим киназу легкой цепи миозина, которая приводит к гидролизу АТФ и запускает цикл образования поперечных мостиков.
ПД скелетной мышцы длится около 2-4- мс и проходит по мембране мышечного волокна со скоростью около 5 м/с. 1 ПД вызывает одиночное мышечное сокращение, которое начинается через 2 мс после начала деполяризации мембраны (латентный период) и завершается сокращение почти одновременно с реполяризацией. Длительность одиночного сокращения различна и зависит от типа мышечной ткани. При частых стимулах развивается суммарное мышечное сокращение всех мышечных волокон, обладающих различным сопротивлением мембран к электрическому току. Однако, незначительные отличия порогов возбуждения обеспечивают синхронность мышечного сокращения целой мышцы. Наличие абсолютного рефрактерного периода около 1-3 мс, обуславливает возникновение различных видов тетанусов (суммарных мышечных сокращений). Существует зубчатый и гладкий тетанусы. Частота стимуляции мышцы для развития гладкого тетануса должна быть выше, чем для развития зубчатого. Стимул должен попадать в фазу укорочения мышцы, если же мышцы начала расслабляться, а мы ее стимулирует, то получаем – зубчатый тетанус. Минимальный промежуток времени между последовательными эффективными стимулами во время тетануса не может быть меньше рефрактерного периода, которые приблизительно соответствует длительности ПД. Поскольку мышцы состоят из мышечных волокон с различным уровнем возбудимости, имеется определенная зависимость между величиной стимула и ответной реакцией. Увеличение силы сокращения возможно до определенного предела, после которого амплитуда сокращения остается неизменной при увеличении амплитуды стимула (надо отметить, то в мышце суммируются не ПД, а сокращения). При этом все волокна, входящие в состав мышцы принимают участие в сокращении.
В организме человека имеются быстрые, фазные мышечные волокна (белые), длительность сокращения которых до 7,5 мс, и медленные, тонические (красные), которые обеспечивают сильные и мощные движения, длящиеся до 100 мс. Красные (тонические) имеют много волокон миозина типа I, которые отличаются низкой активностью АТФ-азы миозина. Скорость расщепления АТФ является фактором, предопределяющим частоту гребковых движений, и таким образом, скорость скольжения нитей актина вдоль миозина. Из СПР Са2+ транспортируется медленно, высокая окислительная способность, много капилляров, много миоглобина в структуре миозина (тяжелые цепи), много митохондрий. На стимул реагируют медленно, имеют длительный латентный период сокращения, поэтому способны к длительным, медленным, тоническим сокращениям, более резистентны к утомлению. Главная функция – поддержание положения тела. Белые мышцы содержат волокна миозина II типа. Гликолитический тип окисления, мало миоглобина, митохондрий, это волокна большого диаметра с высокой активность АТФ-азы миозина, способны развить значительную силу, но быстро утомляются.
Сила мышц определяется тем максимальным грузом, который мышца в состоянии чуть-чуть приподнять. Сила различных мышц неодинакова. Для сравнения силы разных мышц максимальный груз, который мышца в состоянии поднять делят на число квадратных сантиметров ее физиологического поперечного сечения. Силовые характеристики выше у мышц с перистым (косым) расположением волокон, при этом физиологическое сечение больше геометрического поперечного сечения. Сумма поперечного сечения не всегда совпадает с физиологическим сечением мышцы (только при параллельном расположении волокон.
Сила сокращения изолированной скелетной мышцы при прочих равных условиях зависит от исходной длины мышцы. Умеренное растяжение мышцы приводит к тому, что развиваемая ею сила возрастает по сравнению с силой, которую развивает нерастянутая мышца. Происходит суммирование пассивного напряжения, обусловленного наличием эластических компонентов мышцы, и активного сокращения (переход к правилу средних нагрузок – физиологический механизм данного закона). Способность совершать работу определяется произведением величины поднятого груза на высоту подъема. Величина работы мышцы постепенно увеличивается с увеличением массы поднимаемого груза, но до определенного предела, после которого увеличение массы груза приводит к снижению величины работы, так как высота подъема груза резко падает. Следовательно, максимальная работа совершается мышцей при средних величинах нагрузок. Сила сокращения и работа не остаются постоянными при статической и динамической работе. В результате продолжительной деятельности работоспособность скелетной мускулатуры понижается. Это явление называют утомлением. При этом снижается сила сокращений, увеличивается латентный период сокращения и период расслабления. Статический режим работы более утомителен, чем динамический (почему объяснить). Накапливаются продукты процессов окисления- молочная пировиноградная кислота, которые снижают возможность генерирования ПД. Нарушаются процессы ресинтеза АТФ и креатинфосфата, необходимых для энергетического обеспечения мышечного сокращения. В естественных условиях мышечное утомление при статической работе в основном определяется неадекватным регионарным кровотоком. Возникает «кислородное голодание» и утомление прогрессивно нарастает.
В 1903 году Сеченов – восстановление работоспособности утомленной мышцы значительно ускоряется при совершении работы другой мышцей в период отдыха утомленной – такой отдых называют активным. Однако высокий уровень умственной деятельности ускоряет процессы развития утомления в мышечной системе (утомление нервных центров).