Поствакцинальный иммунитет к Коронавирусу
При введении вакцины в организм человека попадают отдельные белки вируса (безопасная часть), стимулирующие синтез антител еще до контакта с вирулентным микроорганизмом. При правильной реакции иммунитета на вакцинацию или вирусное вторжение в организме вырабатывается достаточный уровень иммуноглобулинов для дальнейшей защиты.
Вакцинальные препараты, зарегистрированные в 2020 году, содержат ген гликопротеина S. Спустя время у привитых людей ожидается появление антител, специфичных к S-протеину SARS-CoV-2. С учетом этого напряженность (степень защиты) поствакцинального иммунитета определяют при помощи теста на антитела класса IgG к спайковому (S) белку коронавируса.
Что представляет собой спайковый протеин (S)?
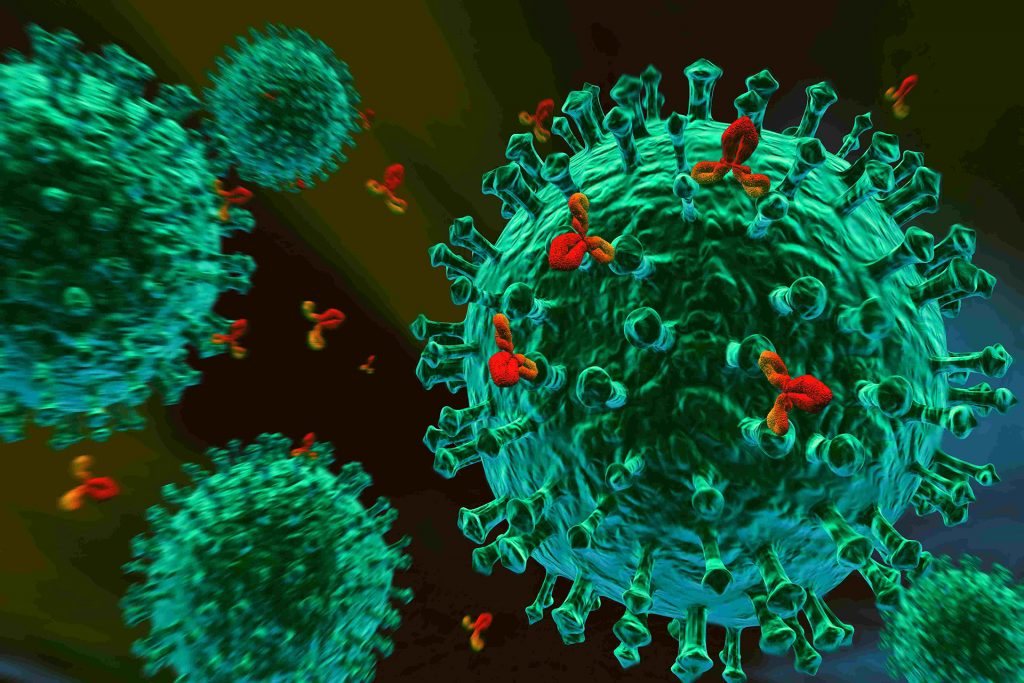
Одним из 4-х структурных белков коронавирусной оболочки является спайковый (spike — S). Именно он придает коронообразное очертание («шипики») этой вирусной частице. Хорошо рассмотреть его можно при электронной криомикроскопии. Протеин S обеспечивает проникновение вируса в клеточные структуры, что приводит к заражению.
Формирование иммунного ответа
После проникновения вирулентного агента в организм, иммунитет инициирует выработку иммуноглобулинов. Они необходимы для распознавания и связывания потенциально опасных антигенов. Если человек заболел недавно, во время острой стадии инфицирования в его организме первыми синтезируются IgM-антитела. Спустя 2-3 недели в ответ на антигенный стимул синтезируются антитела класса IgG.
Особенно активный ответ иммунитета вызывают 2 иммуногенных протеина коронавируса:
Для тех, кто провакцинировался и хочет проверить эффективность проведенной процедуры, целесообразно выбрать тип теста, который определяет антитела к спайковому (S) антигену вируса.
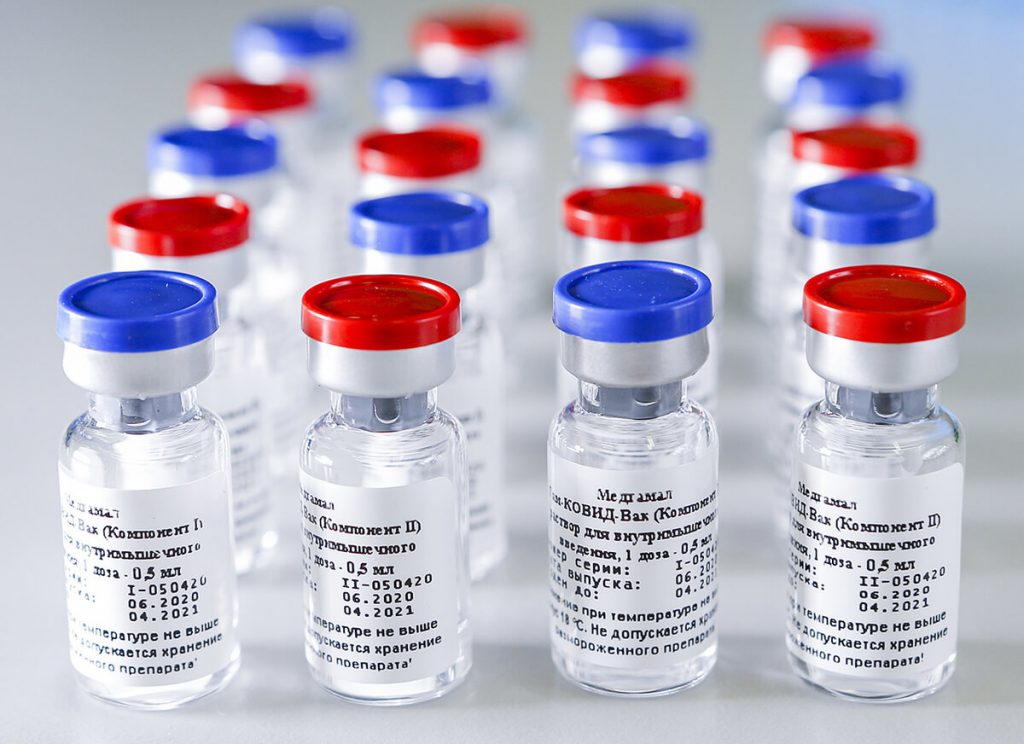
Механизм действия вакцины «Спутник V»
«Спутник V» — это российская вакцина с двухвекторной структурой. Вирусные векторы не способны размножаться и провоцировать заболевание. Но с их помощью можно доставить внутрь клетки вирусный генетический материал. Когда вектор с геном, кодирующим спайковый протеин, оказывается внутри человеческой клетки, начинается выработка S-белка.
Иммунитет человека, получившего вакцину, синтезирует иммуноглобулины класса G к антигену белка Spike SARS-CoV-2. Если в будущем такое лицо окажется в зоне воздействия коронавирусной инфекции, то в его крови уже будут присутствовать антитела. Именно они являются показателями поствакцинального иммунитета. После применения российского препарата судить об иммунитете можно после введения 2-х доз вакцины с интервалом в 21 день.
Оценка поствакцинального иммунного ответа
Антитела, нейтрализующие активность коронавируса, препятствуют связыванию гликопротеина S с ACE2. Последний является мембранным белком человека, который служит рецептором и точкой входа для коронавируса. RBD — структурный домен гликопротеина S принимает в этом непосредственное участие. Когда антитела его связывают, то контакт вируса с мембранным белком ACE2 блокируется.
Защищают от COVID не любые IgG-антитела, а именно анти-RBD. Даже после перенесенной болезни их может быть недостаточно в организме. Или же они могут полностью исчезнуть через полгода после инфицирования. Для оценки реальной устойчивости к COVID у пациента на момент тестирования, необходимо использовать только тест-системы нового поколения, которые выявляют наличие нейтрализующих антител к RBD (Anti-SARS-CoV-2).
В результате исследования можно подтвердить или опровергнуть наличие защитных свойств приобретенного иммунитета. А также такой тест позволяет увидеть динамику роста нейтрализующих антител к RBD и оценить степень защиты поствакцинального иммунитета. Для динамического наблюдения за показателями иммунитета рекомендуется выполнять исследование в одной лаборатории и по одной технологии.
В нашей клинике Вы можете сдать все анализы, в том числе и на АТ к новой Коронавирусной инфекции. Посмотреть цены
Спай белок коронавируса что это
В журнале Nature опубликован очень подробный обзор, характеризующих особенности строения и жизненный цикл SARS-CoV2, механизмы инфицирования и избегания своевременного иммунного ответа, обозначены потенциальные мишени для создания противовирусных препаратов. Также представлены результаты компьютерного моделирования строения вируса и механизмов проникновения в клетку.
Особенностью данного вируса является наличие очень большого количества гликанов на поверхности спайк-протеина, маскирующих его от иммунной системы человека. Поэтому на первом этапе заболевания вирус подобен «волку в овечьей шкуре» и остается невидим для иммунной системы. В дальнейшем, когда вирус уже размножился, иммунный ответ может развиться даже избыточно, что, по-видимому, лежит в основе тяжелого течения заболевания.
В S2- субъединице спайк-протеина есть три участка, делающих «ножку» спайк-протеина гибкой, что позволяет ей «искать» рецепторы на клетках хозяина более эффективно. Такая структура довольно редка для вирусов, обычно аналогичные «шипики» на поверхности вириона ригидны (такова, например, ситуация у вируса гриппа).
Важной частью спайк-протеина является RBD-домен, функцией которого является связь с рецептором ACE2 на поверхности клетки-хозяина. У SARS-CoV2 эта связь в 2-4 раза сильнее, чем у вируса SARS. Во время взаимодействия с рецептором этот домен «выдвигается» из-за двух маскирующих его молекул гликанов. Исследования in vitro показали, что мутации в этих двух гликанах могут полностью нарушать процессы проникновения вируса в клетку. Для эффективного взаимодействия RDB и ACE2 предпочтительна более «высокая» позиция этого домена на остальными структурами. У альфа варианта вируса найдено 10 дополнительных мутаций, приводящих RBD – домен в более «высокое» положение, а у дельта вируса – еще 3 мутации.
Попав в клетку, вирус подавляет экспрессию генов клетки-хозяина, в том числе – образование интерферонов, сигнализирующих о вирусной инфекции. Для ковидной инфекции типична очень низкая концентрация интерферонов в крови.
В дальнейшем может происходить формирование синцитиев из клеток легочной ткани. Считается, что синцитии позволяют дольше и эффективнее вырабатывать вирусные белки. Такой тип агрессии типичен для персистирующих вирусов – например, ВИЧ. SARS-CoV2 индуцирует даже формирование синцитиев клеток респираторного эпителия с лимфоцитами, что мешает нормальному иммунному ответу. Такой тип «маскировки» от иммунитета типичен для опухолей, а не вирусов.
В дальнейшем перестраивается эндоплазматический ретикулум с формированием шарообразных двухмембранных структур, в которых происходит активный синтез белков вируса. Выход вирионов наружу осуществляется в лизосомах, формирующихся в комлексе Гольджи, путем экзоцитоза. Считается, что молекулярные механизмы, ответственные за описанные процессы, могут быть мишенями для противовирусной терапии.
В месте соединения S1 и S2 субъединиц спайк-протеина есть зона, которая способна связывать и быть расщепленной фурином – протеазой клетки-хозяина, содержащейся в лизосомах. Такое предварительное расщепление значительно упрощает в дальнейшем взаимодействие с трансмембранной протеазой TMPRSS2 и значительно увеличивает проникновение вирусной частицы в следующую клетку. Для вируса SARS показано, что порядка 10% вирусных частиц на выходе из клетки – хозяина связано с фурином. У вируса SARS-CoV2 в соответствующем локусе, отвечающем за связь с фурином, идентифицированы мутации. Как следствие, до 50% вирионов альфа-разновидности SARS-CoV2, выходящих из клетки-хозяина, связаны с фурином, а в случае дельта-вируса – до 90%, что, по-видимому, и объясняет более агрессивное распространение этого варианта вируса. Есть данные, что у пациентов с дельта-формой в тканях легких и носоглотки содержание вирионов достоверно выше, чем у носителей альфа-формы.
По материалам: Megan Scudellari. How the coronavirus infects cells — and why Delta is so dangerous. Nature 595, 640-644 (2021). doi:
Анализ на IGg к спайковому (S) белку SARS CoV-2
Лабораторные методы диагностики коронавируса продолжаются совершенствоваться и дополняться. Сегодня клиника «ПрофМедЛаб» может предложить анализ на иммуноглобулины класса G к спайковому (S) белку SARS CoV-2. Рассказываем о том, кому будет полезно это исследование.
Продукция организмом IgG является результатом ответа иммунной системы на присутствие возбудителя в организме. Обычно они вырабатываются через 3–4 недели после инфицирования и сохраняются на протяжении длительного времени. Такие антитела вырабатываются к нуклеокапсидному белку вируса и позволяют подтвердить факт перенесенной инфекции. Говоря другими словами, с помощью такого анализа можно понять, болел человек в прошлом или нет. Однако при этом определить уровень иммунной защиты в результате такого исследования нельзя.
Вопрос решается с помощью другого анализа — определение иммуноглобулинов G к спайковому (S) белку. Эти антитела обычно используют для определения специфического иммунитета, который формируется после перенесенного заболевания. Наиболее целесообразно выполнять такой анализ до и после вакцинации. Таким образом, можно понять, какой уровень защиты имеется у конкретного человека. Определять уровень антител к спайковому (S) белку можно и у тех людей, которые болеют в настоящий момент.
Стоимость исследования в клинике «ПрофМедЛаб» — 1300 рублей. Материалом для анализа является венозная кровь. Для получения информации звоните по телефону: +7 (495) 120-08-07.
Нейтрализующие антитела к коронавирусу SARS‑CoV‑2, спайковый (S) белок, IgG, количественно ( Тест анти-RBD)
Доступен анализ на нейтрализующие антитела класса g после вакцинации или перенесенного COVID-19. ( Количественное определение антител класса IgG к RBD-домену спайкового (S) белка SARS-Co-V-2, пре- и поствакцинальные).
АКЦИЯ: все анализы со скидкой 25 %. (переходите по ссылке)
Что за тест анти-RBD и что он показывает?
В ответ на заражение организм начинает реагировать выработкой антител различных классов. Именно их обнаружение позволяет установить факт инфицирования даже у бессимптомных пациентов. IgG начинают выявляться в среднем на 3-й неделе заболевания, перемещаясь по сосудистому руслу пациентов длительно время. При лабораторном тестировании возможно определение IgG к различным белкам вируса. Наличие антител класса IgG к нуклеокапсидному белку является показателем перенесенной инфекции.
Выявление IgG к рецептору связывающего домена (RDB) – позволяет судить о наличии защитного иммунитета, который мог сформироваться после перенесенного заболевания, так и после вакцинации. Антитела к рецептору связывающего домена S белка обладают нейтрализующими свойствами и препятствуют связыванию вируса с клетками человека, тем самым обеспечивая важную роль в определении индивидуального протективного (защитного) иммунного ответа к SARS-CoV-2.
Кому показан и когда нужно сдавать тест на наличие антител к S-белку?
В первую очередь анализ на определение нейтрализующих антител класса g ( АНТИ RBD) показан лицам переболевшим новой коронавирусной инфекцией и лицам, после вакцинации препаратом «Спутник V» (Центр Гамалеи), а также другими вакцинами, разрешенными к применению на территории РФ. Рекомендуемый срок сдачи анализа на антитела после вакцины «Спутник V» 35-42 дня с момента постановки первого компонента. Для выявления антител после вакцины ЭпиваКкорона необходимы специальные тест системы «Вектор».
Чувствительность теста в диапазоне 80-99 %, специфичность 95-99%
Расшифровка результатов исследования
Некоторые регионы планируют выдачу QR-кода при высоком уровне нейтрализующих антител даже у неофициально переболевших лиц ( Лица переболевшие дома с отрицательным тестом ПЦР). Анализ нужно будет сдать в специальных аккредитованных лабораториях.
Образец анализа на антитела к коронавирусу (ABBOT)
При каком уровне антител нужно прививаться от коронавируса?
Положительные антитела и опасность для окружающих
Антитела могут сохранятся и определятся в сыворотке в течении 5-7 месяцев после начала заболевания. Уровень антител зависит от нескольких факторов, перечисленных выше. (Вес, пол, влияние вредных факторов, степень тяжести перенесенного заболевания и тд.). Все чаще и чаще высказывается в научных кругах мнение, что в связи с появлением нового штамма «Дельта» ( Индийский штамм) необходим более высокий уровень антител, поэтому рекомендуем периодически сдавать анализ, с целью отслеживания динамики титров антител. В случае снижения титров до низких показателей, следует рассмотреть вопрос о ревакцинации.
По последним исследованиям, (статья опубликована 12.10.2021 ) проведенного в Швеции и Италии, показали, что у большинства переболевших COVID-19 в первые полгода количество антител снижалось постепенно, после чего показатель ( в течении 8-9 месяцев) до 15 месяцев был стабильным.
Авторы собрали 188 анализов крови у 136 пациентов, у которых заболевание сопровождалось характерными симптомами и протекало в различной форме, от легкой до тяжелой. В качестве контрольной выборки использовали плазму 108 человек с подтвержденным отрицательным ПЦР-тестом.
Ученые измеряли титры анти-S и анти-RBD антител в плазме. Первые специфически направлены на спайковый белок, или S-белок вируса целиком, а вторые — на рецептор-связывающий домен (RBD) S-белка, играющий ключевую роль в связывании вируса с клетками. Известно, что со временем в структуре S-белка и RBD-домена накапливаются мутации, которые снижают нейтрализующую способность антител. Задачей ученых было определить время, в течение которого антитела плазматических клеток сохраняют активность.
Результаты показали, что на пике иммунного ответа у выздоравливающих пациентов уровни анти-RBD иммуноглобулинов IgM и IgG были увеличены на 77 и 85 процентов соответственно, но затем в течение шести-пятнадцати месяцев упали до 4,5 и 11 процентов. Антитела IgM и IgG к S-белку показали значения чуть выше — соответственно 88 и 90 процентов в первые один-три месяца и вполовину меньше через 55-56 дней.
Титры специфических антител IgG к RBD и S-белку у 94 процентов пациентов достигли максимума через 15-28 дней после появления симптомов, потом, после прохождения пика ответа антител, они постепенно уменьшились примерно в четыре раза к концу шестого месяца, а затем оставались стабильными до 15 месяцев. Дольше сохранялся высокий уровень антител у тех, кто переболел COVID-19 в тяжелой форме.
Для сравнения ученые оценили уровень специфических IgG антител в плазме вакцинированных. Оказалось, что через 14-35 дней после введения первой дозы вакцины титры антител были аналогичны таковым у переболевших через шесть месяцев после заражения, а после второй соответствовали максимальному уровню естественного ответа у выздоравливающих пациентов.
Помимо основного штамма SARS-CoV-2, авторы проверили эффективность антител в отношении бета, гамма и дельта-вариантов (мутировавшие штаммы) в течение 15 месяцев после заражения и подтвердили, что нейтрализующая активность антител, хоть и в меньшей степени, сохраняется и для этих вариантов коронавируса.
Кроме того, ученые определяли уровень Т-клеточного ответа, пик которого был отмечен между третьим и шестым месяцами после заражения, за которым последовало значительное снижение через 12-15 месяцев. Однако интенсивность и продолжительность ответа при этом не зависели от тяжести заболевания.
Авторы исследования уточняют, что для оценки длительного иммунитета, сохраняющегося в В-клетках памяти, 15 месяцев, в течение которых проводили исследование, недостаточно, но очевидно, что у большинства перенесших COVID-19 пациентов циркулирующие В- и Т-клетки памяти и нейтрализующие антитела присутствуют в плазме крови до 15 месяцев после заражения.
Несколько слов про новый штамм «Омикрон»
Где можно сдать анализ на нейтрализующие антитела к S белку?
Спайк-белок коронавируса сам по себе вызвал нарушения свертываемости крови
Lize M. Grobbelaar et al. / medRxiv, 2021
Биологи провели микроскопические исследования образцов крови здоровых людей с добавленным спайковым белком коронавируса и без него, а также пациентов, больных ковидом. Исследователи заметили, что добавление в кровь свободного S-белка вызывало формирование амилоидных сгустков и изменения формы клеток крови. Кроме того, ученые смоделировали ток плазмы в сосудах и экспериментально показали, что у пациентов с ковидом он может быть сильно затруднен. Препринт статьи опубликован на портале medRxiv.
Вызываемую SARS-Cov-2 инфекцию можно охарактеризовать беспрецедентными для других респираторных инфекций патологиями. Среди них – нарушения свертываемости крови (коагулопатии), которые могут приводить либо к кровотечениям, либо тромбозам. Связывание спайкового S-белка с рецепторами в момент проникновения вируса в клетку может вызывать клеточные патологии, но само по себе не может объяснить такую распространенность коагулопатии у пациентов. Однако S-белок путешествует в организме и сам по себе отдельно от вируса, высвобождаясь из инфицированных клеток: его, например, находили в мочеиспускательном канале. Частицы этого белка также могут проникать сквозь гематоэнцефалический барьер.
Ученые из Университета Стелленбоша под руководством Итерезии Преториус (Etheresia Pretorius) изучили способность частиц S-белка взаимодействовать напрямую с тромбоцитами и белком фибриногеном, вызывая в нем изменения и, как следствие, нарушения свертываемости крови. Сначала исследователи при помощи флуоресцентной микроскопии проверили, накапливаются ли аномальные амилоидные комплексы в плазме здоровых людей с добавлением частиц S-белка и без них. В образцы с добавлением одного нанограмма на миллилитр S-белка добавляли тромбин (активатор коагуляции) и делали микрофотографии. В тех образцах, куда попал вирусный белок, формировались более плотные фибриновые сгустки. В образцах цельной крови спайковый белок вируса вызывал гиперактивацию тромбоцитов.
Плазма здоровых людей без добавления спайк-белка (А) и с ним (В). После добавления тромбина в образцах с S-белком формируются более плотные сгустки.