Сосудистые заболевания почек: факторы риска и симптомы
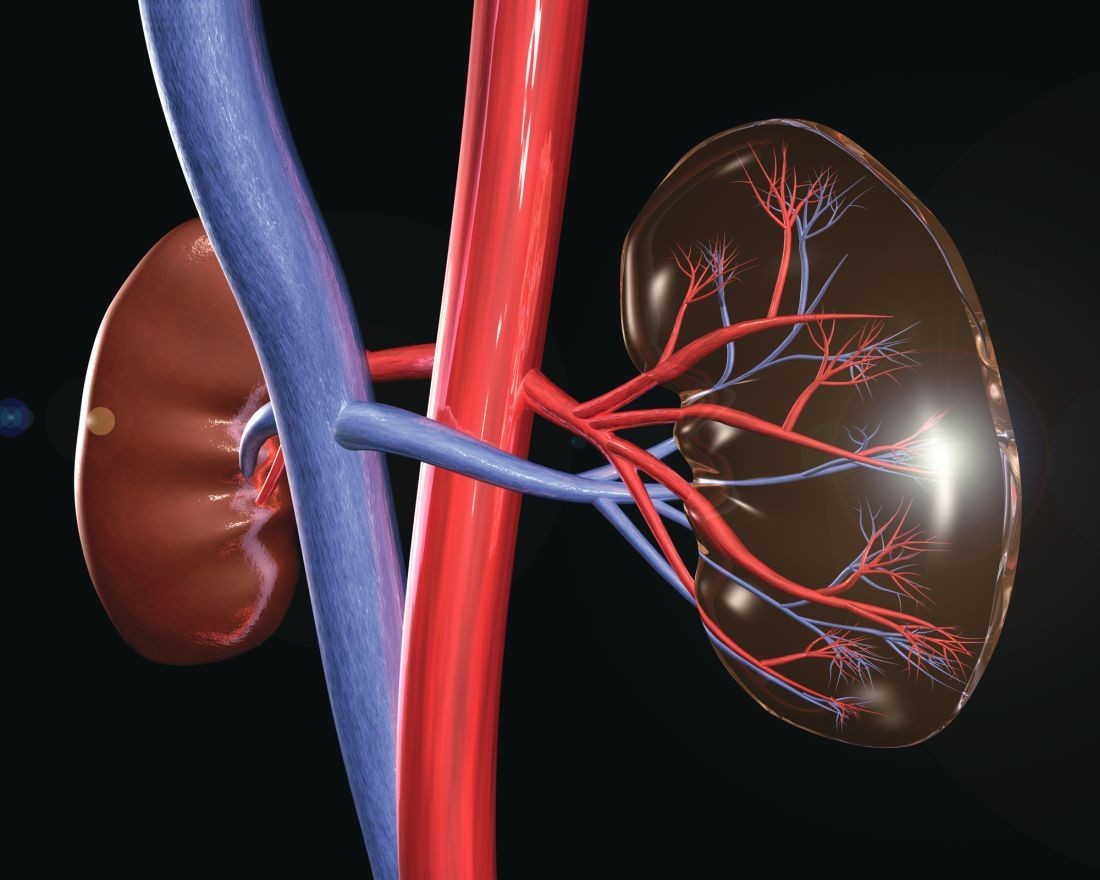
Стабильный приток крови и здоровое состояние сосудов – необходимое условие для нормального функционирования всех систем органов. Почки реагируют на сосудистые изменения в числе первых – появляется гипертензия, в обратном случае – инфаркт почки. Состояния опасны тем, что могут привести к неспособности органа перерабатывать продукты жизнедеятельности – почечной недостаточности.
Виды сосудистых заболеваний почек
Заболевания сосудов почек и мочевыделительной системы классифицируются по группам:
К врожденным аномалиям развития сосудов почки относят лишний, добавочный сосуд. Изменения в количестве артерий нарушает кровяной приток, необходимый для полноценного функционирования.
Причины патологий
Заболевания выделительной системы имеют факторы риска и прямые причины появления. К последним относят:
Факторы риска включают:
При наличии почечных патологий в семейном анамнезе, нужно проходить обследование регулярно!
Клиническая картина
Патология сосудов почек сопровождается яркой клинической картиной, включающей один или несколько симптомов:
Лечение сосудов почек начинается после сбора всей клинической картины, лабораторной и инструментальной диагностики. Сосуды почек проверяют при помощи УЗИ и допплерографии. Исследования показывают наличие, структуру, расположение артерий, позволяют оценить кровоток и обнаружить патологические отклонения.
Возможные осложнения
Своевременное обращение к урологу, нефрологу, комплексная диагностика и лечение помогут предотвратить осложнения сосудистых заболеваний почек:
Специалисты Государственного центра урологии готовы прийти на помощь в лечении сосудистых заболеваний почек. Комплексная диагностика и консультация доктора медицинских наук, современные методы лечения с коротким периодом реабилитации – доверьте свое здоровье врачам высшей категории с многолетним опытом!
Узи почек: норма и расшифровка результатов
Ультразвуковое исследование почек в большинстве случаев является полноценным и достаточно информативным методом диагностики с целью определения заболевания и назначения адекватного лечения, а так же исключения патологии при скрининговых обследованиях.
Что показывает УЗИ почек?
При ультразвуковом исследовании почек УЗИ-аппарат позволяет определить следующие основные параметры:
Количество
В норме почки являются парным органом, но встречаются аномалии.
Возможно врожденное отсутствие почки – односторонняя аплазия (агенезия), либо утрата парности в результате хирургического удаления. Встречается врожденное удвоение почки, чаще одностороннее.
Аплазия левой почки
Удвоенная почка без признаков обструкции
Расположение
В норме почки расположены на разных уровнях относительно друг друга: правая (D) почка находится на уровне позвонков 12 грудного и 2 поясничного, левая (L) почка – на уровне позвонков 11 грудного и 1 поясничного.
На УЗИ можно выявить опущение почки (нефроптоз) или нетипичную локализацию органа (дистопия), вплоть до расположения в малом тазу.
В норме почка имеет бобовидную форму и ровный наружный контур с четкой визуализацией фиброзной капсулы в виде гиперэхогенной линии.
Размеры
Физиологической норме у взрослого человека соответствуют размеры почек:
Толщина слоя паренхимы – еще один очень важный параметр, в норме составляет 18-25 мм. Этот показатель зависит от возраста пациента: у пожилых людей он может уменьшаться до 11 мм в результате склеротических изменений. Паренхима является функциональной частью почки, в ней расположены структурно-функциональные единицы – нефроны. Увеличение показателя может быть признаком отека или воспаления почки, уменьшение свидетельствует о дистрофии органа.
У детей размеры почек зависят от возраста и роста ребенка. При росте до 80 см измеряются только два параметра – длина и ширина органа. У детей ростом 100 см и выше измеряется и толщина паренхимы.
В норме должна четко выявляться граница почечных пирамидок в паренхиматозном слое: эхогенность пирамидок ниже, чем паренхимы. При гидронефрозе дифференциация между ними отсутствует.
Увеличение размеров почки характерно для острого пиело- или гломерулонефрита, а так же если почка утратила парность и испытывает повышенную функциональную нагрузку.
Эхогенность паренхимы
Этот показатель определяет состояние почечной паренхимы, ее структуру. В норме она однородна.
Эхогенность – это степень интенсивности отражения звуковой волны от тканей: чем плотнее ткань, тем интенсивнее отражение и светлее изображение на мониторе. Ткани с низкой плотностью имеют слабую эхогенность и визуализируются темными участками. Жидкости и воздух анэхогенны.
К примеру, полостную кисту, содержащую жидкость, специалист описывает как анэхогенное образование. Гиперэхогенность характерна для склеротических процессов в почке (гломерулонефрит, диабетическая нефропатия, опухоли, амилоидоз).
Состояние полостной системы почек
Полостная система почек или чашечно-лоханочная система (ЧСЛ) выполняет функцию сбора мочи. На УЗИ могут диагностироваться следующие изменения:
Ультразвуковое изображение расширения полостных систем обеих почек у плода
В норме ЧЛС анэхогенна и не визуализируется. Камни размером 4-5 мм и более в УЗИ-заключении описываются как эхотень, гиперэхогенное включение, эхогенное образование. Наличие песка обозначается как микрокалькулез почек.
Состояние почечного кровотока
Для визуализации почечных кровеносных сосудов используют дуплексное сканирование (или допплерографию), при котором УЗИ-сканер выдает информацию в виде цветного изображения или спектрального графика. Методика является неинвазивной и безболезненной.
Исследование позволяет определить состояние сосудистой стенки, наличие внутрисосудистых обструкций и стенозов, определить скорость кровотока. В норме скорость может колебаться от 50 до 150 см/сек.
На цветовой схеме нормальными считаются темные тона. Яркий цвет фиксирует ускоренный кровоток и свидетельствует о наличии стеноза, основным признаком которого считается усиление кровотока в почечной артерии больше 200 см/сек.
Определяется индекс сопротивления кровотока или индекс резистентности, который напрямую зависит от возраста пациента: чем старше, тем выше скорость кровотока и выше индекс. В норме индекс сопротивления для почечной артерии – 0,7, для междолевых артерий – 0,34-0,74.
Кто проводит расшифровку результатов?
Расшифровку ультразвукового исследования почек должен проводить врач-уролог. К словесному заключению обычно прилагается фото УЗИ или сонограмма, где стрелками отмечается место выявленных патологических изменений.
При обнаружении опухолей или сосудистых изменений неплохо, если будет прилагаться видео УЗИ.
Какие заболевания выявляет УЗИ почек?
Ультразвуковая диагностика наиболее информативна относительно следующих почечных заболеваний и синдромов:
Если в заключении УЗИ почек значится «выраженный пневматоз кишечника», это означает неинформативность обследования по причине метеоризма и в этом случае УЗИ придется повторить после подготовки (употребление ветрогонных препаратов).
Видео:
УЗ анатомия почек
Порядок выполнения: ультразвуковое исследование почек
Подготовка к УЗИ почек
Значение нарушений внутрипочечной гемодинамики в формировании и прогрессировании тубулоинтерстициального поражения почек у детей

Проведено сопоставление комплекса клинических и параклинических данных 118 детей с рефлюкс-нефропатией на разных стадиях тубулоинтерстициального поражения почек (ТИПП), 40 детей с пузырно-мочеточниковым рефлюксом (ПМР) без признаков нефросклероза. Параме
We examined 118 children with reflux nephropathy in different stages of renal scarring and 40 patients with vesico ureteric reflux without interstitial fibrosis. Parameters of intrarenal haemodynamics can be used for early diagnostics of reflux nephropathy in patients with vesico ureteric reflux and also for diagnostics of stages of renal scarring.
Тубулоинтерстициальное поражение почек (ТИПП) у детей занимает ведущее место среди хронических заболеваний почек, приводящих к снижению качества жизни и социальной активности пациентов, ранней инвалидизации с формированием хронической болезни почек (ХБП), терминальной почечной недостаточности (тХПН) уже в детском возрасте [1].
Тубулоинтерстициальное поражение почек — это воспалительное (бактериальное и абактериальное) и невоспалительное повреждение интерстициальной ткани почек с расположенными в ней сосудами (артериальными и венозными), лимфатическими протоками, нервными окончаниями, а также чашечно-лоханочной системы врожденного, наследственного или приобретенного генеза с исходом в нарастание необратимых морфологических изменений (интерстициальный фиброз) параллельно со снижением функциональных возможностей почек, формированием ХБП [2].
В настоящее время в литературе широко обсуждается патогенетическое значение нарушений интраренальной гемодинамики в инициации почечного повреждения и прогрессировании ТИПП у детей [3].
Ряд авторов считают, что приоритет в диагностике нефросклероза принадлежит ультразвуковым методам визуализации [4, 5].
Допплерография сосудов почек позволяет оценить внутриорганную гемодинамику. Данный метод в силу своей высокой разрешающей способности и визуализации мельчайших сосудов вплоть до системы микроциркуляторного русла получил название «ультразвуковой ангиографии» [6].
При исследовании почечных сосудов в режиме центрального допплеровского картирования (ЦДК) окрашивается все сосудистое дерево почки: сегментарные, междолевые, дуговые артерии. Исследование позволяет визуализировать эти виды сосудов с оценкой их архитектоники, провести морфометрию, диагностировать локальные и диффузные нарушения внутрипочечной гемодинамики. ЦДК позволяет оценить три параметра кровотока одновременно: направление, скорость и характер (однородность и турбулентность). При этом исключается возможность «наслаивания» близлежащих сосудов, имеющих различные типы кровотока, друг на друга [7].
Обеднение внутрипочечного кровотока свидетельствует о значительной ишемии коркового слоя, отражая такие сосудистые изменения, как нефросклероз, гиалиноз мелких артерий с сужением их просвета [8]. При ТИПП именно процессы фиброзирования тубулоинтерстициальной ткани почек приводят к деформации сосудистого рисунка за счет экстравазального воздействия: уменьшение числа мелких ветвей сегментарных артерий вплоть до картины «обгорелого дерева», уменьшение диаметра почечной артерии, сегментарных артерий, выраженная деформация, извитость сегментарных артерий и хорошая визуализация ренальной ангиоархитектоники вплоть до мелких ветвей викарно увеличенной контралатеральной почки. С. С. Пауновой установлено, что изменения параметров внутрипочечной гемодинамики нередко предшествуют лучевым, радионуклеидным и ультразвуковым данным диагностики ТИПП при ПМР [9].
В режиме допплерографии наиболее важными характеристиками внутрипочечной гемодинамики являются линейные показатели скорости кровотока (систолическая и диастолическая скорости кровотока), позволяющие косвенно судить о состоянии и величине периферического сосудистого сопротивления.
Установлено, что повышение показателей индексов Ri и Рi характерно для вазоспастических реакций при воспалительных и склеротических процессах в периваскулярных тканях почки. Механизм, лежащий в основе повышения Ri при поражении сосудов почек, до конца не ясен. Установлена связь между повышенным внутрипочечным сосудистым сопротивлением и снижением функции почек. Снижение величины указанных выше показателей наблюдается в случаях развития артериовенозного шунтирования при истощении миогенного механизма регуляции внутрипочечной гемодинамики. Подключение данного механизма сопровождается снижением гидростатического давления в клубочках и в сосудах, ишемией клубочка и усугублением его склерозирования [10]. K. Galesic установил, что увеличение почечного сосудистого сопротивления по индексу Ri у пациентов с эссенциальной гипертензией отражает развитие нефросклероза, вызванного гипертензией [11]. Ю. Б. Перевезенцева показала, что при уровне Ri 0,71 можно предположить с высокой вероятностью наличие ТИПП [12]. Е. Б. Ольховой установлено, что уменьшение Vmax на почечной артерии менее 0,4 м/с является признаком снижения функции почки [13].
Таким образом, эхографические методы диагностики позволяют оценить не только анатомические, но и функциональные характеристики почек, в том числе и у больных без явных клинических проявлений ХБП, что позволяет использовать данный метод как для ранней диагностики, так и для диагностики прогрессирования ТИПП.
Материалы и методы исследования
Целью данного исследования было установить изменения параметров внутрипочечной гемодинамики у детей с пузырно-мочеточниковым рефлюксом (ПМР) и рефлюкс-нефропатией (РН) на разных стадиях ТИПП.
Проведено обследование 188 детей, в том числе 118 детей с РН на разных стадиях ТИПП; 40 пациентов с ПМР без признаков ТИПП, 30 детей контрольной группы (табл. 1).
Критерии включения пациентов в клиническое обследование:
Критерии исключения больных из исследования:
В результате проведенного обследования выделены следующие группы клинического наблюдения:
1) дети с ПМР без признаков ТИПП (n = 40);
2) дети с РН А (n = 30);
3) дети с РН В (n = 30);
4) дети с РН С (n = 30);
5) дети с РН D (n = 28).
Контрольную группу составили условно здоровые дети (n = 30).
При постановке диагноза РН использована классификация, предложенная J. M. Smellie, основанная на степени нефросклероза, верифицированного по результатам нефросцинтиграфии (НСГ):
Диагноз ПМР верифицировался на основании критериев, разработанных Комитетом по интернациональному изучению пузырно-мочеточникового рефлюкса в 1981 г. по степени заброса рентгеноконтрастного вещества и дилатации чашечно-лоханочной системы почек.
Клинико-параклиническое обследование детей проводилось в ГАУЗ ГКБ № 6 города Оренбурга.
Нефросцинтиграфия, позволившая верифицировать стадии РН, проводилась на базе отделений радиоизотопной диагностики ГБУЗ Оренбургская ОКБ.
Динамическая и статическая НСГ с фармпрепаратом, меченным 99mTc-пентатех, проводилась на сцинтиляционной γ-камере «МВ-9200» с оценкой обработки данных по программе «Сцинтипро», регистрирующей ангиографические, ренографические и сцинтиграфические показатели почек. По сцинтиграммам определяли форму, размер, положение почек, состояние их паренхимы, очаги патологического распределения радиофармпрепарата (РФП); по уровню накопления и характеру распределения активности в почечной паренхиме оценивали состояние гемодинамики почек и отдельных участков ее сосудистого русла:
Пациентам проводились ультразвуковое исследование почек с определением внутрипочечной гемодинамики в режиме допплерографии почечных сосудов, который состоит в возможности визуализации всех движущихся жидкостей организма в режиме реального времени и проведении анализа их движения. В основе — сочетание изображения органа, включая сосуды в В-режиме с одновременным исследованием кровотока в сосуде, основанном на использовании эффекта Допплера. Данная методика позволяет визуализировать деформации сосудов (изгибы, извитости, петли), которые могут иметь приобретенный характер в случае экстравазального воздействия, например, в результате рубцевания почечной паренхимы при вторичном сморщивании почки. В таком случае сосудистые деформации имеют множественный характер. В деформированных сосудах кровоток приобретает турбулентный характер и, в зависимости от формы и выраженности деформации, в таких артериях происходят различные изменения кровотока.
При дуплексном допплеровском сканировании проводилась последовательная локация почечной артерии в области почечного синуса, на уровне междолевой, сегментарной и дуговой артерий. Обследование начиналось с переднего доступа для визуализации проксимального отдела брюшной аорты в продольном сечении и отходящих от аорты чревного ствола и верхней брыжеечной артерии, которая является хорошим ориентиром при поиске почечных артерий. После получения изображений правой и левой почечных артерий в их устьях в режиме ЦДК определяли основные характеристики сосудов, кровотока. Из заднелатерального доступа получали изображение почки в ее воротах, в режиме ЦДК исследовали ход сосудистого пучка, направление кровотока и его параметры. После получения информации о кровотоке в основном стволе почечной артерии проводили оценку кровотока по внутрипочечным артериям, используя задний и боковой доступы. В режиме ЦДК определяли расположение сегментарных (область центрального эхо-комплекса почки), междолевых (проходят в мозговом веществе вдоль пирамид) и дуговых (огибают основания пирамид на границе коркового и мозгового вещества) артерий, направление кровотока; запись проводили при задержке дыхания пациента, чтобы предотвратить возникновение шумовых сигналов, связанных с движением органа.
Количественный анализ кровотока осуществляли с помощью компьютерной программы для сосудистых исследований по следующим параметрам:
Ri и Pi позволяют косвенно судить о величине периферического сопротивления. Тестирование проводилось в режиме реального времени (real-time imaging), при этом оценивалось функциональное состояние нефрона путем искусственно созданных условий усиленной перфузии почек, а также оценки характера нарушений уродинамики верхних мочевых путей. Показатели сосудистых индексов рассчитывались автоматически по программе УЗ-аппарата при ручной обводке допплеровской кривой кровотока.
Всем детям проведена оценка функционального состояния почек по пробам Реберга с поправкой по формуле Шварца, Зимницкого, суточной экскреции с мочой титруемых кислот, аммиака. Верификация ХБП проводилась на основании критериев NKF/КDOQI (National Kidney Foundation/Kidney Disease Outcomes Quality Initiative) [1].
Статистическая обработка материала произведена путем вычисления средней арифметической (М), ошибки средней (m) с помощью биометрических методов анализа, коэффициента Стьюдента (t) с последующим нахождением уровня достоверности различий (р) по таблицам. Достоверным считали различие при р 0,001) данного показателя у пациентов с ПМР без признаков нефросклероза и пациентов в начальной стадии его формирования (РН А) (0,63 ± 0,01 и 0,63 ± 0,03 соответственно).
Данный факт расценен нами как формирование и развитие у пациентов с начальными склеротическими изменениями (РН А) артериовенозного шунтирования на юкстамедуллярном уровне для снижения периферического сосудистого сопротивления, а следовательно, внутрипочечной гипертензии при нефросклерозе, приводящих к его повышению, что согласуется с данными С. С. Пауновой [15], Е. Б. Ольховой [4]. Таким образом, артериовенозный шунт является компенсаторной мерой при повышенном периферическом сосудистом сопротивлении в почках в условиях склерозирования органа.
По мере прогрессирования ТИПП нами отмечается снижение показателя Ri у больных с РН (табл. 2). Тем не менее, нами не установлены статистически значимые различия (p > 0,001) показателей индекса резистентности (Ri) между пациентами с РН В и РН С (0,54 ± 0,04 и 0,5 ± 0,01 соответственно).
Отсутствие значимых статистических различий показателя Ri у пациентов с ПМР и РН А, РН В и РН С доказывает его низкую информативность и невозможность использования данного показателя как для ранней диагностики ТИПП у пациентов с ПМР, так и для диагностики прогрессирования ТИПП у пациентов с РН.
Нами установлены изменения (p 0,001) у пациентов на начальных стадиях прогрессирования ТИПП. Так, показатель Pi у пациентов с РН А составил 0,76 ± 0,03, а у больных с РН В 0,71 ± 0,02 (p > 0,001).
Таким образом, отсутствие статистически значимых различий (p > 0,001) Pi у пациентов на ранних стадиях формирования РН не позволяет его использовать в качестве критерия диагностики прогрессирования ТИПП. Тем не менее, учитывая существенные статистические различия (p 0,001) показателей Ri у пациентов с ПМР без признаков нефросклероза и пациентов в начальной стадии его формирования (РН А), а также между пациентами с РН В и РН С, то есть по мере прогрессирования ТИПП. Отсутствие статистических различий показателя Ri у пациентов указанных выше групп сравнения доказывает его низкую информативность как для ранней диагностики склеротических изменений у пациентов с ПМР, так и для диагностики прогрессирования нефросклероза у пациентов с РН.
Нами не установлено статистически значимых различий показателей Pi (p > 0,001) у пациентов на начальных стадиях нефросклероза у пациентов с РН А и РН В, что не позволяет использовать его в качестве критерия диагностики прогрессирования ТИПП. Тем не менее, учитывая существенные статистические различия (p
ГБОУ ВПО ОрГМУ МЗ РФ, Оренбург
Трудности и ошибки ультразвуковой и рентгеновской диагностики псевдоопухолей почек
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Опухоли почек составляют 2-3% всех злокачественных новообразований. Наиболее часто они возникают в возрасте 40-60 лет. Среди всех опухолей почек в 80-90% отмечается почечно-клеточный рак. В последние годы вероятность его обнаружения возрастает, что связано как с ростом числа всех злокачественных образований, так и с ранней доклинической диагностикой. Распознать злокачественные образования, прежде всего, позволяют постоянно совершенствующиеся и широко применяющиеся ультразвуковые исследования почек.
В литературе часто встречаются публикации, посвященные ошибкам не только ультразвуковой, но и других методов лучевой диагностики. Существует точка зрения, что до 7-9% всех объемных процессов в почках не могут быть дифференцированы до операций по поводу кист, опухолей, абсцессов и т.д. [6]. Картину опухоли почки при ультразвуковых и других лучевых методах диагностики могут симулировать многие процессы. Среди них: разнообразные аномалии почек; «сложные» или смешанные кисты; острые и хронические неспецифические воспалительные процессы (карбункул, абсцесс, хронический, в том числе ксантогранулематозный пиелонефрит); специфические воспалительные процессы (туберкулез, сифилис, грибковые поражения почек); изменения в почках при лейкозах и лимфомах, в том числе и при ВИЧ-инфекции; инфаркты почки; организовавшиеся гематомы и другие причины.
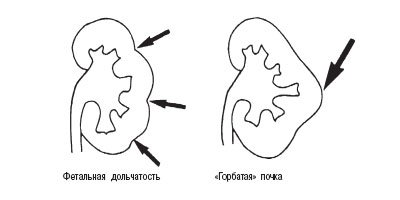
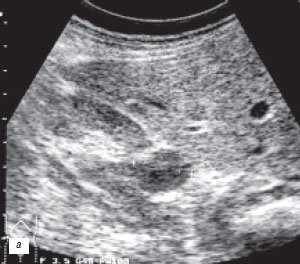
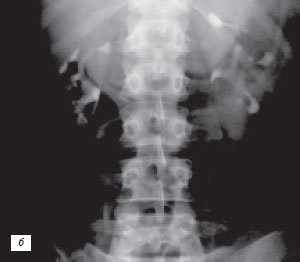
В данном сообщении речь пойдет только об аномалиях почек, которые в литературе определяются термином псевдоопухоли [7]. При них клинические проявления почти всегда отсутствуют или определяются сопутствующими заболеваниями, а установление правильного диагноза возможно только методами лучевой диагностики (рис. 1).
а) Фетальная долчатость, «горбатая» почка.
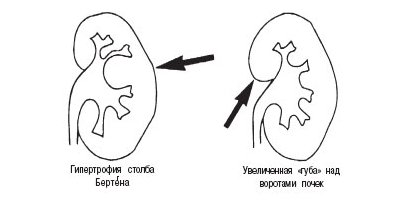
б) Гипертрофия столба Бертена, увеличенная «губа» над воротами почек.
Материалы и методы
Результаты исследований
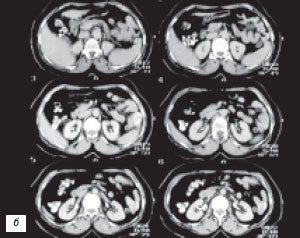
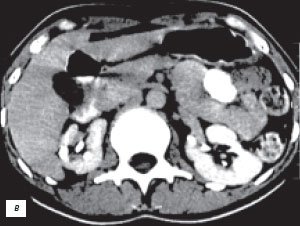
б) Серия компьютерных томограмм.
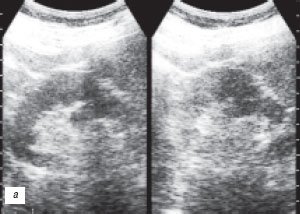
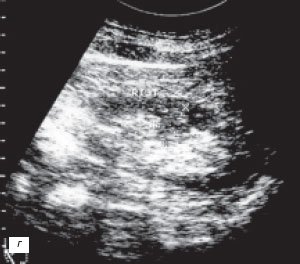
У 2 (1,2%) больных отмечена увеличенная «губа» над воротами почки (рис. 3а-в).
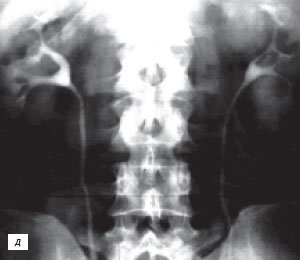
б) Экскреторная урограмма.
в) КТ с контрастным усилением.
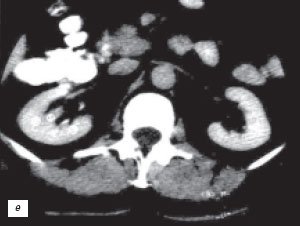
д) Экскреторная урограмма.
е) КТ с контрастным усилением.
В проведении дифференциальной диагностики псевдоопухолей и опухолей почек нуждалось 37 (21%) пациентов. С этой целью проводились, прежде всего, повторные «нацеленные» УЗ-сканирования с использованием различных дополнительных ультразвуковых методик в условиях урологической клиники, а также других методов лучевой диагностики, указанных выше. Только у одного пациента с псевдоопухолью почки для исключения диагноза опухоли произведена эксплоративная люмботомия с интраоперационной биопсией под ультразвуковым контролем. У остальных 36 больных диагноз псевдоопухолей почек был подтвержден с помощью лучевых исследований и ультразвукового мониторинга.
Трудности и ошибки лучевой диагностики при псевдоопухолях почек обычно возникали на первых догоспитальных этапах диагностики. У 34 ( 92%) пациентов они были связаны как с объективными трудностями трактовки необычных эхографических данных, так и их неправильной трактовкой из-за недостаточной квалификации специалистов и сравнительно низкого уровня диагностической аппаратуры. У 3(8%) пациентов отмечены ошибочная трактовка данных рентгеновской компьютерной томографии, когда было отмечено расхождение их с данными повторных УЗ-сканирований и рентгеновской компьютерной томографии в урологической клинике.
Обсуждение
Одна из самых частых причин, симулирующих опухоль почки при ультразвуковом исследовании, так называемая псевдоопухоль, в литературе наиболее часто определяется термином гипертрофия столба Бертена.
Все элементы «перемычки» являются нормальной тканью паренхимы без признаков гипертрофии или дисплазии. Они представляют собой удвоение нормального коркового вещества почки или добавочный слой его, расположенный латеральнее чашечек [7]. Последний является вариантом анатомического строения паренхимы, в частности, кортикомедуллярных взаимоотношений паренхимы и синуса почки [12]. Наиболее четко они могут прослеживаться на ультразвуковых и на компьютерно-томографических срезах почки [9, 11-15].
Отсутствие гипертрофии или дисплазии паренхимы при так называемой гипертрофии столбов Бертена или «перемычках» паренхимы подтвердили и проведенные гистологические исследования биопсийного материала у одного больного с «перемычками» паренхимы, принимавшимися до эксплоративной люмботомии за опухоль почки, а также у двух пациентов при морфологическом исследовании почек, удаленных по поводу сочетания в одной почке опухоли и псевдоопухоли («перемычки» паренхимы).
В связи с этим, на наш взгляд, наиболее часто встречающийся в литературе, термин гипертрофия столбов Бертена не отражает морфологической сути субстрата. Поэтому мы так же, как и ряд авторов [9, 11, 12] считаем, что более правильным является термин «перемычка» паренхимы. Впервые в отечественной литературе по ультразвуковой диагностике он применен нами в 1991 г. [16]. Необходимо отметить, что термин «перемычка» паренхимы имел в литературе и другие названия (таблица ) [11].
| Происхождение или природа ткани | Термины | Авторы |
|---|---|---|
| Гипертрофированная или необычно широкая ткань | Гипертрофированный столб Бертена | Lafortune M et al., 1986 Wolfman NT et al., 1991 Leekman RN et al., 1983 |
| Фокальная кортикальная гиперплазия | Popky GL et al., 1969 | |
| Широкая аркада | Hodson CJ et al., 1982 | |
| Неправильно расположенная или перемещенная ткань | Лобарный дисморфизм | Carghi A et al., 1971 Dacie JE, 1976 |
| Неправильное положение почечной доли | Carghi A et al., 1971 | |
| Складки кортикальной массы | King MC et al., 1968 | |
| «Почка» в пределах почки | Hodson CJ et al., 1982 | |
| Кортикальная инвагинация и пролабирование столбов Бертена | Lopez FA, 1972 | |
| Масса или псевдомасса | Почечный псевдотумор | Felson B et al., 1969 Lopez FA, 1972 |
| Гломерулярная зона псевдотумора | Hartman GW et al., 1969 | |
| Почечно-кортикальный узелок | Wolfman NT et al., 1991 | |
| Первичный кортикальный узелок | Thornbury JR et al., 1980 | |
| Интермедиальная кортикальная масса | Netter F et al., 1979 | |
| Эмбриональная аномалия | Аберрантная долька почечной ткани | Meaney TF, 1969 |
| Доброкачественная кортикальная «цезура» | Flynn VJ et al., 1972 | |
| Кортикальный островок почки | Flynn VJ et al., 1972 | |
| Развившаяся (совершенная) аномалия | Несвершившаяся попытка дупликации почечной паренхимы | Dacie JE, 1976 |
| Сверхкомплектная доля | Добавочная почечная доля | Palma LD et al., 1990 |
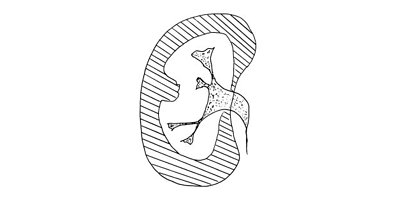
Многолетний опыт экскреторной урографии показал, что чашечно-лоханочные системы имеют крайне большое количество вариантов строения. Они практически индивидуальны не только для каждого человека, но и для левой и правой почек у одного субъекта. С развитием и все более широким использованием УЗИ и РКТ, позволяющим прослеживать как внутренние, так и наружные контуры паренхимы почек, на наш взгляд, аналогичное положение складывается и в отношении вариантов анатомического строения паренхимы почек. Сопоставление эхо- и компьютерно-томографических данных с урографическими при различных вариантах псевдоопухолей почек показало, что между анатомическим строением паренхимы и чашечно-лоханочных систем почек имеется взаимосвязь. Она выражается в конгруэнтности медиального контура паренхимы в эхо- или компьютерно-томографическом изображении с латеральным контуром чашечно-лоханочных систем, условно проведенным на экскреторных урограммах или на компьютерных томограммах с контрастным усилением [4, 17, 18]. Этот симптом прослеживается при обычном строении паренхимы и чашечно-лоханочных систем, а также при «перемычке» паренхимы почки, предсталяющей собой вариант анатомического строения. При опухоли почки, являющейся приобретенным патологическим процессом, конгруэнтность контуров паренхимы и чашечно-лоханочных систем почек нарушается (рис. 4).
Рис. 4. Симптом конгруэнтности контуров паренхимы и чашечно-лоханочной системы почки при неполной «перемычке» паренхимы (объяснение в тексте).
Выводы
Таким образом, впервые выявленные при УЗИ типичные эхографические картины «перемычки» паренхимы почки, «горбатой» почки и увеличенной «губы» над воротами почки без признаков расширения чашечно-лоханочных систем не требуют дальнейшего обследования.
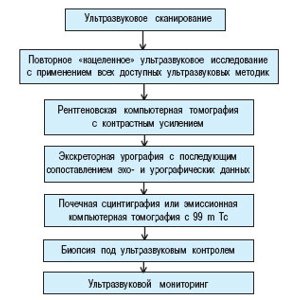
При необходимости дифференциальной диагностики псевдоопухолей и опухолей почек, которая потребовалась у 37(21%) пациентов, мы предлагаем следующий алгоритм их диагностики (рис. 5).
Рис. 5. Алгоритм лучевой диагностики при псевдоопухоли почки.
Литература
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.



.gif)