Вакцинация
Актуальные материалы
Общая информация
Над поиском вакцины против COVID-19 работает группа экспертов под руководством ВОЗ (Всемирной организации здравоохранения), а также около 80 исследовательских компаний и групп. Ученые также трудятся над созданием временного средства, которое позволило бы защитить людей на 1−2 месяца, пока разрабатываются более долгосрочные, серьезные методы.
Согласно данным исследователей из Университета Питтсбурга, на разработку вакцины и прохождение испытательного периода может потребоваться от 12 до 18 месяцев, ведь внедрение вакцины, как правило, подразумевает длительный процесс утверждения. Кроме того, вакцина должна пройти клинические испытания как на животных, так и на людях. Тестирование на людях обычно состоит из трех этапов.
Первая фаза – небольшие испытания, обычно с участием около 100 человек, чтобы оценить, безопасна ли вакцина для людей. Во второй фазе испытаний часто участвуют несколько сотен субъектов для оценки эффективности вакцины против этой болезни. Эта фаза может длиться от нескольких месяцев до нескольких лет. На последнем этапе проводится дальнейшая оценка эффективности вакцины в течение определенного периода времени в еще большем масштабе – участвуют уже тысячи людей, часто в нескольких медицинских учреждениях. Эта фаза может длиться несколько лет.
Кроме того, вакцины могут непреднамеренно вызвать усиление заболевания, при котором у вакцинированных людей развивается более тяжелая форма заболевания, чем у тех, кто никогда не был вакцинирован. Даже при ускоренных испытаниях и быстрой разработке процесс одобрения вакцины COVID-19 все равно займет время. Еще одна потенциальная проблема – как только вакцина будет одобрена, она будет нужна разным странам в огромном количестве. При этом многие производители вакцин просто не имеют таких производственных мощностей.
Тем не менее, есть уже первые успехи. Ученые из Австралии объявили о начале тестов потенциальной вакцины против COVID-19 на хорьках, а команда из Оксфордского университета должна в недалеком будущем испытать тот же препарат уже на людях. Вакцины, изготовленные Оксфордским университетом и американской компанией Inovio Pharmaceutical, были одобрены ВОЗ для тестирования на животных.
Пять компаний уже начали испытание вакцин на людях – первой стала бостонская биотехнологическая компания Moderna. Такая быстрота обусловлена двумя другими прошедшими эпидемиями – тяжелым острым респираторным синдромом (SARS) в Китае в 2002−2004 годах и ближневосточным респираторным синдромом (MERS), который начался в Саудовской Аравии в 2012 году. В обоих случаях была начата работа над вакцинами, но исследования забросили, так как вспышки были локализованы.
Однако компания, базирующаяся в Мэриленде, пришла к выводу, что две имеющиеся у них вакцины могут быть переадресованы для SARS-CoV-2. Между тем, Moderna, построенная на более ранних работах по борьбе с вирусом MERS, проведенных в Национальном институте аллергии и инфекционных заболеваний США, с 15 марта уже проходит клинические испытания.
SARS-CoV-2 разделяет от 80 до 90 % своего генетического материала с вирусом, вызвавшим в 2002−2004 годах в Китае SARS − отсюда и его название. Оба состоят из полоски РНК, заключенной в жировую оболочку, через которую проступает множество белковых шипов. Шипы фиксируются на рецепторах на поверхности клеток, выстилающих легкое человека, − рецепторы одного типа в обоих случаях, − позволяя вирусу проникать в клетку. Оказавшись внутри, он захватывает репродуктивный механизм клетки, чтобы произвести больше копий себя, прежде чем снова вырваться из клетки, убив ее.
Основываясь на этих данных, ученые Питтсбургского университета разработали вакцину под названием «PittCoVacc» − сокращение от Питтсбургской коронавирусной вакцины. Она будет доставляться через «набор микроигл» в небольшом патче – 400 крошечных игл передадут кусочки остроконечного белка в кожу, где иммунная реакция наиболее сильна. Пластырь будет прилипать к коже − точно так же, как лейкопластырь, а микроиглы, полностью состоящие из кусочков сахара и белка, будут растворяться и поглощаться кожей1. При тестировании на мышах вакцина, доставляемая через пластырь размером с кончик пальца, продуцирует антитела, устойчивые к SARS-CoV-2, в количествах, которые считаются достаточными для нейтрализации вируса.
По факту, все создаваемые вакцины работают по одному и тому же основному принципу. Они представляют часть или весь патоген, обычно в форме инъекций и в низких дозах, чтобы побудить иммунную систему вырабатывать антитела к патогену.Антитела представляют собой разновидность иммунной памяти, которая, будучи однажды выявленной, может быть быстро мобилизована снова, если человек подвергается воздействию вируса в его естественной форме.
Ученые из Великобритании заявили о том, что разработка вакцины в одной из самых продвинутых британских команд будет завершена к сентябрю, причем исследователи уверены «на 80 %», что она сработает, – так говорит профессор вакцинологии в Оксфордском университете Сара Гилберт. Она также уточнила, что испытания на людях должны начаться в ближайшее время. Гилберт сказала, что она ведет переговоры с британским правительством о финансировании и начале производства до того, как будут получены окончательные результаты, что позволит общественности немедленно получить доступ к вакцине, если она окажется эффективной.
Еще одна вакцина, разработанная Inovio Pharmaceuticals, была введена первым взрослым добровольцам 6 апреля. Ожидается, что медицинский гигант Johnson & Johnson начнет клинические испытания в сентябре и получит партнерство на сумму около 500 млн долларов США через подразделение Министерства здравоохранения и социальных служб США.
Другая идея быстрого выращивания вакцин − использование растений. В апреле табачный гигант British American Tobacco (BAT) заявил, что он планирует культивировать вакцины (разрабатываемые его дочерней компанией Kentucky BioProcessing) в быстрорастущих растениях табака. Однако такие растительные вакцинные продукты имеют дополнительные нормативные препятствия, включая соблюдение правил для генетически модифицированных организмов, что может замедлить процесс.
Всего в настоящее время в мире насчитывается 83 кандидатных вакцины, из которых 77 находятся на стадии доклинических исследований и 6 проходят клинические исследования на людях.
Ближе к концу марта российские ученые начали тестирование прототипов потенциальных вакцин против нового коронавируса на животных в лаборатории в Сибири, сообщил Роспотребнадзор.
В начале апреля глава Государственного вирусологического и биотехнологического центра «Вектор» заявил, что его учреждение готово провести первую фазу клинических испытаний трех вакцин с 29 июня на 180 добровольцах – группы добровольцев уже сформированы.
Таким образом, девять российских разработок вакцин против COVID-19 включены ВОЗ в перечень перспективных.
В их числе шесть препаратов, созданных в Государственном научном центре вирусологии и биотехнологии «Вектор»:
Две вакцины, разработанные компанией «Биокад»:
Вакцина, разработанная Санкт-Петербургским НИИ вакцин и сывороток:
Источник: Экспертный доклад «Средства диагностики и лечения новой коронавирусной инфекции COVID-19» (НИИОЗММ ДЗМ)
Скорая помощь, вызов врача
(в т. ч. для забора анализа)
Информационная линия по вопросам
диагностики и профилактики коронавируса (круглосуточно)
Заказать больничный лист, задать вопросы,
сообщить о возвращении из-за границы
(ежедневно, с 08:00 до 21:00)
Как разрабатывают вакцины?
Данная статья входит в серию публикаций, посвященных разработке и распределению вакцин. Узнайте больше о вакцинах, о принципах их действия и о том, как обеспечивается их безопасность и справедливое распределение, в серии публикаций ВОЗ «Все о вакцинах».
Какие ингредиенты входят в состав вакцины?
Вакцины содержат крошечные фрагменты болезнетворного микроорганизма или программы для создания этих крошечных фрагментов. Они также содержат другие ингредиенты, необходимые для обеспечения безопасности и эффективности вакцины. Эти последние ингредиенты включены в большинство вакцин и использовались на протяжении десятилетий в миллиардах доз вакцин.
Каждый компонент вакцины служит конкретной цели, и каждый ингредиент тестируется в процессе производства. Все ингредиенты тестируются на безопасность.
Антиген
Все вакцины содержат активный компонент (антиген), который генерирует иммунный ответ, или программу для создания активного компонента. Антиген может быть небольшой частью болезнетворного микроорганизма, такой как белок или сахар, или же это может быть весь микроорганизм в ослабленной или инактивированной форме.
Консерванты
Консерванты предотвращают контаминацию вакцины после открытия флакона, если она используется более чем для одного человека. Некоторые вакцины не имеют консервантов, поскольку они хранятся в однодозовых флаконах, которые выкидываются после введения одной дозы. Наиболее широко используемым консервантом является 2-феноксиэтанол, который используется в течение многих лет в ряде вакцин и ряде продуктов по уходу за младенцами. Этот консервант безопасен для использования в вакцинах, поскольку он мало токсичен для людей.
Стабилизаторы
Стабилизаторы предотвращают химические реакции внутри вакцины и удерживают компоненты вакцины от прилипания к флакону.
Стабилизаторы могут быть сахарами (лактозой, сахарозой), аминокислотами (глицином), желатином и белками (рекомбинантным человеческим альбумином, полученным из дрожжей).
Поверхностно-активные вещества
Поверхностно-активные вещества сохраняют все ингредиенты вакцины в смешанном состоянии. Они предотвращают образование осадка и склеивание элементов, находящихся в жидкой форме вакцины. Они также часто используются в пищевых продуктах, таких как мороженое.
Примеси
Примеси представляют собой крошечные количества различных веществ, используемых во время изготовления или производства вакцин, которые не являются активными ингредиентами готовой вакцины. Вещества варьируются в зависимости от используемого производственного процесса и могут включать яичные белки, дрожжи или антибиотики. Остаточные следы этих веществ, которые могут присутствовать в вакцине, находятся в столь малых количествах, что их необходимо измерять в частях на миллион или в частях на миллиард.
Разбавители
Разбавитель – это жидкость, используемая для разбавления вакцины до правильной концентрации непосредственно перед ее использованием. Чаще всего в качестве разбавителя используется стерильная вода.
Адъюванты
Некоторые вакцины содержат также адъюванты. Адъювант улучшает иммунную реакцию на вакцину иногда путем более длительного удержания вакцины в месте инъекции или стимулирования местных иммунных клеток.
Адъювантом может быть незначительное количество алюминиевых солей (например, фосфат алюминия, гидроксид алюминия или сульфат калия-алюминия). Было продемонстрировано, что алюминий не вызывает каких-либо долговременных проблем со здоровьем, и люди регулярно потребляют алюминий во время еды и питья.
Как разрабатывают вакцины?
Наиболее часто используемые вакцины применяются уже на протяжении десятилетий, и каждый год миллионы людей получают их, не подвергаясь при этом опасности. Как и все лекарственные средства, каждая вакцина должна пройти широкомасштабное тщательное тестирование для оценки ее безопасности, прежде чем она может быть включена в программу вакцинации в странах.
Каждая разрабатываемая вакцина должна сначала пройти проверки и оценки, помогающие определить, какой антиген следует использовать, чтобы вызвать иммунную реакцию. Эта доклиническая фаза испытаний проводится без участия людей. Экспериментальные вакцины сначала тестируются на животных для оценки их безопасности и способности предотвращать болезнь.
Если вакцина вызывает иммунную реакцию, она затем тестируется в рамках клинических испытаний с участием людей, которые состоят из трех фаз.
Фаза 1
Вакцина вводится небольшому числу добровольцев, чтобы оценить ее безопасность, убедиться, что она генерирует иммунную реакцию, и определить правильную дозу. Как правило, во время этой фазы испытаний вакцины тестируются на молодых взрослых добровольцах.
Фаза 2
Затем вакцина вводится сотням добровольцев для дальнейшей оценки ее безопасности и способности генерировать иммунную реакцию. Участники этой фазы испытаний обладают теми же характеристиками (такими как возраст и пол), что и люди, для которых предназначается вакцина. Обычно на этом этапе проводится несколько испытаний для оценки разных возрастных групп и разных составов вакцины. На этом этапе в испытания обычно включается группа, не получавшая вакцину, в качестве группы сравнения для определения того, относятся ли изменения, произошедшие в вакцинированной группе участников, к вакцине или же они произошли случайно.
Фаза 3
Затем вакцина вводится тысячам добровольцев, и проводится сравнение с аналогичной группой людей, которые не получали вакцину, но получали продукт сравнения, с целью определить, эффективна ли вакцина против болезни, для защиты от которой она предназначается, и изучить ее безопасность среди гораздо большего числа людей. Большую часть времени испытания на этом этапе проводятся в разных странах и в разных местах внутри стран, с тем чтобы удостовериться в том, что полученные результаты в отношении эффективности вакцины применимы к разным группам населения.
Во время испытаний второй и третьей фазы добровольцы и ученые, проводящие исследование, не знают, какие добровольцы получили испытываемую вакцину, а какие – продукт сравнения. Этот метод, называемый «ослеплением», необходим для обеспечения того, чтобы ни добровольцы, ни ученые не подвергались влиянию в своей оценке безопасности или эффективности в связи с тем, что знали, кто какой продукт получил. После завершения испытаний и получения всех результатов добровольцы и ученые-испытатели информируются о том, кто получил вакцину, а кто – продукт сравнения.
После получения результатов всех этих клинических испытаний необходимо предпринять ряд шагов, включая проведение обзоров эффективности и безопасности для утверждения нормативных актов и политики в области общественного здравоохранения. Должностные лица в каждой стране внимательно изучают данные исследования и принимают решение о том, следует ли санкционировать использование вакцины. Вакцина должна быть признана безопасной и эффективной для широких слоев населения, прежде чем она будет утверждена и включена в национальную программу иммунизации. Уровень безопасности и эффективности вакцин чрезвычайно высок при том понимании, что они вводятся людям, которые здоровы и, в частности, не имеют той болезни, для защиты от которой они предназначаются.
После внедрения вакцины проводится постоянный мониторинг. Существуют системы для мониторинга безопасности и эффективности всех вакцин. Это позволяет ученым отслеживать воздействие вакцин и их безопасность, даже если они используются среди большого числа людей в течение длительного времени. Эти данные используются для корректировки политики в отношении использования вакцин в целях оптимизации их воздействия и для безопасного отслеживания воздействия вакцины во время ее использования.
Как только вакцина начинает применяться, необходимо проводить постоянный мониторинг для удостоверения в том, что она остается безопасной.
Российские вакцины не прошли все фазы клинического исследования?
Клинические исследования во всем мире являются неотъемлемым этапом разработки препаратов, который предшествует его регистрации и широкому медицинскому применению. В ходе клинических исследований новый препарат изучается для получения данных о его эффективности и безопасности. На основании этих данных уполномоченный орган здравоохранения принимает решение о регистрации препарата или отказе в регистрации.
Проведение клинических исследований в РФ регламентируют: Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» (Статья 40. Проведение клинического исследования лекарственного препарата для медицинского применения), ГОСТ Р 56701-2015 от 2016-07-01 ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ (УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2015 г. N 1762-ст.), ГОСТ Р 52379-2005 от 2006-04-01 НАДЛЕЖАЩАЯ КЛИНИЧЕСКАЯ ПРАКТИКА (УТВЕРЖДЕН Приказом Федерального агентства по техническому регулированию и метрологии от 27 сентября 2005 года N 232-ст), Правила надлежащей клинической практики ОСТ 42-511-99 (согласно международного стандарта этических норм и качества научных исследований Good Clinical Practice; GCP), Приказ Минздрава России от 01.04.2016 N 200н «Об утверждении правил надлежащей клинической практики» (Зарегистрировано в Минюсте России 23.08.2016 N 43357), приказ Минздрава России от 09.01.2014 № 2н «Об утверждении порядка проведения оценки соответствия медицинских изделий в форме технических испытаний, токсикологических исследований, клинических испытаний в целях государственной регистрации медицинских изделий».
Обычно выделяют четыре фазы клинических испытаний. Фаза I. Цель этапа — убедиться, что препарат можно применять у людей. Фаза II. Цель этапа — дополнительно оценить безопасность лекарства и выяснить, работает ли препарат. Фаза III. Цель этапа — сравнить новый препарат со стандартным лечением. Фаза IV называется постмаркетинговой — этот этап клинического испытания начинается, когда готовое лекарство уже поступает в продажу.
Существует государственный реестр лекарственных средств, который содержит перечень лекарственных препаратов, прошедших государственную регистрацию (Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» Статья 33), другими словами реестр разрешений на проведение клинических исследований (РКИ).
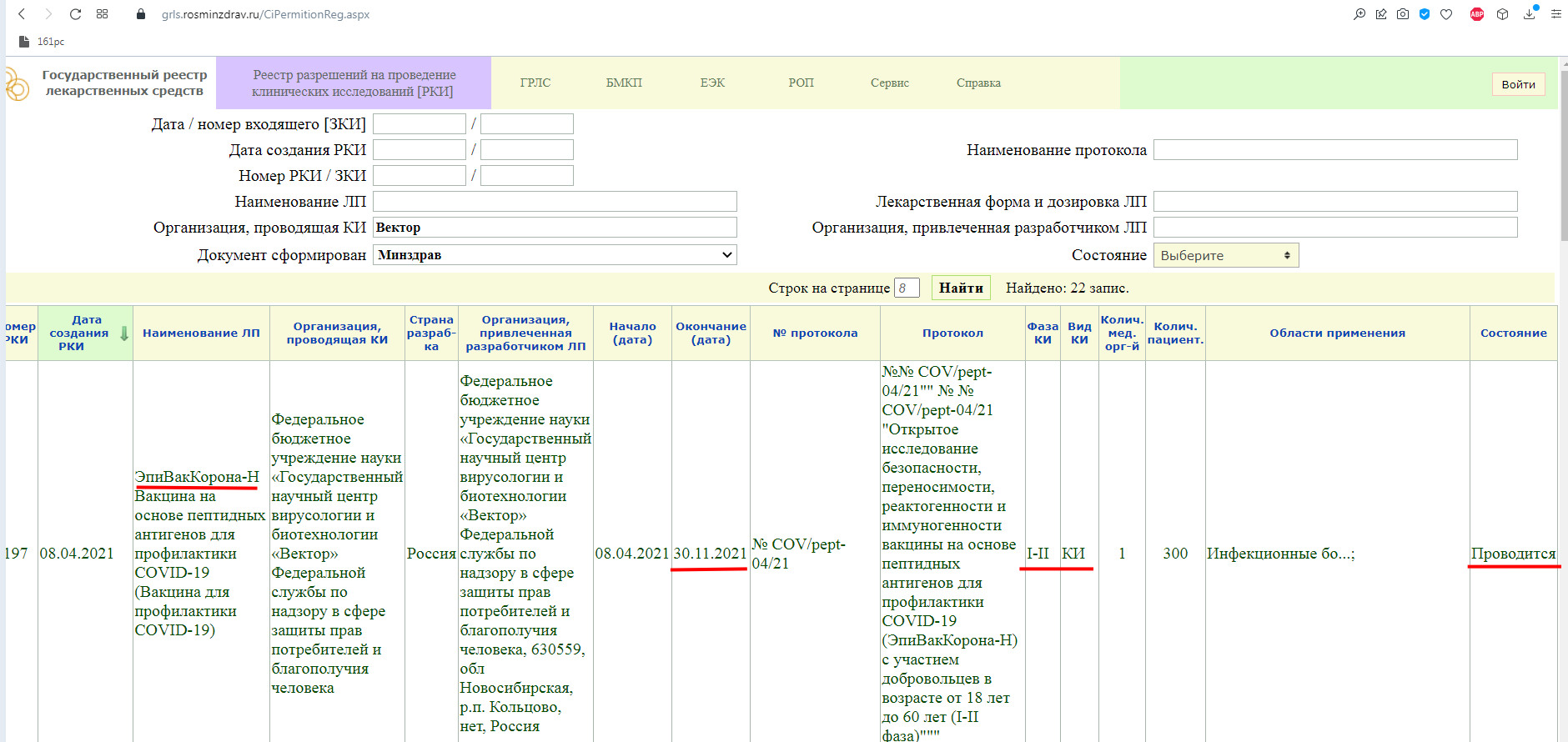
В настоящий момент, у Российской Федерации известно существование нескольких вакцин от коронавируса: «Спутник V» и «Спутник Лайт» («Гам-КОВИД-Вак», Национального исследовательского центра эпидемиологии и микробиологии имени Н. Ф. Гамалеи), «ЭпиВакКорона» (Федерального бюджетного учреждения науки «Государственный научный центр вирусологии и биотехнологии Вектор» Роспотребнадзора), «КовиВак» (Федерального научного центра исследований и разработки иммунобиологических препаратов имени М.П. Чумакова Российской академии наук).
Как мы видим, в настоящий момент, проводится фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, и завершится она 30 ноября 2021 года.
Так же, проводится фаза клинического исследования 3-4 с участием добровольцев от 18 лет, и завершится она 31 августа 2021 года.
Завершенная фаза 3 клинического исследования, с участием добровольцев от 60 лет, и завершилась она 15 мая 2021 года.
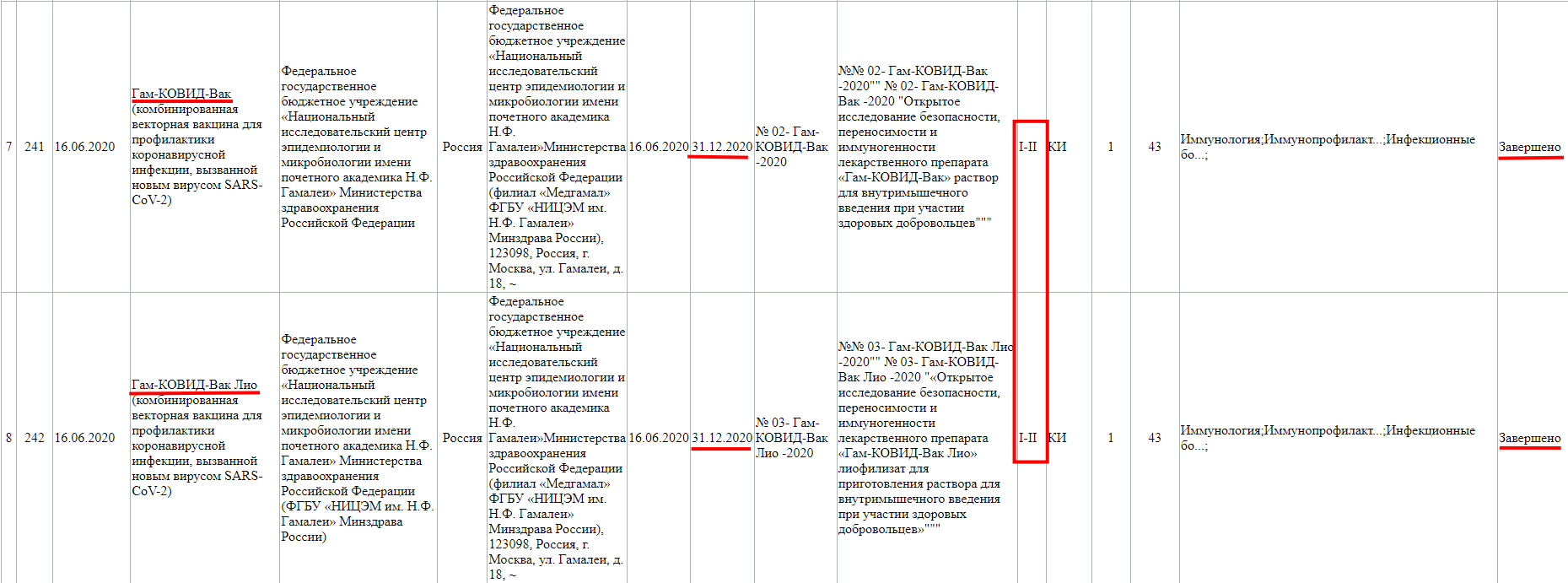
Фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, проводится до 30 декабря 2021 года.
Тут так же видно, что проводится фаза клинического исследования 3 с участием добровольцев от 18 до 60 лет, и завершится она 30 декабря 2022 года.
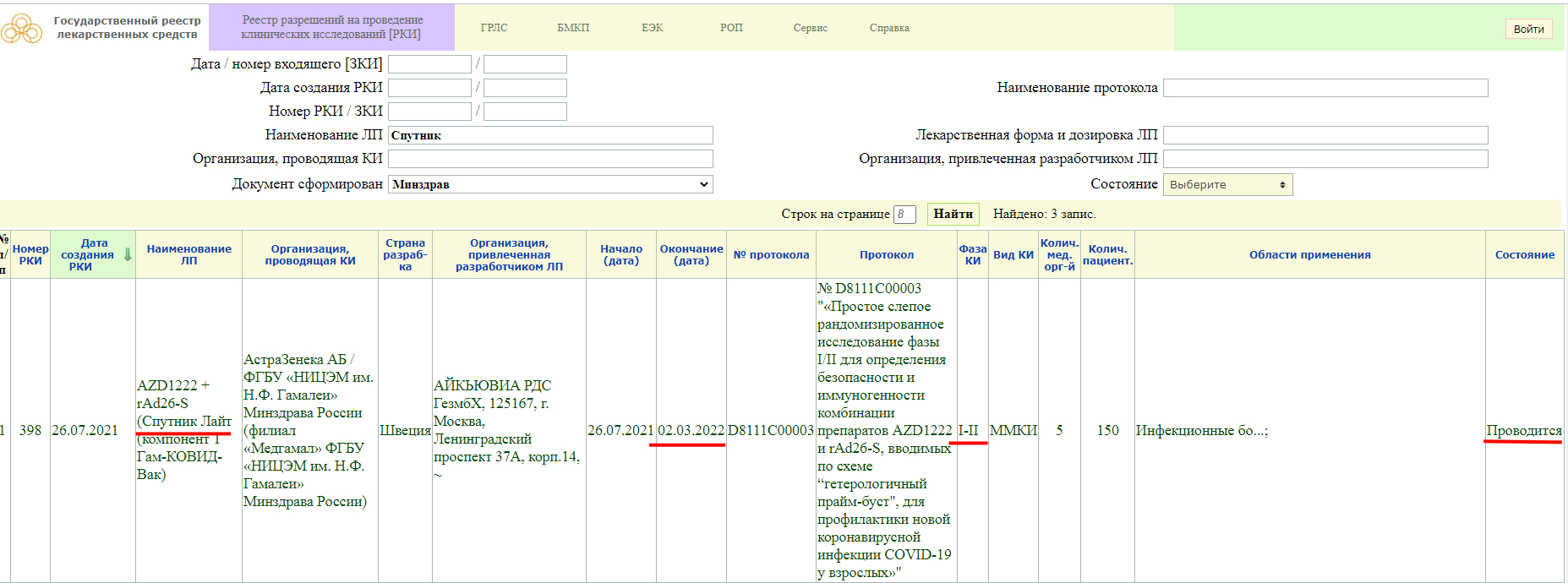
Как мы видим, в настоящий момент, у «Спутника Лайт» проводится фаза клинического исследования 1-2, и завершится она 2 марта 2022 года. Кстати обратите внимание, страна разработки Швеция.
Так же, проводится фаза клинического исследования 3, и завершится она 28 января 2022 года.
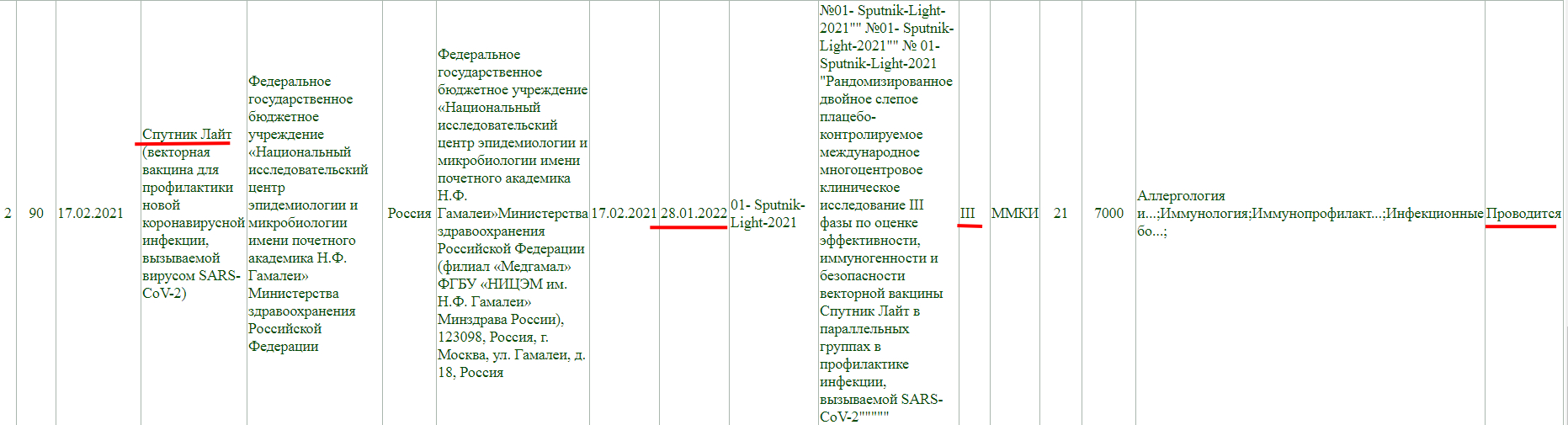
Фаза клинического исследования 1-2, проводится до 31 декабря 2021 года.
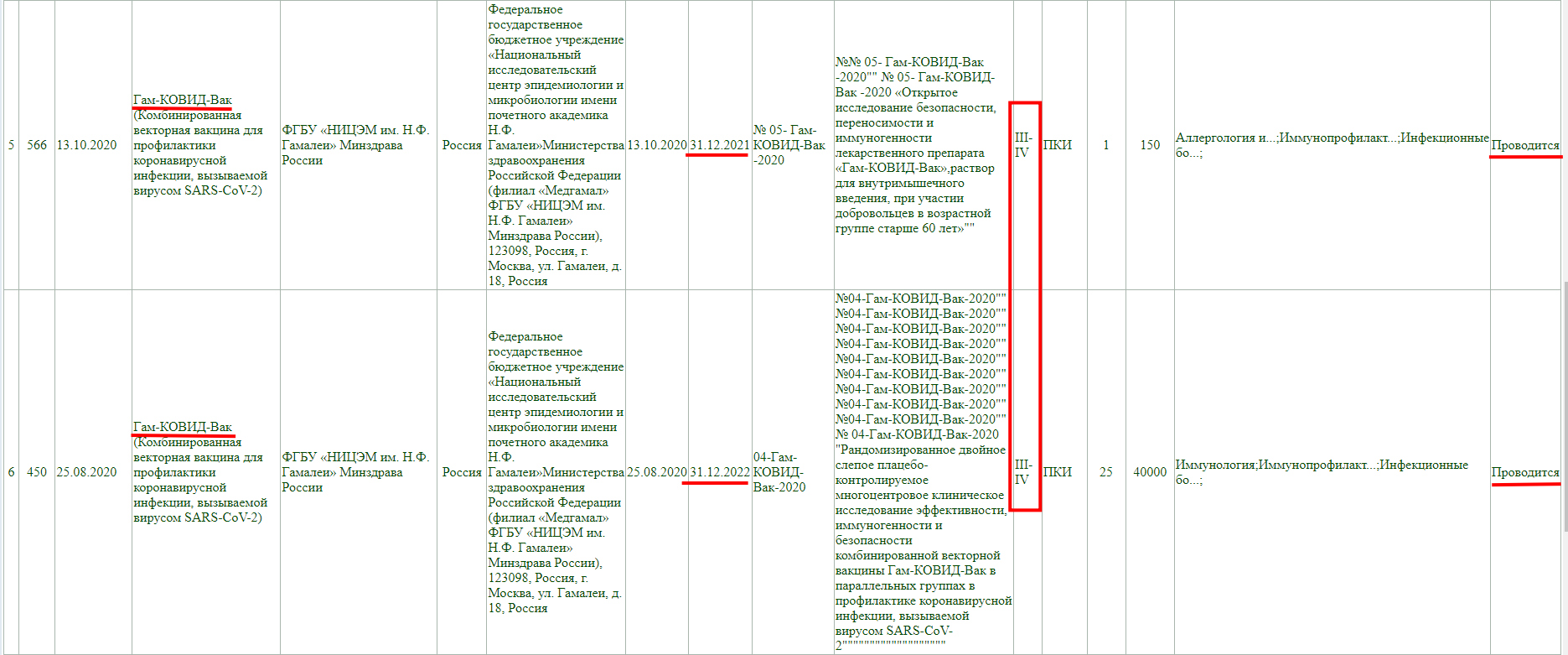
Как и у остальных, клинические исследования не завершены, и в настоящий момент проводится фаза 3 с участием добровольцев от 18 до 60 лет, а завершится она 30 декабря 2022 года.
Тут аналогично, клинические исследования не завершены, проводится фаза 3-4, и завершится она 30 декабря 2022 года.
А тут клиническое исследование завершено, но только фазы 1-2.
Кроме того, отсутствие данных о клинических испытаниях вакцины «Спутник V» необходимых для ее регистрации в Европе, 15 мая 2021 года, уже сообщало одно из крупнейших в мире международных агентств новостей и финансовой информации, Reuters.
И в завершение, по данным ВОЗ на 14 марта 2021 г., российские вакцины против COVID-19, в перечне безопасных и эффективных, отсутствуют.
Станьте членом КЛАНА и каждый вторник вы будете получать свежий номер «Аргументы Недели», со скидкой более чем 70%, вместе с эксклюзивными материалами, не вошедшими в полосы газеты. Получите премиум доступ к библиотеке интереснейших и популярных книг, а также архиву более чем 700 вышедших номеров БЕСПЛАТНО. В дополнение у вас появится возможность целый год пользоваться бесплатными юридическими консультациями наших экспертов.
Как тестируют вакцины и лекарства?
Врач-терапевт, медицинский редактор
Читайте дальше
Как выбрать идеальный контрацептив?
Чуть позже стало понятно, что ставить вопрос: будем лечить или пусть живёт, — не гуманно. Постепенно появилась сложная, долгая и дорогостоящая процедура испытания медицинских препаратов.
Сейчас от появления прототипа нового лекарства или вакцины до их регистрации в качестве медицинских препаратов проходит около 10-12 лет испытаний. Но и после обретения торгового названия и своего места на аптечной полке препарат многократно проверяют, корректируют показания, противопоказания и перечень побочных действий.
Вакцины от коронавируса не пустили по этому длинному пути. В связи с пандемией, их регистрируют по ускоренной процедуре и выпускают в гражданский оборот. Из всех этапов испытаний эти препараты проходят только первые два, где задействованы животные и совсем небольшая группа добровольцев из числа людей.
Давайте разбираться, что и как проверяют!
Опыты на животных — проверка на вредность
Доклинические испытания — это масштабный этап исследования кандидатов в лекарства и вакцины. Он может длиться до 10 лет и проводится преимущественно на животных.
Некоторые тесты традиционно выполняют на культурах клеток, бактериях, мухах дрозофилах или аквариумных рыбках. В продвинутых лабораториях отдельные эксперименты научились моделировать в виртуальной реальности. Однако основные испытуемые — это грызуны: мыши, крысы, хомяки, морские свинки и кролики. Ряд тестов требует участия более крупных млекопитающих: собак, обезьян, реже — мини-пиги, кошек, хорьков и др.
Цель доклинических исследований:
Важнейший аспект доклинических испытаний — проверка вещества на вредность. Определяют, какие органы и ткани животных оказываются более подвержены действию препарата? Какие побочные эффекты вызывает вещество?
Сначала препарат вводят с короткими 3-6-часовыми промежутками в течение суток и отслеживают результаты острой токсичности. Затем приступают к тестированию хронической токсичности. Эта часть исследования зависит от предполагаемой продолжительности лечебного курса у человека и может длиться от нескольких недель до года и более. У вакцин длительность зависит от схемы введения первых доз и последующей ревакцинации.
Далее испытывают влияние препарата на фертильность у самцов и самок животных. Определяют эмбриотоксичность и фетотоксичность — отрицательное влияние вещества на эмбрион, плод, а также отслеживают рост и развитие детёнышей после рождения.
Отдельно изучают мутагенность — способность вызывать мутации у взрослого животного и канцерогенность — вероятность злокачественных опухолей.
Сведения о канцерогенности вещества обязательно необходимы для получения разрешения на клинические исследования в нашей стране. Лекарства, которые будут продаваться без рецепта или предназначенные для длительного использования тестируются с особой тщательностью. Например, гормональные препараты проходят тестирование на канцерогенность около 7-10 лет, и подопытными, помимо крыс и мышей, должны быть собаки или обезьяны.
Данные проверки на вредность являются опорными для последующих экспериментов. Существуют коэффициенты пересчёта доз исходя из массы тела. Ориентируясь на эти цифры, можно проецировать влияние препарата на человека.
Второй аспект доклинических исследований — фармакокинетика — путь, который проделывает вещество в организме: как всасывается, как распределяется, вступает ли в химические превращения, какими органами и с какой скоростью выводится. Знание фармакокинетики позволяет точнее подобрать эффективную дозу для человека, выбрать оптимальную форму введения препарата в организм: через рот или с помощью инъекций.
Третий вопрос, на который отвечают лабораторные изыскания — предположительная эффективность кандидата в лекарства. Методология этой части исследования значительно отличается в зависимости от целевой сферы применения вещества. Например, при тестировании нейролептиков у животных исследуют их поведенческие реакции и двигательную активность. Для тестирования сердечных лекарств проводят испытания на собаках, кошках или обезьянах, у которых искусственно нарушают кровообращение сердца, имитируя стенокардию.
На территории России принят единый стандарт проведения доклинических исследований — ГОСТ 33044-2014, который соответствует международному стандарту GLP (Good Laboratory Practice — «Надлежащая лабораторная практика»). Только успешно прошедшие все фазы доклинических исследований кандидаты допускаются к изучению на людях, в среднем это 2 вещества из 100, остальные отбраковываются как слишком вредные или неэффективные. С учетом этих цифр трудно переоценить значение лабораторных животных в медицинской науке.
Ковидные вакцины прошли этот этап исследований, но продолжительность его была значительно короче положенного.
Испытания на добровольцах: 1 фаза
«По-взрослому» будущие лекарства испытывают на здоровых и больных людях, которые должны добровольно выразить своё согласие на участие в эксперименте после того, как ознакомятся со всеми «за» и «против». Для здоровых людей аргументом «за» чаще является финансовая заинтересованность — за участие в клинических исследованиях можно заработать в среднем 15-20 тысяч рублей.
Здоровых добровольцев привлекают на клинические исследования 1 фазы. Группа подопытных здесь не более 100 человек. Людям дают различные дозы препарата и динамически определяют его концентрацию в крови, отслеживают побочные действия и их связь с дозой.
В 1 фазе клинических исследований уточняют максимальную безопасную дозировку у человека. На этом этапе отсеиваются около 30% веществ.
Быстрым и дешёвым видом клинического испытания является исследование на биоэквивалентность. Такие тесты применяют для регистрации дженериков — копий оригинальных лекарственных препаратов, но не вакцин.
Исследования биоэквивалентности проводят на небольшой группе из 12-24 здоровых добровольцев. Испытуемым вводят новый препарат и в течение 1-2 дней берут пробы крови с определённым интервалом. После измерения концентрации вещества в крови строят график и сравнивают его с таковым у оригинального лекарства.
Успешные испытания биоэквивалентности позволяют считать схожими данные о токсичности и эффективности воспроизведённой копии и оригинального препарата. Таким образом, производитель дженерика не тратит время и деньги на полный цикл исследования лекарственного препарата. Всё, что нужно — это доказать идентичность оригинальному лекарству.
2 фаза клинических исследований
Это исследование на группе больных из 100-200 человек. Для испытания вакцин на 2 фазу набирают добровольцев с разным состоянием здоровья, в том числе с хроническими заболеваниями.
Люди с различными заболеваниями обычно становятся участниками 2 фазы испытаний по рекомендации врача. Медицинское обследование на протяжении эксперимента, все виды лечения по профилю исследования в этом случае бесплатные. Для некоторых пациентов участие в клинических испытаниях — это шанс отстоять свою жизнь у смертельного заболевания, так как получить ещё незарегистрированный и потенциально более эффективный лекарственный препарат другим путём невозможно.
Во время 2 фазы препарат используют в терапевтических дозировках и оценивают его эффективность, а также выявляют оставшиеся незамеченными ранее побочные эффекты.
Требования к качеству 2 фазы значительно выше. В идеале это рандомизированные двойные слепые исследования с плацебо-контролем.
Рандомизированные — значит всех участников делят на группы случайным образом, а не по желанию врача. Одна из групп будет получать вместо лекарства пустышку — плацебо.
Двойное слепое — значит ни пациенты, ни врачи, участвующие в эксперименте, не будут знать о том, кто какое лечение получает. Для этого плацебо и традиционные препараты должны выглядеть одинаково, а данные о них и пациентах шифруются.
Если препарат оказался эффективнее плацебо, лекарство допускают до следующего этапа. Отсев на этом этапе — около 70% вступивших в него веществ.
Собственно, преодолев это этап испытаний, вакцины от коронавируса получают сейчас временную регистрацию на особых условиях и поступают в поликлиники и прививочные пункты для свободной вакцинации населения. Хотя по правилам мирного времени впереди ещё главные тесты.
3 фаза клинических испытаний
Самая ответственная для кандидата. Успешно прошедшие его получают постоянную регистрацию в качестве лекарственного препарата.
В 3 фазе участвуют от нескольких сотен до 3000 людей с соответствующим заболеванием — для тестирования лекарств или с разным состоянием здоровья — для вакцин.
Главная цель — сравнить эффективность вещества с уже имеющимися препаратами или методами лечения. При испытании вакцины — получить данные по эффективности и безопасности на большой группе людей, так как результаты наблюдений за одной-двумя сотнями испытуемых могут совсем не соответствовать тому, что получится при массовой вакцинации.
Кроме того, важно отследить долгосрочные результаты использования препарата у людей.
Исследование, как и в предыдущей фазе, должно соответствовать рандомизированному с двойным ослеплением. Каждый участник исследования подписывает договор, в котором указаны все риски, а также условия эксперимента. Организация, которая проводит клинические исследования обязана застраховать жизнь и здоровье каждого участника исследования за собственный счёт. Сумма страховки составляет от 300 тысяч до 2 млн в случае смерти.
Заключительный этап испытаний преодолевают в среднем не более 30% кандидатов. Однако и после регистрации лекарства продолжают тестировать.