Диоксид титана (Е171)

Описание добавки
Химический состав Е171: двуокись титана (отвечает за отбеливание) и титановые белила. Во время нагревания вещество окрашивается в бледно желтый цвет. Это инертное вещество, которое не растворяется в воде, подсолнечном и оливковом маслах, спирте.
В природе титановый диоксид содержится в некоторых минералах, например, бруките, рутиле и анатазе. Краситель представляет собой беленький порошок без отличительного вкуса и аромата. Характеризуется длительной устойчивостью к воздействию солнечных лучей, кислотной среде, щелочей и температурных колебаний.
Белые кристаллы в дробном виде используются в промышленных отраслях. Их получают двумя самыми распространенными способами. Первый – сульфатный из ильментированого концентрата, второй – хлоридный из титанового тетрахлорида.
Главные свойства диоксида титана: он вовсе не токсичен, имеет химическую стойкость, не меняет запах (только меняется оттенок во время нагревания), отличается высокой влагостойкостью, полностью совместим с абсолютно любыми пленочными изделиями, имеет высокую отбеливающую и в тот же момент красящую способность.
Titanium oxide в косметологии
Е171 используется в производстве различных кремов для равномерного и качественного загара, в мазях от аллергических реакций. Он признан одним из лучших веществ, которые защищают кожный покров от ультрафиолетовых лучей, вызывающих меланому кожи.
Титановый диоксид можно найти в косметике и косметических средствах, таких как пудра, губная помада, тени для век, антиперспиранты, мыло и зубная паста. Любители натуральных косметических средств готовят мыло самостоятельно и отбирают нужные и качественные компоненты. В мыле обязательным компонентом является Е171, который не только придает нужный оттенок, но и защищает его от солнечных лучей. С помощью добавки получается качественный косметический материал, в том числе титановый слюд (насыщенный перламутр).
Титана диоксид в пищевом производстве

Краситель – это незаменимый компонент в производстве сухих смесей, молочных продуктов и завтраков быстрого приготовления. В качестве натурального отбеливателя используется для массового изготовления жвачек. При помощи титанового диоксида осуществляется отбеливание крабовых палочек (их белых частей) и прочих морепродуктов.
Пищевая сфера нуждается в Е171, потому что краситель диоксид титана есть первоочередной составляющей для создания печенья, булочек, конфет и иных продуктов. Суточная норма для человека данной пищевой добавки не должна быть более 1 процента.
Титановый диоксид в медицине
Фармацевтическая отрасль тоже не осталась в стороне, поскольку Е171 является одним из компонентов многих лекарственных средств. Он предназначен для того, чтобы:
Белый диоксид титана широко используется в медицинской отрасли в производстве таблетированных препаратов и витаминных комплексов. Добавление порошка в основы кремов, суппозитории, пасты и иные фармакологические лекарственные средства, стало привычным делом.
Титановый диоксид в других сферах
Также titanium oxide можно встретить в производстве лакокрасочных изделий (например, ламинированной бумаги и пластмассы). Вещество обладает огнеупорными способностями, поэтому необходимо для изготовления оптических стекол. Также известно его использование для создания белил для обмазки сварочных электродов. Благодаря данной добавке повышается стойкость к выцветанию и старению топографической краски, улучшается структурные особенности бумажной пульпы в картонно-бумажной индустрии.
| Страна | Максимальная годовая производительная мощность |
|---|---|
| Америка | 300 |
| Канада | 20 |
| Германия | 140 |
| Великобритания | 150 |
| Франция | 105 |
| Финляндия | 120 |
Двуокись титана применяется в виде микрочастиц в сфере нанотехнологий, но это пока еще новое направление в применении Е171. Поэтому мировой объем потребления микрочастиц равен приблизительно двум тысячам тонн в год. Спрос на титановый диоксид объясняется тем, что произошел за последние несколько лет рост производства товаров широкого потребления и иных отраслей экономики государств. В развитых странах потребление добавки должно составлять 2 кг на одного человека, но этого добиться довольно сложно, например, в России этот показатель равен только 300 граммам. Стремительно увеличивается емкость рынков сбыта и потребления, а это говорит о том, что данная пищевая добавка на мировом рынке имеет неплохие перспективы.
Для масштабного производства керамики, стекла и резины титановую двуокись используют как катализатор химических реакций, благодаря этому можно пользоваться готовой продукцией при повышенных температурах. Благоприятно воздействует титановый диоксид на древесину, он защищает ее от радиации солнечных лучей.
Как влияет Е171 на здоровье?
Влияние на организм человека пищевой добавки исследуется до нынешних дней. В мае 2021 года Европейское агентство продовольственной безопасности пришло к выводу, что Е171 нельзя считать безопасной для здоровья в качестве пищевой добавки. Как оказалось, опасным свойством диоксида титана является генотоксичность – способность повреждать молекулы ДНК, что может приводить к развитию онкологических заболеваний. Добавка на момент редактирования статьи разрешена во многих государствах: Российской Федерации, в некоторых странах Европейского Союза, США, Канаде и других. Данный краситель состоит в Кодексе Алиментариус (своде пищевых международных стандартов) как ценная пищевая добавка. Но по результатам многих современных исследований было выяснено, что вещество причиняет вред человеку.
Не рекомендуется употреблять пищевую добавку людям, у которых слабая иммунная система, заболевания почек и печени. При вдыхании белого порошка увеличивается вероятность появления рака. Это подтверждают эксперименты, проведенные на крысах. Грызунам в еду подсыпали краситель, спустя пять дней, было проверено самочувствие и общее состояние крыс. За этих 5 дней у грызунов деформировались хромосомы, была нарушена цепочка ДНК. Обмен веществ у крыс протекает в несколько раз быстрее, нежели у человека, поэтому при тестировании организма человека после употребления Е171 результаты могут значительно отличаться.
Считалось, что Е171 безвредное вещество, которое не вызывает химических реакций в живых организмах, но это не так. Добавка оказывает сильнейшее механическое воздействие на живые клетки и может полностью разрушить их природное строение. Есть большая вероятность, что пыль диоксида титана имеет канцерогенные особенности и может негативно повлиять на самочувствие человека.
Несмотря на длительные исследования и эксперименты, краситель Е171 используется в качестве пищевой добавки и считается безопасным, при условии, если его будут добавлять в пищу в минимальных дозировках.
Диоксид титана, где бы ни использовался, он является незаменимой и натуральной добавкой. В первую очередь это связано с его технологическими особенностями: он предотвращает, полностью устраняет нежелательное окрашивание продуктов питания, известен как краситель для продуктов и смесей, придает привлекательный внешний вид готовым изделиям. Самое главное, что эта добавка получена из природных экологически чистых источников. Специалисты утверждают, что только в случае передозировки могут возникнуть побочные эффекты, поэтому добавка разрешена во многих государствах, так как ее вредные стороны не оказывают какого-либо значительного риска для здоровья людей.
Оксид титана (двуокись титана)
Понятие и общие сведения
Титан является металлом четвертой группы, который при соединении с кислородом может образовывать до 15 различных оксидов. Однако, наиболее характерен для него диоксид или оксид титана (IV), или двуокись титана.
В зависимости от вида кристаллической решетки титановый диоксид образует следующие минералы:
— Рутил, обладающий тетрагональной кристаллической решеткой.
— Анатаз, имеющий тетрагональную решетку.
— Брукит, характеризующийся ромбической решеткой.
Кроме того, известны две другие модификации титаноксида высокого давления: ромбическая и гексагональная. В лаборатории под давлением 60 000 бар синтезировали еще одну модификацию двуокиси титана с наиболее высокой твердостью из известных.
Свойства
Оксиды титана различных степеней окисления сильно отличаются друг от друга по своим физико-химическим характеристикам. Рассмотрим свойства наиболее распространенных оксидов.
Монооксид (оксид титана II) формулой TiO представляет собой кристаллы, обладающие цветом в гамме от золотисто-желтого до коричнево-фиолетового цвета. Это вещество не растворимо в воде, но растворимо в разбавленных соляной и серной кислотах. В случае нагревания в воздушной среде монооксид окисляется до двуокиси титана TiO2. Это свойство используется в катализаторах, где находит применение окись титана (II).
Сесквиоксид (оксид титана III), химически описываемый как Ti2O3, выглядит как кристаллы темно-фиолетового или черного цвета. Не является устойчивым соединением, при сильном нагреве до испарения диссоциирует на два других оксида TiO и TiO2. В среде воздуха подвергается окислению лишь при очень высокой температуре. Не реагирует с водой и неорганическими кислотами. Растворяется при нагреве в концентрированной серной кислоте с выходом сульфата титана (III) фиолетового цвета.
Двуокись титана (оксид титана IV) формулой TiO2 – это, как ни странно, в кристаллической форме представляют собой неокрашенные кристаллы, желтеющие при нагревании, однако вновь теряющие цвет при последующем охлаждении. Диоксид титана не растворим в воде, набухает в неорганических кислотах и разбавленных растворах щелочей. С трудом растворим в концентрированных серной кислоте и щелочных растворах. При нагревании в азотной кислоте образуется карбид титана (III) TiN. Титаноксид (IV) восстанавливают до оксидов титана (III и II) нагревая первый в среде водорода, углерода, щелочных или щелочноземельных металлов – натрия, магния, кальция и т.д. При нагревании в среде газообразного хлора и восстановителей, например углерода получается хлорид титана (IV).
Получение
Титаноксид (IV) производят различными способами, например путем прокаливания кислородсодержащих солей и оснований, гидролизом или сжиганием титансодержащих соединений и другими способами.
Чаще всего двуокись титана получают прокаливанием гидроокиси, полученной после гидролиза сульфатных растворов или сжиганием хлорида титана (IV) при температурах от 1200 градусов С. Высокочистый диоксид титана получается при помощи гидролиза титанорганических веществ с последующим прокаливанием.
Из полученной таким образом двуокиси титана можно произвести оксиды с более низкими степенями окисления при помощи частичного восстановления водородом или элементарным титаном при температурах порядка 1500 градусов С по схеме:
Оксиды с большим количеством атомов титана и наличествующими связями типа Ti-Ti, например Ti6O, Ti3O, Ti2O образуются в ходе растворения кислорода в непосредственно в титане. В случае повышения температуры более 300 градусов С такие соединения окисляются далее вплоть до двуокиси титана.
Применение титаноксида
Титан образует множество оксидов, однако подавляющее большинство применений имеет только оксид титана (IV) или двуокись. Среди других подобных соединений она является важным керамическим материалом и важнейшим пигментом.

Рис.1. Гранулированный суперконцентрат пигмента TiO2.
Суть применения двуокиси титана в современной индустрии базируется на способности мелкодисперсного порошка оксида с размером частиц от 20 до 50 нанометров демонстрировать очень высокую отражательную способность. Это свойство позволяет применять диоксид титана в качестве белого пигмента при изготовлении красок, известных как «титановые белила». Кроме того, пигмент повсеместно применяется при производстве эмалей, окраске бумаги, пластмасс и эластомеров, синтетических волокон, керамической продукции, стекла и многого другого. Титановые краски имеют ряд преимуществ перед аналогами и прежде всего ранее широко применяющимися свинцовыми белилами:
— отсутствие токсичности (кроме порошкообразной формы – см. ниже),
— имеют более высокие эксплуатационные характеристики, надежность и долговечность.
В промышленности производства и переработки пластмасс и эластомеров диоксид титана является одним из самых важных пигментов. Он применяется в основном в двух формах:
Порошкообразной форме для приготовления смесей, применяемых при экструзии изделий из ПВХ (оконные и дверные профили, подоконники, водостоки, сайдинг, отделочные панели и т.д.). Также применяется для приготовления пластизолей и при других нераспространенных применениях.
В виде гранулированных суперконцентратов пигментов на основе различных полимеров, чаще всего полиэтилена, сэвилена, полипропилена, полистирола. Такая форма, с наполнением оксидом титана до 80% суперконцентрата, широко используется при литье под давлением, выдувном формовании, экструзии гранулированных пластмасс.
Также двуокись титана используется при приготовлении жидких красителей для пластмасс, опудривании гранул непосредственно пигментами и т.д.

Рис.2. Типичное изделие из ПВХ окрашенное в массе
Возможный вред здоровью
В действующих стандартах указано, что пыль диоксида титана обладает раздражающим действием. Она в определенных концентрациях может стать причиной бронхитов, пневмосклероза и прочих болезней легких человека. Предельно-допустимая концентрация титаноксида в воздухе рабочей зоны составляет 10 мг/куб.м, в атмосферном воздухе 0,5 мг/куб.м, в воде 0,1 мг/литр.
Вредность и теоретическая опасность диоксида титана привела к пристальному вниманию к этому соединению со стороны законодателей ряда стран, прежде всего государств Евросоюза. В 2019 году в новостных лентах стали появляться сообщения об ограничении использования титаноксида и его возможном запрете в будущем. В частности, Европейское Химическое Агентство в 2017 году подтвердило опасность порошкообразного титаноксида. В сентябре 2019 года эксперты Competent Authorities for REACH and CLP предложили Европейской Комиссии внести двуокись титана в перечень потенциально опасных веществ. Пока речь идет только о пигменте в порошкообразной форме, однако и это наносит большой ущерб полимерной отрасли, т.к. порошок TiO2 практически незаменим при экструзии в частности ПВХ-профилей.
Объявления о покупке и продаже оборудования можно посмотреть на
Обсудить достоинства марок полимеров и их свойства можно на
Зарегистрировать свою компанию в Каталоге предприятий
Оксид титана
Оксид титана(IV) (диоксид титана, двуокись титана, титановые белила, пищевой краситель E171) TiO2 — амфотерный оксид четырёхвалентного титана. Является основным продуктом титановой индустрии (на производство чистого титана идёт лишь около 5 % титановой руды). [1]
Содержание
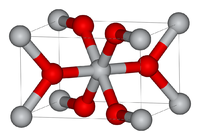
Строение
Оксид титана существует в виде нескольких модификаций. В природе встречаются кристаллы с тетрагональной сингонией (анатаз, рутил) и ромбической сингонией (брукит). Искусственно получены ещё две модификации высокого давления — ромбическая IV и гексагональная V.
| Модификация/Параметр | Рутил | Анатаз | Брукит | Ромбическая IV | Гексагональная V | |
|---|---|---|---|---|---|---|
| Параметры элементарной решётки, нм | a | 0,45929 | 0,3785 | 0,51447 | 0,4531 | 0,922 |
| b | — | — | 0,9184 | 0,5498 | — | |
| c | 0,29591 | 0,9486 | 0,5145 | 0,4900 | 0,5685 | |
| Число формульных единиц в ячейке | 2 | 4 | 8 | |||
| Пространственная группа | P4/mnm | I4/amd | Pbca | Pbcn | ||
Нахождение в природе
Третье в мире по запасам рутила месторождение находится в Рассказовском районе Тамбовской области. Крупные месторождения находятся также в Чили (Cerro Bianco), канадской провинции Квебек, Сьерра-Леоне.
Свойства
Физические, термодинамическе свойства
Чистый диоксид титана — бесцветные кристаллы (желтеет при нагревании). Для технических целей применяется в раздробленном состоянии, представляя собой белый порошок. Не растворяется в воде и разбавленных минеральных кислотах (за исключением плавиковой).
Температура плавления, кипения и разложения для других модификаций не указана, т.к. они переходят в рутильную форму при нагревании (см. выше).
| Модификация | Интервал температуры, K | |||||
|---|---|---|---|---|---|---|
| 298—500 | 298—600 | 298—700 | 298—800 | 298—900 | 298—1000 | |
| рутил | 60,71 | 62,39 | 63,76 | 64,92 | 65,95 | 66,89 |
| анатаз | 63,21 | 65,18 | 66,59 | 67,64 | 68,47 | 69,12 |
| Модификация | ΔH°f, 298, кДж/моль [6] | S°298, Дж/моль/K [7] | ΔG°f, 298, кДж/моль [8] | C°p, 298, Дж/моль/K [9] | ΔHпл., кДж/моль [10] |
|---|---|---|---|---|---|
| рутил | -944,75 (-943,9 [3] ) | 50,33 | -889,49 (-888,6 [3] ) | 55,04 (55,02 [3] ) | 67 |
| анатаз | -933,03 (938,6 [3] ) | 49,92 | -877,65 (-888,3 [3] ) | 55,21 (55,48 [3] ) | 58 |
Вследствие более плотной упаковки ионов в кристалле рутила увеличивается их взаимное притяжение, снижается фотохимическая активность, увеличиваются твёрдость (абразивность), показатель преломления (2,55 — у анатаза и 2,7 — у рутила), диэлектрическая постоянная.
Химические свойства
Диоксид титана амфотерен, то есть проявляет как осно́вные, так и кислотные свойства (хотя реагирует главным образом с концентрированными кислотами).
Медленно растворяется в концентированной серной кислоте, образуя соответствующие соли четырёхвалентного титана:
В концентрированных растворах щелочей или при сплавлении с ними образуются титанаты — соли титановой кислоты (амфотерного гидроксида титана TiO(OH)2)
То же происходит и в концентрированных растворах карбонатов или гидрокарбонатов:
C перекисью водорода даёт ортотитановую кислоту:
При нагревании с аммиаком даёт нитрид титана:
При сплавлении с оксидами, гидроксидами и карбонатами образуются титанаты и двойные оксиды:
При нагревании восстанавливается углеродом и активными металлами (Mg, Ca, Na) до низших оксидов.
При нагревании с хлором в присутствии восстановителей (углерода) образует тетрахлорид титана.
Нагревание до 2200 °C приводит сначала к отщеплению кислорода с образованием синего Ti3O5 (то есть TiO2·Ti2O3), а затем и тёмно-фиолетового Ti2O3.
Гидратированный диоксид TiO2·nH2O [гидроксид титана(IV), оксо-гидрат титана, оксогидроксид титана] в зависимости от условий получения может содержать переменные количества связанных с Ti групп ОН, структурную воду, кислотные остатки и адсорбированные катионы. Полученный на холоде свежеосажденный TiO2·nH2O хорошо растворяется в разбавленных минеральных и сильных органических кислотах, но почти не растворяется в растворах щелочей. Легко пептизируется с образованием устойчивых коллоидных растворов. При высушивании на воздухе образует объёмистый белый порошок плотностью 2,6 г/см³, приближающийся по составу к формуле TiO2·2H2O (ортотитановая кислота). При нагревании и длительной сушке в вакууме постепенно обезвоживается, приближаясь по составу к формуле TiO2·H2O (метатитановая кислота). Осадки такого состава получаются при осаждении из горячих растворов, при взаимодействии металлического титана с HNO3 и т. п. Их плотность
3,2 г/см³ и выше. Они практически не растворяются в разбавленных кислотах, не способны пептизироваться.
При старении осадки TiO2·nH2O постепенно превращается в безводный диоксид, удерживающий в связанном состоянии адсорбированные катионы и анионы. Старение ускоряется кипячением суспензии с водой. Структура образующегося при старении TiO2 определяется условиями осаждения. При осаждении аммиаком из солянокислых растворов при рН Токсические свойства, физиологическое действие, опасные свойства
TLV(предельная пороговая концентрация, США): как TWA (среднесменная концентрация, США) 10 мг/м³ A4 (ACGIH 2001).
Добыча и производство
Полная статья получение оксида титана(IV)
Мировое производство диоксида титана на конец 2004 года достигло приблизительно 5 миллионов тонн. [11]
Основными производители и экспортёры диоксида титана:
В последние годы чрезвычайно быстро растет производство диоксида титана в Китае.
В России пигментный диоксид титана не производят, но производят технические марки, используемые в металлургии. На территории СНГ диоксид титана производится на Украине предприятиями «Сумыхимпром», город Сумы, «Крымский титан», г. Армянск) и КП «Титано-магниевый комбинат» (г. Запорожье). Сумский государственный институт минеральных удобрений и пигментов (МИНДИП) в своих научно-исследовательских работах особое место уделяет технология получения оксида титана (IV) сульфатным способом: исследование, разработка новых марок, модернизация технологии и аппаратурного оформления процесса.
Как указано выше, диоксид титана встречается в виде минералов, однако этого источника недостаточно, поэтому значительная его часть производится. Существуют два основных промышленных метода получения TiO2: из ильменитового (FeTiO3) концентрата и из тетрахлорида титана.
Производство диоксида титана из ильменитового концентрата
Технология производства состоит из трёх этапов:
Производство диоксида титана из тетрахлорида титана
Существуют три основных метода получения диоксида титана из его тетрахлорида:
Применение
Основные применения диоксида титана:
Другие применения — в производстве резиновых изделий, стекольном производстве (термостойкое и оптическое стекло), как огнеупор (обмазка сварочных электродов и покрытий литейных форм), в косметических средствах (мыло и т.д.), в пищевой промышленности (пищевая добавка E171).
Цены и рынок
Нормативы
В настоящее время диоксид титана по ГОСТ 9808-84 не выпускается.
По данным техническим условиям работает ГАК «Титан» (г. Армянск).
По данным техническим условиям работает ОАО «Сумыхимпром» (г. Сумы).
Использованная литература
Ссылки
Разное: Воск (E900-909) • Глазурь (E910-919) • Восстановитель (E920-929) • Газ для упаковки (E930-949) • Заменители сахара (E950-969) • Вспениватель (E990-999)
Примечания
Полезное
Смотреть что такое «Оксид титана» в других словарях:
Оксид титана(IV) — Общ … Википедия
Оксид титана(II) — Общие Систематическое наименование Оксид титана(II) Традиционные названия Окись титана Химическая формула TiO Физические свойства Состояние ( … Википедия
оксид титана — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN titanium oxide … Справочник технического переводчика
Оксид титана (IV) — Порошок оксида титана Оксид титана(IV) (диоксид титана, двуокись титана, титановые белила, пищевой краситель E171) TiO2 амфотерный оксид четырёхвалентного титана. Является основным продуктом титановой индустрии (на производство чистого титана… … Википедия
Оксид титана(III) — Общие Систематическое наименование Оксид титана(III) Традиционные названия трёхокись титане Химическая формула Ti2O3 Физические свойства … Википедия
Дигидроксид-оксид титана — Общие Систематическое наименование Дигидроксид оксид титана Традиционные названия Метатитановая кислота, β титановая кислота Химическая формула TiO(OH)2 Физические свойст … Википедия
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
ТИТАНА СЕМЕЙСТВО — ПОДГРУППА IVB. СЕМЕЙСТВО ТИТАНА ТИТАН, ЦИРКОНИЙ, ГАФНИЙ К переходным металлам относятся также элементы семейства титана Ti, Zr и Hf, отличающиеся удивительным сходством свойств. Последние два элемента (Zr и Hf) особенно близки по свойствам.… … Энциклопедия Кольера
Оксид цинка — Оксид цинка … Википедия
Оксид цинка(II) — Оксид цинка Общие Систематическое наименование Цинка оксид Химическая формула ZnO Отн. молек. масса N а. е. м. Молярная масса … Википедия