Чем отличается доброкачественная опухоль от злокачественной
В медицине понятие доброкачественности означает лёгкое течение болезни, хорошие результаты лечения и неопасность для жизни. Под злокачественным процессом подразумевают разрушительное течение, сложность терапии, высокий риск смертности.
Для опухолей такое разделение условно. Тем не менее пациентам и врачам крайне важно определить вид опухоли. От этого зависят тактика лечения и прогноз.
Характеристика доброкачественных и злокачественных опухолей
Существуют чёткие критерии:
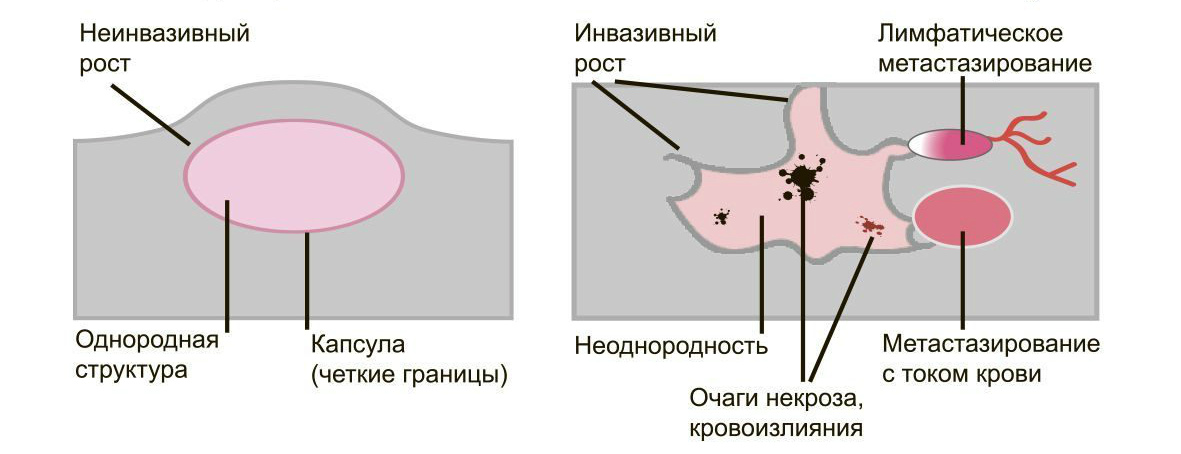
Доброкачественные опухоли чётко отграничены от здоровых тканей, часто имеют капсулу. Рак прорастает окружающие ткани, внедряется в сосуды, его контуры более аморфны.
Большинство доброкачественных опухолей могут расти годами, не проявляя симптомов. Карциномы растут быстро, нарушая функции органов и отравляя организм. Рост сопровождается утомляемостью, слабостью, потерей веса, болью.
Доброкачественные образования “сидят” на одном месте, постепенно растут и раздвигают здоровые ткани, подвижны при прощупывании. Раковые клетки слабо скреплены друг с другом, легко отделяются и разносятся лимфой и кровью по организму. Они оседают в лимфоузлах, костях, внутренних органах, образуя новые опухолевые очаги — метастазы. При пальпации узел спаян с тканями и не сдвигается.
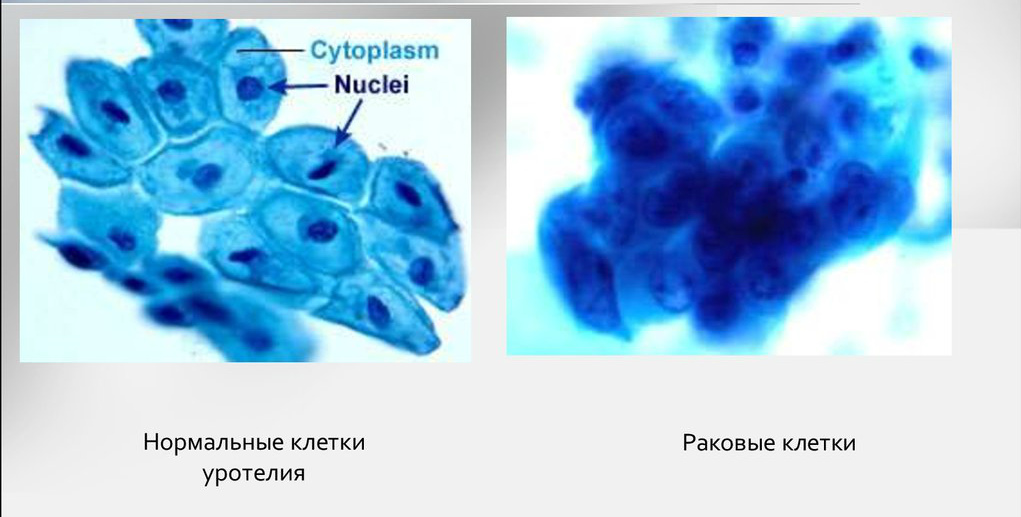
Много информации даёт биопсия. Исследование показывает, что доброкачественные клетки похожи на здоровые, их структура более чёткая. Структура злокачественных клеток сильно изменена из-за выраженных мутаций. Чем меньше клетки напоминают ткань, из которой выросли, тем хуже прогноз для лечения и жизни.
Доброкачественную опухоль, такую как аденома простаты, можно удалить и добиться полного излечения. Если возникнет рецидив, он будет на том же месте, где нашли первичный очаг. Злокачественные образования трудно удалить полностью. Даже одна оставшаяся клетка даст новую опухоль либо на старом месте, либо там, куда она попала по сосудам. Выживаемость больных существенно ниже.
Общие свойства доброкачественных и злокачественных опухолей
Есть моменты, объединяющие оба вида новообразований:
Тяжесть симптомов зависит не только от степени сдавления тканей опухолью, но и от неспособности новообразования выполнять функцию здоровых клеток.
Виды опухолей
Различия не всегда очевидны. Нужна тщательная диагностика для поиска атипичных клеток.
Может ли доброкачественная опухоль стать злокачественной
Любая опухоль способна к малигнизации. Миомы, липомы, фибромы редко переходят в рак. Кисты — крайне редко. Невусы, аденомы, полипы в желудке или кишечнике — очень часто. Многое зависит от условий, в которых находится опухоль, питания, экологии, уровня стресса, гормональных сбоев, наличия предраковых болезней.
В Клинике урологии имени Р. М. Фронштейна доступна современная диагностика опухолей, разработаны эффективные методики лечения. Обращайтесь на консультацию и наши специалисты вам помогут.
Объемное образование что это
а) Терминология:
• Патологическое образование в грудной клетке с максимальным диаметром > 3 см
— Обычно солидное, но может содержать участок некроза или полость
• Объемные образования могут локализоваться в любой анатомической области:
— Легкие, плевра, средостение, грудная стенка, диафрагма
б) Рентгенография объемного образования легкого:
— Выявление патологического образования в определенной анатомической области
— Объемное образование в легком: окружено легочной паренхимой, характеризуется четкими или нечеткими границами, спикулообразным или дольчатым контуром
— Объемное образование в плевре: может образовывать тупой угол с прилежащей плеврой и характеризоваться симптомом неполного контура
— Объемное образование в средостении: изменение контуров средостения; ограниченного размера или заполняет все средостение; на рентгенограмме в боковой проекции можно установить точную локализацию в определенном отделе средостения
— Объемное образование в грудной стенке: симптом неполного контура; может вызывать эрозию или деструкцию костных структур, а также вовлекать в процесс мягкие ткани
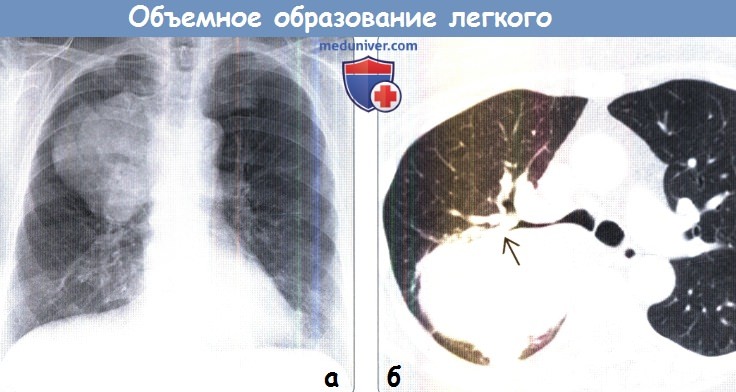
(б) У того же пациента при КТ с контрастным усилением в верхней доле правого легкого визуализируется мягкотканное объемное образование больших размеров.
Образование прорастает прилежащие отделы средостения, сдавливает правый верхнедолевой бронх и вызывает облитерацию просвета заднего сегментарного бронха. Объемные образования в легком обычно соответствуют злокачественным новообразованиям и чаще всего — первичному раку легких.
в) КТ объемного образования легкого:
— Объемное образование в легком: определение морфологических характеристик и стадирование (местнодеструирующий рост, лимфаденопатия, метастазы)
— Объемное образование в плевре: ограниченного размера или заполняет все средостение; выявление местнодеструирующего роста, лимфаденопатии, плеврального выпота
— Объемное образование в средостении: оценка морфологических характеристик патологического образования и его плотности, выявление лимфаденопатии, местнодеструирующего роста
— Объемное образование в грудной стенке: выявление вовлечения в опухолевый процесс костных структур и мягких тканей
г) Дифференциальная диагностика:
• Легкие: рак легких, абсцесс, метастаз
• Плевра: локализованная фиброзная опухоль плевры, метастаз
• Средостение: тимома, нейрогенная опухоль, лимфома, метастатическая лимфаденопатия
• Грудная стенка: метастаз, хондросаркома, миелома
д) Диагностические пункты:
• Объемные образования грудной клетки с высокой вероятностью являются злокачественными
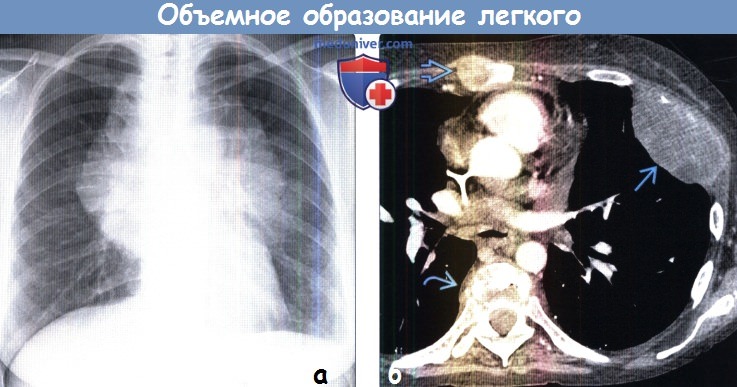
(б) У женщины 30 лет с гинекологическим раком на поздней стадии при КТ с контрастным усилением в передних отделах грудной стенки слева визуализируются объемное образование больших размеров 1-3 и деструкция ребра.
В грудине и позвонке выявляются дополнительные патологические образования и деструкция костной ткани, что соответствует метастатическому поражению грудной стенки.
Редактор: Искандер Милевски. Дата публикации: 22.1.2019
Доброкачественные и злокачественные опухоли почек
Опухоль почки бывает как доброкачественного, так и злокачественного происхождения. Занимая третье место среди онкологических патологий мочеполовой системы, болезнь поражает преимущественно людей, достигших 40-летия, причем среди мужчин больных в 2 раза больше, чем среди женщин.
Существуют различные варианты злокачественной трансформации почечной ткани. Нередко рак почки длительное время протекает бессимптомно. Латентное течение болезни затрудняет диагностику, однако даже при позднем выявлении можно рассчитывать на благоприятный исход.
Более подробно вопросы возникновения, развития и лечения опухоли почек описаны в соответствующем разделе этого сайта.
Для определения вида опухоли почки, ее локализации к основным структурам органа и показаний к операции, а также выбора правильной тактики хирургического лечения необходимо прислать мне на личный электронный адрес puchkovkv@mail.ru puchkovkv@mail.ru копировать полное описание УЗИ почек, данные МСКТ почек с контрастом, указать возраст и основные жалобы. Тогда я смогу дать более точный ответ по вашей ситуации.
Основные симптомы
На протяжении длительного времени заболевание может протекать бессимптомно. Со временем появляются симптомы, среди которых основными являются гематурия (кровь в моче), прощупываемая в животе опухоль и боли. Гематурия, как правило, появляется внезапно и носит кратковременный характер. Нередко в моче можно обнаружить червеобразные кровяные сгустки. Прощупать опухоль можно лишь в том случае, если ее размеры достигают 5 см, но у пациентов с излишним весом сделать это затруднительно и при больших размерах образования. Боль носит тупой характер, отмечается со стороны поражения. Кроме того, человека беспокоит слабость, повышение температуры, присоединяется артериальная гипертензия. В результате сдавления нижней полой вены развиваются отеки ног, расширение подкожных вен брюшной стенки, варикоцеле. При распространении метастазов в отдаленные ткани и органы появляются симптомы, характерные для поражения конкретного органа: кашель и кровохарканье при поражении легких, патологические переломы и боли при в костях, желтуха при распространении раковых клеток в печень и т.д.
В каких случаях показана операция
Операция является основным методом лечения опухоли почки, особенностью данного заболевания можно назвать отсутствие чувствительности к лучевой и химиотерапии. При отсутствии лечения гематурия может спровоцировать развитие анемии, сгустки крови на поздней стадии способны привести к обтурации мочеточника либо к тампонаде мочевого пузыря, что вызовет острую задержку мочи. Кроме того, отказ от лечения при злокачественном образовании означает неуклонное прогрессирование болезни. При этом метастазы, распространяясь по всему организму, поражают жизненно важные органы: печень, легкие, мозг и др.
Методы диагностики
Прежде всего, проводится общеклиническое обследование, на основании которого назначаются биохимическое и цитологическое исследования. Для уточнения диагноза необходим ряд исследований: ультразвуковое обследование, экскреторная урография, компьютерная томография.
Операция при раке почки
В большинстве лечебных учреждений выполняется удаление всей почки открытым способом. Однако при опухоли небольшого размера операцию можно провести с сохранением органа. Конечно, если новообразование большого размера, либо расположено в центре, приходится выполнять нефрэктомию — удаление. Однако в клиниках Европы и США при лечении рака почки «золотым» стандартом является парциальная резекция — удаление части почки вместе с опухолью. И лишь при невозможности резекции проводится нефрэктомия — удаление почки.
 |
СТВ: Скат. Мастер-класс К. В. Пучкова
Во время проведения малоинвазивной операции при раке почки я всегда стараюсь сохранить орган, выполнив лапароскопическую резекцию. Почка при этом выделяется из окружающих ее тканей, затем с помощью специального лапароскопического ультразвукового датчика уточняется локализация опухоли по отношению к лоханке и почечным сосудам (Рис.1). При благоприятной «хирургической» ситуации проводится резекция почки – отступя на 5-8 мм от опухоли, в пределах здоровых тканей, выполняется иссечение образования ультразвуковыми ножницами (Рис. 2). Для ушивания раны применяются синтетические рассасывающиеся нити, а также гемостатический клей производства США и гемостатическую систему PerClot (Италия), благодаря которому почечную рану можно герметично закрыть (Рис. 3).
В сложных случаях я использую шовную систему V-lock (Covidien, Швейцария), которая выполнена из монофиламентной рассасывающейся полидиоксаноновой нити с насечками на ней. Насечки ориентированы в пространстве под заданным углом в одном направлении. Это позволяет нити свободно скользить в одном направлении и быть практически не смещаемой в противоположном. Такие системы фиксируют ткани по анкерному типу и не требуют завязывания узлов. При использовании этой шовной системы отмечается более тщательное сопоставление краев раны на матке (что приводит к еще лучшему заживлению ) и в 3-4 раза возрастает скорость формирования шва.
Кроме того, огромным плюсом для профилактики развития спаечной болезни можно считать использование противоспаечных барьеров и жидких сред, а также применение современного компрессионного трикотажа в качестве профилактики тромбоэмболии и ТЭЛА. Через год, как правило, место операции нельзя определить даже с помощью УЗИ.
При проведении лапароскопической нефрэктомии я в обязательном порядке удаляю все лимфоузлы, в которых могут находится клетки опухоли. Этот шаг является чрезвычайно важным, ведь исключить до операции метастатическое поражение регионарных лимфоузлов невозможно даже с помощью самого современного диагностического метода. Если же пораженные метастазами лимфоузлы оставить, процесс будет прогрессировать. При мобилизации почки используются современные ультразвуковые хирургические ножницы, а также аппарат электротермического дозированного лигирования тканей «LigaSure» (США) — благодаря которому этот этап операции бескровен. Резецируемый фрагмент с опухолью удаляется из полости брюшины в специальном пластиковом контейнере — таким образом можно избежать контаминации окружающих тканей опухолевыми клетками. На этом же этапе на брюшной стенке выполняется разрез около 4 см.
Я располагаю огромным опытом проведения малоинвазивных хирургических вмешательств, мною успешно выполнено около 500 операций по поводу опухолей почек различной формы — и доброкачественных и злокачественных. Результаты проведенных вмешательств обобщены в более чем 20 научных публикациях, которые можно найти в различных рецензируемых профессиональных научных изданиях, как в российских, так и зарубежных.
Подобные операции я выполняю с 2000 г., за это время мною разработан оригинальный способ установки троакаров во время проведения лапароскопической операции на почке и забрюшинном пространстве. Это позволяет расположить инструменты под оптимальным манипуляционным углом, поэтому ушивание раны на почке при ее резекции и удалении лимфатических узлов при радикальной нефрэктомии происходит легко и быстро.
Посмотреть видео операций в моем исполнении можно на сайте «Видео операций лучших хирургов мира».


Владея всеми основными методами операций на почках, обладая опытом успешного проведения операций при кистах, опухолях доброкачественного характера, а также при раке почки, я в каждом конкретном случае стремлюсь подобрать оптимальную тактику хирургического лечения. Используемые мною оперативные методики дают возможность провести с применением лапароскопического доступа такие операции, которые большая часть хирургов выполняет лишь с помощью открытого доступа, например, при резекции крупной кисты с диаметром более 10 см или при нефрэктомии по поводу рака почки.
На моих семинарах, посвященных лапароскопическому лечению опухоли почки, сегодня присутствуют врачи — специалисты крупных научных Центров, больниц республиканского, краевого или областного значения, а также курсанты факультетов постдипломного образования.
За разработку методов лапароскопических операций при хирургическом лечении опухолей почки, а также других органов организма, профессору Константину Викторовичу Пучкову была присвоена одна из наиболее престижных в области хирургии наград — «Золотой лапароскоп».
Послеоперационный период
После выполненной операции на коже живота остаются 3-4 разреза, их длина не более 5 мм, один разрез — 4 см, он служит для извлечения удаленного органа. Вставать и принимать жидкую пищу пациент может уже с первого дня. Клинику больной покидает на 6-8 день. Трудоспособность восстанавливается к 14-21 дню после хирургического вмешательства. В дальнейшем рекомендовано динамическое наблюдение онколога и уролога, УЗИ необходимо пройти спустя 3 и 6 месяцев после проведенной операции.
Важно! При отсутствии метастазирования в удаленных лимфатических узлах у пациентов с раком почки назначения радио- и химиотерапии не требуется. В послеоперационный период пациенты ведут обычный образ жизни.
Вопросы, задаваемые пациентами чаще всего
Нужна ли какая-либо подготовка к лапароскопической операции по поводу рака почки?
Если Вы планируете оперативное лечение рака почки, предлагаю Вам внимательно изучить раздел, который посвящен предоперационной подготовки.
Какой вид анестезии используется при лапароскопической операции при опухоли почек?
Для того, чтобы подробнее узнать о методах обезболивания при лапароскопических вмешательствах при опухоли почки, Вам следует внимательно изучить информацию, размещенную на сайте.
Где можно прооперироваться по поводу опухоли почки?
Первичную консультацию больных с опухолями почек я провожу в Швейцарской университетской клинике. Ознакомьтесь с основными клиническим базами в Москве и в Швейцарии.
Что нужно знать о новообразованиях в матке и яичниках
В женских репродуктивных органах — матке, яичниках и маточных трубах — могут возникать аднексальные (дополнительные) патологии. Это любые объемные новообразования, причины появления которых могут быть как гинекологическими, так и другими.
Для контроля над объемными доброкачественными образованиями достаточно участия семейного врача. Но для медицинской помощи при злокачественном процессе, например, для лечения рака шейки матки, следует обратиться к узкому специалисту.
Каковы симптомы таких нарушений?
Клинические проявления во многом зависят от природы новообразования. Но среди распространенных симптомов можно выделить:
Какие бывают новообразования в области репродуктивных органов?
Как диагностируют такие нарушения?
Врач устанавливает диагноз на основании:
Не все эти новообразования представляют опасность для жизни женщины. Так, например, воспалительные поражения и кисты почти никогда не приводят к развитию рака и нередко требуют лишь консервативного лечения и внимательного врачебного наблюдения.
С другой стороны, крайне важно знать признаки острых гинекологических патологий, которые требуют немедленной медицинской помощи. К ним относятся перекрут яичника и внематочная беременность. Заподозрить последнюю можно, если тест на беременность имеет положительный результат, при этом женщина жалуется на боль в животе или тазовой области и влагалищное кровотечение. Перекрут яичника проявляется внезапной сильной болью на стороне поражения, которая сопровождается тошнотой и рвотой.
Какое лечение требуется при объемных новообразованиях?
Это зависит от характера выявленной дополнительной массы:
1. При внематочной беременности требуется оперативное ее прерывание. Для этого могут быть выбраны следующие способы:
2. Пациенткам с воспалительными заболеваниями органов малого таза потребуются курсы внутривенного введения антибиотиков. Наиболее часто назначают:
В некоторых случаях возможно и амбулаторное лечение с помощью перорального приема доксициклина (вибрамицина) и внутримышечного введения цефтриаксона (роцефина). Возможен другой антибиотик, который относится к цефалоспоринам третьего поколения. Иногда в схему терапии включают и пероральный прием метронидазола. Сегодня воспалительно-инфекционные абсцессы в маточных трубах и яичниках уже не требуют хирургического вмешательства. Срочная операция показана только в случае разрыва капсулы абсцесса, что угрожает развитием обширного перитонита.
3. Об оптимальных способах лечения эндометриомы в медицинском сообществе до сих пор нет единого мнения. Сегодня используются такие подходы, как:
4. Лечение доброкачественных миом заключается в приеме гормональных препаратов и симптоматической терапии нестероидными противовоспалительными средствами. Но при отмене этих назначений чаще всего доброкачественная опухоль продолжает прогрессировать, а риск перехода ее в злокачественную форму возрастает. Поэтому сегодня хирургическое вмешательство представляется наиболее оптимальным методом лечения миом. Впрочем, у него есть один существенный недостаток — иногда вместе с опухолью приходится полностью удалять женские репродуктивные органы. В связи с этим специалисты медицинского центра «Анадолу» начали проводить ультразвуковую абляцию миомы: во многих случаях эта процедура позволяет избавиться от новообразования без операции и с сохранением матки и яичников.
5. Перекрут яичника — это острая гинекологическая патология, при которой единственным способом лечения является немедленная операция. Она призвана предотвратить серьезное повреждение и некроз тканей.
6. Лечение рака яичников, рака шейки матки и других репродуктивных органов женщины может включать хирургические вмешательства, традиционную химиотерапию и таргетную терапию, радиационную терапию. В последнее время в лечении онкогинекологических заболеваний также стал успешно применяться такой новый метод, как «горячая химиотерапия» (НIPEC). Он показывает особенно хорошие результаты при раке яичников. Конкретная схема лечения разрабатывается индивидуально с учетом следующих факторов:
Каковы факторы риска появления объемных новообразований в малом тазу?
Перечень таких факторов зависит от характера новообразования. Так, например, более 80% случаев перекрута яичников возникает у женщин с крупными яичниками (более 5 см). Риск образования миомы возрастает при:
Злокачественные новообразования нередко имеют генетическую предрасположенность, и вероятность их появления возрастает при наличии таких патологий в семье. Кроме того, факторами риска для раковых поражений являются эндометриоз, гормональная терапия в постменопаузе, ожирение, высокий рост, пожилой возраст.
Резюме
Не все объемные новообразования в области малого таза являются злокачественными, и не всегда они нуждаются в немедленном интенсивном лечении. Важную роль здесь играет качественная диагностика, позволяющая выяснить природу такого новообразования и его точную локализацию.
Не стоит также пренебрегать регулярными профилактическими обследованиями у специалистов. Врачи клиники «Анадолу» обладают обширными знаниями в области диагностирования и применяют в своей практике передовые и эффективные методики лечения.
Материал подготовлен по согласованию с врачом «Анадолу» профессором акушером-гинекологом Муратом Деде.
Опухоли средостения: что это такое, классификация.
Опухоли средостения – общее название новообразований, которые расположены в медиастинальном пространстве груди. В 40% случаев диагностирования опухоли являются злокачественными, и тогда ставится диагноз рак средостения. Все опухоли делятся на две большие группы – первичные и вторичные. В первом случае речь идет о тех новообразованиях, которые формируются непосредственно в области средостения, во втором – опухоли образуются сначала в тканях, расположенных вне обозначенной области, а рак средостения развивается уже из метастаз. Иногда опухоли средостения называют рак тимуса, но это не совсем корректное обозначение диагноза. Дело в том, что он обозначает наличие злокачественных клеток в вилочковой железе, тогда как опухоли средостения могут начать свой рост и из других структур.
В зависимости от локализации опухоли различают следующие виды злокачественных новообразований:
Злокачественные новообразования средостения диагностируются чаще всего в возрасте 18-45 лет, какой-то гендерной предрасположенности не отмечается.
Отдельно в медицине рассматриваются мезенхимальные опухоли – представляют собой рак мягких тканей, к таковым относятся липомы и гемангиомы, лейомиосаркомы и фибромы. Поражают разные части средостения, относятся к группе вторичных, потому что «вырастают» из метастаз.
К редким опухолям средостения относятся липо- и фибросаркомы. Их опасность заключается в том, что они долгое время протекают бессимптомно и пациент обращается за помощью к врачу при выраженных нарушениях, когда рак находится уже на 3 и 4 стадии развития. Также к этой группе относится рак тимуса (тимома) – развивается в клетках вилочковой железы.
Какие симптомы укажут на рак средостения?
Рак может протекать в двух стадиях – бессимптомной и с выраженными признаками. Продолжительность прогрессирования опухоли средостения без симптомов зависит от нескольких факторов – место локализации новообразования, уровень общего иммунитета, возраст человека. Часто бессимптомно протекающий рак диагностируется случайно, во время проведения стандартной процедуры флюорографии в рамках диспансеризации.
К основным признакам рака средостения относятся:
Злокачественные опухоли растут достаточно быстро, поэтому переход из бессимптомной стадии в форму с выраженной клинической картиной недолгий. Могут проявляться и дополнительные симптомы типа отечности верхней части туловища и лица, синюшного цвета лица, расширения подкожных вен шеи.
Самым ранним проявлением рака средостения считается болевой синдром, особенно часто он проявляется при раке тимуса. В таком случае боли идентичны приступам стенокардии. Существует и ряд специфичных признаков опухолей средостения:
Общие симптомы, слабовыраженная клиническая картина, многообразие признаков, которые присущи и другим патологиям, делают диагностику только по жалобам пациента и стандартным обследованиям практически невозможной. Кроме этого, опухоли средостения могут быть и доброкачественными – например, рак тимуса по своей клинической картине полностью идентичен признакам доброкачественных новообразований в вилочковой железе.
Диагностика опухоли средостения.
Опухоль средостения может быть диагностирован инструментальными методами, которые являются самыми информативными:
Если перечисленных обследований недостаточно, то назначается хирургическая биопсия. Морфологическое исследование биологического материала позволяет полностью охарактеризовать рак средостения. Эта манипуляция важна для классификации опухоли – будет ли диагностирован именно рак тимуса или опухоль представляет собой доброкачественное образование.
Если есть подозрение на тимому (рак тимуса), то целесообразно проводить ультразвуковое исследование. Оно не выявит опухоль средостения, но даст возможность оценить состояние лимфатических узлов и жировой ткани в подключичной области.
К общим методам диагностики относятся анализы крови (общий, биохимический, коагулограмма), анализ мочи (общий), ЭКГ.
Лечение опухолей средостения.
Самым эффективным методом лечения опухолей средостения считается его хирургическое удаление, которое всегда сопровождается и специфической терапией. Если диагноз был поставлен на ранней стадии, врач может четко определить размер и форму опухоли, то применяется радиохирургический метод ее удаления по системе КиберНож. В случае больших размеров опухоли средостения удаляются классическим хирургическим методом с последующей химиотерапией. Диагностирование рака на поздней стадии делает нецелесообразным оперативное удаление новообразования, поэтому пациенту назначают только поддерживающее лечение (химиотерапия или лучевая) – рак средостения прекращает стремительно разрастаться, снижается вероятность распространения метастаз, облегчается симптоматика.
Если диагностирован рак тимуса (тимома), то врач опирается на данные исследований – каков размер опухоли средостения, есть ли ее разрастание. В некоторых случаях сначала проводится несколько курсов химиотерапии и только после этого назначается хирургическое лечение. Дополнительно, после проведения операции по удалению опухоли средостения, пациенту назначают гормональные препараты, иммуноподдерживающие средства.
Принимать решение о проведении терапевтического лечения или хирургического удаления опухоли средостения может только лечащий врач. Операция выполняется только в том случае, если специалист будет уверен в том, что он сможет удалить сразу все новообразование. Так как диагноз рак средостения часто ставится на поздних стадиях заболевания, то даже хирургические методы могут быть бесполезными по причине распространения метастаз, поражения внутренних органов и мягких тканей вокруг средостения.
Прогноз рака средостения.
Теоретически прогнозы на выздоровление при диагностировании опухоли средостения (рака тимуса) положительные. Но проблема заключается в сложностях диагностики – клиническая картина не типичная для злокачественных образований, часто люди либо предпринимают попытки лечения сами, либо обращаются со стандартными жалобами к врачу и им ставят неверный диагноз. Пока проводится лечение неверного заболевания, время проходит и наступает рак, средостения достигает тяжелой стадии. При своевременном выявлении рака тимуса вероятность благоприятного исхода составляет 68%.
Опухоли средостения (рак тимуса) возможно вылечить, но при условии своевременного выявления. Хирургический метод и последующая химиотерапия дают возможность полностью выздороветь. По причине неспецифической клинической картины диагностирование на ранней стадии затруднено, поэтому важно проходит диспансеризацию – это реальный шанс полностью избавиться от злокачественных образований.
Филиалы и отделения, в которых лечат опухоль средостения (рак тимуса)
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
В Отделе торакоабдоминальной онкохирургии
Заведующий отделом – д.м.н. А.Б. РЯБОВ
В Отделении торакальной хирургии
Контакты: (495) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Заведующий Отделом торакоабдоминальной онкологии – д.м.н. В.Ю. СКОРОПАД