Как защитить желудок от НПВП — советы эксперта
Что вы делаете, когда болит голова, поднялась высокая температура или беспокоит боль в суставах? 90% опрошенных ответят: «Пью таблетку».
«Волшебные» пилюли
Существует группа препаратов, под общим названием нестероидные противовоспалительные (НПВП), которые мы все хотя бы раз в жизни, а многие регулярно, принимали. Это препараты, обладающие обезболивающим противовоспалительным и / или жаропонижающим действием. В качестве примера можно назвать Аспирин, Нурофен, Найс, Кетанов, Кетопрофен и прочие. Учитывая «волшебные эффекты» от их действия — снятие воспаления, боли и жара, — их назначают практически все, всем и всегда. Назначают травматологи, ревматологи, терапевты, лоры, стоматологи. Плюс, их можно совершенно свободно приобрести в любой аптеке. Но, наряду с «волшебными свойствами» эти лекарства обладают рядом побочных действий, которые можно разделить на 2 группы: кардиориски и гастро риски. Собственно о гастрорисках и пойдёт речь в данной статье.
НПВП-гастропатия
В научной литературе эта проблема называется «НПВП-гастропатия». Впервые термин был предложен в 1986 году для разграничения специфического поражения слизистой оболочки желудка, возникающего при длительном употреблении НПВП, от классической язвенной болезни.
Отличие НПВП-гастропатии от язвенной болезни можно проследить и по зоне поражения. Чаще всего язвы можно увидеть в желудке, а не в кишке. Плюс, изменения встречаются чаще у пожилых, а не у молодых людей.
Немного цифр
Немного статистики. В Великобритании назначается около 24 млн. НПВС в год. 70% лиц старше 70 лет принимают НПВС 1 раз в неделю, а 34% ежедневно. В США продается НПВС на сумму до 6 млрд. в год. Как следствие, риск развития желудочно-кишечных кровотечений (ЖКК) возрастает прободения — в 6 раз, риск смерти от осложнений до 8 раз. До всех случаев острых ЖКК связаны с НПВС.
Проблема эта актуальна и в нашей стране, к примеру по данным Научного Центра сердечно-сосудистой хирургии им. А.Н. Бакулева из 240 больных, ежедневно принимающих аспирин даже в малых дозах, на гастроскопии поражения желудка и 12 п.к выявлены у 30% (из них язвы — у 23,6%, эрозии — у 76,4%). Аналогичная картина у коллег из ВНИИ ревматологии РАМН — у 2126 пациентов, принимающих НПВС без «прикрытия» (защиты) желудка, эрозии и язвы гастродуоденальной зоны найдены в 33,8% случаев. Это очень впечатляющие и драматические цифры осложнений от приема НПВС, учитывая количество употребляющих эти препараты людей в развитых странах.
Как это работает?
Как же действуют эти препараты в наших желудках? Всё очень просто, негативное воздействие реализуется за счёт дисбаланса защитных и агрессивных сил. У нас в желудке существует ряд защитных механизмов, позволяющих противостоять натиску агрессоров. Среди последних:
Защищается желудок за счет мощного слоя слизи и бикарбонатов, которые нейтрализуют кислоту, адекватного кровоснабжения, способности очень быстро регенерировать. Когда мы используем НПВС препараты, баланс сил изменяется в сторону агрессивных механизмов и происходит поражение слизистого и подслизистого слоя желудка и кишки.
Диагностика
Для диагностики подобных изменений используется гастроскопия, являющаяся «золотым стандартом». Интересный факт, дело в том, что порядка 40% больных с эрозивно-язвенными изменениями, принимающих эти препараты длительно (более 6 недель) не ощущают никакого дискомфорта или неприятных, болезненных ощущений. Проблемы с желудком диагностируются лишь при походе к другим врачам, а не к гастроэнтерологу. И, наоборот, у 40% пациентов, на фоне жалоб, которые они предъявляют, ничего не находят.
Что же делать в таком случае?!
Алгоритм действий для пациентов, не имеющих проблем с желудком, и тех, у кого в анамнезе была язвенная болезнь или эрозивные изменения, различен. Для первой группы, при назначении нестероидных противовоспалительных препаратов более, чем на 5 дней, обязательно назначение препаратов из группы ингибиторов протонной помпы (ИПП). Таких как, омепразол, пантопразол, рабепразол и т. д. (на весь курс приема). Для второй группы, любые назначения из группы НПВС, независимо от срока приёма, требуют параллельного назначения ингибиторов протонной помпы. Так же обязателен прием ИПП пациентам, принимающих длительно аспирин.
Мифы, с которыми мы сталкиваемся в ежедневной практике
Миф 1. Использование НПВС препаратов в виде свечей является менее агрессивным для желудка, нежели приём таблеток
Это 100% миф. Патогенное, разрушительное действие лекарства реализуется через кровь, доставляющую его по сосудам в желудок.
Миф 2. В качестве «гастропротекторов» можно использовать лекарства из группы антацидов — Ренни, Маалокс, Фосфалюгель и H2-блокаторы (Ранитидин и Фамотидин)
В данном случае они не эффективны.
Миф 3. Принимать ингибиторы протонной помпы можно нерегулярно
Дело в том, что если пожилому человеку назначили на всю жизнь противовоспалительный препарат, абсолютно бессмысленно назначать гастропротекцию на месяц. В подобных случаях лекарства должны приниматься строго параллельно.
Миф 4. В качестве «гастропротекторов» могут выступать пищевые продукты (кисели и пр.)
Этот миф, как абсолютно фантастический, мы оставим без комментариев.
Как выбрать лекарство
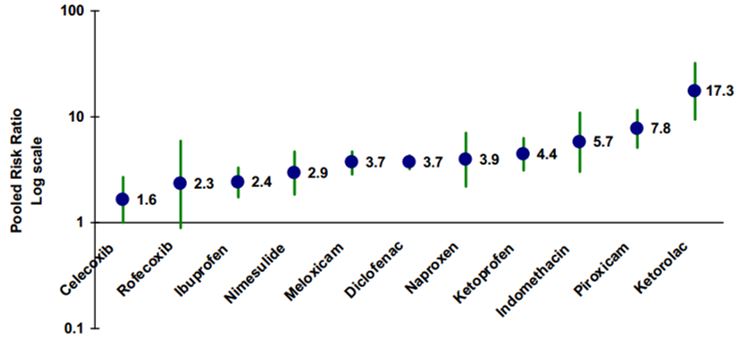
На самом деле, самым важным моментом является то, какие именно лекарства мы принимаем. На рисунке можно увидеть шкалу агрессивности различных препаратов из группы НПВС по отношению к желудку.
Самыми агрессивными препаратами являются Аспирин, Кеторолак, Пироксикам, Индометацин. По возможности рекомендуется использовать селективные препараты, которые обладают минимальными гастро-рисками. Их применение всегда более желательно, к ним относится Целекоксиб и Рофекоксиб. Но несмотря на их относительную безопасность, назначать их должен строго по показаниям лечащий доктор, не забывайте об этом.
Про Helicobacter pylori
Еще одним очень важным компонентом профилактики осложнений, является диагностика инфекции Helicobacter pylori у пациента планирующего длительно принимать НПВС (особенно аcпирин). Наличие бактерии увеличивает риски эрозивно-язвенных поражений ЖКТ и кровотечения в При её выявлении должна в обязательном порядке проводится эрадикация (уничтожение этой бактерии).
Резюме
Итак делаем выводы:
Опыт лечения гастроэзофагеальной рефлюксной болезни
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для
Обеспечение эффективного контроля над желудочной секрецией — одно из главных условий успешной терапии так называемых «кислотозависимых» заболеваний верхних отделов желудочно-кишечного тракта. В клинической и поликлинической практике в настоящее время для ингибирования соляной кислоты париетальными клетками слизистой оболочки желудка чаще всего используются блокаторы Н2-рецепторов гистамина второго (ранитидин) и третьего (фамотидин) поколений, несколько реже — ингибиторы протонного насоса (омепразол, рабепразол), а для нейтрализации уже выделенной в полость желудка соляной кислоты — антацидные препараты. Антацидные препараты иногда применяются в лечении больных, страдающих так называемыми «кислотозависимыми» заболеваниями, в сочетании с Н2-блокаторами рецепторов гистамина; иногда в качестве терапии по «требованию» в сочетании с ингибиторами протонного насоса. Одна или две «разжеванные» антацидные таблетки не оказывают значительного эффекта [10] на фармакокинетику и фармакодинамику фамотидина, применяемого в дозе 20 мг.
Между этими медикаментозными препаратами существуют определенные различия, перечислим основные из них: различные механизмы действия; скорость наступления терапевтического эффекта; продолжительность действия; разная степень эффективности их терапевтического действия в зависимости от времени приема препарата и приема пищи; стоимость медикаментозных препаратов [1]. Вышеперечисленные факторы не всегда учитываются врачами при лечении больных.
В последние годы в литературе все чаще обсуждаются вопросы фармакоэкономической эффективности использования в терапии «кислотозависимых» заболеваний различных медикаментозных препаратов, применяющихся по той или иной схеме [2, 7]. Стоимость обследования и лечения больных особенно важно учитывать в тех случаях, когда больные в силу особенностей заболевания нуждаются в продолжительном лечении [4, 6], например при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Это весьма распространенное заболевание, обследование и лечение таких пациентов требуют значительных расходов.
Как известно, у большей части больных ГЭРБ отсутствуют эндоскопические признаки рефлюкс-эзофагита. Однако по мере прогрессирования ГЭРБ появляются патологические изменения слизистой оболочки пищевода. Симптомы этого заболевания оказывают на качество жизни такое же воздействие, что и симптомы других заболеваний, включая и ишемическую болезнь сердца [5]. Замечено [8] отрицательное воздействие ГЭРБ на качество жизни, особенно на показатели боли, психическое здоровье и социальную функцию. У больных, страдающих ГЭРБ, высок риск появления пищевода Барретта, а затем и аденокарциномы пищевода. Поэтому при первых же клинических симптомах ГЭРБ, особенно при возникновении эндоскопических признаков эзофагита, необходимо уделять достаточное внимание своевременному обследованию и лечению таких больных.
В настоящее время лечение больных ГЭРБ проводится, в частности, препаратом фамотидин (гастросидин) в обычных терапевтических дозировках (по 20 мг или по 40 мг в сутки). Этот препарат обладает рядом достоинств: удобство применения (1-2 раза в сутки), высокая эффективность в терапии «кислотозависимых» заболеваний, в том числе и по сравнению с антацидными препаратами [9], а также большая безопасность по сравнению с циметидином. Однако наблюдения показали [1], что в ряде случаев для повышения эффективности терапии целесообразно увеличение суточной дозы гастросидина, что, по некоторым наблюдениям [1], снижает вероятность появления побочных эффектов по сравнению с использованием в повышенных дозах блокаторов Н2-рецепторов гистамина первого (циметидин) и второго (ранитидин) поколений. Преимущество фамотидина [11] перед циметидином и ранитидином заключается в более продолжительном ингибирующем эффекте на секрецию соляной кислоты обкладочными клетками слизистой оболочки желудка.
Существуют и другие преимущества блокаторов Н2-рецепторов гистамина (ранитидина или фамотидина) перед ингибиторами протонного насоса; в частности, назначение этих препаратов на ночь позволяет эффективно использовать их в лечении больных из-за отсутствия необходимости соблюдать определенную «временную» связь между приемом этих препаратов и пищи. Назначение некоторых ингибиторов протонного насоса на ночь не позволяет использовать их на полную мощность: эффективность ингибиторов протонного насоса снижается, даже если эти препараты приняты больными вечером и за час до приема пищи. Однако суточное мониторирование рН, проведенное у больных, лечившихся омезом (20 мг) или фамотидином (40 мг), свидетельствует [3] о том, что продолжительность действия этих препаратов (соответственно 10,5 ч и 9,4 ч) не перекрывает период ночной секреции, и в утренние часы у значительной части больных вновь наблюдается «закисление» желудка. В связи с этим необходим и утренний прием этих препаратов.
Определенный научно-практический интерес вызывает изучение эффективности и безопасности использования фамотидина и омеза (омепразола) в более высоких дозировках при лечении больных, страдающих «кислотозависимыми» заболеваниями верхних отделов желудочно-кишечного тракта.
Нами изучены результаты клинико-лабораторного и эндоскопического обследования и лечения 30 больных (10 мужчин и 20 женщин), страдающих ГЭРБ в стадии рефлюкс-эзофагита. Возраст больных — от 18 до 65 лет. При поступлении в ЦНИИГ у 30 пациентов выявлены основные клинические симптомы ГЭРБ (изжога, боль за грудиной и/или в эпигастральной области, отрыжка), у 25 больных наблюдались клинические симптомы, в основном ассоциируемые с нарушением моторики верхних отделов желудочно-кишечного тракта (чувство быстрого насыщения, переполнения и растяжения желудка, тяжесть в подложечной области), обычно возникающие во время или после приема пищи. Сочетание тех или иных клинических симптомов, частота и время их возникновения, а также интенсивность и продолжительность у разных больных были различными. Каких-либо существенных отклонений в показателях крови (общий и биохимический анализы), в анализах мочи и кала до начала терапии не отмечено.
При проведении эзофагогастродуоденоскопии (ЭГДС) у 21 больного выявлен рефлюкс-эзофагит (при отсутствии эрозий), в том числе у 4 больных обнаружена рубцово-язвенная деформация луковицы двенадцатиперстной кишки и у одного больного — щелевидная язва луковицы двенадцатиперстной кишки (5 больных страдали язвенной болезнью двенадцатиперстной кишки, сочетающейся с рефлюкс-эзофагитом). Кроме того, у одной больной обнаружена пептическая язва пищевода на фоне рефлюкс-эзофагита и у 8 больных — эрозивный рефлюкс-эзофагит. У всех больных, по данным ЭГДС, обнаружена недостаточность кардии (в сочетании с аксиальной грыжей пищеводного отверстия диафрагмы или без нее).
В лечении таких пациентов использовался гастросидин (фамотидин) в дозировке 40-80 мг в сутки в течение 4 недель (первые 2-2,5 недели лечение проводилось в стационаре ЦНИИГ, в последующие 2 недели пациенты принимали гастросидин в амбулаторно-поликлинических условиях). Терапию гастросидином всегда начинали и продолжали при отсутствии выраженных побочных эффектов, пациентам назначали по 40 мг 2 раза в сутки в течение 4 недель; лишь при появлении диареи и крапивницы дозировку гастросидина уменьшали до 40 мг в сутки.
Исследование было выполнено с учетом критериев включения и исключения больных из исследования согласно правилам клинической практики.
При проведении ЭГДС определяли НР, используя быстрый уреазный тест (один фрагмент антрального отдела желудка в пределах 2-3 см проксимальнее привратника) и гистологическое исследование биопсийного материала (два фрагмента антрального отдела в пределах 2-3 см проксимальнее привратника и один фрагмент тела желудка в пределах 4-5 см проксимальнее угла желудка). При обследовании больных при необходимости проводили УЗИ органов брюшной полости и рентгенологическое исследование желудочно-кишечного тракта. Полученные данные, включая и выявленные побочные эффекты, регистрировали в истории болезни.
В период проведения исследования больные дополнительно не принимали ингибиторы протонного насоса, блокаторы Н2-рецепторов гистамина или другие так называемые «противоульцерогенные» препараты, включая антацидные препараты и средства, содержащие висмут. 25 из 30 пациентов (84%) из-за наличия клинических симптомов, ассоциируемых чаще всего с нарушением моторики верхних отделов пищеварительного тракта, дополнительно получали прокинетики: домперидон (мотилиум) в течение 4 недель или метоклопрамид (церукал) в течение 3-4 недель.
Лечение больных ГЭРБ в стадии рефлюкс-эзофагита всегда начинали с назначения им гастросидина по 40 мг 2 раза в сутки (предполагалось, что в случае появления существенных побочных эффектов доза гастросидина будет уменьшена до 40 мг в сутки). Через 4 недели от начала лечения (с учетом состояния больных) при наличии клинических признаков ГЭРБ и (или) эндоскопических признаков эзофагита терапию продолжали еще в течение 4 недель. Через 4-8 недель по результатам клинико-лабораторного и эндоскопического обследования предполагалось подвести итоги лечения больных ГЭРБ.
При лечении больных гастросидином (фамотидином) учитывались следующие факторы: эффективность гастросидина в подавлении как базальной и ночной, так и стимулированной пищей и пентагастрином секреции соляной кислоты, отсутствие изменений концентрации пролактина в сыворотке крови и антиандрогенных эффектов, отсутствие влияния препарата на метаболизм в печени других лекарственных средств.
По результатам анализа обследования и лечения больных ГЭРБ в стадии рефлюкс-эзофагита в большинстве случаев терапия была признана эффективной. На фоне проводимого лечения у больных ГЭРБ с рефлюкс-эзофагитом (при отсутствии эрозий и пептической язвы пищевода) основные клинические симптомы исчезали в течение 4-12 дней; у пациентов с эрозивным рефлюкс-эзофагитом боль за грудиной постепенно уменьшалась и исчезала на 4-5-й день от начала приема гастросидина; у больной с пептической язвой пищевода на фоне рефлюкс-эзофагита — на 8-й день.
Двое из 30 больных (6,6%) через 2-3 дня от начала лечения отказались от приема гастросидина, с их слов, из-за усиления болей в эпигастральной области и появления тупых болей в левом подреберье, хотя объективно состояние их было вполне удовлетворительным. Эти больные были исключены из исследования.
По данным ЭГДС, через 4 недели лечения у 17 пациентов из 28 (60,7%) исчезли эндоскопические признаки рефлюкс-эзофагита, у 11 — отмечена положительная динамика — уменьшение выраженности эзофагита. Поэтому в дальнейшем этих больных лечили гастросидином в амбулаторно-поликлинических условиях в течение еще 4 недель по 40 мг 2 раза в сутки (7 больных) и по 40 мг 1 раз в сутки (4 больных, у которых ранее была снижена дозировка гастросидина).
Весьма спорным остается вопрос — рассматривать ли рефлюкс-эзофагит, нередко наблюдаемый при язвенной болезни (чаще всего при язвенной болезни двенадцатиперстной кишки), как осложнение этого заболевания или же считать его самостоятельным, сопутствующим язвенной болезни заболеванием? Наш многолетний опыт наблюдений показывает, что, несмотря на некоторую связь ГЭРБ и язвенной болезни (их относительно частое сочетание и даже появление или обострение рефлюкс-эзофагита в результате проведения антихеликобактерной терапии), все же язвенную болезнь и ГЭРБ (в том числе и в стадии рефлюкс-эзофагита) следует считать самостоятельными заболеваниями. Мы неоднократно наблюдали больных с частыми обострениями ГЭРБ в стадии рефлюкс-эзофагита (при наличии у них рубцово-язвенной деформации луковицы двенадцатиперстной кишки). Последнее обострение язвенной болезни (с образованием язвы в луковице двенадцатиперстной кишки) у этих больных отмечалось 6-7 и более лет назад (значительно реже, чем рецидивы ГЭРБ в стадии рефлюкс-эзофагита), однако при очередном обострении язвенной болезни с образованием язвы в луковице двенадцатиперстной кишки всегда при эндоскопическом исследовании выявляли и рефлюкс-эзофагит. Мы уверены, что при наличии современных медикаментозных препаратов лечить неосложненную язвенную болезнь значительно легче, чем ГЭРБ: период терапии при обострении язвенной болезни двенадцатиперстной кишки занимает значительно меньше времени по сравнению с терапией ГЭРБ; да и в период ремиссии этих заболеваний пациенты с язвенной болезнью двенадцатиперстной кишки чувствуют себя более комфортно, в то время как больные ГЭРБ вынуждены для улучшения качества жизни отказываться от приема значительно большего количества продуктов и напитков.
При обследовании (через 8 недель лечения) трое из 11 больных по-прежнему предъявляли жалобы, ассоциированные с нарушением моторики верхних отделов желудочно-кишечного тракта. Трое больных при хорошем самочувствии отказались от проведения контрольной ЭГДС через 8 недель. По данным ЭГДС, у 7 из 8 больных отмечено исчезновение эндоскопических признаков эзофагита (в том числе у одной больной — заживление пептической язвы пищевода).
Определение НР проводилось у всех 30 больных: в 11 случаях выявлена обсемененность НР слизистой оболочки желудка (по данным быстрого уреазного теста и гистологического исследования материалов прицельных гастробиопсий). Антихеликобактерная терапия в период лечения больным ГЭРБ в стадии рефлюкс-эзофагита не проводилась.
При оценке безопасности проведенного лечения каких-либо значимых отклонений в лабораторных показателях крови, мочи и кала отмечено не было. У 4 больных (13,3%), у которых ранее наблюдался «нормальный» (регулярный) стул, на 3-й день лечения гастросидином (в дозе 40 мг 2 раза в сутки) был отмечен, с их слов, «жидкий» стул (кашицеобразный, без патологических примесей), в связи с чем доза гастросидина была уменьшена до 40 мг в сутки. Через 10-12 дней после снижения дозы стул нормализовался без какой-либо дополнительной терапии. Интересно отметить, что еще у 4 больных, которые ранее страдали запорами, на фоне проводимого лечения стул нормализовался на 7-й день. У 3 из 30 больных (10%) на 3-4-й день приема гастросидина появились высыпания на коже туловища и конечностей (крапивница). После уменьшения дозировки гастросидина до 40 мг в сутки и проведения дополнительного лечения диазолином (по 0,1 г 3 раза в день) высыпания на коже исчезли.
Проведенные исследования показали целесообразность и эффективность терапии ГЭРБ в стадии рефлюкс-эзофагита гастросидином по 40 мг 2 раза в сутки, особенно при лечении больных с выраженными болевым синдромом и изжогой. Такое лечение может успешно проводиться в стационарных и амбулаторно-поликлинических условиях. Изучение отдаленных результатов проведенного лечения позволит определить продолжительность периода ремиссии этого заболевания и целесообразность лечения гастросидином в качестве «поддерживающей» терапии или же терапии «по требованию».
По вопросам литературы обращайтесь в редакцию
Топчий Н.В., Топорков А.С. Стратегия выбора ингибитора протонной помпы нового поколения декслансопразола в терапии гастроэзофагеальной рефлюксной болезни // Медицинский совет. 2018. №3. С. 32–41.
Стратегия выбора ингибитора протонной помпы нового поколения декслансопразола в терапии гастроэзофагеальной рефлюксной болезни
Н.В. Топчий, к.м.н., А.С. Топорков, к.м.н.
Российская медицинская академия непрерывного профессионального образования; Ассоциация врачей общей практики (семейных врачей) РФ; Российская гастроэнтерологическая ассоциация, Москва
Гибкость дозирования в сочетании с увеличением продолжительности поддержания терапевтической концентрации в плазме декслансопразола с модифицированным высвобождением и длительным подавлением секреции кислоты после приема препарата позволяет предположить, что декслансопразол обладает рядом преимуществ для пациентов с кислотозависимыми заболеваниями. Фармакокинетический профиль декслансопразола характеризуется наличием двух пиков Тmax через 1–2 и 4–5 ч после приема препарата и обеспечивает устойчивую концентрацию его в крови. Эффективность декслансопразола в рамках терапии различных форм гастроэзофагеальной рефлюксной болезни была подтверждена несколькими рандомизированными контролируемыми клиническими исследованиями.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, ингибиторы протонной помпы, приверженность пациентов терапии, декслансопразол.
The strategy for choosing a new-generation proton pump inhibitor dexlansoprazole in the treatment of gastroesophageal reflux disease
N. V.Topchiy, PhD in medicine, A.S.Toporkov, PhD in medicine
Russian Medical Academy of Continuing Postgraduate Education; Association of General Practitioners (Family Physicians) of the Russian Federation Russian Gastroenterological Association
The flexible dosage form combined with the increased maintenance of a therapeutic dextensoprazole concentration in plasma with a modified release and prolonged inhibition of acid secretion after administration of the drug suggests that dexlansopro-zole has several advantages for patients with acid-dependent diseases. The pharmacokinetic profile of dexlansoprazole is characterized by two Tmax peaks in 1–2 and 4–5 hours after administrating the drug and ensures a stable concentration of it in the blood. The efficacy of dexlansoprozole in the treatment of various forms of gastroesophageal reflux disease has been confirmed by several randomized controlled clinical trials.
Keywords: gastroesophageal reflux disease, proton pump inhibitors, patient adherence to therapy, dexlansoprozole.
Жалобы на диспепсию предъявляют 75% пациентов на приеме у гастроэнтеролога, 25% – на приеме у амбулаторного терапевта или врача общей практики. При этом в термин «диспепсия» врач включает симптомы, вызванные нарушением пищеварения: тошнота, изжога, отрыжка, неприятные ощущения в верхних отделах живота и в нижних отделах грудной клетки, чувство переполнения или тяжести в эпигастрии, метеоризм. К сожалению, не всегда четко пациенты обозначают и разделяют такие термины, как тошнота и рвота. Многие пациенты не могут определить наличие у них изжоги, ссылаясь на отсутствие четких представлений об этом ощущении. Часто вместо изжоги пациенты отмечают наличие регургитации или неприятного, в основном кислого, привкуса во рту. Таким образом, изжога, которая является «визиткой» гастроэзофагеальной рефлюксной болезни (ГЭРБ), далеко не всегда может быть учтена при анкетировании пациентов, что требует от врачей применения во время приема дополнительных целенаправленных вопросов и существенно затрудняет определение истиной частоты ГЭРБ и изжоги в популяции. Кроме того, изучение истиной распространенности
ГЭРБ и изжоги в популяции затруднено из-за отсутствия возможности повсеместного суточного мониторирования рН в амбулаторной практике. Таким образом, истинная распространенность ГЭРБ в несколько раз превышает все данные статистики, что обусловлено высокой вариабельностью симптомов и недостаточной обращаемостью пациентов за медицинской помощью [4]. Однако раннее выявление и адекватная терапия ГЭРБ не только важны для улучшения качества жизни пациента, но и являются важным компонентом канцеропревенции аденокарциномы пищевода, хронизации воспалительных заболеваний верхних и нижних дыхательных путей. Пациенты, страдающие ГЭРБ, имеют более высокий риск развития аденокарциномы желудка по сравнению со здоровыми лицами, причем этот риск возрастает с увеличением частоты и интенсивности симптомов ГЭРБ.
Общепризнанным базисным средством фармакотерапии ГЭРБ являются антисекреторные препараты класса ингибиторов протонной помпы (ИПП). Ингибиторы протонной помпы подавляют секрецию ионов водорода в желудке путем ингибирования фермента (H+, K+)-АТФазы (протонной помпы) на секреторной поверхности париетальных клеток желудка, что приводит к выраженному снижению секреции кислоты в желудке с последующим длительным повышением уровня pH желудка. Кислотосупрессивный эффект ИПП по отношению как к базальной, так и к стимулированной секреции может длиться до 24 ч и более. Показано, что однократный прием ИПП в средней терапевтической дозе приводит к угнетению желудочной кислотопродукции на 80–98%, что существенно больше по сравнению с блокаторами гистаминовых Н2-рецепторов – 4,17. Более высокая эффективность ИПП при терапии ГЭРБ по сравнению с блокаторами гистаминовых Н2-рецепторов была продемонстрирована в ряде клинических исследований и метаанализах [11, 17]. В большинстве случаев применение ИПП эффективно купирует симптомы ГЭРБ, способствует заживлению эро-зивно-язвенных повреждений пищевода и предотвращает осложнения [6, 10, 15]. Однако в ряде случаев встречается рефрактерная ГЭРБ, предположительно обусловленная вариативной эффективностью ИПП для различных пациентов, с эпизодами ночного кислотного прорыва, которые характеризуются снижением интрагастрального рН 80% препарата в крови, характеризуется более низким клиренсом и в пять раз более выраженным системным действием по сравнению с S-энантиомером [16, 33]. Метаболизм лансопразола как рацемата (смесь энантиомеров) происходит под действием как CYP2C19, так и CYP3A4 примерно в равной степени [13]. Для более длительного поддержания концентрации в плазме декслансопразола и продолжительного снижения кислотности желудочного сока была предложена инновационная технология двойного высвобождения активного вещества, которая обеспечивает длительное подавление продукции соляной кислоты в желудке. Такая технология предусматривает наличие гранул с различной растворимостью в зависимости от рН и высвобождение действующего средства сначала в проксимальном отделе тонкого кишечника, а через несколько часов в дистальном. Технология двойного высвобождения декслансопразола обеспечивает существенное увеличение площади под фармако-кинетической кривой и пролонгированное присутствие препарата в плазме крови по сравнению с ИПП с традиционным высвобождением – эзомепразолом (рис. 1 А и Б).
Рис. 1 (А). Технология двойного высвобождения декслансопразола. График зависимости концентрации декслансопразола с модифицированным высвобождением активного вещества от времени характеризуется наличием двух отдельных пиков. Профиль зависимости средней концентрации в плазме от времени (92 здоровых добровольца: 5-й день)
Адаптировано из: 1. Vakily M, et al. Curr Med Res Opin, 2009, 25: 627–38; 2. Wu J, et al. Am J Gastroenterol, 2007,102(Suppl 2): S124).
Рис. 1 (Б). Сывороточная концентрация декслансопразола сохраняется достоверно выше, чем у эзомепразола. График зависимости средней концентрации от времени (44 здоровых добровольца; однократный прием)
Адаптировано из: Kukulka M, et al. Comparator pH study to evaluate the single-dose pharmacodynamics of dual delayed-release dexlansoprazole 60 mg and delayed-release esomeprazole 40 mg. Clin Exp Gastroenterol 2011;4:213–20.
Площадь под фармакокинетической кривой (AUC) коррелирует с продолжительностью антисекреторного эффекта ИПП и отражает количество препарата, достигшего протонной помпы (биодоступность). Фармакокинетический профиль декслансопразола характеризуется наличием двух пиков Тmax через 1–2 и 4–5 ч после приема препарата и обеспечивает устойчивую концентрацию его в крови до 6,4 ч, в то время как традиционная лекарственная форма лансопразола с однократным высвобождением обеспечивает устойчивую концентрацию препарата в крови только до 2,8–3,2 ч [24, 32]. Аналогичные результаты демонстрируются и при сравнении профиля концентрации декслансопразола в крови с эзомепразолом, что позволяет декслансопразолу обеспечивать более длительное снижение кислотной продукции по сравнению с эзомепразолом, особенно ночью, снижая при этом риск ночных кислотных прорывов (рис. 1 б, рис. 2) [4, 9]. Так, в рандомизированном одноцентровом открытом исследовании с перекрестным дизайном и двумя периодами сравнивали фармакодинамические эффекты однократного приема декслансопразола с модифицированным высвобождением 60 мг и эзомепразола 40 мг на 24-часовой профиль рН желудка у здоровых взрослых. В течение 24-часового периода после приема препарата средний процент времени с рН желудка > 4 составил 58% для декслансопразола по сравнению с 48% для эзомепразола; отличия были статистически значимыми (р = 0,003). Также спустя > 12–24 ч после приема препарата средний процент времени с рН желудка > 4 был 60% после приема декслансопразола и 42% после приема эзомепразола, отличия были статистически значимыми (р = 0,001). В течение 0–12 ч после приема препарата средний процент времени с рН > 4 для декслансопразола и эзомепразола составил 56 и 53% соответственно, и отличия не были статистически значимыми. За 24-часовой период после приема препарата средний уровень рН желудка для декслансопразола составил 4,3 по сравнению с 3,7 для эзомепразола, и отличия были статистически значимыми (р 12–24 ч после приема препарата средний уровень рН желудка составил 4,5 для декслансопразола и 3,5 для эзомепразола; отличия были статистически значимыми (р 12–24 ч после приема по сравнению с эзомепразолом. Два ингибитора протонной помпы показали сопоставимую фармакодинамическую активность в течение 0–12 ч после приема. Таким образом, однократный прием декслансопразола с модифицированным высвобождением в дозе 60 мг обеспечивал статистически значимо лучше контроль рН в течение всего 24-часового периода после приема препарата по сравнению с однократной дозой эзомепразола 40 мг. Это отличие было в основном обусловлено статистически значимым большим контролем рН после приема декслансопразола с модифицированным высвобождением по сравнению с эзомепразолом спустя > 12–24 ч после приема препаратов (рис. 2) [21].

Пролонгированный профиль антисекреторного действия декслансопразола позволяет рекомендовать его как эффективное средство терапии при ГЭРБ даже при однократном приеме препарата
Независимо от исходного ИПП, не менее чем у 84% пациентов изжога оставалась хорошо контролируемой после смены терапии. Среди пациентов с ГЭРБ, у которых изжога была хорошо контролируемой на терапии ИПП с приемом два раза в день, подавляющее большинство из них были успешно переведены на однократный прием декслансопразола с модифицированным высвобождением 30 мг. Перевод на терапию декслансопразолом с модифицированным высвобождением 30 мг один раз в день хорошо переносился и не вызывал каких-либо серьезных нежелательных явлений, связанных с лечением. Понижающую терапию при ведении пациентов с ГЭРБ, достигших хорошего контроля изжоги на режиме приема ИПП два раза в день, авторы рассматривали как возможность сократить расходы, возможно, улучшить приверженность терапии и снизить риск побочных эффектов, связанных с применением высоких доз ИПП [16]. С учетом факта снижения приверженности к терапии и досрочного ее прекращения при приеме ИПП два раза в день, прием декслансопразола один раз в день может способствовать улучшению комплаенса [4].
Применение декслансопразола обеспечивает эффективный контроль над изжогой в течение суток, полное и стойкое заживление эрозий и язв (в 92–93% случаев) в 8-й нед. терапии и поддержание длительной стойкой ремиссии эрозивного эзофагита
За счет поддержания рН в среднем более 4 в течение суток Дексилант® уменьшает нарушения сна у пациентов с клиническими проявлениями ГЭРБ
Рис. 4. Частота нарушений сна у пациентов с клиническими проявлениями ГЭРБ через 4 нед. терапии (n = 305)
Если удается поддерживать внутрипищеводный рН более 4 в течение 16–22 часов в сутки, заживление эрозий пищевода происходит почти в 100% случаев. Увеличение продолжительности времени в течение суток, когда интрапищеводный pH более 4, означает повышение вероятности выздоровления дополнительного количества пациентов.
Рис. 5. Правило Белла – заживление эрозий при эзофагите прямо зависит от значений интрагастрального рH в течение суток
Адаптировано из: Bell NJ, Burget D, Howden CW, et al.Digestion. 1992; 51(Suppl 1):59-67; Sharma P, et al. Aliment Pharmacol Ther 2009;29:731–41; Kukulka M, et al. Clin Exp Gastroenterol 2011;4:213-20.
Следует помнить об осторожности при назначении препаратов любых классов, в том числе и ИПП, хотя побочные эффекты, связанные с приемом ИПП, до конца не уточнены. При этом, например, анализ врачебных назначений в Дании показал частую необоснованность ИПП и отсутствие соответствующих показаний в медицинской документации. ИПП должны назначаться при наличии показаний, в индивидуальной, но рекомендованной дозе, на протяжении отрезка времени, рекомендованного для конкретного заболевания, но индивидуально для каждого пациента. В режиме безрецептурного отпуска, т.е. приема не более 2 нед, для купирования изжоги, возникающей два раза в неделю, ИПП, в частности декслансопразол, рассматриваются как самый безопасный класс препаратов [2, 18, 26]. Гибкость режима приема может способствовать повышению удобства для пациента и увеличению его приверженности терапии. Гибкость дозирования в сочетании с увеличением продолжительности поддержания терапевтической концентрации препарата в плазме и длительным подавлением секреции кислоты после приема декслансопразола с модифицированным высвобождением позволяет предположить, что этот ИПП обладает дополнительными преимуществами для пациентов с кислотозависимыми заболеваниями. Пробелы в знаниях врачей в отношении применения ИПП относительно приема пищи приводят к формированию пробелов в знаниях пациентов, и в результате большая часть пациентов получает рекомендации, не соответствующие инструкции по применению ИПП [30]. Понимание пробелов в знаниях врача и пациента может иметь ключевое значение для принятия необходимых мер, направленных на получение больным правильных рекомендаций, с целью улучшения приверженности специфическим инструкциям по приему препарата, достижения положительного исхода терапии.