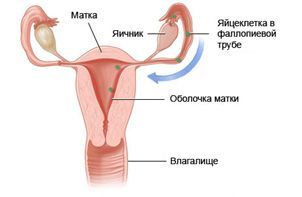
Нейроэндокринные синдромы
Работа женской репродуктивной системы регулируется двумя железами, расположенными в головном мозге: гипоталамусом и гипофизом. Они выделяют гормоны, которые оказывают влияние на половые железы, заставляя их работать более или менее интенсивно.
Патологические состояния, обусловленные нарушением функции гипофиза и гипоталамуса, называют нейроэндокринными синдромами.
Основные нейроэндокринные синдромы:
Предменструальный синдром
Предменструальный синдром представляет собой совокупность психологических, нервных и эндокринных нарушений, которые возникают перед месячными и проходят или уменьшаются во время менструации. Синдром встречается примерно у 2 – 30% женщин репродуктивного возраста. Тяжелее всего протекает после 35 лет.
Симптомы очень разнообразны.
Климактерический синдром
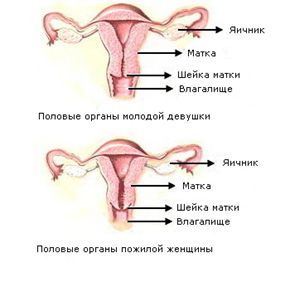
Климактерический синдром – это симптомокомплекс, возникающий в связи с прекращением менструаций. Как правило, развивается у женщин в возрасте 48 – 50 лет. Основная причина – возрастная перестройка гормональной системы, переход от репродуктивного к старческому возрасту.
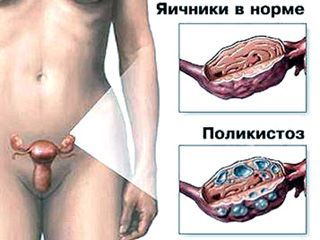
Синдром поликистозных яичников
Синдром поликистозных яичников – патологическое состояние, при котором в организме женщины вырабатывается повышенное количество мужских половых гормонов – андрогенов.
Основными симптомами заболевания являются: аменорея (отсутствие месячных), бесплодие, повышенное оволосение (по мужскому типу), ожирение.
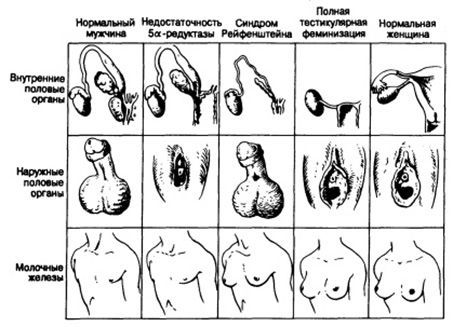
Адреногенитальный синдром
Адреногенитальный синдром возникает вследствие нарушения функции надпочечников и проявляется в виде вирилизации – развития мужских признаков.
Посткастрационный синдром
Возникает после операции удаления яичников (кастрации). При этом в организме полностью прекращается выработка женских половых гормонов – эстрогенов.
Нейроэндокринные опухоли
Нейроэндокринные опухоли – гетерогенная группа эпителиальных новообразований, происходящих из клеток APUD-системы. У большинства больных нейроэндокринными опухолями развивается карциноидный синдром, включающий в себя приливы, боли в животе, диарею, нарушения дыхания, поражение сердечных клапанов и телеангиэктазии. Возможны также гипогликемия, чувство голода, расстройства сознания, судороги, пептические язвы, похудание, диабет, дерматит, тромбозы и тромбоэмболии. Диагноз выставляется с учетом симптомов, данных лабораторных и инструментальных исследований. Лечение – операция, химиотерапия, симптоматическая терапия.
Общие сведения
Нейроэндокринные опухоли (НЭО) – группа новообразований различной степени злокачественности, происходящих из клеток диффузной нейроэндокринной системы, способных продуцировать пептидные гормоны и биогенные амины. Нейроэндокринные опухоли относятся к числу редко встречающихся онкологических заболеваний. Обычно поражают пищеварительную и дыхательную системы, но могут выявляться и в других органах. Возникают спорадически или являются следствием одного из нескольких наследственных синдромов, сопровождающихся развитием множественных нейроэндокринных опухолей в различных органах.
Статистические показатели заболеваемости составляют 2-3 человека на 100 тыс. населения, однако специалисты указывают на то, что в процессе аутопсии нейроэндокринные опухоли обнаруживаются у 8-9 человек на 100 тыс. населения, что свидетельствует о низком уровне прижизненной диагностики. Обычно выявляются у взрослых, мужчины страдают чаще женщин. Лечение осуществляют специалисты в сфере онкологии, гастроэнтерологии, пульмонологии, эндокринологии и других областей медицины (в зависимости от локализации новообразования).
Классификация нейроэндокринных опухолей
С учетом особенностей эмбриогенеза различают три группы нейроэндокринных опухолей:
С учетом локализации выделяют бронхопульмональные нейроэндокринные опухоли и новообразования пищеварительной системы. НЭО бронхов и легких составляют около 3% от всех онкологических заболеваний дыхательной системы и примерно 25% от общего количества нейроэндокринных опухолей. НЭО пищеварительной системы составляют около 2% от всех онкологических процессов данной локализации и более 60% от общего числа нейроэндокринных опухолей. Поражения пищеварительной системы, в свою очередь, подразделяются на эндокринные карциномы (устаревшее название – карциноиды) и другие новообразования (инсулиномы, випомы, глюкагономы, соматостатиномы, гастриномы). Эндокринные карциномы чаще всего встречаются в аппендиксе и тонкой кишке, другие неоплазмы – в поджелудочной железе.
В отдельных случаях нейроэндокринные опухоли образуются из клеток, являющихся производными эндодермы, нейроэктодермы и эмбрионального нервного гребешка, и локализуются в передней доле гипофиза, щитовидной железе, паращитовидных железах, надпочечниках, предстательной железе, молочной железе, почках, коже или яичниках. Нейроэндокринные опухоли, расположенные за пределами дыхательной системы и желудочно-кишечного тракта, составляют около 15% от общего количества новообразований данной группы.
Согласно классификации ВОЗ, все нейроэндокринные опухоли пищеварительной системы вне зависимости от их вида и локализации подразделяются на три категории:
В отличие от новообразований ЖКТ, нейроэндокринные опухоли дыхательной системы сохранили старое название карциноид. В соответствии с классификацией ВОЗ выделяют четыре категории таких неоплазий:
Наряду с перечисленными «обобщенными» классификациями существуют классификации ВОЗ для нейроэндокринных опухолей различной локализации, созданные с учетом диаметра первичного новообразования, глубины прорастания подлежащих тканей, степени вовлечения нервов, лимфатических и кровеносных сосудов, наличия или отсутствия метастазов и некоторых других факторов, оказывающих влияние на течение и прогноз заболевания.
Симптомы нейроэндокринных опухолей
Нейроэндокринные опухоли ЖКТ
Нейроэндокринные опухоли ЖКТ (эндокринные карциномы, карциноидные опухоли ЖКТ) чаще всего выявляются в области червеобразного отростка. Второе место по распространенности занимают неоплазии тонкого кишечника. Нейроэндокринные опухоли толстого кишечника и прямой кишки составляют 1-2% от общего количества онкологических процессов этой анатомической зоны. Новообразования желудка и двенадцатиперстной кишки встречаются относительно редко. У 10% пациентов выявляется генетическая предрасположенность к возникновению множественных нейроэндокринных опухолей.
Все эндокринные карциномы выделяют пептиды и биогенные амины, однако перечень биологически активных соединений и уровень активности секреторных клеток новообразований может существенно варьировать, что обуславливает возможные различия в клинической картине заболевания. Наиболее характерным признаком нейроэндокринных опухолей ЖКТ является карциноидный синдром, обычно возникающий после появления метастазов в печени, сопровождающийся приливами, диареей и болями в животе. Реже при данном синдроме встречаются поражения сердечных клапанов, расстройства дыхания и телеангиэктазии.
Приливы наблюдаются у 90% пациентов с нейроэндокринными опухолями. В качестве основной причины развития приступов рассматривают выброс в кровь большого количества серотонина, простагландинов и тахикининов. Приливы развиваются спонтанно, на фоне употребления алкоголя, эмоционального напряжения или физической нагрузки и длятся от нескольких минут до нескольких часов. Во время приливов у пациентов с нейроэндокринными опухолями выявляется гиперемия лица или верхней половины туловища в сочетании с гипотонией (редко – гипертонией), тахикардией и головокружением.
Диарея может отмечаться как на фоне приступов, так и в их отсутствие и выявляется у 75% больных нейроэндокринными опухолями. Поражение сердечных клапанов развивается постепенно, встречается у 45% пациентов. Патология обусловлена фиброзом сердца, возникающим в результате длительного воздействия серотонина. У 5% пациентов с карциноидным синдромом наблюдается пеллагра, проявляющаяся слабостью, нарушениями сна, повышенной агрессивностью, невритом, дерматитом, глосситом, фотодерматозом, кардиомиопатией и когнитивными расстройствами.
У 5% больных нейроэндокринными опухолями отмечается атипичное течение карциноидного синдрома, обусловленного выбросом в кровь гистамина и 5-гидрокситриптофана. Обычно этот вариант выявляется при НЭО желудка и верхней части двенадцатиперстной кишки. Атипичный карциноидный синдром при нейроэндокринных опухолях проявляется головной болью, приливами, бронхоспазмом и слезотечением. Во время приливов выявляется непродолжительная гиперемия лица и верхней половины туловища, сопровождающаяся жаром, потливостью и кожным зудом. По окончании приливов в области покраснения образуются многочисленные телеангиэктазии.
Опасным осложнением нейроэндокринных опухолей является карциноидный криз. Обычно такой криз развивается на фоне хирургического вмешательства, инвазивной процедуры (например, биопсии) или сильного стресса, но может возникать и без видимых внешних причин. Состояние сопровождается резким падением артериального давления, выраженной тахикардией и сильным брохноспазмом. Представляет опасность для жизни, требует проведения неотложных лечебных мероприятий.
Другие нейроэндокринные опухоли
Инсулиномы – нейроэндокринные опухоли, в 99% случаев возникающие в тканях поджелудочной железы, в 1% случаев – в области двенадцатиперстной кишки. Как правило, протекают доброкачественно, обычно бывают одиночными, реже – множественными. Женщины страдают чаще мужчин. У 5% больных нейроэндокринные опухоли развиваются на фоне генетических нарушений. Проявляются гипогликемией, чувством голода, нарушениями зрения, спутанностью сознания, гипергидрозом и дрожанием конечностей. Возможны судороги.
Випомы – нейроэндокринные опухоли, обычно возникающие в поджелудочной железе, реже – в легких, надпочечниках, тонкой кишке или средостении. Панкреатические нейроэндокринные опухоли, как правило, протекают злокачественно, внепанкреатические – доброкачественно. Наследственная предрасположенность выявляется у 6% больных. Основным симптомом нейроэндокринной опухоли являются опасные для жизни, изнуряющие хронические поносы, вызывающие нарушения водно-электролитного баланса с развитием судорог и сердечно-сосудистых расстройств. Среди других проявлений болезни – гиперемия верхней половины тела и гипергликемия.
Глюкагономы – нейроэндокринные опухоли, всегда локализующиеся в поджелудочной железе. В 80% случаев протекают злокачественно, обычно метастазируют в печень, реже – в лимфоузлы, яичники и позвоночник. Возможна диссеминация брюшины. Средний размер нейроэндокринной опухоли на момент постановки диагноза составляет 5-10 см, у 80% больных при первичном обращении выявляются метастазы в печени. Глюкагономы проявляются снижением веса, диабетом, расстройствами стула, стоматитом и дерматитом. Возможны тромбозы, тромбоэмболии и психические нарушения.
Диагностика и лечение нейроэндокринных опухолей
Диагноз устанавливается на основании клинических симптомов, результатов лабораторных и инструментальных исследований. При эндокринных карциномах определяют уровень серотонина в крови и 5-ГИУК в моче. При инсуломах проводят исследование крови на содержание глюкозы, инсулина, проинсулина и С-пептида. При глюкагономах выполняют анализ крови на глюкоген, при випомах – на вазоактивный интестинальный пептид, при гастриномах – на гастрин. Кроме того, план обследования больных с подозрением на нейроэндокринную опухоль включает в себя УЗИ органов брюшной полости, КТ и МРТ органов брюшной полости, ПЭТ, сцинтиграфию и эндоскопические исследования. При подозрении на злокачественный характер опухоли осуществляют биопсию.
Радикальным методом лечения нейроэндокринной опухоли является ее оперативное иссечение в пределах здоровых тканей. Из-за множественности новообразований, затруднений при определении расположения небольших узлов и высокой частоты метастазирования полное удаление нейроэндокринных опухолей у значительной части больных не представляется возможным. Для уменьшения клинических проявлений заболевания назначают симптоматическое лечение с использованием октреотида и других аналогов соматостатина. При быстром росте злокачественных новообразований показана химиотерапия.
Прогноз при нейроэндокринных опухолях
Прогноз зависит от типа, степени злокачественности и распространенности неоплазии. Средняя пятилетняя выживаемость больных эндокринной карциномой составляет 50%. У пациентов с карциноидным синдромом этот показатель снижается до 30-47%. При гастриноме без метастазов до пяти лет с момента постановки диагноза удается дожить 51% больных. При наличии метастазов пятилетняя выживаемость пациентов с такой нейроэндокринной опухолью снижается до 30%. Прогноз при глюкагономе неблагоприятен, однако средние показатели выживаемости точно не установлены из-за редкой встречаемости данного типа нейроэндокринной опухоли.
Эндокринная система. Норма и патология
Эндокринная система как явление природы
Эндокринная система, она же система нейрогуморальной регуляции (досл. «нервно-жидкостного управления»), чрезвычайно сложна. Ее структура, состав и функционирование находятся, по всей видимости, на пределе того, что в принципе может исследовать и постичь современная наука, вооруженная могучим (как ей кажется) инструментальным, лабораторно-аналитическим и вычислительным арсеналом. Целый раздел медицины, называемый эндокринологией, занимается изучением этой системы, ее нормальной работы, различных ее дисфункций и заболеваний, а также способов лечения последних. Целый сектор фармакологии занят разработкой, синтезом и совершенствованием т.н. гормонсодержащих препаратов; несмотря на хроническую проблему побочных эффектов, обойтись без этой группы лекарственных средств сегодня уже невозможно.
Относящиеся к эндокринной системе органы (железы), ткани или клетки определенного типа, – к примеру, клетки Кульчицкого в слизистой кишечника, – вырабатывают особые органические соединения, которые обычно называют биоактивными регуляторами, нейромедиаторами, сигнальными биохимическими веществами, но чаще всего просто гормонами. Это слово в переводе с греческого означает «возбуждать», «побуждать» или, более современным языком, «активировать». Гормоны поступают непосредственно в кровоток; малейшие колебания их концентрации в живых тканях улавливаются специфическими клетками-рецепторами, чувствительными к той или иной группе гормонов и способными реагировать на гормональные «команды», – например, повышением температуры тела, снижением кровяного давления в сосудах, интенсивным лактогенезом в молочных железах, и мн.др. Таким способом запускаются, форсируются, тормозятся или полностью подавляются, – словом, контролируются, – практически все физиологические и психические процессы в организме. При этом каждая железа секретирует, как правило, несколько гормонов, а каждый гормон в свою очередь влияет на несколько взаимосвязанных процессов.
Синонимический термин «нейрогуморальная регуляция» не случайно содержит корень «нейро-». Согласно современным представлениям, эндокринная система играет важнейшую, исключительную роль в жизнедеятельности организма, но все же не является по отношению к нему «верховной властью». Иерархическое главенство принадлежит центральной нервной системе (ЦНС), т.е. головному и спинному мозгу. Гормоны отвечают за всё, однако секреторной активностью самих эндокринных желез управляют особые церебральные образования и придатки, – прежде всего, связка гипоталамус-гипофиз в нижней области головного мозга, в т.н. промежуточном мозге, – используя для этого сигнальные электрохимические импульсы и целую паутину нейронных каналов связи (в IT такую внутреннюю сеть назвали бы интранетом). Учитывая сказанное, эндокринологию сегодня все чаще отождествляют с нейроэндокринологией (которая полвека назад считалась отдельным направлением), а группу расстройств, ранее традиционно называемых гормональными, интерпретируют как нейроэндокринные заболевания или дисфункции.
Трудно сказать, почему у эволюционирующих млекопитающих возникла столь сложная, многоступенчатая и многоэлементная нейроэндокринная система. Как известно, природа больше всего заботится о целесообразности, и меньше всего – о том, чтобы человеку было удобно ее изучать. Возможных путей и вариантов у природы всегда очень много; скорее всего, бесконечно много. Регулировать жизнедеятельность высших организмов наверняка можно было бы как-нибудь иначе, и желательно – попроще. Однако нельзя отрицать следующее. Человек современный, разумный и технологический, пока еще очень далек от создания искусственной системы, подобной ему самому, – системы столь же компактной, энергетически экономной и эффективной, обладающей сразу пятью автономными сенсорными блоками и двумя универсальными манипуляторами; системы, оптимально сочетающей силу, гибкость и подвижность, безусловные и условные рефлексы, сознание и бессознательное; вдобавок системы самовоспроизводящейся, в какой-то степени самообучающейся и, главное, сохраняющей гомеостаз (постоянство внутренних условий), т.е. самонастраивающейся практически под любые внешние условия. Поэтому сегодня нам остается только восхититься, поблагодарить природу за нашу удивительную эндокринную систему – и продолжить упорное исследование ее бесчисленных загадок.
Основные эндокринные железы
Нередко можно встретить выражение «главная эндокринная железа», причем в разных источниках эта роль отводится то гипофизу, то гипоталамусу. Никто не знает, какие открытия будут сделаны завтра, поэтому ограничимся осторожным повторением вышесказанного: насколько нам известно сегодня, активность нейроэндокринной системы (по крайней мере, большинства желез внутренней секреции) контролируется парой гипоталамус-гипофиз. Кроме того, к важнейшим функциям гипофиза относится продукция соматотропного гормона, регулирующего процессы роста и формирования организма.
Эпифиз (шишковидное тело головного мозга) один из центральных нейроэндокринных регуляторов. Является своеобразным тормозом или ограничителем, который блокирует чрезмерный «разгон» эндокринных желез. В частности, нормализует секрецию соматотропина и половых гормонов, предотвращает опухолевые процессы.
Щитовидная железа участвует в регуляции метаболизма, прежде всего усвоения йода и кальция; влияет на многие зависимые системы и процессы (от общего энергообмена и интеллектуальной продуктивности до регенерации тканей опорно-двигательного аппарата).
Паращитовидные (околощитовидные) железы регулируют состояние костных и мышечных тканей, внутриглазных структур, почек.
Надпочечники вырабатывают, по современным данным, около полусотни сигнальных веществ. Наиболее известные и изученные функции – обеспечение водно-солевого, углеводного, минерального, белкового обмена, продукция мужских и женских половых гормонов (наряду с половыми железами-гонадами). Знаменитые глюкокортикостероидные гормоны, вырабатываемые корой надпочечников, не являются, конечно, панацеей и могут приводить к многочисленным нежелательным эффектам (особенно при пероральном приеме), однако зачастую оказываются единственным «спасательным кругом» благодаря выраженному противовоспалительному, антиаллергическому, иммуномодулирующему, противошоковому и антистрессовому действию. Не менее известны такие биорегуляторы, как адреналин и норадреналин (катехоламиновые гормоны, продуцируемые мозговым веществом надпочечников).
Параганглии особые скопления клеток, которые с полным правом можно назвать нейроэндокринными: отвечают за чувствительность, регулируют обмен хрома и одновременно секретируют катехоламины, подобно надпочечникам.
Поджелудочная железа функционально относится к пищеварительной системе, однако содержит незначительный (1-3% от массы железы) объем эндокринных клеток, сконцентрированных в т.н. островках Лангерганса и продуцирующих инсулин – гормон-регулятор уровня глюкозы в крови.
Яички (у мужчин), яичники (у женщин) – секретируют половые гормоны (андрогены и эстрогены). Эндокринную роль выполняет также плацента при вынашивании беременности.
Вилочковая железа (тимус) производит, в основном, иммунорегулирующие гормоны.
Следует отметить, что к настоящему времени известны далеко не все функции эндокринных желез и вырабатываемых ими гормонов; здесь приводятся лишь наиболее важные и исследованные из них.
Наиболее распространенные эндокринные заболевания
Количество самостоятельных болезней и синдромов, связанных с нарушениями гормонального баланса, сегодня оценивается на уровне примерно шести тысяч. Иными словами, большинство известных современной медицине болезней (около десяти тысяч) действительно являются гормональными. Некоторые из них сегодня грозят приобрести пандемический характер, другие встречаются спорадически редко; одни являются врожденными и генетически обусловленными, другие приобретаются в течение жизни под действием многочисленных этиопатогенетических факторов (травмы, опухоли, воспаления и т.д.).
Наиболее распространенным и известным эндокринно-метаболическим заболеванием следует, по-видимому, считать сахарный диабет. Очень распространена также патология щитовидной железы, в частности, эндемичные йододефицитные состояния, гипертиреоз, тиреоидит и мн. др. Выраженное негативное влияние на весь организм, его формирование, строение, внешний облик, функционирование, – оказывают аномалии и поражения желез, продуцирующих половые гормоны, кортикоиды, соматотропин. Даже известный предменструальный синдром у женщин представляет собой не что иное, как транзиторный, циклически повторяющийся и преходящий гормональный дисбаланс.
В целом, эндокринологии приходится мыслить воистину глобально и системно, имея дело с огромным количеством перекрестно-связанных процессов, нормальных и патологических. Однако заболевания этой группы, некогда бывшие совершенно непостижимыми, в настоящее время успешно диагностируются и лечатся. Важно лишь обратиться к врачу вовремя, – то есть как можно раньше, – пока изменения не приобрели необратимый характер.
Нейроэндокринная система что это такое простыми словами
ФГБУ «Эндокринологический научный центр» МЗ РФ, Москва
Организация и функционирование нейроэндокринной системы
Журнал: Проблемы эндокринологии. 2013;59(1): 62-69
Бабичев В. Н. Организация и функционирование нейроэндокринной системы. Проблемы эндокринологии. 2013;59(1):62-69.
Babichev V N. Organization and functioning of the neuroendocrine system. Problemy Endokrinologii. 2013;59(1):62-69.
ФГБУ «Эндокринологический научный центр» МЗ РФ, Москва
Достижения нейроэндокринологии в последние годы дали возможность сформулировать цельное представление о системном подходе к лечению эндокринных заболеваний. В обзоре приведены экспериментальные и клинические доказательства присутствия в гипоталамусе специфических рецепторов к гормонам периферических эндокринных желез и тропным гипофизарным гормонам. Продукция гипоталамусом специфических веществ (рилизинг-гормонов) обеспечивает связь нервных и эндокринных структур. Прямые и обратные связи в организме способствуют устойчивой работе всех систем организма.
ФГБУ «Эндокринологический научный центр» МЗ РФ, Москва
Эндокринная система вместе с нервной составляет единое целое. Объединяющим и координирующим центром нейроэндокринной системы является область промежуточного мозга — гипоталамус, который не только проводит нервные импульсы, но и секретирует различные физиологические вещества [1].
Гипоталамус расположен на основании мозга и ограничен спереди перекрестом зрительных нервов, сзади — маммилярными телами, по бокам — расходящимися трактами зрительных нервов. Сверху в гипоталамическую область внедряется третий желудочек мозга, превращая гипоталамус в парный орган с симметричным расположением клеточных образований. В основании гипоталамуса располагается срединное возвышение, переходящее в ножку гипофиза.
Эндокринные функции гипоталамуса осуществляют преимущественно его передняя и медиальная части. Нервные клетки гипоталамуса группируются в многочисленные ядра, часть которых обладает секреторными свойствами. Крупноклеточные ядра переднего гипоталамуса (супраоптические и паравентрикулярные) связаны нервными волокнами с задней долей гипофиза. Многочисленные ядра медиобазального и части заднего гипоталамуса, часть паравентрикулярных, вентромедиальные и аркуатные — продуцируют нейросекрет в систему воротных вен гипофиза. Многочисленные комиссуральные пути гипоталамуса обеспечивают взаимодействие между нейроэндокринными ядрами. Нервные клетки паравентрикулярных и аркуатных ядер имеют многочисленные контакты с вышележащими структурами ЦНС.
Роль гипоталамуса в регуляции эндокринных функций была выяснена в 1955 г. Гиллемин впервые показал, что гипоталамический экстракт при введении его животным стимулирует секрецию гипофизом АКТГ. В 60-х годах XX века интенсивно исследовали влияние экстрактов гипоталамуса и срединного возвышения на секрецию гипофизом гормона роста (соматотропин, СТГ) и тиреотропного гормона (тиреотропин, ТТГ). Благодаря достижениям аналитической химии пептидов, разработке радиоиммунологических методов определения гормонов, развитию техники культивирования клеток сделан революционный скачок в исследованиях гипоталамической регуляции функций эндокринной системы.
Наличие в гипоталамусе специфических рецепторов к периферическим гормонам эндокринных желез и тропным гипофизарным гормонам определяет его особое положение в системах обратной связи. В гипоталамусе происходит переключение информации с нервно-медиаторного на нейрогормональный путь, которой составляют либерины и статины: кортиколиберин (АКТГ-рилизинг гормон, КРГ), люлиберин (гонадолиберин, ЛГ/ФСГ-рилизинг-гормон, ГнРГ), тиролиберин (ТРГ), соматолиберин (РГГР), соматостатин, меланолиберин, а также дофамин (ДА) и энкефалины, оказывающие влияние на функции гипофиза.
Гипоталамус является высшим вегетативным центром, осуществляющим сложную интеграцию и различных внутренних систем. В организме нет ни одной функции, к регуляции которой гипоталамус не имел бы отношения: он играет существенную роль в поддержании оптимального уровня обмена веществ (белкового, углеводного, жирового, водного и минерального) и энергии, в регуляции температурного баланса организма, деятельности пищеварительной, сердечно-сосудистой, выделительной, дыхательной и эндокринной систем.
Нейроэндокринологи имеют полное право рассматривать гипоталамус как главный нейроэндокринный орган, который осуществляет взаимосвязь между ЦНС и железами внутренней секреции. Он является интегрирующим звеном, пультом управления, на котором замыкаются все пути между ЦНС и эндокринной системой. Естественно, возникает вопрос, каким образом маленькая структура промежуточного мозга справляется со столь многочисленными функциями.
Для эндокринологов, в первую очередь, важен вопрос о регуляции гормональной системы.
Связь между гипофизом, который является основным продуцентом всех тропных гормонов (АКТГ, ТТГ, ЛГ, ФСГ, СТГ, пролактин) и гипоталамусом осуществляется через портальную систему сосудов, а также через гипоталамо-гипофизарный тракт — самый короткий, но хорошо очерченный пучок аксонов нейронов гипоталамуса. Волокна их берут начало в супраоптическом и паравентрикулярных ядрах и проходят через гипофизарную ножку к нейрогипофизу.
Биохимиками было показано существование в гипоталамусе специфических веществ, которые синтезируются нервными клетками и освобождаются в капилляры портальной системы, достигая передней доли гипофиза. На сегодняшний день выделено и охарактеризовано более 10 гипоталамических нейрогормонов, каждый из которых обладает специфическим влиянием (стимуляцией или торможением) секреции того или иного тропного гормона гипофиза. Такие соединения получили название ингибирующих и рилизинг-гормонов (либерины и статины), обладающие высокой специфичностью действия и чрезвычайно высокой биологической активностью. Установлена и подтверждена химическим синтезом их структура.
Основной точкой приложения гипоталамических рилизинг-гормонов являются клетки гипофиза, и некоторое время считалось, что каждый гормон стимулирует один тип клеток аденогипофиза, который в свою очередь синтезирует лишь один тропный гормон.
В дальнейшем было показано, что в ряде случаев гипоталамические гормоны стимулируют секрецию нескольких гипофизарных гормонов. Например, ТРГ усиливает выделение и ТТГ, и ПРЛ. ГнРГ способствует секреции ЛГ и ФСГ; соматостатин угнетает секрецию и гормона роста, и ТТГ. Каждый клеточный элемент аденогипофиза подвергается действию многих регуляторных факторов, и клетки в аденогипофизе не строго специализированы: в одной клетке могут синтезироваться несколько гормонов, например ЛГ и ФСГ, АКТГ и β-липотропин, СТГ и ПРЛ, но не ТТГ или ЛГ. Бифункциональность некоторых гормонов объясняется по-разному. Способность ГнРГ вызывать секрецию как ЛГ, так и ФСГ, причем несовпадающую по времени, определяется разной чувствительностью гонадотрофов, секретирующих ЛГ или ФСГ, а также длительностью воздействия с учетом влияния половых стероидов на гипофизарные клетки в разные стадии полового цикла. Большие концентрации эстрогенов в плазме, предшествующие овуляторному выбросу ЛГ, увеличивают чувствительность гипофиза к ГнРГ, а минимальные количества эстрогенов и прогестерона, секретируемого после овуляции, напротив, снижают эту чувствительность. Секреция ФСГ более чувствительна к ингибирующему эффекту эстрогенов. Нельзя исключить наличие в аденогипофизе и двух видов рецепторов. Одни из них характеризуются высоким сродством к ГнРГ и низкой связывающей способностью; за их счет осуществляется быстрая секреция ЛГ; вторые — более низким сродством к ГнРГ, но большей силой связывания, что и определяет более медленное освобождение ФСГ. Возможно существование двух различных нейрогормонов — ЛГ-РГ и ФСГ-РГ.
Анатомия и физиология гипофиза
Гипофиз расположен в турецком седле в основании черепа. Сверху он отделен от мозга выростом твердой мозговой оболочки. Гипофиз состоит из трех долей: передней, задней и средней (промежуточной). Последняя, как правило, анатомически не обособлена и вместе с передней входит в состав аденогипофиза, который составляет около 80% массы железы; задняя доля — нейрогипофиз — анатомически и функционально объединена со срединным возвышением, являющимся частью гипоталамуса. Аденогипофиз образуется из задней стенки ротовой полости зародыша (карман Ратке), задняя доля — из дивертикула дна третьего желудочка мозга.
Структурно-функциональная связь гипофиза с гипоталамусом осуществляется нервным и гуморальным путем. Нервные волокна из крупноклеточных гипофизотропных ядер гипоталамуса (паравентрикулярного и супраоптического) через срединное возвышение и ножку гипофиза достигают задней его доли. По аксонам этих клеточных ядер в заднюю долю гипофиза поступают окситоцин и вазопрессин. На стенках капилляров срединного возвышения оканчиваются терминали пептидергических волокон. Аксоны гипоталамических нейронов, идущие к аденогипофизу, прерываются на уровне срединного возвышения, где и происходит секреция гипоталамических статинов и либеринов.
Нейрогормоны попадают в переднюю долю гипофиза с кровотоком по системе воротных вен гипофиза. Стенки каппиляров, образуемых ветвями верхних гипофизарных артерий в срединном возвышении, проницаемы для рилизинг-гормонов. Концентрация последних в крови воротных вен гипофиза во много раз выше, чем в периферической крови.
Кровоток через переднюю долю гипофиза значительнее, чем через любой другой орган, что, наряду с высоким содержанием нейрогормонов в крови сосудов гипофиза, создает оптимальные условия для регуляции функций аденогипофиза и зависимых от него эндокринных желез. Задняя доля гипофиза снабжается кровью нижних гипофизарных артерий.
Являясь анатомически целостным органом, гипофиз образован двумя онтогенетически разными образованиями: передним (железистым) и задним (нервным). Клетки аденогипофиза разделяются по своей гистологической окраске на базофилы, ацидофилы (эозинофилы), хромофобы. Однако выявление специализированных клеток—лактотрофов, тиреотрофов, соматотрофов, кортикотрофов, гонадотрофов, продуцирующих соответствующие гормоны, осуществляется иммуноцитохимическим методом, выявляющим специализацию клеток с помощью высокоспецифических антител к конкретному гормону. Большую часть популяции аденогипофизоцитов составляют лактотрофы и соматотрофы. Обнаруживаются и камбиальные элементы, способные при необходимости дифференцироваться в те или иные специализированные клетки.
Гипофиз как центральный орган эндокринной системы получает афферентную и эфферентную информацию. Из срединного возвышения по сосудам портальной системы в аденогипофиз поступает кровь, содержащая гипоталамические нейрогормоны. К гипофизу поступает также большое количество гормонов периферических эндокринных желез и биологически активных метаболитов. Переработка этой информации позволяет гипофизу осуществлять тонкую интегральную функцию и посылать периферическим эндокринным железам адекватные, строго дозированные регуляторные сигналы путем выделения в кровь тропных гормонов. Периферические эндокринные железы, реагируя на тропные гормоны гипофиза, секретируют в кровь собственные гормоны, регулирующие биохимические процессы в тканях-мишенях. Циркулирующие в крови гормоны и биологически активные метаболиты контактируют со всеми структурами нейроэндокринной системы: ЦНС, гипоталамусом, гипофизом, другими железами внутренней секреции, клетками АПУД-системы (которые присутствуют в различных органах и тканях и продуцируют полипептидные гормоны за счет поглощения и декарбоксилирования предшественников аминов).
Вопрос и о локализации биосинтеза гипоталамических гормонов окончательно не решен. Имеются данные об их образовании в нервных окончаниях — синаптосомах, так как именно в них обнаруживается скопление этих гормонов и биогенных аминов. В настоящее время биогенным аминам отводится главная роль в регуляции секреции и синтеза гипоталамических гормонов. В гипоталамусе присутствуют специфические рецепторы гормонов и периферических аминорецепторов.
Воспринимая регуляторные сигналы сверху, железа ускоряет или тормозит выделение собственного гормона и, более того, она получает информацию о результатах действия ее гормонов на периферии. Механизм такой организации эндокринной железы, называемой в литературе принципом обратной связи (положительной и отрицательной), был впервые сформулирован М.М. Завадовским (1935). Он обеспечивает надежность работы нейроэндокринной системы в организме. Классическим примером может служить функционирование щитовидной железы, когда ТТГ стимулирует секрецию тиреоидных гормонов, которые в свою очередь, достигнув высоких концентраций в крови, тормозят секрецию гипофизом ТТГ. Обратная связь реализуется на четырех уровнях (ЦНС, гипоталамус, гипофиз, сама железа), и в ней различают длинные, короткие и ультракороткие звенья. Эндокринные регуляторы — гормоны дистантного действия — достигают своих целевых объектов с кровотоком.
Концентрация и ритм секреции гормонов определяют направленность действия и точку приложения в организме. Так, эстрогены, стимулируя секрецию пролактина гипофизом, увеличивают выделение ДА гипоталамусом, что приводит к торможению лактотропной функции гипофиза. На телах нейронов, синтезирующих ДА, обнаружены рецепторы эстрадиола. В этом процессе участвуют и метаболические регуляторы, такие как глюкоза [10].
В одной и той же железе имеется возможность обмена химической информацией между клетками, в которой принимают участие и гормоны. Показано, в частности, наличие рецепторов инсулина на альфа-клетках, секретирующих глюкогон (паракринная регуляция). Биологически активные вещества, в том числе гормоны, могут выделяться и связываться рецепторами той же клетки (аутокринная регуляция).
Чувствительность тканей к конкретному гормону определяется количеством специфических рецепторов, связывающих этот гормон. Высокие концентрации гормона, связывая большую часть рецепторов, снижают их биосинтез и уровень активных форм рецепторов, что предохраняет клетки-мишени от чрезмерного гормонального воздействия. Возможна и ситуация, когда гормон увеличивает концентрации собственных рецепторов.
Гормон может влиять не только на свои рецепторы, но и на рецепторы других гормонов. Так, ПРЛ стимулирует образование рецепторов ЛГ и ФСГ в гонадах, тиреоидные гормоны влияют на уровень эстрогенных и катехоламиновых рецепторов и т.д. Обратная связь реализуется довольно быстро, что обеспечивает постоянный относительный гомеостаз в организме; замедление или ускорение этого процесса свидетельствует о развитии патологического процесса.
Нарушения гормональной рецепции ведут к развитию патологического процесса (например, инсулинорезистентность при ожирении и сахарном диабете 2-го типа).
В срединном возвышении обнаружены многочисленные синаптические и аксональные контакты нейронов, вырабатывающих нейропептиды, а также анастомозы между капиллярами сосудов, идущими к аденогипофизу и нейрогипофизу, что и обеспечивает тесное взаимодействие различных эндокринных подсистем (гипоталамус—гипофиз—кора надпочечников, гипоталамус—гипофиз—щитовидная железа, гипоталамус—гипофиз—гонады и др.).
Главным достижением нейроэндокринологии последних лет является доказательство причастности нейромедиаторов к нейроэндокринной интеграции действия нейросекреторных нейронов, регулирующих секрецию тропных гормонов гипофиза. К ним относятся норадреналин (НА), адреналин (А), ДА, серотонин, гистамин, гамма-аминомасляная кислота (ГАМК), ацетилхолин, соматостатин, ТРГ, КРГ, соматолиберин и многие другие соединения. Все эти вещества несут нейрогенную информацию, необходимую для нормального функционирования нейросекреторных нейронов, регулирующих секрецию тропных гормонов гипофиза. Прежде всего это люлиберинпродуцирующие нейроны, регулирующие выделение ЛГ и ФСГ, нейроны, секретирующие пролактинингибирующий гормон, ТРГ, вазоактивный интестинальный полипептид, а также ДА. Полное понимание нейроэндокринного контроля требует точного знания топографии нейросекреторных и обычных проводниковых нейронов. Необходимо определить главные проекции нейронов и идентифицировать нейромедиаторы, содержащиеся в них. Обнаружены синапсы между норадренергическими нейронами и ГАМК-содержащими нейронами в этой области. Следует отметить также возможность несинаптического взаимодействия катехолсодержащих нейронов в ЦНС.
Дофаминергические нейроны, иннервирующие гипоталамус, имеют клеточные тела в трех областях мозга: во-первых, это тубероинфундибулярные нейроны, которые составляют 3—5% клеточных тел нейронов аркуатной области и обозначаются как А12. Терминали этих нейронов обнаружены в срединном возвышении в тесном контакте с первичными капиллярами гипофизарного портального сплетения. Эти нейроны выделяют большое количество ДА в портальную кровь и играют ведущую роль в регуляции секреции ПРЛ, а также ГнРГ. Две другие группы дофаминергических нейронов расположены в каудальном таламусе, заднем гипоталамусе и перивентрикулярных ядрах. Диффузное распределение дофаминергических нейронов в гипоталамусе затрудняет изучение их роли в регуляции секреции гонадотропинов и других тропных гормонов.
Изложение контрольных функций адренергических нейронов в секреции гонадотропинов целесообразно начать с их роли в регуляции пульсирующего выделения ЛГ, которая определяется квантовым выделением ГнРГ. Большинство исследователей, занимающихся этой проблемой, приходят к выводу, что норадренергические нейроны в физиологических условиях включаются в этот процесс, хотя на отдельных нейронах обнаружены адренергические рецепторы, активация которых вызывает торможение пульсирующего выделения ЛГ. Направленность действия ДА-нейронов зависит, скорее всего, от уровня половых гормонов.
При изучении роли биогенных аминов в регуляции овуляторного выброса гонадотропинов особое внимание обращается на значение половых гормонов в активации или торможении катехолсодержащих нейронов в системе обратной связи. На модели овариэктомированных крыс с имплантацией эстрадиола показано, что выброс ЛГ каждые 24 ч сопровождается увеличением скорости обмена НА в преоптической и аркуатной областях и супрахиазматических ядрах, а также срединном возвышении. Аналогичные данные получены и в опытах на интактных животных, у которых отмечено увеличение скорости обмена НА в преоптической области во 2-й половине проэструса, т.е. во время овуляторного выброса ЛГ, тогда как в другие стадии цикла подобных изменений в обмене НА в этой области не зарегистрировано. О негативном действии эстрадиола на обмен НА свидетельствуют эксперименты на овариэктомированных животных, у которых скорость обмена НА в преоптической области увеличивалась через 3 сут, а введение эстрадиола приводило к снижению скорости его обмена в этой области и срединном возвышении уже через 3 ч. Действие эстрогенов на обмен НА может осуществляться как непосредственно на уровне норадренергических нейронов, содержащих эстрогенные рецепторы, так и через опиоидные или ГАМК-содержащие интернейроны, которые также содержат рецепторы стероидных гормонов. Скорость обмена адреналина в некоторых областях гипоталамуса также увеличивается одновременно с овуляторным выбросом ЛГ. Это касается, главным образом, медиобазального гипоталамуса и преоптической области. Возникает вопрос о степени сродства адренергических рецепторов нейронов к половым гормонам в ходе менструального цикла.
Влияние половых гормонов на активность дофаминергических нейронов проявляется менее отчетливо. Дело в том, что изменение состояния тубероинфундибулярных дофамин-содержащих нейронов теснее связано с секрецией ПРЛ. Введение эстрогенов повышает уровень ПРЛ, который в свою очередь усиливает обмен ДА в этих нейронах. Показано также наличие рецепторов к эстрадиолу в дофаминергических клеточных телах нейронов аркуатного ядра и повышение скорости обмена ДА в этом ядре и срединном возвышении во второй половине стадии проэструса. В преоптической области изменения дофаминергической активности в это время не наблюдается. Овариэктомия незначительно влияет на обмен ДА в некоторых областях гипоталамуса, тогда как введение эстрадиола вызывает снижение обмена ДА в преоптической области и срединном возвышении и увеличение в медиобазальном гипоталамусе.
Имеется ряд сообщений о влиянии катехоламинергических агентов на овуляторный выброс ЛГ в проэструсе и вызванный эстрогенами выброс ЛГ. Начало этим исследованиям было положено в 1950 г. Сойером, который показал, что α-адренергические антагонисты блокируют овуляцию у крыс. В дальнейшем были исследованы более специфические фармакологические агенты, такие как α-метил-р-тирозин и диэтилдитиокарбомат, блокирующие синтез НА и А соответственно. Они тормозили овуляторный выброс ЛГ. Блокада α-адренергических рецепторов также прерывает овуляцию, причем наиболее эффективным является препарат празозин, избирательно блокирующий подтип α1-рецепторов, тогда как блокада другого подтипа рецепторов (α2) пипероксаном неэффективна.
Приведенные данные позволяют утверждать, что норадренергические и адренергические нейроны включаются в стимуляцию овуляторного выброса ЛГ, и действие их опосредуется через α1-адренергические рецепторы, локализованные в основном в медиобазальной преоптической области гипоталамуса. Роль дофаминсодержащих нейронов в регуляции овуляторного выброса ЛГ спорна: введение относительно специфического антагониста ДА пимозина в утренние часы проэструса снижало выброс ЛГ у крыс во второй половине дня. Этот же препарат, введенный женщинам за 2 ч до ожидаемого выброса ЛГ в середине менструального цикла, снижает величину выброса. В другом случае внутрижелудочковое введение ДА в проэструсе у крыс способствует увеличению уровня ЛГ в крови. Исследования in vitro также дают спорные результаты. Так, перфузия ДА фрагментов медиобазального гипоталамуса самцов крыс увеличивает выделение ГнРГ, которое блокируется введением антагониста α-адренергических рецепторов (фентоламина), но не антагониста ДА (пимозина). ДА обладает способностью ускорять выделение НА из терминалей срединного возвышения, но не влияет на обратный захват и обмен НА. Противоречивые данные затрудняют интерпретацию роли и значения ДА в решении системы ГнРГ—ЛГ.
Серотонинергическая система ЦНС представляет собой популяцию нейронов ствола мозга, которые берут начало в ядрах шва среднего мозга. Аркуатные ядра получают плотную серотонинергическую иннервацию, тесно контактирующую с дофаминергическими клеточными телами аркуатного ядра и медиальной зоны инсепта. Описаны контакты между нейрональными элементами, содержащими ГнРГ и серотонин, в преоптической области, концевой пластинке и срединном возвышении. Серотонин обнаружен в нервных окончаниях, локализованных вокруг больших кровеносных сосудов аденогипофиза, а также в секреторных гранулах гонадотрофов. Причастность серотонина к регуляции гонадотропной функции гипофиза доказана многочисленными исследованиями. Он может как стимулировать, так и тормозить эту функцию в зависимости от гормонального фона. Действие серотонина на секрецию ЛГ и овуляцию опосредовано регуляцией секреции ГнРГ нейросекреторными нейронами. Серотонинергическая система является одной из многих нейросекреторных систем, тесно связанных с гонадотропинрегулирующей системой преоптикопереднего и медиобазального отделов гипоталамуса и срединного возвышения. Половые гормоны модулируют активность этой нейротрансмиттерной системы. Анализ роли нейромедиаторов адренергического ряда в регуляции гонадотропной функции гипофиза позволяет утверждать, что НА следует рассматривать в качестве ведущего агента в регуляции секреции ЛГ, основной точкой приложения которого является преоптическая область. ДА реализует свой эффект через аркуатную область гипоталамуса, а серотонин играет роль синхронизирующего агента.
Новый класс соединений, выделяемых в группу пептидных нейромедиаторов, вносит свой вклад в наши представления об участии нервной системы в регуляции эндокринных функций гипофиза. Обнаружение регуляторных пептидов, общих как для нервной, так и для эндокринной систем, вызвало революцию в наших представлениях. Возникло новое направление исследований — психонейроэндокринология.
Практически каждый из перечисленных выше нейропептидов причастен к регуляции секреции гонадотропинов, ПРА, АКТГ, ТТГ. Большинство из них обнаружено в медиобазальном гипоталамусе. Нейропептиды, выделяясь в гипофизарную портальную систему, действуют на несколько типов аденогипофизарных клеток и, кроме того, взаимодействуют с многими нейромедиаторами непептидной природы, поступающими в медиобазальный гипоталамус из других структур, что в свою очередь обеспечивает их прямое или опосредованное действие на гормональный контроль.
Гипоталамические нейроны, продуцирующие нейропептиды, составляют общую систему. Большинство их клеточных тел локализовано в паравентрикулярных ядрах, медиальной перивентрикулярной области и аркуатных ядрах. Незначительная часть таких нейронов обнаружена в преоптической области и супрахиазматических ядрах. Бóльшая часть всех этих нейронов заканчивается в области срединного возвышения. Аксональные коллатерали иннервируют ряд гипоталамических и экстрагипоталамических структур. Нервные клетки паравентрикулярных и аркуатных ядер в свою очередь имеют многочисленные контакты с большим числом других структур ЦНС, что и определяет их стратегическую позицию в координации гормональной регуляции, а также ряда поведенческих реакций. Особенно это касается полового поведения, требующего синхронизации поведенческих компонентов с процессами менструального цикла. Окончания нейронов, синтезирующих нейропептиды, тесно контактируют не только с перикарионами, вырабатывающими нейротрансмиттеры, но и с нейронами, синтезирующими нейропептиды. Например, ГнРГ-продуцирующие нейроны и их волокна могут оканчиваться на аналогичных клеточных телах; имеют место также аксо-аксональные контакты.
Учитывая большое число нейропептидов, принимающих участие в регуляции репродуктивной системы, целесообразно сгруппировать их по месту синтеза. Такими группами могут быть: 1) нейропептиды, продуцируемые нейронами, локализованными, главным образом, в преоптической области (соматостатин, ГнРГ, тахикинины, нейротензин, предсердный натрийуретический гормон); 2) нейропептиды, продуцируемые нейронами аркуатной области (панкреатический нейропептид, пептид YY, нейропептид Y); 3) нейропептиды, синтезирующиеся в перикарионах паравентрикулярных или супраоптических ядер (ТРГ, КРГ, холецистокинин, вазопрессин, окситоцин, ангиотензин, брадикинин, бомбезин); 4) гастроинтестинальные пептиды (ВИП, гастроинтестинальный пептид); 5) семейство опиоидных пептидов.
Механизм действия этих нейропептидов как на гипоталамическом, так и на гипофизарном уровне можно проследить на примере модуляции секреции гонадотропинов, ПРЛ, окситоцина, т.е. тех гормонов, которые имеют отношение к репродуктивной функции. Например, соматостатин, который обнаружен во многих структурах ЦНС и главным действием которого является угнетение продукции гормона роста и частично ТТГ и ПРЛ, способен изменять активность нейромедиаторных систем мозга, вызывая блокаду секреции ГнРГ.
Группа классических пептидов (тахикинины А и Б, субстанция Р) стимулирует выделение ПРЛ и тормозит выделение гормона роста. Пептид нейротензин широко распространен в ЦНС и проявляет свой эффект за счет стимуляции секреции инсулина, ингибиции секреции глюкагона и модуляции гастроинтестинальной перистальтики. Внутрижелудочковое введение нейротензина снижает уровень ЛГ в крови, что делает возможным его участие в контроле гонадотропной функции гипофиза. Предсердный натрийуретический гормон угнетает выделение вазопрессина и может стимулировать выделение ЛГ и пролонгировать действие ГнРГ. Семейство панкреатических пептидов также причастно к функционированию репродуктивной системы, они чаще всего блокируют секрецию ЛГ и снижают частоту пульсации ГнРГ в срединном возвышении.
Пептиды, синтезирующиеся в паравентрикулярных и супрахиазматических ядрах, основными из которых являются вазопрессин и окситоцин, наиболее активно влияют на репродуктивную систему. Основная гормональная функция вазопрессина на уровне аденогипофиза — стимуляция выделения АКТГ за счет усиления действия КРГ. Имеются данные о тормозном влиянии вазопрессина на секрецию ПРЛ за счет повышения обмена ДА в тубероинфундибулярных нейронах. Стимулирующий эффект вазопрессина на выделение ПРЛ может опосредоваться опиатными нейронами. ТРГ, синтезирующийся в паравентрикулярных ядрах, помимо своего прямого действия на секрецию ТТГ, способен стимулировать выделение ПРЛ и гормона роста, и его эффект усиливается под влиянием эстрогенов. ТРГ также оказывает влияние на обмен нейромедиаторов в мозге. Из группы гастроинтестинальных пептидов следует выделить вазоактивный интестинальный полипептид (ВИП), основное нейроэндокринное действие которого сводится к стимуляции выделения ПРЛ, а также гормона роста и ТТГ. Этот эффект является эстрогензависимым.
Особое внимание в регуляции гонадотропной функции гипофиза в последние годы уделяется опиоидным пептидам. Главным действием опиоидов является их способность повышать выделение ПРЛ и гормона роста и блокировать секрецию ЛГ, ФСГ и ТТГ. Они специфически ингибируют овуляторный выброс ЛГ и ФСГ. Опиаты способны регулировать амплитуду и частоту пульсации ЛГ за счет модуляции гипоталамического пейсмекера, контролирующего периодичность активации ГнРГ-продуцирующих нейронов. Влияние опиатов на секрецию ЛГ опосредовано повышением секреции ПРЛ. Опиаты блокируют тоническую секрецию ГнРГ на фоне высокого уровня ПРЛ. Регуляция процессов биосинтеза и секреции ПРЛ, как и ЛГ, опиоидными пептидами осуществляется через специфические рецепторы.
Приведенные выше данные о влиянии различных нейромедиаторов адренергической природы и нейропептидов ставят вопрос о том, каким образом разные вещества с различными механизмами действия координируют работу репродуктивной системы. В ряде случаев отмечен синергизм их действия как на гипоталамическом, так и на гипофизарном уровне, в других — антагонизм их влияния. Можно отметить параллелизм в действии различных медиаторов, вырабатываемых в одних и тех же структурах. В настоящее время наблюдается быстрый прогресс в изучении химии и нейроанатомии нейросекреторных нейронов, участвующих в регуляции репродуктивной функции.
В настоящее время цельное представление о функционировании гипоталамо-гипофизарной системы распалось на отдельные направления исследований с использованием новых специфических методических приемов. Интенсивно используются достижения смежных дисциплин, таких как иммунология. Показана тесная взаимосвязь нейроэндокринной и иммунной систем в различные периоды жизни и при различных физиологических состояниях. Например, с возрастом снижается реакция иммунной системы и параллельно снижается активность гормона роста. При беременности снижается секреция пролактина и окситоцина и повышается секреция половых гормонов — эстрогенов, прогестерона. Доказана взаимосвязь нервной, иммунной и эндокринной систем регуляции секреции инсулина. Разработка фундаментальных аспектов нейроэндокринологии открывает широкие перспективы лечения нарушений репродуктивной системы, заболеваний щитовидной железы или надпочечников гормональными средствами или препаратами, обладающими нейрогенными свойствами. Такими препаратами могут быть производные нейромедиаторов адренергической, холинергической природы, а также нейропептиды.
Начиная с конца 50-х годов прошлого столетия внимание исследователей всего мира все больше стало привлекать изучение воздействия гормональных факторов на функцию головного мозга. В результате многочисленных исследований родилась новая наука — психонейроэндокринология. Ее задачами является изучение вопросов, связанных с влиянием гормонов на высшие функции мозга, — от молекулярного уровня до различных сторон психической деятельности.
Проблема воздействия гормональных факторов на высшие интегративные функции мозга чрезвычайно сложна как по существу, так и в силу отсутствия объективной модели, отражающей зависимость между уровнем гормонов в организме и его влиянием на когнитивные функции.
Показано, что гормоны, взаимодействуя с нейромедиаторами, образуют на уровне ЦНС единую координирующую нейрогуморальную систему, контролирующую интегративную деятельность головного мозга. Нарушение биосинтеза или обмена нейромедиаторов, нарушения их взаимодействия с соответствующими рецепторами могут играть патогенетическую роль в развитии ряда нервно-психических состояний. Сложились устойчивые представления о том, что функция гормонов в ЦНС связана с контролем экспресии гормонзависимых генов и регуляции таких процессов, как развитие и старение мозга, регенерация, адаптация, память.
Различают геномный и негеномный механизм действия гормонов. Полипептидные гормоны действуют на специфические рецепторные зоны мембраны клетки. Связывание лиганда поверхностными рецепторами клетки индуцирует внутриклеточный сигнал (цАМФ и/или кальций) и приводит к быстрому результату (активации остеокластов, секреции кортизола и т.п.). Трансдукция сигнала полипептидных гормонов может вовлекать фосфатидилиновый путь или фосфорилирование рецепторов.
Стероидные и тиреоидные гормоны проявляют свое действие главным образом через специфические внутричерепные связывающие белки, которые взаимодействуют с элементами генов клеток-мишеней, что сопровождается изменением транскрипции специфических генов.
Гипофиз — главный регулятор функционирования эндокринных желез
В аденогипофизе секретируются следующие гормоны: ТТГ, АКТГ, ЛГ и ФСГ, которые оказывают стимулирующее влияние соответственно на клетки щитовидной железы, коры надпочечников и половые железы. Попадая в кровь, гормоны периферических желез активизируют деятельность всех органов и тканей организма, в том числе и аденогипофиза. Осуществляя обратную связь, они блокируют избыточное поступление тропных гормонов гипофиза. Наступает равновесие между мутацией гормонов гипофиза и потребностью организма в гормонах периферических желез. Несколько иной результат наблюдается в отношении ПРА и гормона роста, не имеющих специализированного целевого органа, секреция которого оказывала бы тормозной эффект на выделение этих гормонов. Помимо блокирующего эффекта гормонов периферических желез на синтез и секрецию тропных гормонов гипофиза, аналогичным эффектом обладают также ингибиторные факторы гипоталамического происхождения.
Синдромы эндокринной недостаточности, обусловленные полным или частичным выпадением функций передней и задней долей гипофиза, обозначаются как гипопитуаризм. Гипофункция гипофиза может быть следствием поражения самого гипофиза или гипоталамуса. Результат один — сниженная секреция гипофизарных гормонов с последующим дефицитом гормонов периферических желез.
Уровень гормона роста в крови в норме очень низок, но увеличивается при физической нагрузке, во время сна и при стрессе. Наиболее надежные стимулирующие тесты для данного гормона — индуцированная инсулином гипогликемия, инфузия аргинина или введение L-допа. Эти тесты сопровождаются увеличением секреции гипоталамического соматолиберина.
Секреция пролактина у здоровых людей обычно низкая в течение дня, увеличивается во сне, при стрессе и родах. В клинике используют провоцирующий тест с внутривенным введением ТРГ