Урсосан: эффективная защита печени
Указана минимально возможная цена на товар в городе.
Цены на товар в разных аптеках отличаются.
Когда надо принимать препарат
Как принимать Урсосан
При жировом гепатозе врачи проводят комплексную терапию. В её состав включают Урсосан. Доза лекарственного средства зависит от выраженности клинических симптомов, тяжести течения болезни и веса пациента. На один килограмм массы тела назначают от десяти до пятнадцати микрограмм лекарственного средства. То есть, пациент весом 100 кг должен в сутки принимать от 1000 до 1500 мг Урсосана. 100мкг препарата содержится в двух таблетках или четырёх капсулах, 1500 – в трех таблетках или шести капсулах. Длительность медикаментозной терапии варьирует от шести месяцев до года. Капсулы и таблетки не следует разжевывать.
Когда нужно принимать Урсосан – до еды или после еды
Капсулы или таблетки препарата следует выпить во время или после приема пищи и запить очищенной негазированной водой.
Для растворения желчных камней следует принимать ежедневно по 10 мкг препарата на килограмм веса. Суточная доза может быть повышена до 15 мкг на килограмм массы тела. Лекарство принимают до полного растворения камней. Длительность терапевтического курса варьирует от полугода до года.
Пациенты после удаления желчного пузыря принимают по одной капсуле или половине таблетки препарата дважды в день в течение нескольких месяцев для предотвращения повторного образования конкрементов. При хронических гепатитах препарат назначают в дозе 10-15 мкг на килограмм веса. Суточную дозу разделяют на два или три приёма. Длительность курса лечения – от 6 до 12 месяцев.
Пациентам, страдающим холестатическими заболеваниями печени, Урсосан назначают в суточной дозе от 12 до 15 мкг на один килограмм веса. При необходимости дозу повышают до 20-30 мкг. В течение первых трёх месяцев больные делят суточную дозу на 2 две или 3 части. При улучшении показателей биохимического исследования крови её можно принимать за один приём на ночь.
Побочные эффекты после приема Урсосана
При приеме капсул или таблеток Урсосана иногда каловые массы приобретают пастообразную консистенцию или развивается диарея. У больных билиарным циррозом очень редко появлялась боль в правом подреберье. В ходе терапии первичного билиарного цирроза редко происходила декомпенсация заболевания.
Обратное развитие признаков декомпенсации происходило после отмены препарата.
Лекарственные поражения печени и поражение печени при беременности: патогенез, диагностика и лечение
В статье представлены современные данные о патогенезе лекарственных поражений печени, развивающихся в результате непосредственного токсического поражения печеночной ткани или вследствие опосредованного воздействия на метаболические процессы в печени и идиосинкразического ее поражения. Приведена современная классификация лекарственных поражений печени – острых, хронических, сосудистых, опухолевых и др. Представлены диагностические критерии и возможности фармакотерапии. Перечислены и охарактеризованы поражения печени, возникающие иногда при беременности, в том числе индуцированный беременностью внутрипеченочный холестаз и его лечение с использованием препаратов урсодеоксихолевой кислоты, в части случаев – адеметионина. Представлена характеристика острой жировой дистрофии печени, ее патогенез и лечебная тактика, а также HELLP-синдром. Заключительный раздел статьи посвящен течению беременности при наличии различных заболеваний печени (вирусных гепатитов, аутоиммунных заболеваний печени, болезни Вильсона, холелитиаза и др.)
Все лекарственные вещества, принимаемые внутрь, из желудочно-кишечного тракта поступают непосредственно в печень по воротной вене, выполняющей функцию “входных ворот». В печеночной ткани осуществляются метаболизм и биотрансформация лекарственных средств, в результате которых жирорастворимые неполярные соединения, входящие в состав лекарств, превращаются в водорастворимые производные (метаболиты). Эти процессы осуществляются под воздействием ферментов, образующихся в печени. Ферменты, выполняющие указанные функции, относятся к микросомальной оксидазной системе и ассоциируются с гладким эндоплазматическим ретикулумом печеночных клеток (гепатоцитов) [1,2]. Образующиеся промежуточные метаболиты могут обладать даже более высокой активностью, чем сами лекарства, и оказывать токсическое воздействие на печень при участии цитохрома Р 450.
Три семейства цитохрома Р450 обеспечивают превращение липидов в водорастворимые метаболиты с последующей коньюгацией (связыванием) метаболитов с глюкуронидами, сульфатами и глутатионом, а образующиеся соединения выводятся из организма с желчью и мочой [1,3,4]. У одной группы лекарств печеночная экстракция отличается высокой степенью, и они активно захватываются печеночной тканью, в то время как лекарственные препараты другой группы почти не захватываются печенью из портальной системы крови, а их элиминация обусловлена главным образом метаболическими возможностями печеночной ткани. В связи с этим опасность передозировки последних невелика и повышается только в тех случаях, когда имеется метаболическая недостаточность печени вследствие тех или иных ее заболеваний 1. Активность ферментов, образующихся в печени, частично зависит от врожденных (генетических) факторов, а в качестве потенциальных субстратов ферментной системы цитохрома Р450 выступают эстрадиол, тестостерон, андростерон, прогестерон и гидрокортизон, которые способны подавлять метаболическую актив ность лекарственных веществ [3,4]
Выделяют два варианта воздействия лекарственных веществ на печень: (1) непосредственное токсическое поражение печени с повреждением структуры гепатоцитов (преимущественно их клеточных мембран) или опосредованное воздействие на метаболические процессы в печеночной ткани, например, торможение синтеза белка [1,2] и (2) идиосинкразическое поражение печени по механизму гиперчувствительности, обусловленное иммунными нарушениями, когда экзогенное вещество (лекарство) или его метаболиты, связываясь с белком, приобретают свойство антигена [4]. Соот вет ственно, лекарственные средства можно разделить на истинные гепатотоксины, вызывающие облигатные патологические реакции в печени, и гепатотоксины, обладающие факультативным воздействием на печень (идиосинкразическим) [1,3-7].
Поражение печени после приема гепатотоксических лекарственных препаратов обычно развивается в течение 2–3 месяцев после начала лечения 4.
Диагностика. Важнейшая роль в диагностике ле кар ственных поражений печени принадлежит тщательно собранному анамнезу (связь заболевания с приемом конкретных лекарственных средств).
Большое значение имеет инструментальная диагностика: ультразвуковое исследование печени и поджелудочной железы; лапароскопия; эндоскопическая ретроградная панкреатохолангиография (ЭРПХГ); пункционная биопсия печени с последующим гистологическим изучением биопсийного материала 3.
Из лабораторных диагностических тестов необходимо назвать: общеклинический анализ крови; биохимический анализ крови с определением ферментов цитолиза (АЛТ, АСТ), лактатдегидрогеназы (ЛДГ), гамма-глутамилтранспептидазы (γ-ГТП), ферментов холестаза (щелочная фосфатаза, лейцинаминопептидаза – ЛАП), общего билирубина и его фракций, альбуминов, общего холестерина, холинэстеразы, протромбинового времени, иммуноглобулинов, антинуклеарных (ANA) и антимитохондриальных антител (АМА-М2), вирусных маркеров (HBsAg+; IgM анти-HAV и др.) [1,3-7]. Важно установить время, прошедшее с начала приема гепатоксичного лекарственного средства до появления клинической реакции на него [11,12,17,18].
Лечение. Прежде всего необходимо немедленно отменить препарат, который предположительно мог стать причиной поражения печени. Для лечения лекарственных поражений печени чаще всего используют адеметионин (S-аденозил-L-метионин), представляющий собой естественный метаболит организма. Он обладает множеством положительных эффектов: гепатопротективным действием; участием в синтезе фосфолипидов, восстанавливая структуру мембраны гепатоцитов; детоксикационным, антиоксидативным эффектом, участвуя в нейтрализации токсинов и свободных радикалов; антидепрессивным; регенерирующим; антихолестатическим действием, активируя выведение желчных кислот из гепатоцитов; нейропротективным, тонизирующим действием; участвует в синтезе АТФ и вос станавливает энергетический баланс гепатоцитов; нормализует биохимические печеночные сдвиги. Показаниями для лечения адеметионином являются: наличие внутрипеченочного холестаза; жировая дистрофия печени; хронический гепатит и токсические поражения печени различной этиологии, в частности при приеме таких гепатотоксических лекарств, как тетрациклин, трициклические антидепрессанты, пероральные контрацептивы, противотуберкулезные, противоопухолевые, противовирусные средства, алкоголь и др. Эффект наступает уже после двухнедельного курса лечения в дозе 1000-1500 мг/сут. Возможно назначение адеметионина в виде внутримышечных и внутривенных капельных инъекций лиофилизата (раствора) при медленном введении препарата 21.
Используют также урсодеоксихолевую кислоту (УДХК), прежде всего при алкогольной и неалкоголь ной жировой болезни печени; при стеатогепатите и аутоиммунном гепатите; при лекарственных гепатитах и гепатитах иной этиологии, протекающих с холестазом. Отмечена также эффективность лечения препаратами УДХК при других холестатических заболеваниях печени и желчевыводящих путей, сопровождающихся повышением уровня токсичных желчных кислот, ферментов цитолиза и ферментов холестаза. УДХК выполняет роль гепатопротектора, а также фактора “прикрытия» в случаях невозможности (по клиническим показаниям) отмены лекарственного препарата, обладающего гепатотоксическим действием. При лечении препаратами УДХК (Урсофальк, Урсосан) отмечается отчетливый клинический эффект: улучшение или даже нормализация нарушенных биохимических печеночных показателей. Уменьшаются кожный зуд и желтуха. Из побочных эффектов УДХК можно назвать тошноту и (редко) рвоту, анорексию, однако обычно лечение переносится хорошо, а общее состояние больных, как правило, не страдает [26–32]. Средняя суточная доза Урсофалька (Урсосана) – 10-15 мг/кг в 2–3 приема в течение 6–12 месяцев (таблетки по 500 мг).
Глюкокортикоиды используют в основном при среднетяжелых и тяжелых формах лекарственных поражений печени, прежде всего при развитии печеночной энцефалопатии и высокой активности патологического процесса в печени (увеличение активности аминотрансфераз в 5-10 раз по сравнению с верхней границей нормы, высокий уровень билирубина и т.п.). В течение первых 3–5 дней глюкокортикоиды вводят внутривенно, после чего переходят на их пероральный прием (30 мг/сут в пересчете на преднизолон) в течение 2–3 недель [35,37].
Некоторые авторы рекомендуют использовать для лечения лекарственных поражений печени эссенциальные фосфолипиды (Эссенциале форте-Н), но, по нашему мнению, их применение недостаточно обосновано, поскольку они могут усугублять внутрипеченочный холестаз и активировать воспалительный процесс в печени [36].
При приеме некоторых лекарственных препаратов повышается риск развития холелитиаза, неудачно именуемого у нас в стране желчекаменной болезнью, поскольку присоединение к названию болезни слова “болезнь» является тавтологией. Развитие внутрипеченочного холестаза может быть следствием приема таких фармакологических средств, как анаболические стероиды, парацетамол, галотан, половые гормоны, пероральные контрацептивы, вызывающие застой (стаз) желчи в желчном пузыре, перенасыщение желчи холестерином (гиперсатурация желчи) с последующей нуклеацией и осаждением (преципитацией) в виде кристаллов холестерина моногидрата, образованием в желчном пузыре билиарного сладжа, а затем его агрегацией в микролиты и их дальнейшим ростом до крупных желчных камней (конкрементов). В подобных случаях эффективно применение гимекромона (Одестон), обеспечивающего купирование билиарного болевого синдрома и диспепсических явлений за счет спазмолитического действия на сфинктер Одди и усиления холереза, не связанного с продукцией желчных кислот. Гимекромон является фенольным производным кумарина, обладающим способностью повышать синтез желчных кислот в печени, оказывать избирательное спазмолитическое действие на сфинктер Одди в отсутствие сокращений желчного пузыря, купировать болевой и диспепсический синдромы и снижать выраженность воспалительного процесса в желчном пузыре. Фармакотерапия гимекромоном обеспечивает его высокую концентрацию в желчи благодаря почти 100% печеночной экстракции препарата из портального кровотока. Гимекромон не оказывает влияния на глюкуронилтрансферазу почек. Назначают по 200–400 мг (1–2 таблетки) 3 раза в день перед едой; курс лечения составляет 3–4 недели [38].
Беременность и печень
Нормально протекающая беременность обычно не сопровождается какими-либо изменениями в печени. Но существуют болезни печени, индуцированные исключительно беременностью: внутрипеченочный холестаз беременных, острая жировая дистрофия печени беременных, НЕLLР-синдром.
Внутрипеченочный холестаз беременных (ВХБ). Для обозначения этого синдрома используют и другие термины: идиопатическая желтуха беременных, рецидивирующая семейная желтуха беременных. ВХБ представляет собой доброкачественное семейное заболевание, проявляющееся преимущественно на поздних стадиях беременности появлением мучительного кожного зуда и желтухи, которые обычно исчезают вскоре после родов, но часто рецидивируют при повторных беременностях. Этиология неизвестна. Распространен ность не превышает 0,04–0,6%, но в скандинавских странах и в Чили достигает 3%.
В патогенезе ВХБ имеют значение генетические факторы, передающиеся по аутосомно-доминантному типу, а само заболевание (или синдром) характеризуется склонностью (предрасположенностью) к развитию внутрипеченочного холестаза в процессе беременности, который обусловлен гормональной дисфункцией – воздействием эстрогенов, прогестерона и других плацентарных гормонов, вызывающих торможение выработки гонадотропных гормонов гипофиза, что приводит к повышенному синтезу холестерина в печени и нару шению желчеобразования и желчевыведения. ВХБ отличается семейным характером и встречается у родственников первой степени родства.
Клинические симптомы ВХБ обычно появляются в третьем триместре беременности, редко – раньше и включают в себя мучительный кожный зуд (в 100% случаев), нарастающий в ночное время суток, и желтуху (в 20%) с выделением гипохоличного кала и темной мочи. Иногда наблюдаются тошнота и рвота, анорексия, однако общее состояние больных, как правило, не страдает. В сыворотке крови отмечают повышение активности холестатических ферментов (щелочной фосфатазы, лейцинаминопептидазы), 5-нуклеотидазы, γ-глутамилтранспептидазы (γ-ГТП), а также содержания желчных кислот, конъюгированного билирубина. Определяются билирубинурия и снижение уровня стеркобилина в кале. Активность аминотрансфераз остается в норме; снижается уровень протромбина и витамина К. В биоптате печени определяется центролобулярный холестаз без признаков повреждения гепатоцитов, воспаления и некроза, а при электронной микроскопии обнаруживают расширение желчных канальцев, потерю микроворсинок и аномальные митохондрии. Уже на 2–3-и сутки после родоразрешения все перечисленные клинические симптомы и отклонения в биохимических тестах, указывающие на внутрипеченочный холестаз, постепенно исчезают, но обычно рецидивируют при повторных беременностях, а также при приеме эстрогенов (в 60–70% случаев).
Иногда ВХБ может иметь негативные последствия для матери и плода. Возможны преждевременные роды (у 36–40% женщин) и мертворождение. Отдельные авторы полагают, что женщины, страдающие ВХБ, находятся в группе повышенного риска по отношению к таким заболеваниям, как неалкогольный стеатогепатит и панкреатит, вирусный гепатит С.
При дифференциальной диагностике ВХБ необходимо исключить вирусные, алкогольные и лекарственные гепатиты, аутоиммунный гепатит [39,40]. Кроме того, известны и другие наследственно обусловленные заболевания печени, протекающие с внутрипеченочным холестазом, такие как синдром Аагенеса-Саммерскилла (возвратный доброкачественный внутрипеченочный семейный холестаз) и болезнь Байлера (прогрессирующий семейный внутрипеченочный холестаз с фатальным исходом). Это генетически обусловленные заболевания и синдромы с аутосомно-рецессивным типом наследования. Как стало известно, патологический ген локализован в 18 хромосоме [20,21].
При лечении ВХБ используют препараты УДХК (Урсофальк, Урсосан) в дозе 750–1000 мг/сут коротким курсом. Иногда назначают адеметионин, являющийся антагонистом холестатического действия эстрогенов и снижающий выраженность холестаза [1–4].
Острая жировая дистрофия печени беременных – наиболее опасное заболевание, связанное с беременностью и характеризующееся высокой летальностью. В основе этого заболевания лежит микровезикулярное жировое поражение печени, которое характеризуется накоплением в гепатоцитах микровезикулярных капель жира, что осложняется нарушением функций их митохондрий и рибосом. В патогенезе острой жировой дистрофии печени имеет значение нарушение митохондриального окисления жирных кислот и дефицит внутриклеточной энергии в гепатоцитах.
Клинически болезнь протекает с фульминантной печеночной недостаточностью и желтухой (у 98% больных), тошнотой и рвотой. В биохимическом анализе крови характерны повышение ферментов цитолиза (АЛТ, АСТ), ферментов холестаза (щелочной фосфатазы, лейцинаминопептидазы), гипербилирубинемия (без признаков гемолиза), тромбоцитопения, нейтрофилез, повышенная концентрация мочевой кислоты. У части больных наблюдается анемия (при кровотечении и синдроме диссеминированного внутрисосудистого свертывания).
В инструментальной диагностике используют компьютерную томографию, ультразвуковое исследование (эндоскопическую ультрасонографию), биопсию печени с гистологическим изучением биоптатов, выявляющую массивное отложение жира – жировую инфильтрацию печеночной ткани.
При дифференциальной диагностике следует исключить острый холецистит и холангит; вирусные гепа титы, протекающие с фульминантной печеночной недостаточностью.
Лечение. Скорейшее родоразрешение, вплоть до кесарева сечения, без чего материнская смертность достигает 80%, а после родов – варьируется от 8 до 33% [1-4,28,29].
HELLP-синдром (Hemolisis – H; Elevated Liver enzy mes – EL; Low Platelets – LP). В переводе на русский язык означает: гемолиз; повышение уровня ферментов печени; тромбоцитопения. Впервые описан в 1982 году L. Weinstein.
Этиология этого синдрома неизвестна. Развивается обычно на поздних стадиях беременности. HELLP-синдром принято рассматривать как вариант преэклампсии, протекающей с гемолитической анемией, тромбоцитопенией, снижением уровня гаптоглобина и признаками нарушения функций печени.
HELLP-синдром клинически характеризуется артериальной гипертонией за счет нарушения механизма регуляции артериального давления, рецидивирующим абдоминальным болевым синдромом, желтухой, оте ками, рвотой, появлением судорог. Встречается у 5-10% беременных женщин, чаще – у молодых, первородящих. В части случаев возможен переход от преэклампсии к эклампсии. Протекает с выраженными нарушениями функций печени.
В диагностике используют биохимическое исследование крови, при котором определяются: высокий уровень ферментов цитолиза (АЛТ, АСТ), лактатдегидрогеназы (ЛДГ) и неконъюгированного билирубина.
Отмечается снижение уровня гаптоглобина в крови и присутствие шизоцитов, представляющих собой фрагментированные пойкилоциты. Этот синдром обозначают, как “микроангиопатический гемолиз». При биопсии печени определяются некрозы гепатоцитов, неспецифические дегенеративные изменения. В дифференциальной диагностике необходимо исключить вирусные гепатиты путем определения соответствующих антигенов и антител.
Материнская смертность составляет в среднем 3% (от 1,5 до 25%), а перинатальная смертность новорожденных превышает 20%.
Лечение. Специфического лечения синдрома HELLP не существует. Наиболее эффективно досрочное родоразрешение. Используют также глюкокортикостероиды, трансфузии крови и ее компонентов 1.
Беременность при наличии заболеваний печени. При беременности течение острого вирусного гепатита А существенно не отличается от такового у небеременных. При этом инфицирования плода не происходит.
Вирусные гепатиты В и С при беременности протекают более тяжело с длительным периодом желтухи, выраженной интоксикацией и печеночной энцефалопатией. Что касается плода, то его инфицирование возможно при наличии на коже ссадин и повреждений. При выявлении в крови у матери HBeAg+ риск инфицирования плода достигает 2-15%.
При наличии у беременных женщин аутоиммунных заболеваний печени – аутоиммунного гепатита, первичного билиарного цирроза или первичного склерозирующего холангита – вопрос об искусственном прерывании беременности решается индивидуально. Высокоактивное аутоиммунное поражение печени сопровождается гипогонадизмом, аменореей и может стать причиной бесплодия. Беременность может оказать иммуномодулирующее влияние на течение всех аутоиммунных заболеваний, поэтому у беременных женщин не наблюдается обострения патологического процесса в печени и становится возможным нормальное завершение беременности (у 74%). Однако у части больных отмечается ухудшение течения заболевания, нарастает активность патологического процесса, развивается печеночная недостаточность, возможны отслойка плаценты и кровотечение [39,40].
Болезнь Вильсона развивается, как правило, в молодом возрасте, сопровождается самопроизвольными абортами или бесплодием. Однако лечение Д-пеницилламином и препаратами цинка при наступлении беременности у этих больных улучшает функциональное состояние печени и восстанавливает репродуктивную способность больной, создает условия для деторождению. Вместе с тем, после рождения ребенка на фоне лечения Д-пеницилламином грудное вскармливание противопоказано [41,42].
При наличии у беременной женщины холелитиаза или калькулезного холецистита беременность усугубляет течение болезни, способствует длительному застою желчи в желчном пузыре и росту конкрементов, особенно во вторую половину беременности, когда давление в брюшной полости резко возрастает и нарушается отток желчи. Все это приводит к тому, что исходно скрытое течение холелитиаза (до беременности) приобретает клинически выраженный характер с приступами желчной колики и диспепсическими явлениями (горечь во рту, тошнота и рвота и др.). При возникновении показаний к холецистэктомии ей должно предшествовать родоразрешение [43,44].
Лечение болезней печени и желчных путей при беременности проводится теми же лекарственными средствами, что и до беременности, но следует по возможности отказаться от лекарств, обладающих гепатотоксическим действием. Так, при вирусных гепатитах противовирусная терапия при наличии беременности не проводится. Можно назначить Гептрал, препараты УДХК (Урсофальк, Урсосан), Хофитол и др. Следует помнить, что назначение фармакопрепаратов беременным при наличии у них различных заболеваний печени – это ответственная задача, а лечащий врач несет личную ответственность за здоровье беременной женщины и еще не родившегося ребенка.
Что можно пить для печени при беременности
Физиологические изменения печени во время беременности
Нормально протекающая беременность не сопровождается нарушением функционального состояния печени. Однако при беременности мобилизуются функциональные резервы печени для обезвреживания продуктов жизнедеятельности плода и обеспечения его пластическим материалом. Существенно увеличивается продукция многих гормонов, особенно эстрогенов и прогестерона. Отклонения отдельных показателей от нормы следует рассматривать как выражение повышенной метаболической активности и адаптации организма беременной.
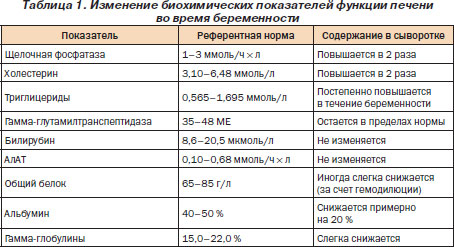
При осмотре женщин с нормальным течением беременности можно обнаружить эритему ладоней и сосудистые звездочки. Печень не пальпируется. Биохимическое исследование сыворотки крови в III триметре беременности выявляет умеренное повышение активности щелочной фосфатазы (а именно ее плацентарной фракции), уровня холестерина, триглицеридов. При этом активность ГГТП остается в пределах нормы. Уровень желчных кислот незначительно повышен. Уровень билирубина и активность аминотрансфераз сохраняются в пределах нормы. Уровни альбумина, мочевины и мочевой кислоты в сыворотке снижаются (табл. 1). Функциональные пробы печени нормализуются спустя 2–6 недель после родов. Гистологическое исследование биоптата печени при нормальной беременности не обнаруживает патологических изменений.
Классификация заболеваний печени у беременных
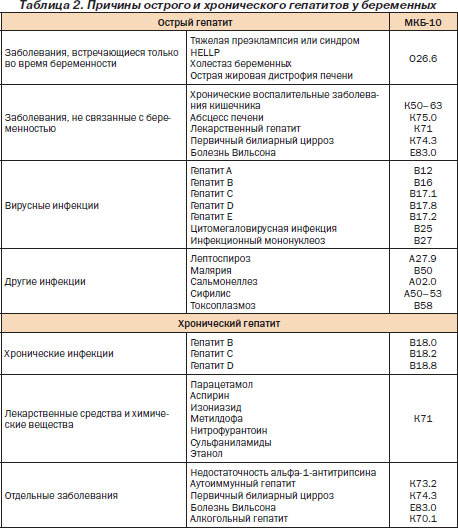
С практической точки зрения целесообразно выделить две группы заболеваний, вызывающих дисфункцию печени у беременных (табл. 2):
1) встречающиеся только во время беременности;
2) встречающиеся и вне беременности.
Наиболее частыми причинами нарушения функции печени у беременных являются вирусные гепатиты (42 %), холестаз беременных (21 %), более редкими причинами являются желчнокаменная болезнь, неукротимая рвота беременных, преэклампсия и HELLP-синдром.
Вирусные гепатиты
Клиническая классификация вирусных гепатитов у беременных (приказ № 676 МЗ Украины, 2004 г.)
Выделяют вирусные гепатиты:
1. Вирусный гепатит А.
2. Вирусный гепатит В.
3. Вирусный гепатит С.
4. Вирусный гепатит Е.
5. Вирусный гепатит D.
6. Вирусный гепатит G.
7. Вирусный гепатит F.
Б. По выраженности клинических проявлений:
1. Бессимптомные формы:
2. Манифестная форма:
В. По цикличности течения:
1. Циклическая форма.
2. Ациклическая форма.
Г. По степени тяжести:
4. Очень тяжелая (фульминантная).
1. Острая и подострая дистрофия печени (острая печеночная энцефалопатия).
2. Функциональные и воспалительные заболевания желчных путей и желчного пузыря.
3. Внепеченочные поражения (индукция иммунокомплексных и аутоиммунных заболеваний).
2. Остаточные признаки патологии (постгепатитная гепатомегалия и гипербилирубинемия, затяжная реконвалесценция — астеновегетативный синдром).
3. Хронический гепатит.
5. Первичный рак печени (гепатоцеллюлярная карцинома).
Классификация острого и хронического гепатита по клинико-биохимическим и гистологическим критериям (приказ № 676 МЗ Украины)
Степень активности (определяется тяжестью воспалительно-некротического процесса):
а) минимальная (увеличение АлАТ не более чем в 3 раза);
б) умеренная (увеличение АлАТ от 3 до 10 раз);
в) выраженная (увеличение АлАТ более чем в 10 раз).
Стадия (определяется распространением фиброза и развитием цирроза печени):
1 — слабо выраженный перипортальный фиброз;
2 — умеренный фиброз с портопортальными септами;
3 — выраженный фиброз с порто-центральными септами;
Примеры формулировки диагноза:
— Острый вирусный гепатит В, высокая степень активности, тяжелое течение.
— Острый вирусный гепатит ни А, ни В, желтушная форма средней тяжести, циклическое течение.
— Хронический вирусный гепатит С (anti-HCV+, HCV-PHK+, 3a-генотип), умеренной степени активности, с выраженным фиброзом (стадия).
— Хронический вирусный гепатит В, НВeАg-позитивный (HBsAg+, HBV ДНК+), выраженной степени активности.
Диагностика гепатитов при беременности
Анамнез (вирусный гепатит В, или С, или D; профессиональные, химические вредные факторы; медикаментозные интоксикации; злоупотребление алкоголем; подпеченочный холестаз; метаболические нарушения и др.).
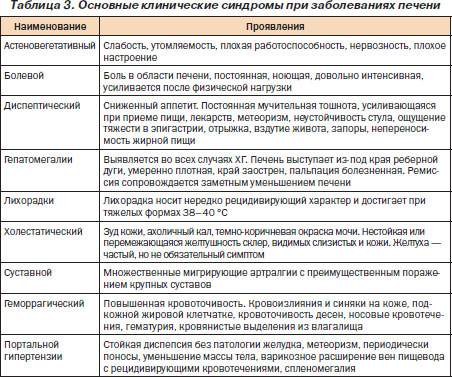
Клинические синдромы патологии печени показаны в табл. 3.
Лабораторные показатели
Маркеры вирусных гепатитов (табл. 4):
1) гепатит А — анти-HAV IgM — даже однократное выявление является абсолютным доказательством заболевания (появляется в крови за 4–5 дней до выявления симптомов заболевания и исчезает через 6–8 мес.);
— HBsAg (основной маркер инфицирования НВ-вирусом, выявляется с 3–5-й недели заболевания, в течение 70–80 дней);
— HBeAg (маркер эпидемиологического риска, активной репликации вируса и трансмиссии от матери к плоду; риск заражения плода повышается до 90 %);
— HBcAg (в крови не определяется, но могут быть антитела к нему — анти-HBcIgM и HBcIgG, свидетельствующие об этиологии острого вирусного гепатита В (ОВГВ) и перспективе вирусоносительства, HBcorAg, HBxAg, анти-HBc IgМ;
3) гепатит С — анти-HСV IgM (диагностическое значение при хроническом гепатите);
— HBsAg (маркер активной репликации вируса при остром гепатите);
— анти-HDV IgM (появляется на 10–15-й день заболевания и сохраняется 2,5–3 мес.);
5) гепатит Е — анти-HЕV IgM.
Методом ПЦР (по возможности):
— гепатит А — РНК HAV;
— гепатит В — ДНК HВV;
— гепатит С — РНК HСV;
— гепатит D — РНК HDV;
— гепатит Е — РНК HЕV.
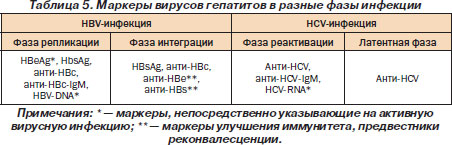
В течении HBV-инфекции выделяют фазу репликации и интеграции (табл. 5).
HCV-инфекция характеризуется чередованием латентной фазы и фазы реактивации.
Исчезновение HВeAg и выявление анти-НBе называется сероконверсией, свидетельствует о включении (интеграции) вирусной ДНК в геном гепатоцита, сопровождается обострением болезни.
Наличие HbsAg в сочетании с анти-НВе класса IgG и/или с анти-НВс характеризует фазу интеграции вируса гепатита В в геном гепатоцита.
Сыворотка крови больных HDV содержит маркеры дельта-антигена (IgE и IgМ-анти-D, а также маркеры В инфекции).
Сывороточной пробы для диагностики ВГG пока не существует.
Биохимические показатели вирусных гепатитов:
— тимоловая проба > 4 МЕ (не изменяется при ОВГВ);
— повышение АлАТ, в меньшей степени АсАТ;
— билирубин > 22 мкмоль/л, преимущественно за счет прямого;
— лейкопения (возможно, лейкоцитоз), лимфопения, снижение СОЭ, тромбоцитопения;