Что можно есть при полипах в желудке
Полипэктомия в толстой кишке – это операция, в ходе которой удаляются полипы, образовавшиеся на внутренней поверхности кишки. В статье освещаются вопросы:
Полный текст статьи:
Узнайте, как проводится колоноскопия для удаления полипов, какие инструменты при этом используются, и сколько времени длится операция.
Что представляет собой эта операция
Полип – доброкачественное опухолевидное образование на ножке или широком основании, свисающее из стенок полого органа в его просвет. В некоторых случаях возможно перерождение тканей в злокачественные новообразования. Удаление полипов делается в рамках профилактики онкологических заболеваний прямой кишки.
Есть случаи, когда полипы доставляют неприятные ощущения: боли в животе и ректальные кровотечения. Их удаление также помогает избавиться от болезненных симптомов.
Показания
От того, как быстро будет диагностировано заболевание и проведено удаление полипов посредством колоноскопии, зависит успешность лечения. Диагностирование полипа в кишке является прямым показанием к его удалению. Операция показана и в случае, когда новообразование не доставляет беспокойства. Разрастание ткани приводит к запорам, непроходимости и воспалительным процессам. Характер симптомов зависит от количества и типа патологической ткани.
Правила подготовки
Операция назначается после комплексного обследования. Оно подразумевает:
Может потребоваться отмена препаратов, которые принимаются для разжижения крови. За 3 дня до удаления полипов в кишке соблюдается диета. В этот период рекомендован приём жидкой пищи и большого количества воды. Подготовка такая же как на колоноскопии.
Порядок проведения операции
Колоноскопия с удалением полипов под наркозом занимает от 30 до 60 минут. Пациент ложится на спину или на бок. Через анальное отверстие в полость тела вводится наконечник эндоскопа. Эндоскопист медленно продвигает его по прямой кишке. Для открытия толстой кишки в неё подаётся небольшое количество воздуха.
Когда камера, закреплённая на конце трубки эндоскопа, фиксирует место расположения полипа, врач приступает к этапу его удаления. Он проводится с помощью специальных мини-ножей. Полипы могут прижигаться электрическим током. По завершению операции все инструменты извлекаются из кишечника.
Диета после удаления полипов в толстой кишке
Через день после операции пациент может вернуться к приёму пищи. Она не должна быть твёрдой. В ближайшее время нужно избегать употребления:
В меню после удаления полипов в толстой кишке должны входить продукты, не вызывающие раздражения или вздутия. Рекомендуется употреблять куриный бульон и небольшое количество овсяной каши. Переедание в течение нескольких дней после операции грозит запорами.
Что делать после удаления полипов?
Диета после удаления полипов методом колоноскопии очень важна. В реабилитационный период нужно соблюдать правила гигиены зоны кожного покрова, если использовалась методика лапароскопии. В течение двух недель нельзя поднимать грузы более 3 килограмм. На будущее нужно запланировать прохождение колоноскопии для контроля рецидивов.
Полипы желудка
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Дальнейшее отношение к выявленному во время видеоэзофагогастродуоденоскопии (ВГДС) полипу зависит от его гистологической верификации, этиологии (причины возникновения), естественной истории (развитие в динамике). После оценки полученных данных решается вопрос о необходимости лечения в данном клиническом случае или о проведении динамического наблюдения.
Классификация полипов желудка
Наиболее рациональным является классифицирование полипов по клиническим, морфологическим и гистологическим признакам. Чаще всего полипы имеют бессимптомное течение. Однако, осложненный вариант может проявляться кровотечением (признаки анемии, кровь в стуле), непроходимостью (тошнота, рвота), гастритоподобным течением (боли в верхних отделах живота) и малигнизацией (снижение массы тела и др. симптомы онкологического заболевания).
По морфологическим критериям полипы разделяют на солитарные (одиночные) и множественные, мелкие и крупные, мягкие и плотные. Учитывая, что видеогастроскопия является «золотым» стандартом в диагностике данной патологии, во всем мире признанной является Парижская классификация эпителиальных новообразований, согласно которой выделяют выступающие (0-Ip – на узкой ножке, 0-Isp – на зауженном основании, 0-Is – сидячие) и поверхностные (0-IIa – приподнятые, 0-IIb – поверхностные плоские, 0-IIc – слегка углубленные, смешанные варианты).
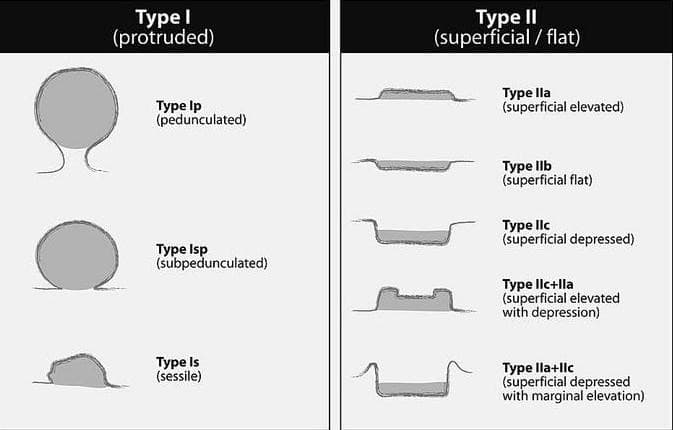
Ключевым моментом при выполнении эндоскопического исследования является не только правильная интерпретация найденного образования, но и возможность забора материала с последующим гистологическим подтверждением, что главным образом влияет на дальнейшую тактику лечения. В связи с этим представлены четыре группы полипов с их подробными характеристиками.
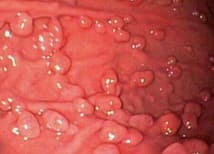
При хромоскопии и узкоспектральной эндоскопии (NBI) поверхность представлена рисунком по типу «пчелиных сот» с густой сосудистой архитектоникой. Изначально фундальные полипы связывали с гамартомами (образованиями, представляющими тканевую аномалию развития), однако, в большом числе исследований подтверждено, что механизмы, подавляющие секрецию соляной кислоты ингибиторами протонной помпы (ИПП), могут также участвовать в патогенезе развития фундальных полипов желудка.
Гистологически фундальные полипы представлены дилятированными (расширенными) кислотопродуцирующими железами, покрытыми плоскими париетальными и слизистыми клетками без признаков дисплазии. Выявление характерных полипов желудка у пациентов, принимающих ИПП, с большой долей вероятности диагностируют как полипы фундальных желез. При первичном осмотре один или более представленных полипов после взятия биопсии подвергают морфологической оценке для подтверждения диагноза. Большие полипы (более 10 мм), эрозированные, расположенные нетипично, например, в антральном отделе желудка, должны быть подвергнуты более агрессивной тактике ведения – эндоскопической полипэктомии.
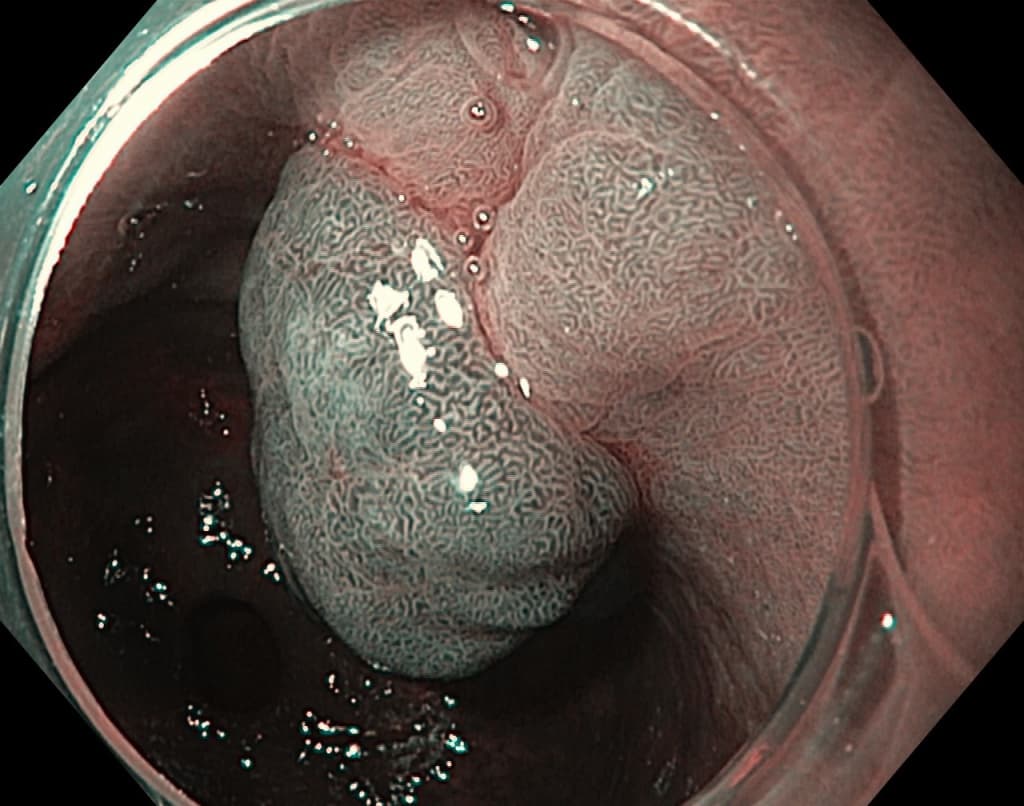
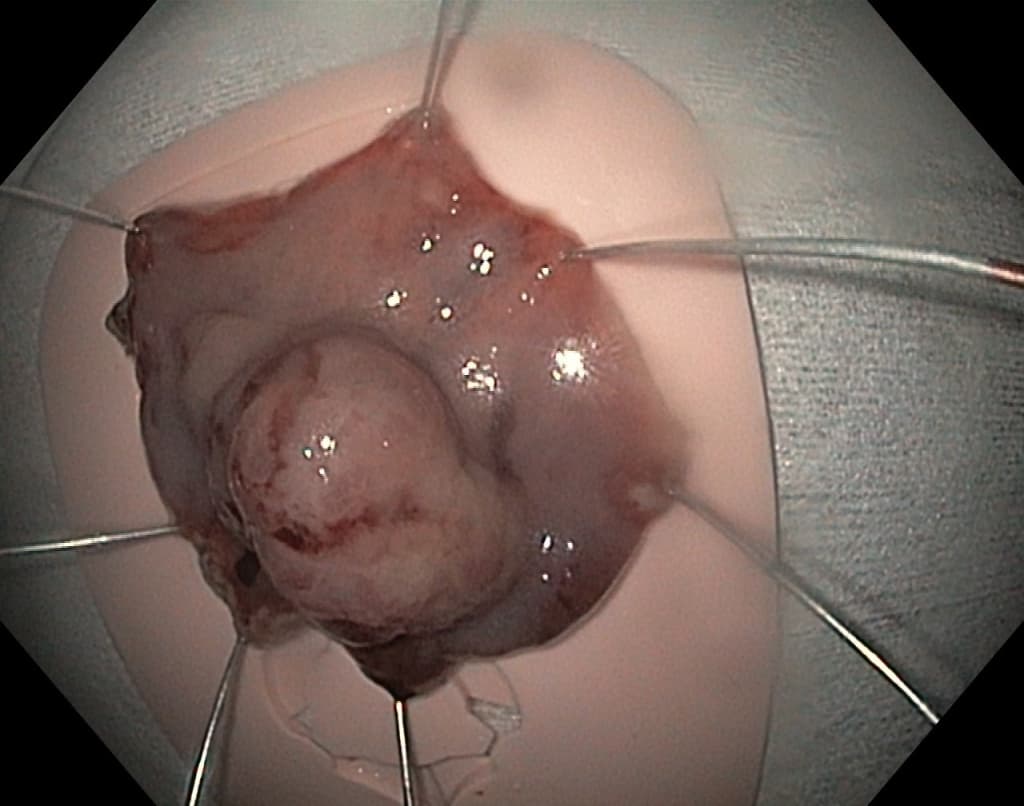
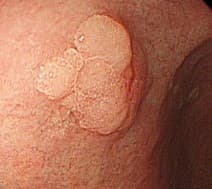
Эндоскопически они представлены солитарным одиночным образованием дольчатой формы с бархатистой поверхностью. Хотя они могут быть найдены в любом отделе, наиболее часто локализуются в антральном отделе желудка.
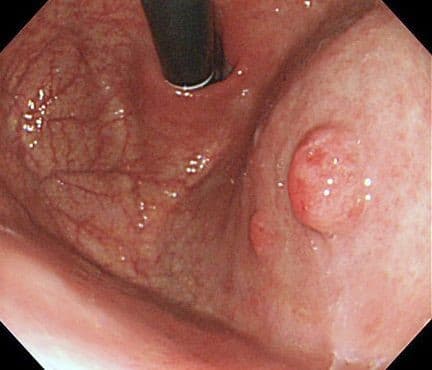
Лечение полипов желудка
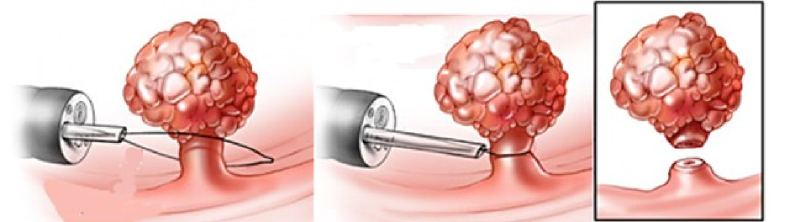
Как говорилось ранее, все аденоматозные и крупные полипы более 10 мм должны быть подвергнуты удалению. Каким же образом выполняется эндоскопическая полипэктомия или резекция слизистой?
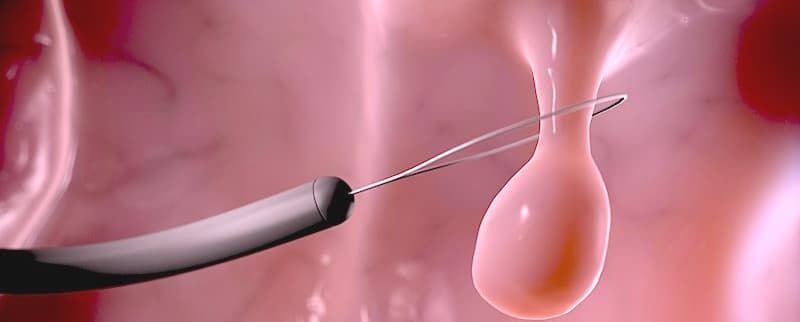
Крупные экзофитные (выступающие) полипы на широком основании или плоские образования, которые невозможно удалить эндопетлей, подвергаются технически более сложному варианту эндоскопического удаления – диссекции в подслизистом слое. Данный вид операции направлен на радикальное удаление образования единым блоком: после создания «гидростатической подушки» выполняется циркулярный разрез вокруг образования специальными инструментами, после чего рассекаются соединительнотканные сплетения подслизистого слоя с полной ликвидацией патологического очага.
По современным представлениям, наиболее рациональным является наблюдение за пациентами после проведенной полипэктомии через 1 год. При этом оценивается состояние слизистой оболочки на предмет появления новых образований или рецидива на месте ранее выполненной операции. Если же после резекции образований гистологический ответ подтверждает наличие дисплазии высокой степени или же раннего рака, то контрольная гастроскопия должна проводиться в интервале: 1,5 мес.- 3 мес.- 6 мес. – 1 год и в последующем каждый год.
Профилактика полипов желудка
Целью профилактики является выявление образований желудка на ранних этапах развития. Рекомендуется выполнение эндоскопического исследования лицам старше 45 лет в качестве скрининга даже при отсутствии клинической симптоматики, так как заболевание проявляет себя лишь на поздней стадии, когда уже требуется хирургическое лечение. Следуя принципам онкологической настороженности, пациентам с отягощенным наследственным анамнезом, то есть при наличии онкологических заболеваний со стороны ЖКТ у ближайших родственников, требуется незамедлительный профилактический осмотр желудка и толстой кишки.
Как получить услугу в Клинике
В нашей Клинике проводятся все виды эндоскопических исследований на высококачественном оборудовании как под местной анестезией, так и под наркозом. Все выявленные патологические образования подвергаются гистологической верификации. Также проводится забор материала на наличие инфекции H.pylori и для определения стадии и степени выраженности воспалительных и атрофических изменений слизистой оболочки желудка (класс.OLGA), что свидетельствует, как говорилось ранее, о риске развития онкологического процесса.
Что касается оперативного эндоскопического лечения, то в клинике возможно его выполнение в амбулаторных и стационарных условиях. Решение принимает лечащий врач, опираясь на размеры патологических очагов, их количество, результаты гистологии и сопутствующую патологию.
Полип желудка

Полип желудка – это доброкачественное разрастание его слизистой оболочки, которое в большинстве случаев протекает бессимптомно и выявляется случайно при проведении эндоскопии по поводу других состояний. У мужчин полипы регистрируются в 2 раза чаще, чем у женщин. Значительно выше частота выявления полипов в среднем и пожилом возрасте (после 40 лет). Полипы желудка у детей встречаются очень редко и часто являются симптомом врожденной патологии (например, аденоматоза).
Наиболее часто полипы образуются в пилорическом отделе желудка, на втором месте – его тело. В остальных частях желудка полипы встречаются довольно редко. Полипы в желудке могут быть одиночными или множественными, и те, и другие встречаются примерно с одинаковой частотой. Чем больше размер полипа, тем более вероятны клинические проявления и перерождение в злокачественную опухоль.
Виды полипов желудка:
- Аденоматозный полип желудка – это доброкачественная опухоль, представляющая собой разрастание железистой ткани. Гиперпластический полип желудка – разрастание эпителия, которое не считается доброкачественной опухолью. Данный тип встречается значительно чаще (приблизительно в 16 раз) и имеет более благоприятный прогноз. Он никогда не перерождается в рак, в отличие от аденоматозных полипов. Гиперплазиогенный полип желудка формируется при нарушении регенерации желез слизистой оболочки желудка. Преимущественная локализация гиперплазиогенных полипов – тело желудка.
Причины появления полипов в желудке
Клинические проявления полипов желудка
Небольшие по размерам немногочисленные полипы обычно не вызывают никаких симптомов, но чем крупнее и многочисленнее они становятся, тем выше вероятность появления различных проблем. Большие полипы затрудняют прохождение пищевого комка, что может вызывать чувство тяжести в желудке, боли в эпигастрии, отрыжку, изжогу, тошноту, в некоторых случаях даже рвоту.
Постепенно диспепсия приводит к снижению аппетита. Изменение пищевого поведения и пищеварения в целом приводит к снижению массы тела, астенизации (быстрая утомляемость, слабость, плохая сопротивляемость инфекциям). Изменяется характер стула, часто беспокоит метеоризм. Пища может повреждать полипы, что становится причиной кровотечений. Признак желудочного кровотечения – черная кровь в стуле. Кровотечения носят хронический характер, поэтому приводят к снижению содержания гемоглобина в крови (постгеморрагическая анемия).
. Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу. Легче предупредить болезнь, чем бороться с последствиями.
Серьезным осложнением данного заболевания может стать ущемление полипа. Это характерно для полипов на ножке, расположенных рядом с привратником. Попадая в полость двенадцатиперстной кишки, они ущемляются при сокращении сфинктера, что сопровождается сильными болями в животе. Другим возможным осложнением является озлокачествление (малигнизация), которому в некоторых случаях подвергаются аденоматозные полипы.
Диагностика полипов в желудке
Выявить наличие полипов в желудке можно только при помощи визуализирующих методов исследования, к которым относятся фиброгастродуоденоскопия и рентгенологическое обследование.
Рентгенологическое обследование с введением контраста позволяет увидеть на снимке наличие дефектов наполнения желудка, неровности стенки, обусловленные полипами. Но при выявлении полипов на рентгенографии желудка необходимо будет провести ФГДС с биопсией полипа.
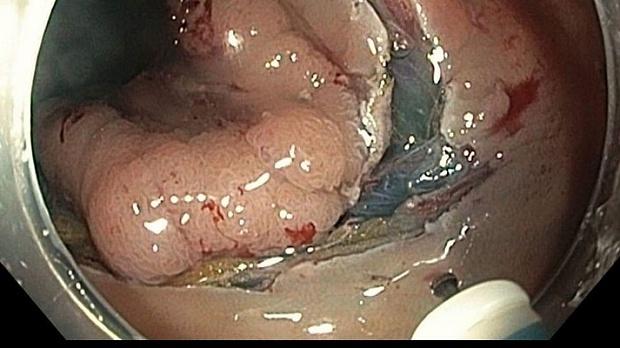
Фиброгастродуоденоскопия (ФГДС) – эндоскопическое исследование, во время которого полость желудка осматривается изнутри. При выполнении ФГДС можно не только увидеть полипы, но и выполнить биопсию – взять кусочек ткани для исследования. ФГДС может быть не только диагностической, но и лечебной, когда новообразования удаляют полностью. Биопсия полипа желудка необходима для оценки морфологии образования, чтобы исключить онкологический процесс и провести дифференциальную диагностику с другими патологическими состояниями.
При выявлении полипов обязательно проводится полное обследование пациента для определения сопутствующей патологии, которая может быть причиной появления полипов (гастрит, хеликобактерная инфекция, дуоденогастральный рефлюкс и пр.).
Лечение полипов желудка может быть консервативным и хирургическим. Нужно ли удалять полип желудка, решает врач, основываясь на размерах полипа и клинических симптомах. Удаление полипов в желудке показано при их больших размерах, при выраженных проявлениях, снижающих качество жизни и утяжеляющих течение сопутствующих заболеваний желудка. Абсолютным показанием к удалению полипов, а иногда и резекции части или всего желудка, является малигнизация полипов или подозрение на нее, а также другие осложнения (кровотечения, ущемление). В большинстве случаев удаление полипов в желудке проводится эндоскопически путем их иссечения или электрокоагуляции. При небольших гиперпластических полипах обычно рекомендуется наблюдение с периодическим обследованием для оценки размера и количества полипов.
В СЕМЕЙНОЙ КЛИНИКЕ Вы сможете сделать ФГДС на современной оборудовании, а также получить консультацию опытного и квалифицированного гастроэнтеролога по всем заболеваниям желудочно-кишечного тракта.
Лечебное питание в послеоперационном периоде
Важнейшим фактором послеоперационной реабилитации больных, перенесших операции на органах пищеварения, является лечебное питание.
Диетотерапия направлена на удовлетворение пластических и энергетических потребностей организма больного. Правильное питание способствует снижению частоты осложнений и приводит к скорейшему выздоровлению. Важнейшей задачей диетотерапии как в условиях стационарного, так и амбулаторного этапов реабилитации считают преодоление белкового, витаминного, минерального и энергетического дефицитов, которые развиваются у большинства больных в связи с операционной травмой, лихорадкой и недостаточным питанием после операции.
Оперативное вмешательство, независимо от вида хирургического воздействия и сопровождающей его анестезии, вызывает мощные метаболические сдвиги в организме. На организм пациента влияют как специфические факторы хирургической травмы (крово- и плазмопотеря, гипоксия, токсемия, нарушения функций поврежденных органов), так неспецифические факторы, такие как болевые импульсы, возбуждение адренергической и гипофизарно-надпочечниковой систем.
Хирургический стресс характеризуется резким усилением процессов катаболизма, выраженными нарушениями метаболизма, особенно белкового и энергетического. Основными причинами этих нарушений являются катаболическое действие адренокортикотропного гормона и глюкокортикоидов, адреналина и вазопрессина, повышенный протеолиз в тканях, потери белка с отделяемым из операционной раны и увеличение энерготрат с утилизацией собственных белков. При этом не только усиливается катаболизм, но и угнетается синтез белков. Разрушение гликогена в печени и мышцах (легкодоступный, но небольшой по объему источник энергии), триглицеридов в жировой ткани считается частью раннего нейроэндокринного ответа на хирургическую травму. Резервы углеводов в организме ограничены, и поэтому в энергетический обмен активно вовлекаются тканевые белки, в первую очередь белки скелетных мышц.
Длительность и выраженность катаболической фазы стресса при тяжелых и обширных хирургических вмешательствах (резекция и пластика пищевода, желудка, гастрэктомия) препятствуют в ранний послеоперационный период реализации фазы долговременной адаптации.
У больных, перенесших оперативные вмешательства, в ближайшем послеоперационном периоде резко повышен энергетический обмен, в основном за счет неадекватного увеличения фактического основного обмена. При этом нередко энергетический дефицит достигает таких величин, что даже при потреблении обычного пищевого рациона (2500–3000 ккал/сут) больные все равно оказываются в условиях выраженной белково-энергетической недостаточности. При этом происходит переход на полное или частичное эндогенное питание, что приводит к быстрому (иногда катастрофическому) истощению резервов углеводов и жиров, а также значительной потере белков. Эти явления значительно ухудшают течение процессов регенерации, затягивают течение послеоперационного раневого процесса. Возникают предпосылки развития послеоперационных осложнений, в том числе пострезекционной дистрофии, спаечной болезни, эрозивно-язвенных осложнений, метаболических расстройств, вплоть до развития сепсиса.
Осложнения, наблюдаемые после операций на пищеварительном тракте (представленно по: J. C. Melchior, 2003):
Осложнения, связанные с поздним началом энтерального питания, приводящие к гастростазу, вздутиям живота, недостаточностью швов анастомозов.
Инфекционные осложнения, вызванные снижением иммунной и неспецифической защиты, обусловленные отсутствием питания, такие как нагноения послеоперационной раны, застойная пневмония, перитонит и сепсис.
Лечебное питание после операций на пищеводе
Диетотерапия – важная часть всего комплекса послеоперационной реабилитации больных, перенесших операции на пищеводе.
В ранние сроки после проведения оперативного лечения больному проводят восстановительное лечение в хирургическом стационаре, а затем в гастроэнтерологическом отделении, куда больной переходит на долечивание. На амбулаторное лечение больного переводят, как правило, через 1,5-2 месяца после операции.
Диетическое питание в первые месяцы после операции на пищеводе осуществляется по принципам проведения парентерального и энтерального искусственного питания.
Лечебное питание после операций на желудке и двеннадцатиперстной кишке
Больным, перенесшим оперативные вмешательства на желудке, в течение всей жизни рекомендуется соблюдать дробное питание (4–5 раз в день), ограничивать продукты и блюда, наиболее часто вызывающие демпинг-синдром (сладкие напитки, сладкие молочные каши, очень горячие и очень холодные блюда), принимать пищу не спеша, тщательно пережевывая ее.
Лечебное питание при постгастрорезекционных синдромах
Среди неблагоприятных последствий операций на желудке выделяют следующие патологические состояния:
Синдром приводящей петли.
Пептическая язва анастомоза.
Гастрит культи желудка.
Питание при демпинг-синдроме
Демпинг-синдром – это наиболее частое осложнение, возникающее в различные сроки после резекции желудка по поводу язвенной болезни.
Основными признаками этого заболевания являются: чувство жара, сердцебиение, одышка, потливость, слабость, головокружение, сухость во рту, тошнота, рвота, «дурнота», боли в животе, вздутие его, понос, сонливость, усталость, непреодолимое желание лечь, обморочное состояние. Все эти явления появляются чаще всего после еды, особенно после приема сладкой, горячей, молочной пищи. В лежачем положении эти явления ослабевают.
Возникновение демпинг-синдрома связано с быстрым переходом (сбросом) недостаточно переваренной пищи из культи желудка непосредственно в тонкую кишку, минуя двенадцатиперстную кишку, удаленную в процессе операции. Стремительный пассаж химуса по тонкой кишке провоцирует нарушения гуморальной регуляции за счет изменения внутрисекреторной функции поджелудочной железы. В результате возникают патологические проявления демпинг-синдрома.
Выделяют три степени тяжести демпинг-синдрома.
Легкая степень тяжести. Характеризуется тем, что приступы возникают только после обильного приема пищи или пищи, богатой простыми углеводами. Приступ сопровождается легкими вазомоторными и кишечными симптомами, которые быстро проходят в положении больного лежа. Трудоспособность у этих больных сохраняется.
Средняя степень тяжести демпинг-синдрома. Проявляется выраженными вазомоторными нарушениями и кишечными симптомами, возникающими ежедневно. Больной вынужден принимать горизонтальное положение, которое улучшает его самочувствие. Общая работоспособность больного снижена.
Тяжелая форма демпинг-синдрома. Проявляется ярко выраженными приступами почти после каждого приема пищи, иногда с обморочным состоянием, что приковывает больного к постели на 1–2 часа. Трудоспособность больных резко снижается или полностью утрачена.
Ведущим методом лечения демпинг-синдрома является правильно построенный диетический режим.
Общие рекомендации по питанию при демпинг-синдроме
Частое дробное питание небольшими порциями (5-7 раз в день). Принимать пищу следует медленно. Пища должна быть медленно и тщательно пережевана.
Ограничение продуктов и блюд, наиболее часто вызывающих демпинг-синдром: сладостей (сахар, мед, варенье), очень горячих или очень холодных блюд, жидких сладких молочных каш и др.
Прием жидкости производить отдельно от остальных блюд, т.е. чай, молоко, 3-е блюдо в обед и кефир вечером следует употреблять через 20-30 минут после основного приема пищи. Количество жидкости за один прием не должно быть обильным (не более 1 стакан).
Пища и напитки должны быть теплыми.
После еды пациент должен принять лежачее положение на 20–30 мин., особенно после обеда.
Пища должна содержать достаточное количество пектина (овощи и фрукты).
Этапность диетотерапии при демпинг-синдроме
При этом в питании резко ограничивают продукты и блюда, содержащие простые (быстро всасывающиеся) углеводы – сладкие жидкие молочные каши, особенно манную, рисовую, сладкое молоко, сладкий чай. Больным противопоказаны холодные и очень горячие блюда. Рекомендуется раздельный прием жидкой и плотной части пищевого рациона, причем жидкость следует употреблять через 30 мин после приема твердой пищи, а во время обеда сначала надо съедать второе блюдо, а затем первое.
При осложнении демпинг-синдрома панкреатитом или при подозрении на пептическую язву культи желудка, анастомоза или тощей кишки рекомендуется диета № 1 с добавлением в 17 часов белкового блюда. При отсутствии осложнений и при хорошем самочувствии больного диету можно постепенно расширять, соблюдая основные ее принципы, и постепенно переходить на обычный пищевой рацион.
Питание при синдроме приводящей петли
В основе патогенеза синдрома приводящей петли лежит нарушение эвакуации содержимого из приводящей петли вследствие ее перегибов, образования спаек, нарушения моторной функции из-за изменения нормальных анатомических взаимоотношений.
Синдром приводящей петли обычно развивается в течение первого года после операции. Он проявляется сильными болями в эпигастрии и правом подреберье, рвотой желчью после еды. В промежутках между приемами пищи больные испытывают чувство тяжести в верхней части живота в результате заброса кишечного содержимого обратно в желудок, накоплением жидкости и пищи в приводящей петле и в культе желудка.
Тактика восстановительного лечения и диетического питания при синдроме приводящей петли такая же, как и при демпинг-синдроме.
Питание при астеническом синдроме
Астенический синдром является поздним послеоперационным осложнением резекции желудка.
Частота его появления находится в прямой зависимости от уровня резекции желудка. Большое значение в патогенезе этого состояния имеет нарушение секреторной и моторной функций культи резецированного желудка, изменение секреции желчи и панкреатического сока. В патогенезе определенное значение имеет быстрый пассаж по тощей кишке, нарушение всасывания железа и витаминов.
Для больных характерны быстрая утомляемость, общее недомогание, похудание, признаки гиповитаминоза, склонность к гипотонии и обморочным состояниям, нервно-психические нарушения. Общая слабость усиливается чаще всего после еды, особенно богатой углеводами. Наблюдаются различные диспептические явления: пониженный аппетит, отрыжка, срыгивание горькой жидкостью, ощущение тяжести в подложечной области. Характерным симптомом является расстройство кишечной деятельности, выражающееся в появлении (особенно после молочной и жирной пищи) громких кишечных шумов и поноса.
Питание при пептических язвах анастомоза и гастрите культи желудка
В механизмах развития пептических язв анастомоза и гастрита культи желудка первостепенное значение придается агрессивному действию желудочного сока и развитию хеликобактерной инфекции. Кроме того, имеет значение забрасывание дуоденального и кишечного содержимого в желудок, слабая перистальтическая функция культи желудка и быстрое опорожнение ее после еды.
Клиника пептической язвы анастомоза сходна с проявлениями язвенной болезни, но симптомы заболевания обычно более интенсивны, периоды обострения более длительны, чем при язве, по поводу которой была произведена операция. Характерны снижение аппетита, потеря массы тела.
Лечебное питание после операций на кишечнике
Правильная диетотерапия после операций на кишечнике способствует снижению частоты осложнений и более быстрому выздоровлению больного.
Традиционные подходы к лечебному питанию больных, перенесших операции на тонкой и толстой кишке, основанные только на принципах сбалансированного питания не приводят к восстановлению всего объема физиологических функций. Целесообразно подходить к реабилитации больных после резекции кишечника, с позиций теории адекватного питания, сформулированной академиком А. М. Уголевым. Необходимо обеспечивать не только элементное восстановление содержания нутриентов в организме, но и максимально восстановить полостное и мембранное пищеварение, всасывание в кишечнике, а также восстановить нормальный микробиоценез. Только при соблюдении этих условий возможна нормализация работы всего пищеварительного тракта.
Принципы питания больных, перенесших операции на кишечнике
Лечебное питание должно обеспечить щажение кишечника, а также других отделов желудочно-кишечного тракта.
Лечебное питание должно способствовать нормализации обмена веществ и восстановлению организма.
Лечебное питание должно повысить сопротивляемость организма при явлениях воспаления и интоксикации.
Лечебное питание должно способствовать заживлению операционной раны.
При отсутствии осложнений желателен более ранний перевод больных на физиологически полноценное питание с широким продуктовым набором.
Этапность диетотерапии после операций на кишечнике
В непосредственно послеоперационном периоде необходимо наладить парентеральное питание больного. В первую очередь это касается введения энергетических субстратов. Объем и состав парентерального питания определяют индивидуально в зависимости от потребности больного.
Стабилизация состояния больного и контролируемая диарея служат показаниями к переходу на питание с использованием желудочно-кишечного тракта. Обычно это происходит через 3–4 дня после операции. В то же время при обширных резекциях тонкой кишки некоторые специалисты рекомендуют начинать энтеральное питание через 2–4 недели после операции. В большинстве клинических случаев назначают стандартные смеси для энтерального питания, однако при резекциях тонкой кишки целесообразно применение деполимеризированных нутриентов (полуэлементных диет). Комбинированное парентерально-энтеральное питание в комплексной реабилитации больных после оперативных вмешательств на кишечнике позволяет сократить сроки и повысить эффективность восстановительного лечения, значительно снизить частоту осложнений и неблагоприятных исходов послеоперационного процесса.
При положительной динамике состояния больного рекомендован переход на естественное питание. Однако, следует помнить, что необоснованно ранний перевод больных на естественное питание после операций на кишечнике существенно ухудшает течение восстановительного периода, стимулирует развитие синдрома энтеральной недостаточности, нарушает естественные механизмы полостного и мембранного пищеварения.
Через 3–4 недели после выписки больного из стационара требуется постепенный переход на непротертый вариант диеты № 1. Постепенность перехода с одного варианта диеты на другой предполагает каждодневное сокращение количества протертых блюд. Хорошая переносимость вводимых блюд является свидетельством нормализации секреторной и моторно-эвакуаторной функций системы пищеварения и позволяет продолжить расширение диеты.
При плохой переносимости молока больными после операций на кишечнике следует надолго (иногда навсегда) исключить потребление молока. Лактозные перегрузки при наличии ферментатной недостаточности способны усугубить секреторные расстройства кишечника. Таким образом, при развитии послеоперационной лактозной недостаточности в диете больных следует максимально и надолго ограничить цельное молоко. К потреблению молочнокислых продуктов это относится в меньшей степени. Замена молочных продуктов может быть с успехом проведена за счет соевых продуктов. Соевые белки являются очень важным источником дополнительного обеспечения организма высокопластичным белком.
Питание при синдроме короткой кишки
Состояние, которое развивается после резекции тонкой кишки и характеризуется диареей, стеатореей, мальабсорбцией нутриентов, принято называть синдромом короткой (или укороченной) кишки.
При удалении менее 50% тонкой кишки синдроме короткой кишки протекает субклинически, но больший объем резекции приводит к нарастающей диарее, стеаторее, дефициту железа и фолиевой кислоты.
У больных с благоприятным течением послеоперационного периода при достаточно быстром восстановлении функций кишечника следует осуществлять постепенный, но обоснованно быстрый переход на полное естественное питание. Однако, то после осуществления обширных резекций кишечника переход от полного парентерального к естественному питанию должен проходить достаточно длительный этап частичного парентерального питания, растянутый подчас на несколько месяцев. Длительность переходного периода определяется сугубо индивидуально. В ряде случаев при обширных резекциях тонкой кишки пациент должен пожизненно получать полное или частичное парентеральное питание.
Введение новых продуктов в рационы лечебного питания должно строго зависеть от индивидуальной переносимости больных. Белково-энергетический дефицит рассматриваемых диет по отношению к физиологическим потребностям организма должен покрываться парентеральными средствами питания. Последовательность применения стандартных диет приведены выше.
После перехода на полное естественное питание больным с короткой кишкой рекомендуется диета с повышенным содержанием белка, углеводов и умеренным количеством жира. Диета должна быть дополнена триглицеридами со средней длиной углеродной цепи, поливитаминами в жидких формах, витамином В12 (внутримышечно 1 мг каждые 2–4 нед), фолиевой кислоты (внутримышечно по 15 мг в неделю), витамином К (внутримышечно по 10 мг в неделю), препаратами железа (парентерально, а затем и перорально).
Необходим динамический лабораторный контроль уровня оксалатов в моче. При появлении первых признаков гипероксалурии необходимо ограничить прием продуктов, содержащих повышенное количество оксалатов (щавель, шпинат, петрушка, картофель, шоколад).
Через 1-2 года после операции могут наблюдаться различные клинические варианты течения заболевания. В зависимости от состояния пациента и назначается лечебное питание.
Возможны следующие индивидуальные сценарии диетотерапии больных:
Естественное нормальное или близкое к нормальному питание.
Естественное питание с использованием индивидуально подобранных специализированных продуктов, содержащих деполимеризированные (короткоуепочечные) нутриенты (белки, жиры и углеводы).
Естественное питание с частичной парентеральной поддержкой.
Полное парентеральное питание.
Лечебное питание после операций на печени
В непосредственно послеоперационном периоде необходимо наладить парентеральное питание больного. В первую очередь это касается введения энергетических субстратов. Объем и состав парентерального питания определяют индивидуально в зависимости от потребности больного. Рекомендуемая в настоящее время продолжительность полного сбалансированного (по белкам, жирам, углеводам) парентерального питания зависит от объема и сложности проведенной операции на печени и составляет в среднем 3–5 дней.
Переход к естественному питанию должен проходить этап комбинированного (парентерально-энтерального) питания продолжительностью не менее 4–5 дней. Это связано с тем, что в результате операционной травмы печени происходит значительное угнетение функции тонкой кишки, восстановление которой занимает не менее 7–10 дней после операции. Зондовое введение элементных питательных смесей в пищеварительную систему в постепенно возрастающих количествах обеспечит у больных после операций на печени адаптацию желудочно-кишечного тракта к усиливающимся пищевым нагрузкам. Сочетание энтерального питания с парентеральным направлено на предотвращение метаболического голода.
Лечебное питание после операций на желчевыводящих путях
Общие правила питания для больных после операций на желчевыводящих путях
Частое, дробное питание. Прием пищи каждые 3,5–4 ч.
Ограничение продуктов, богатых холестерином.
Равномерное распределение жиров на все приемы пищи и перемешивание их с пищей, что способствует лучшему усвоению жиров, профилактике боли и диспепсических явлений.
После операций на желчных путях ухудшается переносимость очень многих продуктов, что требует минимизации их употребления. Особенно плохо больные переносят овощи, богатых эфирными маслами (редьку, редис, зеленый лук), острые блюда (перец, маринады, майонез, консервы). Также больные, перенесшие операцию на желчных путях, часто плохо воспринимают молоко, мороженое, шоколад, какао.
Лечебное питание больных, перенесших холецистэктомию
Через 24 часа после операции – минеральная вода без газа или отвар шиповника без сахара (маленькими глотками, не более 1 литра в сутки).
Через 36–48 часов – минеральная вода без газа, несладкий кисель из сухофруктов, несладкий некрепкий чай, нежирный кефир в объеме 1–1,5 л в течение суток (по 100–150 мл на один прием через каждые три часа).
В дальнейшем осуществляется переход на непротертый вариант диеты № 5а. Соблюдать эту диету рекомендовано в течение 1,5–2 месяцев после холецистэктомии и других видов хирургического лечения заболеваний билиарной системы.
Однако не все больные хорошо переносят диету № 5а: возникают транзиторные поносы, вздутие живота, метеоризм и появление связанных с этим болей в пилородуоденальной зоне и правом подреберье. Для этих случаев разработана диета № 5щ (щадящая), эта диета также назначается на 1–1,5 месяца после операции на желчных путях. Однако диета № 5щ (щадящая) не показана больным с пониженной массой тела из-за низкой ее энергоемкости, к тому же полное исключение растительного масла на фоне резкого ограничения жиров может способствовать формированию холестатического синдрома.
Несоблюдение принципа химического и механического щажения пищеварительной системы в 1,5–2 месяца восстановительного лечения после холецистэктомии способно привести к формированию хронического течения энтеральной недостаточности как одной из форм постхолецистэктомического синдрома.
Лечебное питание при постхолецистэктомическом синдроме
У 20–40% больных после проведения холецистэктомии развивается постхолецистэктомический синдромом. Данный синдром может быть обусловлен самыми разнообразными заболеваниями: камнями в желчных протоках, спазмом или стриктурой сфинктера Одди, гастритом, дуоденитом, язвенной болезнью, панкреатитом, дисбактериозом кишечника. Необходимо уточнить причину постхолецистэктомического синдрома, после чего назначать медикаментозное и диетическое лечение.
При постхолецистэктомическом синдроме используются следующие диеты:
При возникновении после холецитэктомии застоя желчи, гипомоторной дискинезии используют диету № 5 л/ж (липотропно-жировую).
Лечебное питание после операций на поджелудочной железе
Лечебное питание больных, перенесших операции на поджелудочной железе, независимо от характера заболевания, должно складываться из двух этапов: искусственное питание (парентеральное, зондовое, смешанное) и естественное питание.
На исход оперативного вмешательства положительно влияют длительность искусственного питания больного, адекватный компонентный состав и энергетическая ценность нутриционного обеспечения.
Этапность диетотерапии после операций на поджелудочной железе
Первый этап – полное парентеральное питание. Продолжительность полного парентерального питания больных, перенесших тяжелые хирургические вмешательства на поджелудочной железе, должна быть не менее 10–12 дней при условии полной белково-энергетической обеспеченности рациона нутриционной поддержки. Это позволяет свести до минимума послеоперационные осложнения. При менее тяжелых оперативных вмешательствах переход от парентерального к естественному питанию может состояться не ранее 5–7-го дня.
Второй этап – частичное парентеральное питание. Применяется в период перехода к естественному питанию. Сочетание постепенно нарастающего объема естественного питания с постепенно редуцирующимся парентеральным питанием – основное требование к лечебному питанию в условиях послеоперационной реабилитации. Это позволяет сохранить на должном физиологическом уровне белково-энергетическое обеспечение организма в данный период реабилитации и одновременно осуществлять плавно возрастающую пищевую нагрузку за счет механически, химически и термически щадящей гипокалорийной диеты.
Третий этап – естественное питание. Необходимо максимально медленно увеличивать пищевую нагрузку больным после операций на поджелудочной железе. Решение вопросов о расширении пищевого рациона, перехода с одной диеты на другую, требует тщательной оценки показателей состояния организма и особенностей течения заболевания.
Вначале больным после операций на поджелудочной железе назначается диета № 0а на срок 5–7 дней, а не на 2–3 дня, как при операциях на других органах.
На смену диеты № 0а назначают диету № 1а на срок 5–7 дней, также восполняя белково-энергетический дефицит средствами парентерального питания.
В дальнейшем рекомендуется переход на диету № 1б на срок 5–7 дней.
Статья добавлена 27 января 2016 г.